基于數據挖掘和網絡藥理學分析中藥治療痛風的用藥規律及作用機制
李澤宇, 郝二偉, 曹瑞, 林思, 莊培鈞, 楊瀟,杜正彩, 侯小濤, 鄧家剛*
(1.廣西中醫藥大學廣西中藥藥效研究重點實驗室, 南寧 530000; 2.中國-東盟傳統醫學研究國際合作聯合實驗室, 南寧 530200)
痛風是指與高尿酸血癥、尿酸鹽沉積密切相關的代謝性疾病,在中醫藥理論中屬于“痹證”“肢體痹”“白虎歷節”等范疇,臨床表現以急性和慢性痛風性關節炎為主。隨著人們生活條件的改善,蛋白質、糖、脂肪等攝入量大幅提升,導致痛風在全球范圍內發病率顯著提高且有年輕化趨勢,在中國,痛風和高尿酸血癥患病率分別高達1.1%和13.3%[1-2]。痛風還易并發如高血壓、糖尿病、冠心病、阿爾茨海默病等多種疾病[3-4]。痛風的病證表現以關節炎急性發作為主,并伴有劇烈的疼痛感,嚴重影響了患者的生活質量[5]。目前,中外治療痛風常用藥物為秋水仙堿、丙磺舒、苯溴馬隆、非布司他等,但這些藥物多以緩解癥狀為主,且副作用較大、停藥后易復發[6-7]。痛風有著易破壞關節、易造成多器官器質性病變、易反復等多種惡性生物學行為,而中藥具有安全性高、多靶點調節等特點。研究表明,中藥可通過調控酶[如基質金屬蛋白酶(MMPs)、黃嘌呤氧化酶(XOD)、環氧化酶-2(COX-2)]、炎癥因子[如白介素6(IL-6)及核因子κB(NF-κB)等通路發揮抗痛風作用,因此從中藥中尋找能夠有效治療痛風的藥物及藥物組合有著較大的現實意義。
中藥在防治痛風方面優勢顯著,現臨床中已應用多種中藥(如牛膝、黃柏等)及處方來有效應對痛風,但具體用藥體系較為繁雜,揭示這些抗痛風中藥的應用規律及具體機制的必要性及意義重大,本文基于此研究目的,首先采用數據挖掘的方法,從多種數據庫中收集治療痛風的中藥處方,并應用SPSS軟件對這些處方進行頻次及歸類分析,確定了治療痛風的高頻中藥及藥對,根據分析結果確定了治療痛風的核心中藥,然后以這些核心中藥為分析主體,采用網絡藥理學方法具體分析了其重要的作用靶點及通路。
由于中藥成分及其與人體相互作用的多樣性和復雜性,對中藥機制的闡明仍是一大難題,揭示中藥的應用規律及分子作用機制,是突破中醫藥現代化和國際化“瓶頸”的關鍵[8-9]。為此,通過應用數據挖掘、網絡藥理學這兩種新興的中醫藥大數據科學分析技術,擬為中藥治療痛風的應用規律及作用機制提供一定的理論支持和思路方法,同時為臨床中的中藥抗痛風治療提供借鑒與參考。
1 資料與方法
1.1 數據挖掘分析
1.1.1 數據來源
將“中藥”“痛風”“痛風性關節炎”“高尿酸血癥”“處方”設置為關鍵詞,檢索中國知網(CNKI) 、萬方數據知識服務平臺(Wangfang data) 、維普中文科技期刊數據庫(VIP)、Pubmed、中國生物醫學文獻數據庫、等數據庫,擬確定中醫藥治療痛風的相關文獻。
1.1.2 文獻納入標準
用于治療痛風的中藥處方均為納入標準,包括經典名方、病案分析、專家經驗、個案報道等,且處方具有完整藥物組成及劑量。
1.1.3 文獻排除標準
處方數據不完整、重復文獻、綜述、無藥效學驗證、不屬于確切治療痛風藥物等被排除。
1.1.4 文獻數據處理
考慮到錄入藥物因炮制、別名不同而造成對藥物分析的不準確,將中藥的名稱歸一化,即將所錄入中藥參考《中國藥典》[10]《中藥學》[11]進行規范化處理,如將薏米替換成薏苡仁,山萸肉替換成山茱萸,川牛膝、懷牛膝替換成牛膝等。
根據納入標準與排除標準,將篩選得到的處方藥物導入Excel表格中進行藥物頻次統計分析,應用SPSS Modeler18 軟件及SPSS Statistics 24 統計軟件進行關聯規則分析、復雜網絡分析及聚類分析。
1.1.5 治療痛風核心藥物篩選
根據數據挖掘分析結果,將高支持度、高置信度處方結合處方中出現的高頻次單味藥來確定治療痛風的核心藥物。
1.2 網絡藥理學分析
1.2.1 高頻次中藥活性化合物的確定
在TCMSP數據庫搜集數據挖掘確定的高頻次中藥的化學成分,根據口服生物利用度(oral bioavailability,OB)≥30%,類藥性(drug like property,DL)≥0.18篩選得到相應活性化合物。
1.2.2 高頻次中藥與疾病靶點的確定
收集TCMSP中高頻次中藥活性化合物靶點,并從 Genecards 數據庫獲取“痛風”的相關靶點,用Uniprot數據庫將這些靶點進行校正,刪除無效及重復靶點,然后將這些活性化合物的靶點匯總,并與“痛風”的靶點取交集。
1.2.3 高頻次中藥治療痛風核心靶點的確定
將高頻次中藥中藥活性化合物與“痛風”的交集靶點導入String數據庫,構建蛋白互作(protein interaction, PPI)網絡,物種限定為“homo sapiens”,最低相互作用閾值設為中等“medium confidence”(0.4),獲取 PPI 信息,將數據導入Cytoscape軟件中繪制 PPI 網絡,分析網絡拓撲參數,篩選出核心靶點蛋白。
1.2.4 高頻次中藥治療痛風的生物功能富集及作用通路分析
應用Metascape數據庫對高頻次中藥治療痛風靶點進行生物功能富集(biological function enrichment, GO)分析,分析包括生物過程(biological process,BP)、細胞組分(cellular component,CC)、分子功能(molecular function,MF)分析,并利用 Bioinformatic 平臺中高級氣泡圖進行可視化分析。信號通路分析涉及KEGG分析和共有靶點基因組表達分析。
1.2.5 “核心靶點-核心通路”藥理網絡的構建
將核心靶點及核心作用通路構建“核心靶點-核心通路”網絡,先將核心靶點與核心通路信息輸入 Excel 表格中,再將其導入 Cytoscape 3.7.2 軟件中進行可視化處理。研究方法流程圖如圖1所示。
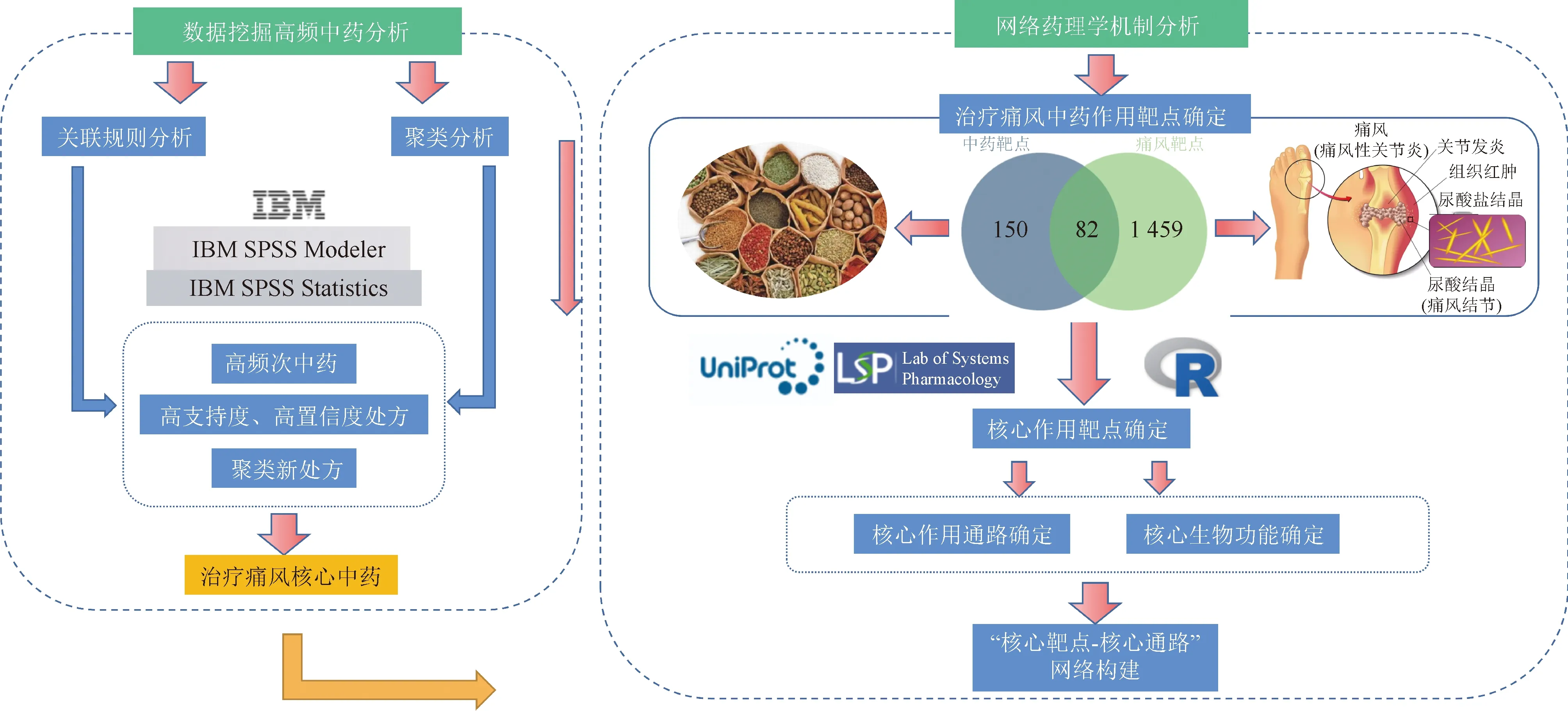
P表示統計量的顯著性圖1 研究方法流程圖Fig.1 Flow chart of research method
2 結果
2.1 高頻次治療痛風中藥分析
根據相關納入標準,共收集治療痛風處方302首,其中茯苓、黃柏、牛膝、薏苡仁、蒼術、萆薢頻次大于100,說明這些藥物為治療痛風的常用藥物,研究這些藥物治療痛風的價值較大,頻次前20的核心藥物及其屬性如表1所示。
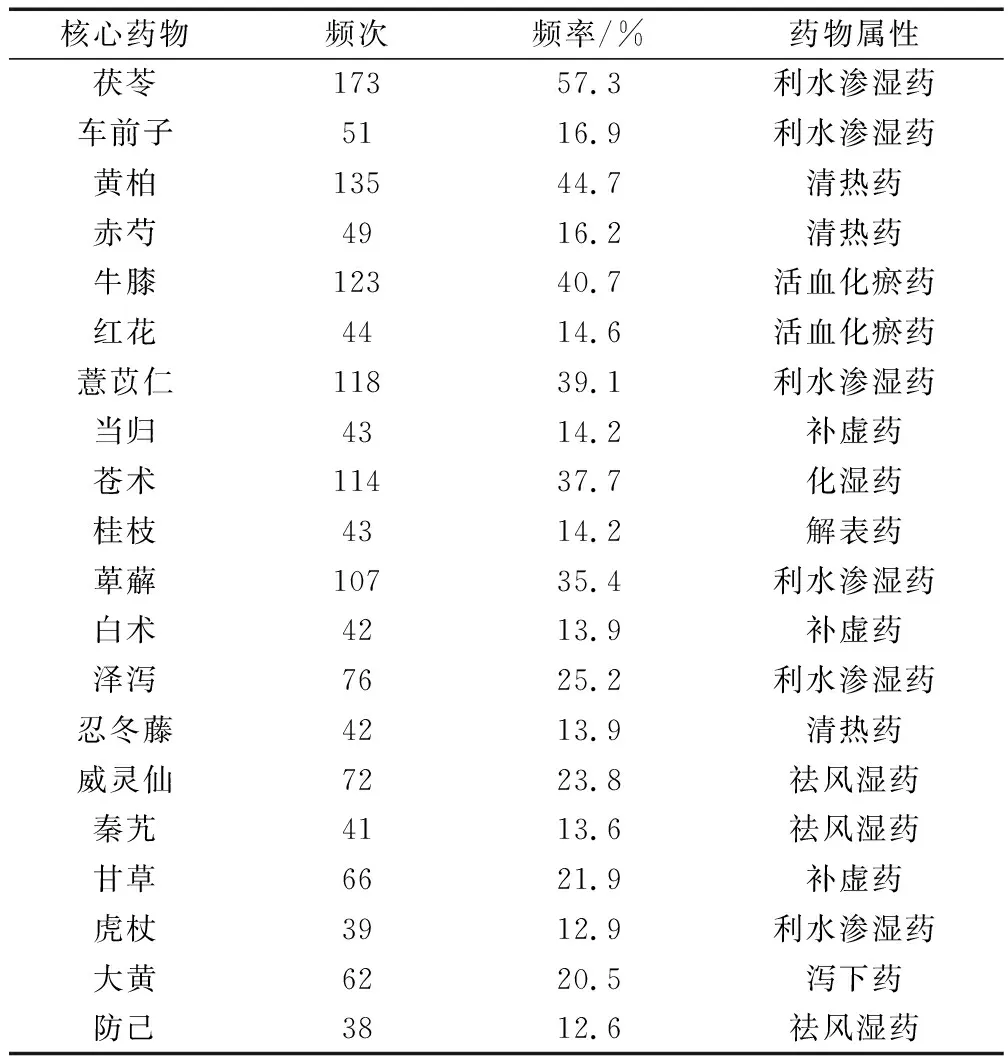
表1 治療痛風高頻次中藥Table 1 high frequency traditional Chinese medicine for the treatment of gout
2.2 高頻治療痛風中藥處方分析
為進一步確定治療痛風中藥的核心配伍關系,通過SPSS Modeler中的 Apriori 功能對高頻藥物進行關聯,三項關聯設置支持度10%,置信度80%,得到核心藥物組合7個,分析結果如表2所示。SPSS Modeler復雜網絡分析如圖2所示,其中藥物間的線條越粗,表明其關聯性越強。 SPSS Statistics聚類分析可得:黃柏、蒼術;牛膝、忍冬藤;赤芍、山慈菇、秦艽;澤瀉、地黃;茯苓、萆薢、威靈仙;紅花、桃仁、川芎;當歸、黃芪;甘草、白術、桂枝。具體聚類分析情況如圖3所示。
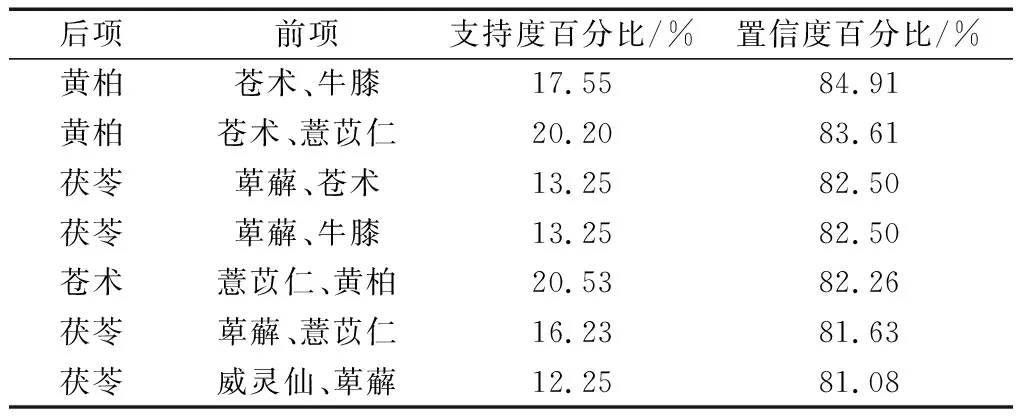
表2 治療痛風高頻次中藥關聯規則分析Table 2 Analysis of association rules of high-frequency traditional Chinese medicine in the treatment of gout
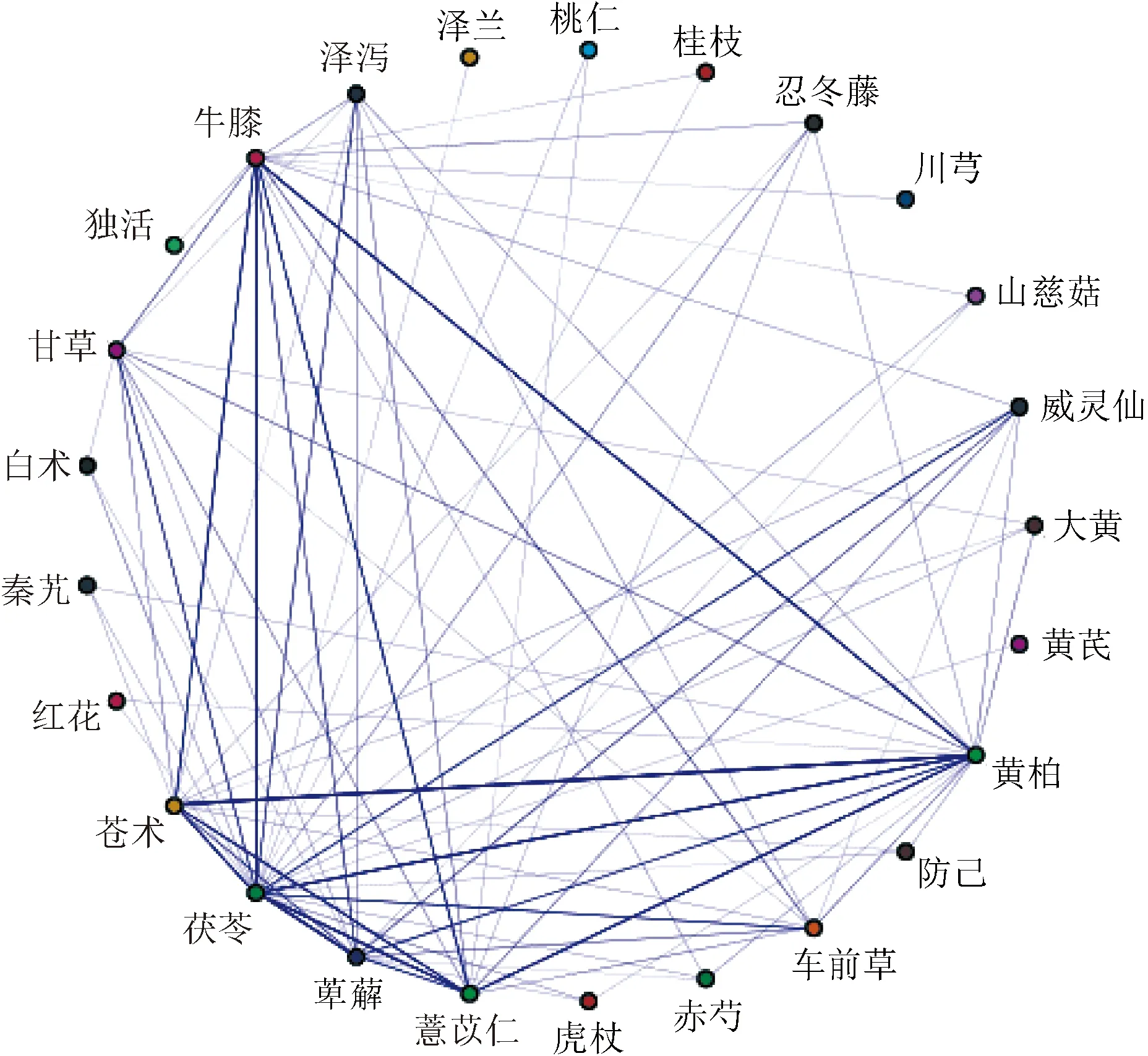
圖2 治療痛風高頻次中藥關聯規則網狀圖Fig.2 Network diagram of association rules of high-frequency and low-frequency traditional Chinese medicine for the treatment of gout
2.3 治療痛風核心中藥篩選
通過綜合以上的高頻次治療痛風中藥及中藥處方分析,擬采用黃柏-蒼術-牛膝、黃柏-蒼術-薏苡仁、茯苓-萆薢-蒼術、茯苓-萆薢-牛膝、蒼術-薏苡仁-黃柏、茯苓-萆薢-薏苡仁、茯苓-威靈仙-萆薢這7大篩選出的高支持度和置信度關聯處方中涉及的相關中藥作為治療痛風核心的核心中藥,這也符合聚類分析的結果,共涉及茯苓、黃柏、牛膝、薏苡仁、蒼術、萆薢、威靈仙,結合高頻次治療痛風中藥表分析發現,根據處方篩選出的這7大中藥處于高頻次治療痛風中藥中的前8位,而澤瀉也處于前八位中但未歸于處方組合中,因此補充治療痛風常用中藥澤瀉。
2.4 治療痛風核心中藥活性化合物的確定
在TCMSP數據庫搜集數據挖掘確定的治療痛風核心中藥的化學成分,根據OB≥30%,DL≥0.18的篩選條件,確定了共計109個活性成分,其中茯苓15個,黃柏37個,牛膝20個,薏苡仁9個,蒼術9個,萆薢2個,澤瀉10個,威靈仙7個,刪除重復成分后,共計95個活性成分。
2.5 治療痛風核心中藥與痛風疾病靶點的確定
將2.4節中95個活性成分導入TCMSP數據庫,并經Uniprot數據庫校正及刪除空白無效靶點后,共確定1 158個作用靶點,去重后共計得231個靶點。從Genecards數據庫篩選得到有關痛風的靶點1 541個。將中藥靶點與疾病靶點取交集后,得到交集靶點82個(圖4),即這82個靶點就是這些中藥發揮抗痛風功用的關鍵作用靶點。
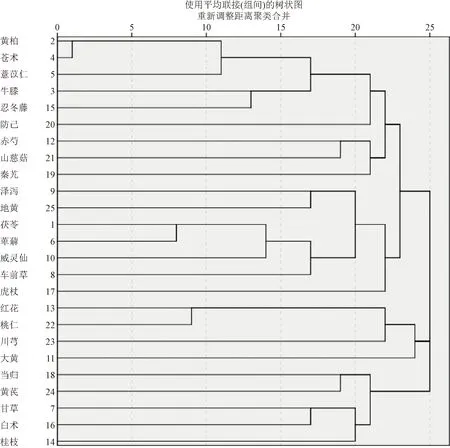
圖3 治療痛風高頻次中藥聚類分析圖Fig.3 Cluster analysis diagram of high-frequency and low-frequency traditional Chinese medicine for the treatment of gout
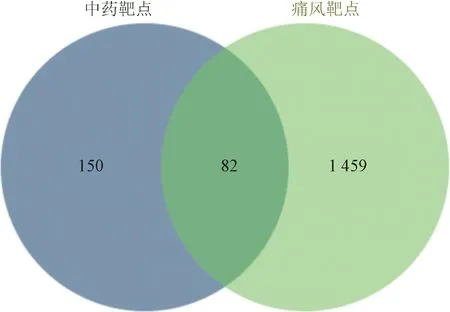
圖4 中藥與疾病靶點交集圖Fig.4 intersection of traditional Chinese medicine and disease targets
2.6 治療痛風核心中藥關鍵靶點的確定
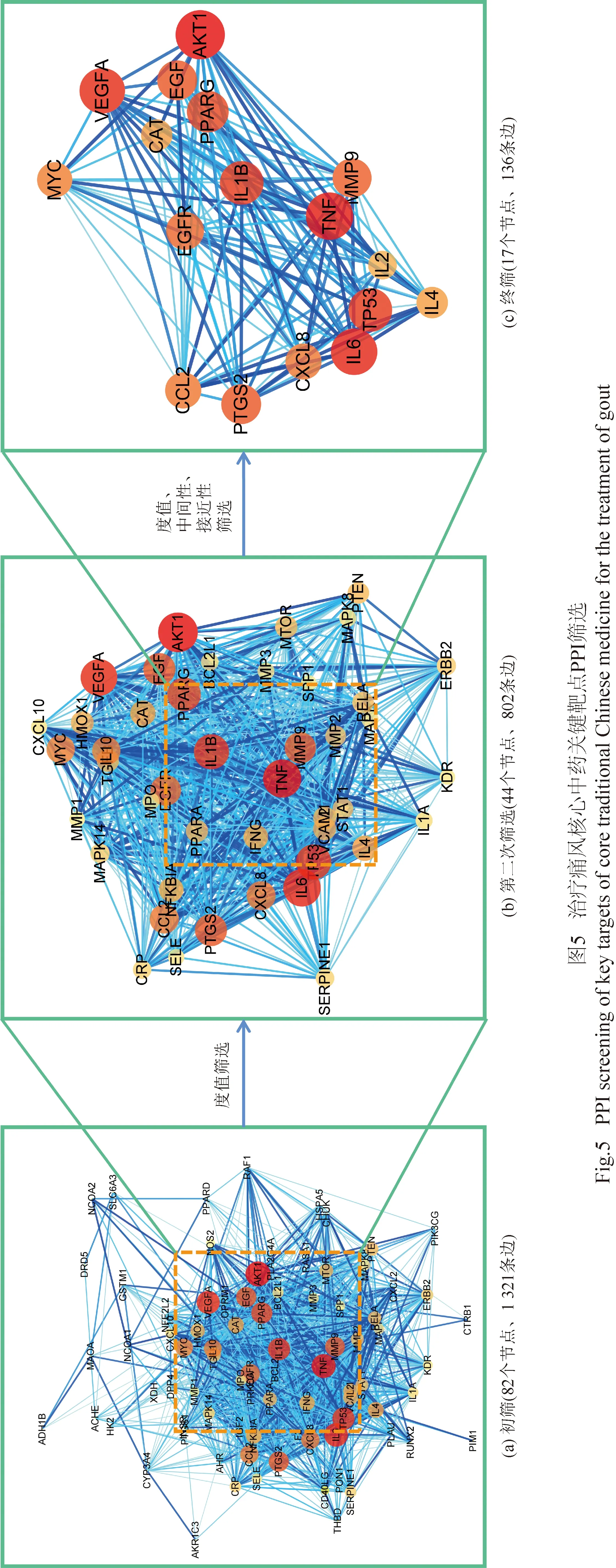
初步構建的PPI網絡共涉及82個節點和 1 321 條邊。具體靶點及拓撲參數信息如表3所示,為了找出這些核心中藥抗痛風的關鍵靶點,首先按照中位數篩選得到44個節點和802條邊的PPI網絡,再按照degree大于45,中間性(betweenness)大于0.007,接近度(closeness)大于0.684的條件篩選得到含17個節點,136條邊的核心靶點PPI網絡,篩選流程如圖5所示,以節點度值為評價參數,節點度值越大其靶點越大,連接線條顏色越深,也說明其在 PPI網絡中越重要,可能在發揮生物學功能中起著重要的作用。
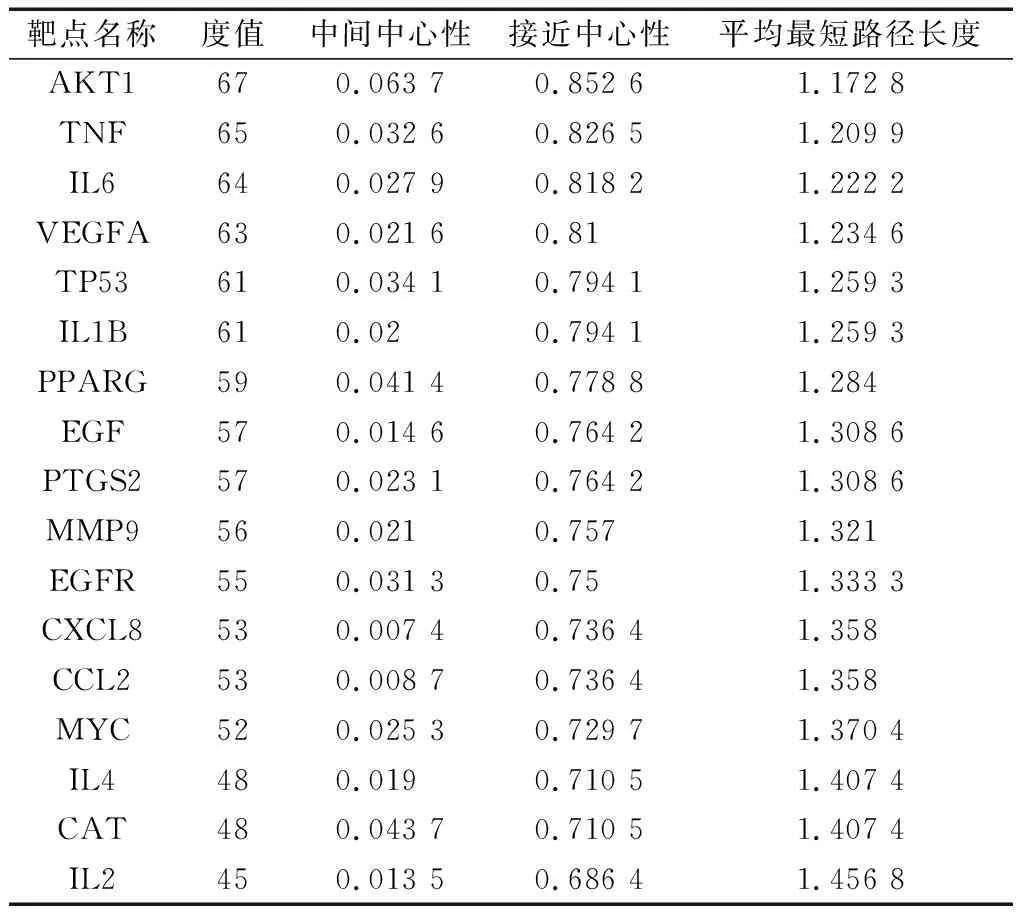
表3 PPI篩選核心拓撲參數Table 3 PPI screening core topology parameters
2.7 治療痛風核心中藥的GO及作用通路分析
GO富集分析結果如圖6所示,生物學過程(BP)富集分析提示,細胞粘附調節、血管發育、傷害反應、對脂多糖的反應、對營養水平的反應、細胞分化的負調控在中藥治療痛風中比較重要;細胞組分(CC)富集分析表明,靶點的產物可能主要在膜筏、膜側、囊腔、細胞外基質、細胞質核周區等部位;分子功能(MF)富集分析表明,靶點可能是通過受體-配體活性、轉錄因子結合、蛋白質同源二聚化活性、蛋白激酶活性等發揮作用。
作用通路分析結果如圖7所示,分析顯示其作用通路包括環境信息處理、細胞過程、組織系統、人類疾病四大類,也說明中藥治療痛風作用靶點主要富集在癌癥、糖尿病并發癥中的AGE-RAGE信號、IL-17信號、MAPK信號、細胞因子-細胞因子受體相互作用、癌癥中的轉錄失調等通路,提示這些經典通路可能在中藥治療痛風作用中發揮著重要作用。
為進一步分析其基因組對通路的調控情況,中藥治療痛風全基因組表達分析如圖8所示,該分析具體涉及的調節過程包括白細胞介素- 4、白細胞介素-10、白細胞介素-13、免疫系統中的細胞因子信號轉導、基質金屬蛋白酶的激活、基因轉錄途徑等,這表明中藥抗痛風作用的發揮與這些生物活性行為密切相關。
2.8 治療痛風核心中藥“核心靶點-核心通路”網絡構建
為進一步直觀分析治療痛風核心中藥的作用靶點和通路之間的關系,將PPI分析確定的17個核心靶點及通路分析確定的20條核心通路進行“核心靶點-核心通路”網絡的構建,去除無連接效應的2條核心通路后,繪制結果如圖9所示,節點字體、形狀越大,顏色越深,表明該節點與其他節點作用關系越密切,在中藥治療痛風中發揮的作用可能越重要。
3 討論
《景岳全書》中記載痛風是由于“外濕侵襲”及“飲食不節”引起的內生濕熱所致,風、寒、濕、熱、瘀為痛風急性發作的病因病機,痛風按照證候分類可分為濕熱蘊結型、瘀熱阻滯型、痰濁阻滯型、肝腎陰虛型[12],而中醫藥能夠更好地把握痛風的病因病機,從而分證論治,在治療痛風、降尿酸、改善關節功能方面更具優勢[13]。首先從文獻中收集到治療痛風的方劑處方302首,分析發現其中的高頻藥物包括利水滲濕藥(茯苓、薏苡仁、萆薢、澤瀉、車前子、虎杖),清熱藥(黃柏、赤芍、忍冬藤),活血化瘀藥(牛膝、紅花),化濕藥(蒼術),祛風濕藥(威靈仙、秦艽、防己),補虛藥(甘草、當歸、白術),瀉下藥(大黃),解表藥(桂枝)。根據以上治療痛風藥物的屬性佐證了痛風的風、寒、濕、熱、瘀的病機特點,且根據分析可得出中藥治療痛風應以祛濕利水、清熱活血為主,瀉下、解表、補虛為輔。
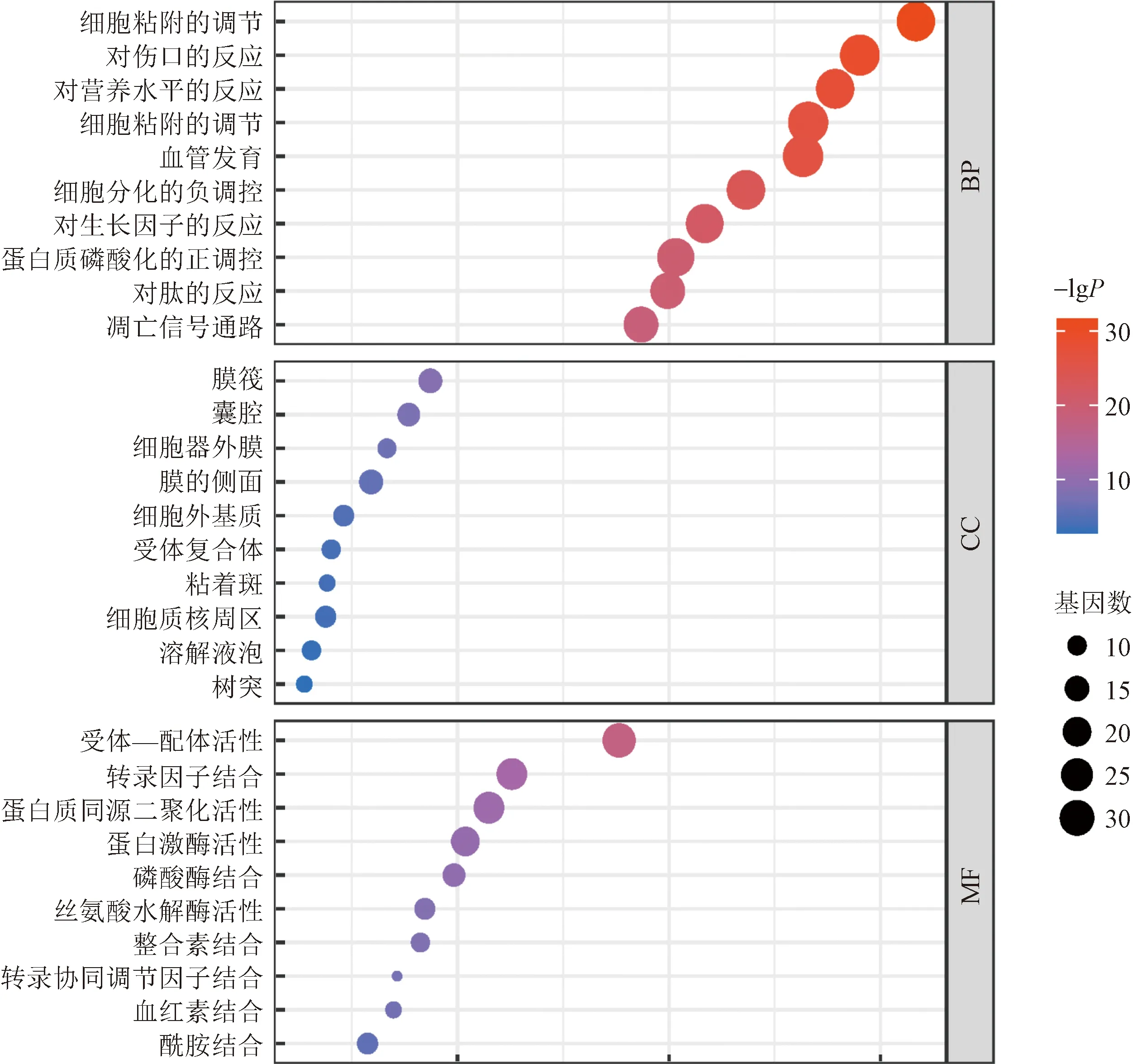
P表示統計量的顯著性圖6 GO分析氣泡圖Fig.6 Go analysis bubble diagram
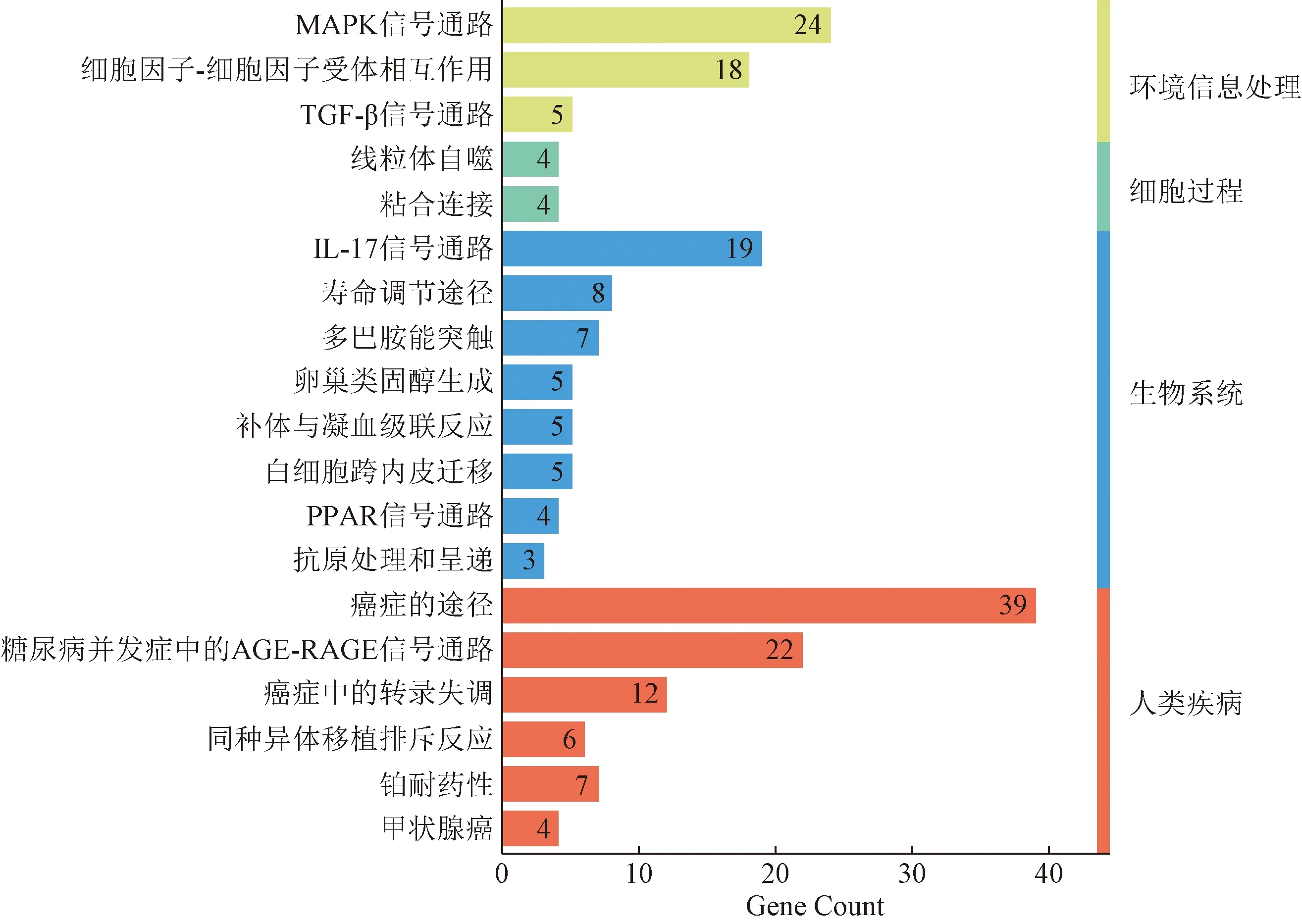
圖7 KEGG通路功能分析圖Fig.7 KEGG channel function analysis diagram
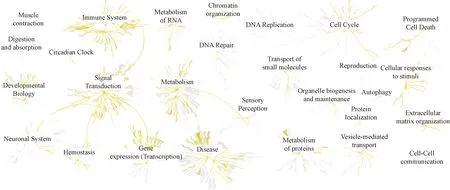
Muscle contraction為肌肉收縮;Digestion and absorption為消化和吸收;Developmental Biology為發育生物學;Neuronal System為神經元系統;Immune System為免疫系統;Circadian Clock為晝夜鐘;Signal Transduction為信號轉導;Hemostasis為止血;Metabolism of RNA為RNA代謝;Metabolism為新陳代謝;Disease為病;Chromatin organization為染色質組織;DNA Repair為DNA修復;DNA Replication為DNA復制;Transport of small molecules為小分子的運輸;Sensory Perception為感官知覺;Cell Cycle為細胞周期;Programmed Cell Death為程序性細胞死亡;Reproduction為生殖;Cellular responses to stimuli為細胞對刺激的反應;Organelle biogenesis and maintenance為器官生物發生和維持;Autophagy為自噬;Protein localization為蛋白質定位;Extracellular matrix organization為細胞外基質組織;Metabolism of proteins為蛋白質代謝;Vesicle-mediated transport為囊泡介導的運輸;Cell-Cell communication為Cell-Cell通信;黃色部分表示在該功能 模塊呈現過表達狀態;灰色部分表示表達狀態不顯著圖8 中藥治療痛風全基因組表達分析圖Fig.8 Whole genome expression analysis of gout treated with traditional Chinese medicine
根據數據挖掘中的關聯規則分析,篩選出了高頻次中藥及藥對,根據得到的中藥及方劑配伍結果,確定了治療痛風的主要中藥組合為黃柏、蒼術;牛膝、忍冬藤;赤芍、山慈菇、秦艽;澤瀉、地黃;茯苓、萆薢、威靈仙;紅花、桃仁、川芎;當歸、黃芪;甘草、白術、桂枝,且篩選得到了茯苓、黃柏、牛膝、薏苡仁、蒼術、萆薢、威靈仙、澤瀉為治療痛風的核心藥物,因此以這些中藥為研究主體,分析了其治療痛風的作用機制。研究表明,黃嘌呤氧化酶(XOD)是尿酸代謝的重要調控酶,能夠催化體內尿酸的形成,從而導致尿酸濃度升高,引起痛風的發作,XOD也能通過級聯反應誘導大量活性氧的生成,而這些活性氧與炎癥、癌癥、細胞損傷等有關[14]。此外,環氧化酶(COX)、基質金屬蛋白酶(MMPs)、炎癥因子也影響著痛風的發展進程。研究證實,茯苓提取物能促進尿酸排泄,有效降低血尿酸水平,且對XOD有顯著的抑制作用,能夠通過調節尿酸轉運蛋白來促進尿酸的排出[15]。茯苓多糖抑制急、慢性炎癥效果顯著,能夠降低TNF-α(巨噬細胞產生的壞死因子)、IL-1β(IL-1為白細胞介素-1,其存在形式有IL-α、IL-β)、IL-6水平,抑制JAK2/STAT3通路[16-17]。黃柏提取物也能顯著降低高尿酸血癥小鼠血清尿酸水平,并降低肝臟XOD活性[18-19],其也可抑制炎癥因子TNF-2、IL-2表達[20]。牛膝擅于強筋骨,能夠“引藥下行”,其含有的牛膝總皂苷能夠降低尿酸水平,從而發揮抗痛風作用[21-22]。薏苡仁具有舒筋除痹之功,《神農本草經》中記載其可除“風濕痹”,治“筋急拘攣”。薏苡仁能夠通過降低血管通透性發揮抗炎作用,其也能夠調控IKK/NF-κB信號通路,降低多種炎癥因子的分泌水平[23-24]。此外,薏苡仁也可使COX含量和抗氧化酶活性顯著降低,說明其可通過抑制促炎性因子表達、抗氧化來發揮治療痛風性關節炎的作用[25]。有研究證實以蒼術為君藥的蒼術白虎湯可以降低高尿酸血癥小鼠的血尿酸水平,這可能與其降低 XOD 活性有關[26],蒼術也能顯著抑制IL-6、IL-8、TNF-α、COX代謝產物前列腺素E2的過度表達[27-28]。萆薢能顯著改善痛風性關節炎的疼痛和腫脹情況,萆薢總皂苷也可有效抑制尿酸鹽轉運蛋白的表達,從而減少尿酸的重吸收,促進尿酸排泄[29-30],這可能與其抑制XOD活性,下調大鼠腎臟尿酸轉運體1(URAT1)表達,上調有機陰離子轉運體1 (OAT1) 、有機陰離子轉運體3 (OAT3) 的表達有關[31-32]。威靈仙祛濕止痛效佳,為治療痹癥的要藥,其能夠顯著降低血清尿酸、減少尿酸鹽結晶沉積和炎性細胞浸潤[33],這可能與其抑制COX-2活性,抑制TNF-α炎癥因子有關[34]。澤瀉利水滲濕作用較強,能夠抑制COX-2、1L-1β 和誘導型一氧化氮合酶(iNOS)活性和NF-κB表達,上調Net2炎癥基因表達,從而減少炎癥因子的產生來發揮抗炎作用[35-38],這也是其治療痛風性關節炎的依據所在。因此,這些中藥用作治療痛風都有著一定的理論基礎。
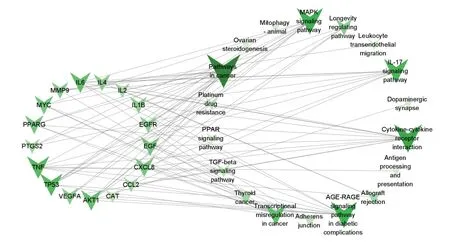
Pathways in cancer為癌癥的途徑;AGE-RAGE signaling pathway in diabetic complications為糖尿病并發癥中的AGE-RAGE信號通路;IL-17 signaling pathway為IL-17信號通路;MAPK signaling pathway為MAPK信號通路;Cytokine-cytokine receptor interaction為細胞因子-細胞因子受體相互作用;Transcriptional misregulation in cancer為癌癥中的轉錄失調;Longevity regulating pathway為長壽調節途徑;Allograft rejection為同種異體移植排斥反應;Platinum drug resistance為鉑耐藥性;Dopaminergic synapse為多巴胺能突觸;Ovarian steroidogenesis為卵巢類固醇生成;drug metabolism為藥物代謝;Thyroid cancer為甲狀腺癌;TGF-beta signaling pathway為TGF-β信號通路;Complement and coagulation cascades為補體和凝血級聯;Leukocyte transendothelial migration為白細胞經內皮細胞遷移;Mitophagy-animal為線粒體吞噬-動物;PPAR signaling pathway為PPAR信號通路;Adherens junction為粘合連接;Antigen processing and presentation為抗原處理和呈遞圖9 中藥治療痛風“核心靶點-核心通路”網絡圖Fig.9 Network diagram of “core target core pathway” of traditional Chinese medicine in the treatment of gout
PPI分析結果顯示,這些抗痛風核心中藥的關鍵作用靶點為AKT1、TNF、IL6、VEGFA、TP53、IL1B、PPARG、EGF、PTGS2(COX-2)、MMP9等,痛風多以關節炎為表現形式,研究證明這些作用靶點能夠有效調控炎癥的表達,此外慢性炎癥也能夠誘導癌癥的發生,這些靶點也能夠影響癌癥通路的表達。AKT1主要參與細胞進程,能夠調控細胞生長和存活,在腫瘤細胞增殖、凋亡、遷移等多種生物過程中發揮作用,其能夠通過自身磷酸化可以調節多種包括VEGF,MAPK,NF-κB在內的下游通路從而調控炎癥作用,如其能夠激活炎癥因子NF-κB的核轉位過程等[39-40]。TNF可作為免疫系統的關鍵靶點,其自身也是一種重要的炎性因子,也可促進IL-6,IL-10等細胞因子的產生,從而進一步加重炎癥反應[41],其也可調控NF-κB途徑,促進IL-6、IL-1β、PTGS2等下游炎癥因子的分泌[42]。IL6為經典的炎癥基因,能夠直接激活血管內皮細胞和炎癥細胞,下調IL-6的表達能夠有效抑制炎癥反應[43],現代研究多通過測量血清中的IL-6表達水平來評估機體炎癥及組織受損的程度大小[44],且IL-6與痛風石的形成密切相關,在痛風性關節炎急性發作期呈現過表達狀態,能引起炎癥急性期反應[45-46],IL-1β對痛風的發病過程有著一定的調控作用,能夠增強巨噬細胞與粒細胞的活性,促進 IL-6、TNF-α等炎性因子的分泌,使軟骨細胞降解加速,從而引發關節功能受損[47-48]。VEGFA是刺激血管生成的主要因子,其能夠誘導內皮細胞增殖,抑制細胞凋亡,其也能夠通過磷酸化過程激活PI3K通路,在多數腫瘤中表達上調,其也與炎癥的表達有關,能夠增加血管通透性,刺激炎癥的形成和發展[49-50]。TP53為強效抑癌基因,可參與細胞周期調控,能夠通過控制細胞周期所需的基因來調控細胞分裂,也有研究證實了TP53基因突變會促使惡性腫瘤的發生[51]。根據這些治療痛風核心中藥的關鍵作用靶點可知,其抗痛風作用的發揮依賴于其對多種炎癥通路的調節,這與這些中藥單味藥抗痛風的作用機制相印證。分析結果也表明,COX、MMP、炎癥因子、AKT通路等也是這些抗痛風中藥發揮作用的核心影響因素。由此可知痛風可通過多種炎癥的“級聯”反應導致關節炎的發作,而這些核心中藥能夠有效抑制炎癥的這一“級聯”效應。
根據GO和作用通路的分析結果可知,治療痛風中藥的這些靶點作用的發揮主要影響細胞粘附調節、血管發育、損傷反應等生物學過程,通過作用在膜筏、膜側、囊腔等部位發揮受體-配體活性、轉錄因子結合、蛋白質同源二聚化活性、蛋白激酶活性等分子功能。這些作用靶點主要影響癌癥、糖尿病并發癥中的AGE-RAGE信號、IL-17信號、MAPK信號、細胞因子-細胞因子受體相互作用、癌癥中的轉錄失調等通路,這些通路涉及到環境信息處理、細胞過程、組織系統和人類疾病方面。全基因組表達分析顯示,中藥抗痛風作用的發揮與其調節多種炎癥白細胞介素密切相關,此外,其還對免疫系統中的細胞因子信號轉導、基質金屬蛋白酶的激活、基因轉錄途徑等過程產生影響。
網絡藥理學以系統生物學和生物網絡平衡為基礎,通過構建成分-靶點-通路之間的網絡關系來探討藥物治療疾病的作用機制,更符合中醫藥的整體觀[52-53]。中醫藥數據挖掘是依托于現代數據軟件,主要用于系統分析傳統中醫藥理論及臨床處方應用規律的技術。這些現代新興技術的發展為中藥用藥規律及作用機制的合理解釋提供了科學的方法,這也契合了中藥“多靶點-多通路”調節的特點。綜上分析,痛風多以關節炎急性發作為表征,中藥治療痛風的作用機制主要依賴于對多種酶(XOD、COX、MMPs)及多種炎癥因子、炎癥通路的調控,其作用的這些蛋白與通路也多與免疫調節及癌癥發展有關,而免疫功能與炎癥的發展進程悉悉相關,慢性炎癥也是多種癌癥產生的誘因,因此這些中藥也可能通過調節免疫功能及調控癌癥相關通路來延緩痛風進程及痛風病變。通過梳理分析中藥治療痛風的相關機制,以期為痛風的深入研究以及痛風治療的合理用藥提供一定的借鑒意義。
4 結論
(1)應用現代數據挖掘和網絡藥理學技術,在大數據作為輔助的前提下系統分析了中藥治療痛風的用藥規律和作用機制,確定了治療痛風的高頻、高置信度中藥,并根據聚類結果確定了新處方,在此基礎上,應用系統藥理學方法初步評價了其作用機制。
(2)從醫藥及生物信息學理論層次分析了中藥抗痛風作用的規律及機制,今后應輔以多組學技術、分子生物技術等多個交叉學科進行體內外實驗的驗證,這對于藥效篩選、新藥研發等意義重大,能夠更好得促進中醫藥的傳承與發展,加速其現代化進程。

