液相色譜-柱后衍生-原子熒光聯用測定 食品中硒形態
◎ 謝佩文
(廣東亨盛維嘉食品工業有限公司,廣東 潮州 515726)
硒作為動物與人類必需微量元素,是合成硒蛋白,包含硫氧蛋白還原酶、谷胱甘肽過氧化酶、碘甲狀腺素脫碘酶的關鍵組成部分,對于甲狀腺激素代謝、繁殖、免疫力與抗氧化具有良好生物學功能。人體如果缺少硒元素,會降低人體免疫力,增加患癌癥與死亡風險。根據營養學會推薦,成人攝硒量每天為50~250 μg,不能超過400 μg,攝入800 μg會出現人體中毒癥狀。硒元素多用于食品功能成分,特別是人們生活水平得到提高后,對硒產品的需求量也逐漸增加,但硒元素過量攝入會對人體造成危害,健康硒食品發展中,也需明確硒是把“雙刃劍”[1]。本文采取液相色譜-柱后衍生-原子熒光聯用方式,分析食品硒形態,推動硒產品實現規范發展。
1 材料與方法
1.1 材料與設備
1.1.1 儀器與設備
液相色譜-原子熒光聯用儀AS-53(廣西路博環保科技有限公司);純水機Direct-Pure(北京中程瑞源科技有限公司);分析天平LE204E/02(上海贊維衡器有限公司);超聲水浴(濟南歐萊博電子商務有限公司);抽濾設備(青島精誠儀器儀表有限公司);超聲波清洗器KH3200B(青島明博環保科技有限公司)。
1.1.2 材料與試劑
硒形態標準品:甲基硒代半胱氨酸(96%純度);硒代胱氨酸(98%純度);亞硒酸鈉(99%純度);硒代蛋氨酸(99%純度),用超純水配制上述標準品為1 mg·L-1濃度溶液,放置于4 ℃下進行保存,配制溶液及處理樣品均使用超純水;硼氫化鈉、碘化鉀、氫氧化鈉、檸檬酸以及磷酸氫二胺,均為分析純(上海宏瑞化工有限公司)。
1.2 方法
1.2.1 溶液配制
(1)碘化鉀堿溶液。氫氧化鈉稱取2.90 g倒入燒杯,以少量水溶解添加1 g碘化鉀,加水超聲溶解,稀釋定容至1000 mL。
(2)硼氫化鈉還原劑。鹽酸稱取100 mL,以水稀釋定容至1000 mL。
(3)超純水溶液。稱取超純水1 L后,超聲脫氣待用,根據實際以磷酸、氨水進行調節pH=8.0。
1.2.2 儀器色譜條件
(1)色譜條件。使用Hamilton 10 μm陰離子色譜柱,利用磷酸氫二胺、硼氫化鈉流動相分離硒形態。
(2)儀器條件。80 mA燈電流;270 V負高壓;500 L·min-1載氣流量;7 mm原子化器高度;1000 L·min-1屏蔽氣流量;2根15 W紫外燈;60 r·min-1泵速A; 70 r·min-1泵速B;300 ℃原子化器溫度。
1.2.3 樣品預處理
稱取1.00 g樣品放置在25 mL錐形瓶內,添加鏈霉蛋白酶E 10 mg溶于水,放入離心管內均勻混合,設置溫度37 ℃完成超聲提取,以60 r·min-1離心 30 min,取上清液通過有機膜過濾[2]。
1.2.4 方法條件
進樣量滿杯100 μL,開啟紫外小結,流動相A為超純水;流動相B為磷酸氫二胺溶液170 mol·L-1、 160 mol·L-1、150 mol·L-1,利用磷酸調節pH=6.3;流動相C為檸檬酸。衍生劑為300 mL·h-1碘化鉀堿溶液;500 mL·h-1鹽酸載流溶液;300 mL·h-1空氣;300 mL·h-1硼氫化鈉還原劑[3]。
2 結果與分析
2.1 優化儀器條件
2.1.1 選擇流動相
流動相選擇對分離目標化合物十分重要,硒形態分析流動相常見有醋酸鹽、檸檬酸、Tris緩沖液及磷酸鹽等,添加甲醇有花粉粒效果,綜合分析硒化合物性質,采取陰離子色譜交換柱,探究檸檬酸與磷酸氫二胺為流動相的分離硒形態,發現以檸檬酸為流動相,降低了硒代蛋氨酸靈敏度,重復性差,甚至實驗不會出峰,使用磷酸氫二胺溶液可避免上述缺陷,采取磷酸氫二胺成為流動相,硒形態分離中20 min即可達到基線。
2.1.2 選擇流動相濃度
流動相濃度分析中,分析磷酸氫二胺170 mmol·L-1、160 mmol·L-1、150 mmol·L-1,pH=6.3的溶液分離硒形態效果,發現溶液濃度是150 mmol·L-1時,靈敏度較低,出峰時間是27 min,時間較長;濃度是170 mmol·L-1時,顯示亞硒酸跟與甲基硒代胱氨酸峰值無法達到分離基線;濃度160 mmol·L-1時,分離硒形態效果更好,以此作為流動相濃度。
2.1.3 流動相pH值
考察流動相不同pH值對硒形態分離影響。流動相pH≤6.0時,未能檢測亞硒酸鈉響應值,逐步增加流動相pH值,pH=6.3可實現硒形態分離,縮短時間至24 min;將流動相pH值繼續提高至pH=6.8時,分離硒代蛋氨酸、甲基硒代半胱氨酸程度降低。所以,選擇最佳流動相pH=6.3,且流動相pH=6.3時,4種硒形態均可分離,且甲基硒代半胱氨酸、硒代胱氨酸、亞硒酸鈉以及硒代蛋氨酸的保留時間分別是 15.771 min、14.434 min、10.317 min以及5.381 min。
2.2 線性關系及檢出限
稱取硒代半胱氨酸0.0202 g,硒代胱氨酸0.0242 g、 亞硒酸鈉0.0234 g以及硒代蛋氨酸0.0226 g定容為100 mL,配制10~200 μg·L-1系列標準溶液,根據 1.2方法操作測定,以硒化合物濃度為縱坐標,橫坐標為對應峰面積繪制標準曲線,獲得方法線性關系及檢出限,結果如表1所示。
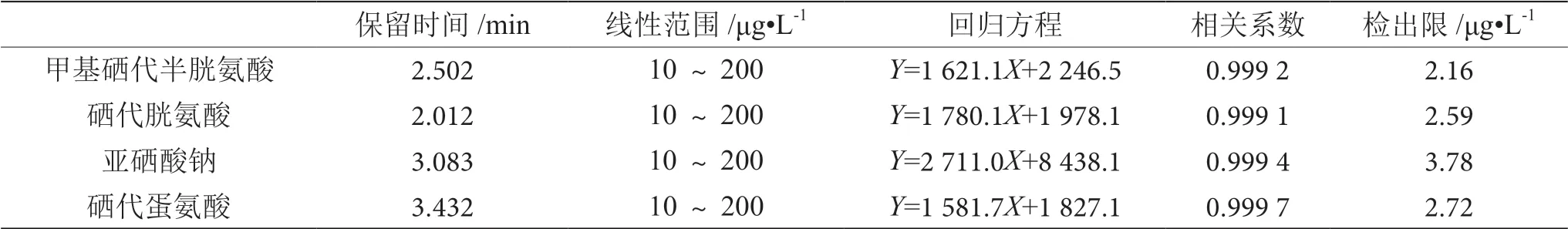
表1 4種硒形態線性關系與檢出限化合物表
結果表明方法在硒化合物濃度為10~200 μg·L-1時線性關系良好,相關系數均大于0.99,檢出限處于2.16~3.78 μg?L-1。4種 硒 化 合 物 色 譜 圖 如 圖1 所示。
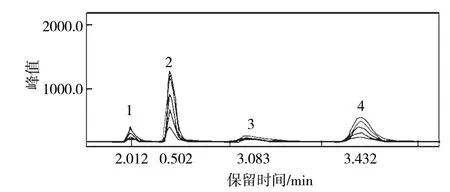
圖1 硒形態色譜圖
2.3 精密度
精密度測試中,以配制的標準濃度試劑進行平行試驗,可獲得精密度。由試驗結果可知,甲基硒代半胱氨酸的精密度是3.6%,硒代胱氨酸精密度是2.8%,亞硒酸鈉精密度是3.2%,硒代蛋氨酸精密度是4.3%,均低于5%,滿足試驗需求。
2.4 加標回收率
選擇富硒大米不同硒含量作為試驗樣品,測定總硒含量是1.25 mg·kg-1,測試樣品不同形態下硒本底值,完成加標回收試驗,對3個濃度加標回收,不同濃度進行6個平行試驗,結果表明硒形態加標回收率為86.3%~104.4%,相對標準偏差低于5.0%, 見表2。
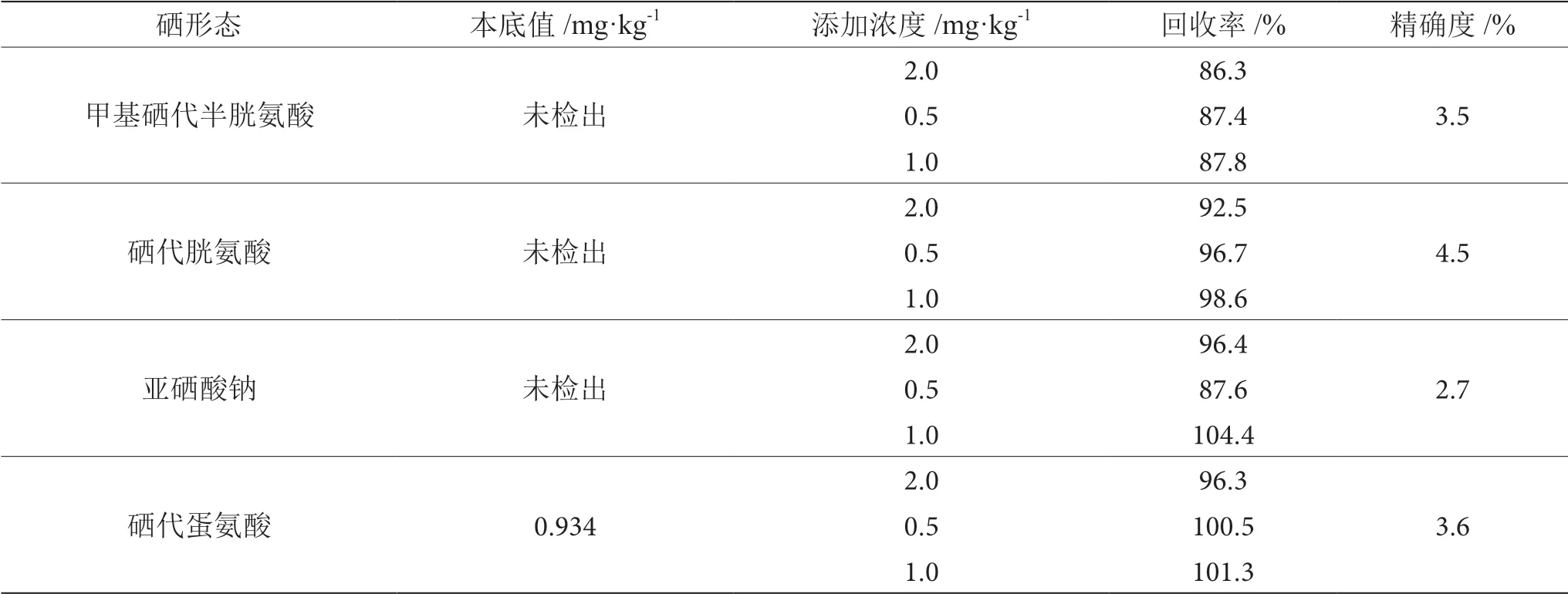
表2 加標回收率表(n=6)
2.5 樣品測定
本實驗中采取液相色譜-柱后衍生-原子熒光聯用方式測定富硒大米的有機硒形態,根據結果可知,富硒大米內僅檢出有硒代蛋氨酸。
3 結論
硒作為典型雙功能元素,是人體必需微量元素的同時,也存在毒性。硒具有抗氧化、抗癌、增強人體免疫力等作用,可對維生素利用與吸收進行調節,且參與調節合成蛋白質。人體如果長期缺硒會引發大骨節病、心腦血管疾病、糖尿病與克山病等[4]。而攝入硒過量超出安全閾值,也會損害人體,引發慢性或急性硒中毒,因此合理、科學攝入硒元素具有重要的作用。硒化合物形態多樣,且硒不同形態生物效應、功能、毒性存在差異,不能僅測定硒總含量,還需分析食品硒形態[5]。食品不同,性質也不同,硒蛋白形態與種類較為復雜,為迅速測定硒形態,本文結合硒的化學和物理性質,通過使用液相色譜-柱后衍生-原子熒光聯用的方式測定硒形態,對食品硒形態進行定量定性分析,精確度較高,可滿足測定要求。

