初診2型糖尿病合并肥胖患者血漿Alarin水平與糖脂代謝及慢性炎癥的相關性分析
楊九芳,汪曉紅,游紅杏,鄒慧蘭,盧曰文,王雪琳
(武漢科技大學附屬武漢市武昌醫院,1.全科醫學科,2.內分泌科,湖北 武漢,430063)
2型糖尿病(T2DM)是一種以高血糖為特征的代謝紊亂性疾病,是多種遺傳因素和環境因素相互作用的結果,主要表現為葡萄糖耐受不良[1]。2型糖尿病主要發病機制是胰島素抵抗和胰島細胞損傷,而胰島素抵抗是T2DM發生和發展的關鍵原因[2]。Alarin是一種由25個氨基酸組成的神經肽,是從人類神經母細胞中分離出來的甘丙氨酸肽家族的最新成員[3],可增強食欲,降低胰島素敏感性和骨骼肌葡萄糖的攝取,被認為是與胰島素抵抗和能量穩態相關的細胞因子[4]。本研究探討初診2型糖尿病合并肥胖患者血漿Alarin水平,并分析其與糖脂代謝及慢性炎癥的相關性,旨在為進一步了解糖尿病發生和發展的作用機制提供參考依據。
1 資料與方法
1.1 一般資料
選取2019年1—12月楊園社區衛生服務中心自愿接受管理的300 例糖尿病患者為研究對象。T2DM的診斷參照中華醫學會糖尿病學分會制定的《中國2型糖尿病防治指南(2013年版)》[5],所有患者均符合T2DM的相關診斷標準。① 患者有糖尿病癥狀,隨機血糖≥11.1 mmol/L;② 空腹血糖≥7.0 mmol/L者;③ 口服葡萄糖耐量試驗2 h血糖≥11.1 mmol/L者。所測血糖均指靜脈血漿葡萄糖,符合上述任意一項標準,經再次驗證后T2DM診斷才能成立。納入標準:① 患者均初次診斷為2型糖尿病;② T2DM臨床癥狀<1年者;③ 未進行任何相關藥物治療者;④ 社區65 歲以上老年人免費體檢人員、糖尿病慢病管理體檢人員和“甜蜜人生”糖尿病社區沙龍活動符合要求的患者。排除標準:① 1型糖尿病、妊娠糖尿病及其他類型糖尿病者;② 合并心、肝、腎等嚴重系統性疾病者;③ 合并分泌系統疾病、惡性腫瘤者;④ 合并精神病、感染性、自身免疫性疾病者;⑤ 合并甲狀腺功能低下者;⑥ 因其他原因導致肥胖者。將300例患者根據肥胖情況分為T2DM肥胖組(n=128例)和T2DM非肥胖組(n=172例)。肥胖診斷標準:根據中國成年人肥胖癥的診斷標準,以體質量指數18.5~<24 kg/m2者為非肥胖,以體質量指數≥28 kg/m2者為肥胖。另選同期體檢的100例健康人員作為對照組,正常對照進行口服葡萄糖耐量試驗(OGTT)和胰島素釋放試驗(IRT),空腹血糖負荷后2 h血糖均正常。所有入組對象均無耳科疾病史、糖尿病史、眼底病變及眩暈史。
1.2 方法
清晨采集各組空腹靜脈血5 mL,3 000轉/min離心10 min,待測。采用酶聯免疫吸附法(ELISA)檢測各組血漿Alarin水平,試劑盒購置美國Phoenix Pharmaceuticals公司。檢測各組空腹胰島素(FINS)、餐后2 h胰島素(2 hINS)及胰島素抵抗指數(HOMA-IR)。采用高壓液相色譜法測定血清糖化血紅蛋白(HbAlc);采用AU680型全自動生化分析儀及配套試劑盒(美國貝克曼庫爾特公司)檢測空腹血糖(FPG)、總膽固醇(TC)、三酰甘油(TG)、低密度脂蛋白膽固醇(LDL-C)和高密度脂蛋白膽固醇(HDL-C)。采用ELISA檢測血清白細胞介素-6(IL-6)、C反應蛋白(CRP)及腫瘤壞死因子-α(TNF-α)水平,所用試劑盒購置美國BIOTANG公司。
1.3 統計學分析

2 結 果
2.1 各組一般資料比較
3組除體質量指數外的一般資料比較,差異無統計學意義(P>0.05),具有可比性,見表1。
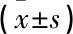
表1 3組一般資料比較
2.2 各組血漿Alarin水平比較
T2DM肥胖組血漿Alarin水平高于T2DM非肥胖組和對照組,差異有統計學意義(P<0.05);T2DM非肥胖組血漿Alarin水平高于對照組,差異有統計學意義(P<0.05),見圖1。

2.3 各組胰島功能水平比較
T2DM肥胖組FINS、2 hINS及HOMA-IR水平高于T2DM非肥胖組和對照組,差異有統計學意義(P<0.05);T2DM非肥胖組FINS、2 hINS及HOMA-IR水平高于對照組,差異有統計學意義(P<0.05),見表2。
2.4 各組糖脂代謝水平比較
T2DM肥胖組HbAlc、FPG、TC、TG、LDL-C水平高于T2DM非肥胖組和對照組,HDL-C水平低于T2DM非肥胖組和對照組,差異有統計學意義(P<0.05);T2DM非肥胖組HbAlc、FPG、TC、TG、LDL-C水平高于對照組,HDL-C水平低于對照組,差異有統計學意義(P<0.05),見表3。
2.5 各組炎性因子水平比較
T2DM肥胖組CRP、IL-6和TNF-α水平高于T2DM非肥胖組和對照組,差異有統計學意義(P<0.05);T2DM非肥胖組CRP、IL-6和TNF-α水平高于對照組,差異有統計學意義(P<0.05),見表4。
2.6 血漿Alarin與胰島功能、糖脂代謝及炎性因子水平的相關性分析
Pearson相關性分析表明,T2DM患者血漿Alarin與FINS、2 hINS、HOMA-IR、HbAlc、FPG、TC、TG、LDL-C、CRP、IL-6和TNF-α水平呈正相關(P<0.05),與HDL-C水平呈負相關(P<0.05),見表5。
3 討 論
近年來,2型糖尿病的發病率不斷升高,且趨于年輕化態勢[6]。遺傳因素、飲食習慣等因素導致肥胖和胰島素抵抗,這是T2DM形成級聯事件的關鍵機制[7],肥胖患者常伴有高胰島素血癥,是造成胰島素抵抗的重要原因之一。肥胖是一種能源內穩態失衡的結果,是能量攝入超過能量消耗,多余的能量儲存在脂肪,進而導致肥胖[8]。脂肪組織在體內以甘油三酯的形式儲存,當膳食攝取的能量持續超過能量消耗時,脂肪組織會通過現有脂肪細胞的增厚和新脂肪細胞的產生而擴張,導致肥胖[9]。異常肥大的脂肪細胞可分泌多種脂肪因子,可進一步干擾糖脂代謝,促進炎性細胞因子的表達和分泌,降低胰島素敏感性,從而導致胰島素抵抗[10]。本研究表明,T2DM肥胖組FINS、2 hINS、HOMA-IR、HbAlc、FPG、TC、TG、LDL-C、CRP、IL-6和TNF-α水平高于T2DM非肥胖組和對照組,T2DM非肥胖組FINS、2 hINS、HOMA-IR、HbAlc、FPG、TC、TG、LDL-C、CRP、IL-6和TNF-α水平高于對照組,T2DM肥胖組HDL-C水平低于T2DM非肥胖組和對照組,T2DM非肥胖組HDL-C水平低于對照組,差異均有統計學意義(P<0.05)。可見,肥胖的T2DM患者胰島功能、糖脂代謝及慢性炎癥變化程度更加明顯,原因可能與胰島素抵抗有關。
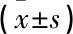
表2 各組胰島功能水平比較
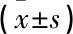
表3 各組糖脂代謝水平比較
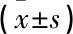
表4 各組炎性因子水平比較

表5 血漿Alarin與胰島功能、糖脂代謝
脂肪細胞因子來源于脂肪組織,在調節葡萄糖、脂質和能量代謝方面的重要性已得到了廣泛的證明,而脂肪因子分泌失調對人類代謝疾病(如肥胖、動脈粥樣硬化、T2DM)的發病起著重要作用[11]。既往研究[12]表明,脂肪因子與肥胖的發病機制密切相關,但新型脂肪因子與肥胖及糖尿病發生的關系仍缺乏研究。Alarin是一種由25個氨基酸組成的血管活性肽[13]。據報道,在小鼠模型中,Alarin可刺激黃體生成素和促性腺激素釋放激素的分泌,促進食欲[14]。另有研究[15-16]指出,Alarin作為一種飲食調節因子對促進食欲、增加體質量有重要作用。飲食調節因子在糖尿病的發生和發展中扮演著重要角色,如由白色脂肪產生的瘦素主要作用于下丘腦,能夠抑制食欲,并通過激活交感神經系統來間接調節糖脂代謝[17-18]。此外,Alarin在代謝障礙患者中表達明顯升高,且與胰島素抵抗顯著相關。本研究同樣發現,T2DM肥胖組血漿Alarin水平高于T2DM非肥胖組和對照組,T2DM非肥胖組血漿Alarin水平高于對照組。由此可見,Alarin是一種與胰島素抵抗和能量穩態相關的細胞因子。Pearson相關性分析表明,T2DM患者血漿Alarin與FINS、2 hINS、HOMA-IR、HbAlc、FPG、TC、TG、LDL-C、CRP、IL-6和TNF-α水平呈正相關,與HDL-C水平呈負相關。可見,血漿Alarin與糖尿病患者的糖脂代謝水平、胰島素抵抗及慢性炎癥程度密切相關,可能在T2DM的發生和發展中扮演重要角色。
綜上所述,初診T2DM患者血漿Alarin 水平明顯升高,且與肥胖、糖脂代謝紊亂、胰島素抵抗以及慢性炎癥反應密切相關,血漿Alarin水平隨代謝異常危險因素的增加而增高。深入研究具體作用機制有助于為防治T2DM合并肥胖患者提供新的藥物靶點。

