標準人群接受人絕經期促性腺激素聯合卵泡期長方案干預的妊娠結局觀察
蔡 鈺,楊 易,宋 娟
1.宜賓市第一人民醫院 婦產科(宜賓 644000);2.四川大學華西第二醫院川南婦女兒童醫院 婦產科(自貢 644000);3.成都市第三人民醫院 婦產科(成都 610066)
促排卵是體外受精-胚胎移植過程中的重要環節,目前臨床上的常規促排卵方案是卵泡期長方案,使用的促性腺激素一般為重組卵泡刺激素(follicle stimulating hormone,FSH)[1];但卵泡期長方案中使用促性腺激素釋放激素(gonadotropin releasing hormone,GnRH-a)降調節會導致外周血黃體生成素(luteinizing hormone,LH)水平降低,而rFSH僅有FSH的生理活性,也會進一步降低LH水平,導致LH的促雄激素生成、募集卵泡、促竇卵泡生長等生理功能受到影響,不僅不利于優勢卵泡的選擇與維持,還會阻礙卵泡正常發育和卵母細胞成熟,最終對妊娠結局造成不良后果[2]。因此,是否應在GnRH-a降調節后補充外源性LH從而調節外周血LH水平,是相關領域的研究熱點及難點,目前國內外均尚無定論[3]。本研究選取接受體外受精-胚胎移植且自身卵巢儲備功能正常的非高齡孕婦作為研究對象,旨在探討標準人群接受人絕經期促性腺激素(human menopausal gonadotropin,hMG)聯合卵泡期長方案干預的妊娠結局。
1 資料與方法
1.1 臨床資料
選取2018年6月至2020年6月成都市第三人民醫院收治的接受體外受精-胚胎移植且自身卵巢儲備功能正常的非高齡孕婦276例進行前瞻性研究。納入標準:1)年齡20~35歲,臨床資料完整,簽署知情同意書;2)符合《婦產科學》[4]中體外受精-胚胎移植相關適應證,于成都市第三人民醫院第一次接受體外受精-胚胎移植干預;3)竇卵泡數≥7個;4)取卵周期移植胚胎≥1個;5)基礎FSH水平<10 U/L;6)體重指數(body mass index, BMI)17~30 kg/m2且觸發日子宮內膜厚度≥6 mm。排除標準:1)確診為輸卵管積水,且未治愈;2)合并盆腔或子宮器質性疾病,影響胚胎著床;3)合并子宮畸形、腫瘤或宮腔粘連;4)基因學檢查示夫妻至少一方存在染色體異常;5)不符合新鮮胚胎移植標準而改為全胚冷凍者;6)無法配合完成研究及隨訪者。本研究經本院倫理委員會審批。患者入院時使用SPSS軟件隨機生成數字進行編號,111例奇數者納入試驗組,165例偶數者納入對照組。
1.2 方法
所有納入對象均采取常規卵泡期長方案促排卵干預。具體方法為,在孕婦月經來潮第2~3天試用GnRH-a 3.75 mg進行降調節,并于第28天檢查B超下竇卵泡、子宮內膜情況以及外周血FSH、LH等激素水平,若滿足子宮內膜厚度≤5 mm,卵泡經線<10 mm,無功能性卵巢囊腫,FSH和LH水平≤5 U/L,雌二醇≤5 ng/L,即達到降調節標準,可進行促排卵干預。皮下注射GnRH-a 100 U/d正式啟動促排卵進程,并從刺激卵巢的第5天開始,動態測量雌激素水平和卵泡大小、數量,并以此為依據調整GnRH-a劑量,最大不超過225 U/d。確認促排卵啟動當日研究對象外周血LH水平<1 U/L。依據《輔助生殖促排卵藥物治療專家共識》[5]中相關標準,啟動日LH<1 U/L的試驗組孕婦自促排卵啟動日起使用hMG 40 U/d與GnRH-a共同干預,而LH≥1 U/L的對照組孕婦不適用hMG干預。待兩側卵巢中主導卵泡直徑≥18 mm后,即可注射hCG 10 000 U以便取卵。取卵操作在hCG注射后36 h進行,由經驗豐富的同一組醫師在超聲引導下完成。取卵后常規進行黃體支持和胚胎培養。3 d后選擇胚胎進行移植,完成后繼續進行常規型黃體支持。胚胎移植完成后14 d取孕婦外周血檢測β-hCG水平,≥10 U/L即可判斷為妊娠。胚胎移植完成后5周,使用經陰道B超檢測到妊娠囊和原始心管搏動,即可診斷為臨床妊娠。
1.3 觀察指標和評價標準
對所有研究對象進行至少12個月隨訪。觀察并記錄兩組孕婦的年齡、BMI、基線竇卵泡數、基礎FSH、基礎LH等一般資料,以及注射hCG日雌二醇、孕酮水平、子宮內膜厚度、移植日子宮內膜厚度、獲卵數、受精率、移植胚胎數、胚胎種植率等臨床參數,對臨床妊娠率、活產率、流產率進行對比和分析。胚胎種植率=臨床妊娠的胚胎數/總移植胚胎數×100%,臨床妊娠率=臨床妊娠的孕婦例數/本組人數×100%,活產率=活產例數/臨床妊娠例數×100%,流產率=流產例數/臨床妊娠例數×100%。
1.4 統計學方法
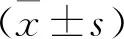
2 結果
2.1 兩組一般資料比較
兩組孕婦年齡、BMI、基礎FSH和LH水平、基礎FSH/LH以及竇卵泡數差異均無統計學意義(P>0.05)(表1)。

表1 兩組一般資料比較
2.2 兩組取卵、受精以及胚胎移植情況比較
試驗組孕婦與對照組孕婦注射hCG日雌二醇、孕酮、子宮內膜厚度、移植日子宮內膜厚度、獲卵數、受精率、移植胚胎數、胚胎種植率差異無統計學意義(P>0.05)(表2)。
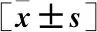
表2 兩組取卵、受精以及胚胎移植情況比較
2.3 兩組妊娠結局比較
試驗組的臨床妊娠率以及活產率均高于對照組,差異有統計學意義(P<0.05)(表3)。
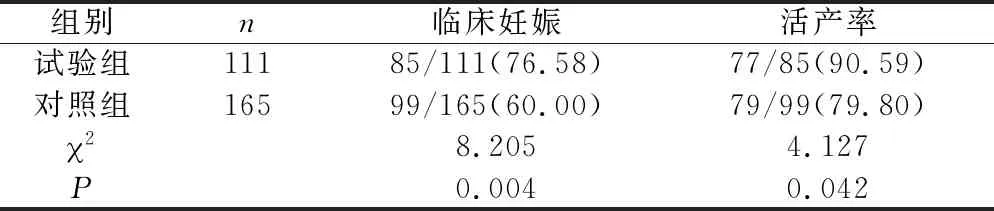
表3 兩組妊娠結局比較(%)
3 討論
LH與FSH的協同作用在促進卵泡發育、卵母細胞成熟以及促排卵過程中意義重大[6]。在卵泡發育早期,LH具有促進膽固醇向睪酮和雄烯二酮轉化的生理作用,是雌激素合成底物的重要來源。此外,適當水平的LH還能夠增加卵巢對FSH的敏感度,由膽固醇轉化合成的雄激素能夠促進卵泡膜細胞上FSH受體的表達,對卵泡募集、竇卵泡生長具有積極影響[7]。但這種促進作用和積極影響的前提是外周血LH水平必須保持在卵泡LH閾值窗內。在卵泡發育的中晚期,卵泡LH閾值會有所上升,這是因為LH部分取代了FSH的生理功能,顆粒細胞表面的LH受體增加,從而有利于優勢卵泡的選擇與維持[8]。因此,對于LH水平不足的孕婦,其雄激素生成會受到影響,導致孕激素水平異常,最終影響卵泡發育和卵母細胞成熟。分子生物學研究[9]發現,LH直接作用于卵巢顆粒細胞與卵母細胞成熟以及后續胚胎質量密切相關。
卵泡期長方案中使用GnRH-a降調節的目的在于減少垂體釋放LH,從而避免內源性LH峰的促排卵作用,達到卵泡發育同步化的效果,這有助于改善體外受精孕婦的子宮內膜種植環境,并獲取質量更好的卵母細胞,但同時也會導致外周血LH水平達不到卵泡LH閾值窗[10]。啟動促排卵時通常使用rFSH,會進一步降低LH水平。國內外大量臨床研究[11]均證實,過低的LH水平不僅會影響獲卵數和受精率,還會降低臨床妊娠率,增加流產率,這也使GnRH-a降調節后是否應該補充外源性LH從而調節外周血LH水平,成為相關領域的研究熱點,目前該問題尚無定論。有國外研究[12]認為,對于GnRH-a降調節后發生垂體抑制的孕婦,在促排卵周期中使用外源性LH可有效提升優質胚胎獲取率,并提高雙原核胚胎率和胚胎種植率,從而改善妊娠結局。但也有研究[13]認為,對于高齡孕婦在促排卵過程中添加外源性LH有利于妊娠結局,但對于非高齡的標準人群意義不大,應謹慎使用。本研究將納入對象限定為卵巢儲備功能正常的非高齡標準人群,旨在探討標準人群在GnRH-a降調節后應用hMG這一人工合成LH制劑對妊娠結局的影響,為該類孕婦的臨床干預和治療方案選擇提供依據。根據相關指南,本研究只納入了促排卵啟動日LH<1 U/L的孕婦,提示卵泡期長方案干預中發生垂體功能過度抑制的孕婦占相當比例[14]。筆者對這部分啟動日LH水平較低的試驗組孕婦實施hMG干預,結果顯示,試驗組孕婦的臨床妊娠率和活產率高于未接受hMG干預的對照組孕婦,說明hMG可彌補垂體抑制和卵巢慢反應產生的LH不足生理效應,改善孕婦妊娠結局,推測這與以下兩點有關:一是hMG中LH的生物活性由hCG驅動,而hCG因其分子結構的關系,較內源性LH有更長的半衰期,且與LH-絨毛膜促性腺激素受體有更強的親和力,故可給卵泡生長提供更穩定的環境,從而提高胚胎質量;二是外源性LH具有類孕激素的作用,可對著床期窗口子宮內膜補體蛋白表達進行調控,并增加胚胎著床環境相關細胞因子水平,最終提升子宮內膜容受性,改善妊娠結局。
此外,本研究還發現,試驗組孕婦在GnRH-a降調節后添加外源性hMG并不會對其獲卵數和受精率產生影響,這與前人的研究[15]結果并不相符,一方面可能是因為觀察對象為標準人群,卵巢儲備功能正常,另一方面可能也與樣本量相對較小有關,有待于進一步研究證實。
綜上所述,在對接受體外受精-胚胎移植且自身卵巢儲備功能正常的非高齡孕婦進行常規卵泡期長方案促排卵過程中,采用hMG干預,能夠有效調節孕婦FSH、LH激素水平及動態平衡,從而提升妊娠率及胚胎質量,改善母嬰妊娠結局。

