強直性脊柱炎合并骨密度異常患者危險因素分析*
劉 雷,洪學志,李嘯天,姜玉欣,許 佳,莫漢有△
(桂林醫學院附屬醫院:1.風濕免疫科;2.影像科,廣西桂林 541001)
強直性脊柱炎(ankylosing spondylitis,AS)是一種慢性、系統性、炎癥性疾病,主要累及骶髂及脊柱等中軸關節,晚期可導致關節融合及脊柱強直而嚴重影響患者生活質量[1]。AS患者早期除出現關節疼痛、僵硬、虹膜睫狀體炎、銀屑病皮損、炎癥性腸病外,骨質疏松(osteoporosis,OP)及椎體骨折可同樣在早期出現[2]。有研究表明,AS合并OP發生率高達19%~62%[3],但由于AS患者存在以下因素導致了AS患者OP檢出率較低:(1)椎體關節新生骨形成使骨密度(bone mineral density,BMD)假性增高;(2)疾病早期主要表現為關節疼痛,患者常自行服用止痛藥可緩解;(3)臨床醫師對AS患者主要以控制癥狀為主,而忽視了對OP的篩選;(4)AS好發于青少年男性,而青年男性常不作為OP的發病對象;(5)臨床醫師對AS患者發生OP的認識不足[4]。本研究分析了本院首診AS患者發生OP的易感因素及臨床特征,旨在為臨床早期發現及治療提供理論依據。
1 資料與方法
1.1 研究對象
選取2014年1月1日至2020年6月1日本院首次診斷為AS的患者作為研究對象。
1.2 納入標準
(1)符合1984年美國風濕病學診斷標準;(2)女性年齡小于或等于45歲,男性年齡20~55歲;(3)運用雙能X射線吸收法(dual energy X-ray absorptiometry,DEXA)行腰椎L1~4或髖關節BMD檢測。
1.3 排除標準
(1)既往已在外院確診并治療;(2)患有甲狀腺功能亢進癥、甲狀旁腺功能亢進癥、庫欣綜合征等影響骨質代謝的內分泌疾病;(3)合并類風濕性關節炎、系統性紅斑狼瘡等其他結締組織病;(4)患有多發性骨髓瘤、白血病、骨髓增生異常綜合征等影響BMD的血液系統疾病;(5)合并嚴重肝、腎功能損害,長期服用糖皮質激素等影響骨代謝的藥物及嚴重營養不良。
1.4 方法
1.4.1資料收集
收集患者年齡、性別、身高、體重、病程[≥10年為長病程組(19例)、<10年為短病程組(64例)]、出院診斷、相關實驗室檢查,如紅細胞沉降率(erythrocyte sedimentation rate,ESR)、C 反應蛋白(C-reactive protein,CRP)、血漿球蛋白(globulin,GLO)、堿性磷酸酶(alkaline phosphatase,ALP)、總25羥維生素D[25-hydroxyvitamin D,25(OH)D]、β-膠原特殊序列等相關指標。
1.4.2測量BMD值
應用WHO推薦的DEXA測量BMD值,BMD值低于同性別、同種族健康成人峰值1個標準差(≥-1.0)為正常;>-2.5~<-1.0為骨量減少;≤-2.5為OP。T<-1.0為骨量異常組(63例),T≥-1.0為骨量正常組(20例)。
1.5 統計學處理
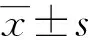
2 結 果
2.1 臨床及實驗室檢測特點
83例首診AS患者中男69例,女14例;年齡20~54歲,平均(31.96±8.39)歲;病程:最短2周內確診,最長確診時間超過20年,中位病程36(12,108)個月;BMI(21.54±3.17)kg/m2,CRP[8.97(2.98,20.68)mg/dL],ESR[32.0(14.0,57.0)mm/h],GLO(33.83±5.68)g/L,ALP(89.08±42.97)U/L,總25(OH)D(28.08±9.20)ng/mL,β-膠原特殊序列[725.4(470.3,919.5)pg/mL],BMD[0.79(0.70,0.88)g/cm2]。出現骨量減少63例(75.9%),OP 24例(28.9%),脆性骨折2例(2.4%)。
2.2 年齡、病程、BMI、疾病活動指標、骨代謝指標與BMD的相關性
BMD與ESR、ALP、β-膠原特殊序列呈顯著負相關,總25(OH)D與腰椎或髖關節BMD呈正相關,年齡、病史、BMI、CRP、GLO與BMD無關,見表1。

表1 不同參數與腰椎BMD相關性分析
2.3 骨量異常組與骨量正常組患者各指標比較
兩組患者總25(OH)D比較,差異有統計學意義(P<0.05),見表2。

表2 骨量異常組與骨量正常組患者各指標比較
2.4 長病程組與短病程組患者各指標比較
兩組患者年齡、BMI、BMD比較,差異均有統計學意義(P<0.05),見表3。

表3 長病程組與短病程組患者各指標比較
3 討 論
本研究結果顯示,AS合并OP發生率為28.9%,脆性骨折發生率為2.4%,低于既往研究的19.0%~62.0%,可能與納入患者為首診有關。本研究相關性分析發現,AS合并OP與ESR呈正相關。ESR升高代表疾病活動,疾病高活動狀態下體內腫瘤壞死因子α(tumor necrosis factor-α,TNF-α)、白細胞介素-1(interleukin,IL-1)、IL-6、IL-17等促炎性細胞因子水平升高。TNF-α主要由單核巨噬細胞及淋巴細胞分泌,在骨吸收中主要通過在細胞核因子κB受體活化因子配體(receptor activator of NF-κB ligand,RANKL)參與下誘導單核祖細胞向破骨細胞分化[5];誘導分泌型蛋白Dickkopf-1與骨硬化蛋白合成進而抑制Wnt/β-聯蛋白(β-catenin) 信號通路促進破骨細胞功能活化促進骨吸收[6]。其他炎性細胞因子同樣可通過上述機制誘導成纖維細胞分泌RANKL促進破骨細胞分化進而導致OP的發生[7]。有研究發現,采用抗TNF-α拮抗劑治療AS不僅改善了患者關節疼痛癥狀,追蹤治療1、2年發現,TNF-α拮抗劑治療同樣可使腰椎BMD分別提高5.1%、8.6%,髖關節BMD分別升高1.8%、2.5%[8]。
本研究結果顯示,AS患者BMD水平與β-膠原特殊序列呈負相關,與孔瑞娜等[9]研究結果一致。因β-膠原特殊序列是成熟Ⅰ型膠原降解產物,可反映破骨細胞活性及骨吸收情況,并且β-膠原特殊序列與疾病活動度呈正相關。ALP主要由肝臟及成骨細胞分泌,本研究結果顯示,ALP與BMD呈負相關,提示體內骨轉換表現為高代謝狀態。本研究結果顯示,腰椎或髖關節BMD與總25(OH)D呈正相關,骨量異常組患者總25(OH)D明顯低于骨量正常組,其原因在于維生素D不僅參與了體內鈣、磷、骨代謝,還通過抑制體內T淋巴細胞活化及增殖而抑制體內炎性反應,降低骨吸收[10]。
AS合并OP常見危險因素包含病程、年齡及消瘦[11]。但本研究骨量正常和異常組患者病程、年齡比較及相關性分析中均未發現異常,并且長病程組患者BMD值高于短病程組。可能與研究中BMD測量方式采用正向DEXA有關,因AS患者易發生椎體皮質骨鈣化、脊柱融合及韌帶鈣化等,同時正向法將腹主動脈鈣化同樣并入BMD計算中,使測量值升高[12]。因此,對病程較長及懷疑存在異位新骨形成的AS患者可采用側向DEXA、髖關節BMD或定量CT、定量超聲法檢測BMD水平,以減少誤診、漏診的發生[13]。同時本研究長病程組患者BMI水平高于短病程組,與BMD水平升高一致,提示鍛煉可促進BMD水平的升高[14]。
綜上所述,AS首診患者合并OP發生率占28.9%,即疾病早期并可出現OP,同時對合并危險因素,如疾病高活動度、高齡、低BMI及低總25(OH)D等患者臨床醫師更應早期、規律行BMD檢測,同時根據患者臨床特點選擇合適的檢測方法。對合并OP患者,即時給予抗炎、抗骨質疏松治療,以改善患者生活質量。

