超聲輔助鈮酸鉀鈉壓電顆粒抑制乳腺癌的研究
郝 玲,戚穗堅
(華南理工大學食品科學與工程學院,廣東 廣州 510641)
乳腺癌是女性中的頭號殺手,臨床上雖然有多種的治療手段,但大多存在較大的毒副作用[1-3]。例如,傳統的化療對腫瘤組織缺乏選擇性,容易對全身正常組織以及免疫功能產生嚴重損害,并產生腫瘤耐藥現象[4]。研究具有低毒副作用并能有效抑制惡性腫瘤的替代手段具有十分重要的意義。對于某些惡性腫瘤的治療,腫瘤治療電場成了一種新的選擇[5-6]。但這種治療一般需使用外加電源,不僅使用不方便,而且還因插入電極而帶來組織損傷。鈮酸鉀鈉(KNN)是典型的無鉛壓電材料,具有優越的壓電常數(較大的d33值)和較高的居里溫度,它能在遠程超聲作用下產生內在電場進而作用細胞調控其行為[7-8]。研究其產生的內在電場對惡性腫瘤的潛在抑制作用可望為癌癥的治療提供方便有效、低毒副作用的替代方案。本文通過水熱合成法制備了尺寸及電學特征可控的壓電鈮酸鉀鈉顆粒(P-KNN),對其進行了結構表征,研究了在超聲輔助下其生物相容性以及對兩種不同乳腺癌細胞的抑制作用。
1 實 驗
1.1 儀器與試劑
無水乙醇,五氧化二鈮,碳酸鉀,碳酸鈉,CCK-8及細胞活死染色試劑盒;
球磨機,烘箱,馬弗爐,高壓反應釜,離心機,超聲機,酶標儀。
1.2 樣品制備
通過水熱合成法制備P-KNN[9]。具體如下,以200 mL無水乙醇預先混合五氧化二鈮34.262 g,碳酸鉀6.831 g和碳酸鈉8.907 g,進行球磨8 h。將球磨所得的混合液取出置于80 ℃烘箱至完全烘干(一般為12 h)。烘干后的樣品轉移至坩堝,放入馬弗爐中以750 ℃煅燒2 h,制得粉體;取出0.02 mol的粉體與50 mL去離子水進行共混后轉移至100 mL聚四氟乙烯密封的高壓反應釜中,于210 ℃下反應24 h后,取出靜置12 h;棄上清,沉淀物攪拌混勻后轉移至離心管中,8000 rpm的轉速下離心20 min;將上清液倒掉后加入30 mL的無水乙醇,將離心管密封好后放入超聲機中分散10 min,隨后將其放入離心機中以同樣的條件進行再次離心。離心后,倒掉上層無水乙醇后加入去離子水清洗兩次;將清洗后的樣品放入80 ℃烘箱烘干,制備出P-KNN。
分別以掃描電子顯微鏡(SEM)、能譜儀(EDS)、粒度分析儀、X射線衍射分析儀(XRD)和拉曼圖譜(Raman)分別對材料的表面形貌、元素組成、粒徑分析、物相分析和化學結構進行分析。
1.3 細胞實驗
實驗選用三種細胞株:具有高轉移性的三陰性乳腺癌細胞株MDA-MB-231;低轉移性乳腺癌細胞株MCF-7以及人正常乳腺上皮細胞MCF-10A。每種細胞在各自官方推薦的最佳培養條件下培養。采用CCK-8試劑以及細胞死活染色法研究材料對正常乳腺上皮細胞的生物相容性以及對乳腺癌細胞的細胞毒性。具體如下,將細胞接種于孔板中,待細胞完全貼附后分別與200,400 μg/mL的材料溶液共培養;超聲組每隔12 h超聲處理2 min,并于材料加入后24 h,36 h,48 h分別以CCK-8試劑盒進行檢測,計算細胞存活率。另外,在材料加入24 h后以試劑盒進行死/活染色,于倒置熒光顯微鏡下進行觀察,在同一位置同時觀察發綠色熒光的活細胞與紅色熒光的死細胞并進行拍照,采用Image J軟件進行處理。用transwell試驗檢測材料對乳腺癌細胞遷移侵襲能力的影響,通過倒置熒光顯微鏡明場觀察transwell小室下層過膜的細胞數量并進行拍照。
2 結果與討論
2.1 材料的表征分析
通過XRD分析材料的晶體結構,如圖1(a)所示,表明制得的材料為ABO3型鈣鈦礦結構,在45度角附近出現(002)與(200)雙峰,表明四方相與正交相共存,制備的顆粒具有良好的壓電性。利用Raman分析材料的化學結構,在265 cm-1位置及621 cm-1位置均有KNN特征振動峰的出現(圖1(b))。EDS分析表明材料的主要成分為氧、鈉、鈮、鉀元素(圖1(c))。
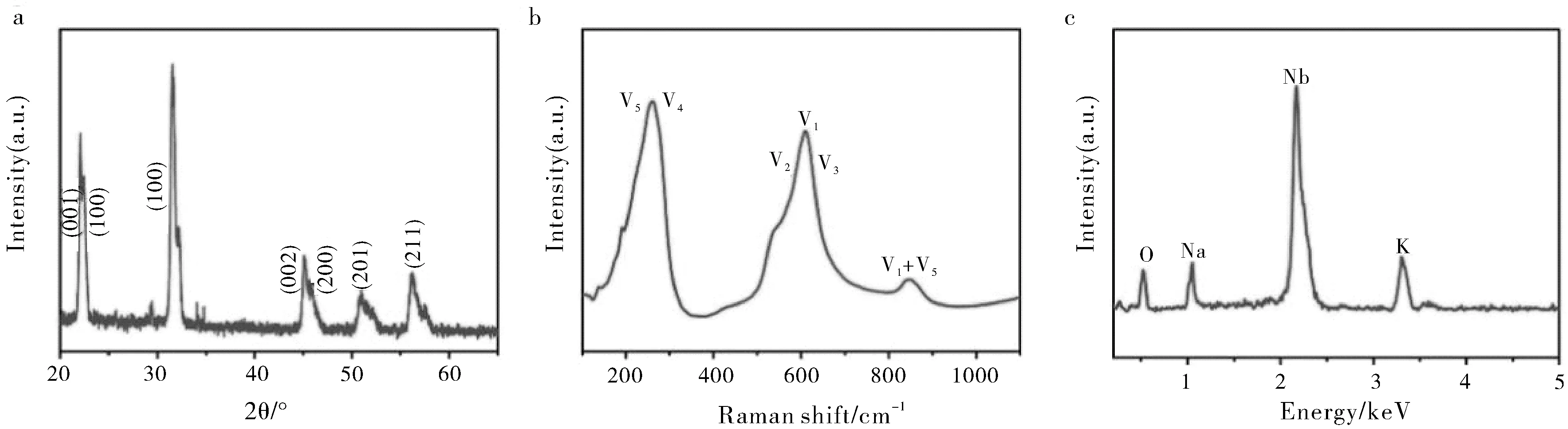
圖1 P-KNN的XRD(a),Raman(b)和EDS(c)Fig.1 XRD(a),Raman(b)and EDS(c)of P-KNN

圖2 P-KNN的SEM(a)和納米粒度(b)分析Fig.2 SEM image(a)and DLS analysis(b)of P-KNN
利用SEM對材料的形貌進行觀察,如圖2(a)所示,P-KNN呈現顆粒狀,材料具有較好的分散性,大小均一。進一步通過粒徑分析表明P-KNN顆粒的大小約457.4 nm(圖2(b)),分布系數(PDI)為0.422,表明樣品的粒徑分布較窄,具有良好的分散性。
綜上表明,水熱合成法成功制備具有壓電特性的P-KNN,具有微納米級的粒徑大小且具有良好的分散性。
2.2 材料對乳腺癌細胞的抑制作用
采用CCK-8活性檢測法在材料加入后24 h,48 h,72 h進行2種不同轉移能力的乳腺癌細胞活性的檢測。由圖3(a)可見,在不施加超聲下,與對照組相比,濃度為200,400 μg/mL的P-KNN對MDA-MB-231的存活率均具有一定的抑制作用;在施加超聲下,MDA-MB-231細胞的存活率進一步明顯受到抑制,在24 h時,400 μg/mL的P-KNN下MDA-MB-231的存活率僅約30%。當對MDA-MB-231細胞繼續培養至48 h,72 h,結果表明,每個組別的細胞存活率都得到進一步的抑制。材料以及超聲處理對MCF-7細胞存活率的影響與MDA-MB-231細胞的結果呈現相似的趨勢(圖3(b))。CCK-8實驗表明P-KNN的作用以及超聲的刺激都能明顯的對兩種乳腺癌細胞進行抑制,且在P-KNN濃度為400 μg/mL并加超聲處理時對乳腺癌細胞的抑制作用最強。
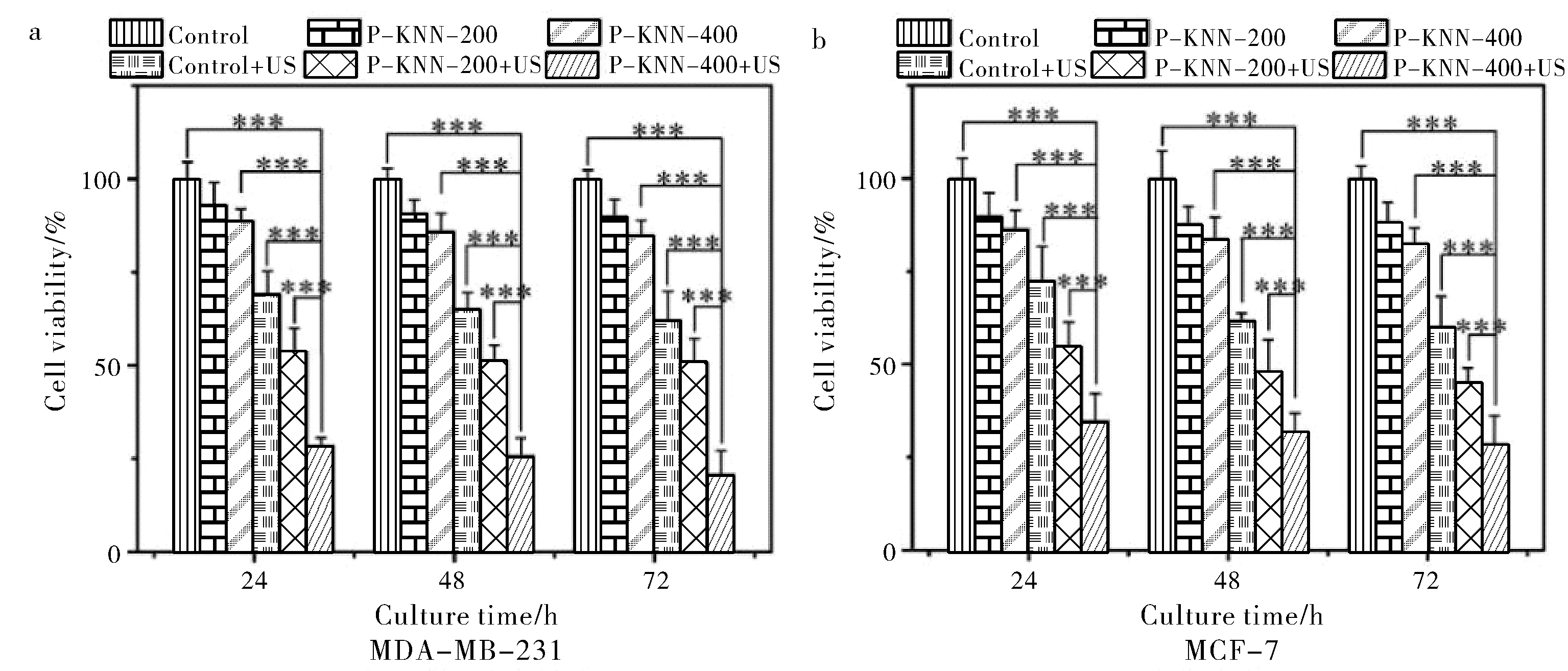
圖3 施加/不施加超聲下不同濃度P-KNN對MDA-MB-231(a)與MCF-7(b)細胞的毒性作用Fig.3 Cytotoxic effects of different concentrations of P-KNN on MDA-MB-231(a)and MCF-7(b)w/o ultrasound
進一步采用細胞死活染色考察材料以及超聲作用對MDA-MB-231和 MCF-7細胞的抑制作用。超聲組在材料加入12 h后進行超聲處理,24 h后對細胞進行死活染色,活細胞呈現綠色的熒光而死細胞呈現紅色的熒光。結果顯示(此處未附上顯色圖),對于兩種乳腺癌細胞,在不加材料不加超聲處理的空白對照組,細胞均為活細胞(綠色熒光)。在不施加超聲下,當細胞與400 μg/mL的P-KNN作用后,死細胞(紅色熒光)出現;進一步施加超聲下,大量的死細胞出現。綜上表明,在超聲輔助下,材料能夠產生非常顯著的乳腺癌細胞抑制效果,此結果也與上述CCK-8實驗的結果一致。
2.3 材料對乳腺癌細胞的遷移侵襲能力的影響
Transwell試驗結果表明(圖4),超聲的刺激與P-KNN材料的作用都能夠對乳腺癌細胞的遷移侵襲能力產生顯著的抑制作用。在超聲的輔助下(P-KNN-400+US組),材料的作用能夠完全抑制MDA-MB-231和 MCF-7兩種乳腺癌細胞的運動,原因可能是由于一方面材料和超聲的同時作用造成了癌細胞的大量死亡,另一方面存活的細胞由于其本身的形態已經發生嚴重的改變甚至破壞,細胞也基本喪失了運動的能力。
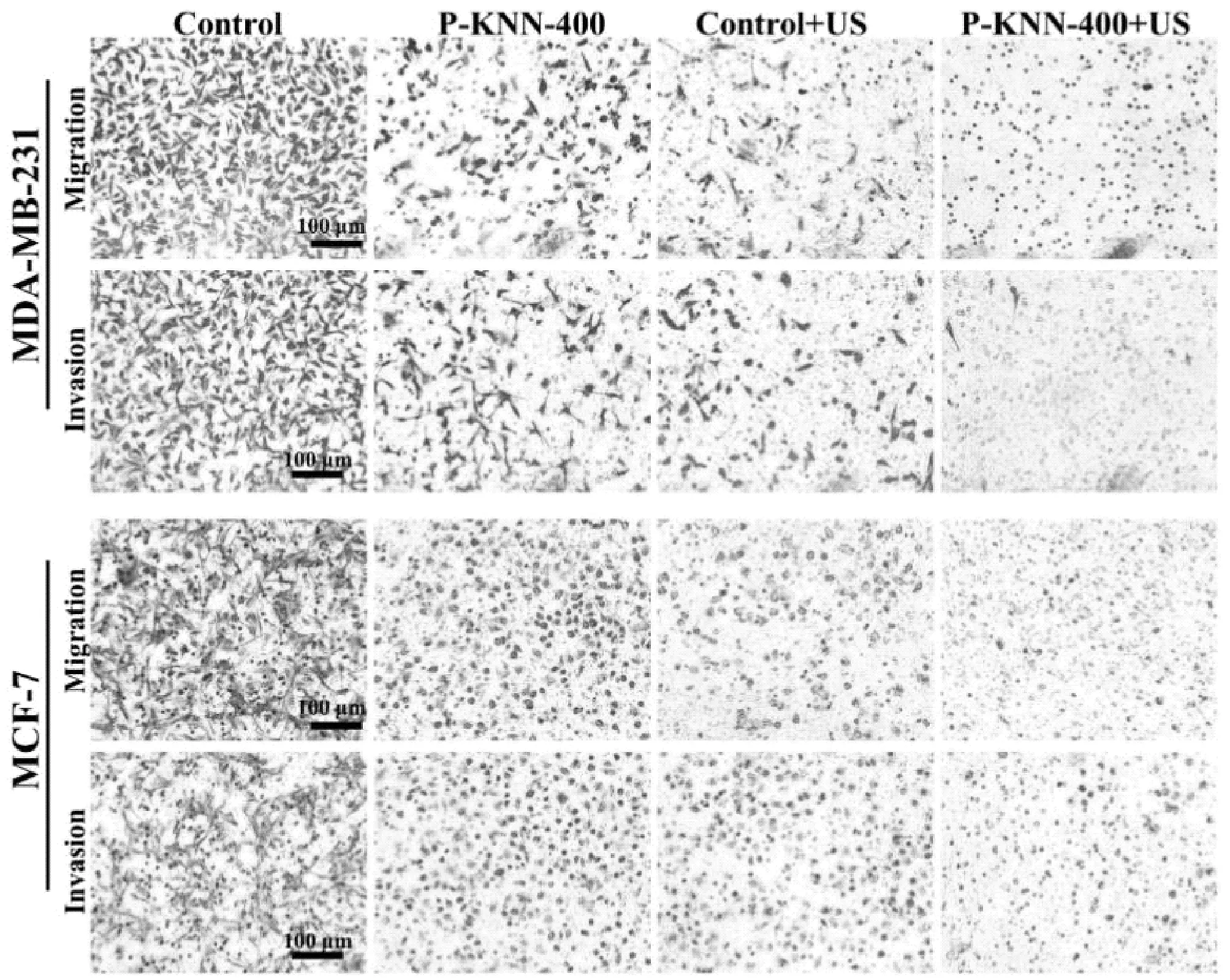
圖4 施加/不施加超聲下400 μg/mL P-KNN對MDA-MB-231和MCF-7細胞的遷移侵襲實驗Fig.4 The migration and invasion assays of MDA-MB-231 and MCF-7 co-cultured with 400 μg/mL P-KNN w/o ultrasound
2.4 材料的生物相容性
CCK-8活性檢測的結果表明(圖5),在不施加超聲下,正常乳腺細胞MCF-10A與不同濃度的P-KNN溶液共培養后48 h后,細胞的存活率均在93%以上,表明KNN具有良好的生物相容性。而在施加超聲下(+US),細胞的存活率雖有一定降低,但MCF-10A的細胞存活率仍能達到75%以上,表明KNN對正常乳腺細胞毒性作用較低。
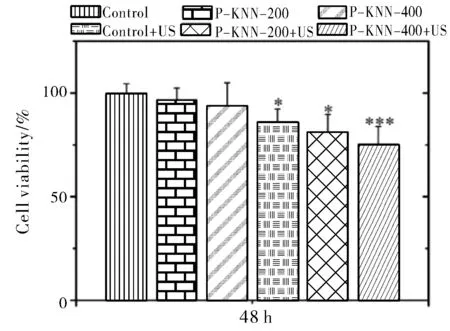
圖5 施加/不施加超聲下不同濃度P-KNN對MCF-10A細胞的細胞毒性作用Fig.5 Cytotoxic effects of different concentrations of P-KNN on MCF-10A w/o ultrasound
細胞死活染色(此處未附上顯色圖)結果與CCK-8定量結果一致,在不施加超聲下,與不同濃度的P-KNN共培養后MCF-10A顯示良好的細胞活性,出現很少死細胞(紅色熒光);在施加超聲下,僅有少量紅色的死細胞出現。綜上結果說明P-KNN具有良好的生物相容性,施加超聲刺激會造成細胞的少量死亡,但對比以上實驗結果,在具有顯著乳腺癌細胞抑制作用的P-KNN-400+US組,正常乳腺上皮細胞的存活率仍然能夠達到75%以上。
3 結 論
本研究制備具有壓電性能的鈮酸鉀鈉顆粒,研究其在超聲輔助下在體外抑制乳腺癌細胞增殖與遷移的潛在能力。通過對樣品的形貌、物相、化學結構等的分析,證實獲得了分散性良好、尺寸均一的壓電性鈮酸鉀鈉顆粒(P-KNN);通過細胞的活性檢測表明,400 μg/mL P-KNN在超聲的輔助作用下能夠達到對兩種不同乳腺癌細胞高達70%左右的抑制作用,對這兩種乳腺癌細胞的遷移侵襲具有明顯的抑制作用。而另一方面,材料以及超聲的作用并沒有給正常乳腺上皮細胞帶來明顯的毒性作用。此研究為進一步研究具有壓電性能的生物相容性材料用于癌癥治療提供了重要的實驗基礎。

