中藥保留灌腸配合蒸熱療法對慢性盆腔炎性后遺癥患者Th17/Treg免疫平衡的影響*
張巖雪,孫軍華,李紅艷,王 穎
河北省民政總醫院,河北 邢臺054000
盆腔炎是臨床常見的婦科疾病,若沒能得到及時正確的診治,可引起以月經不調、異位妊娠、精神萎靡及盆腔痛等后遺癥,嚴重者會出現不孕不育,臨床稱之為盆腔炎性疾病后遺癥(sequelae of pelvic inflammatory disease,SPID)[1]。據報道[2],SPID常發生于20~40歲女性,我國SPID發病率約占性成熟女性人數1%~2%,且呈逐年上升趨勢。SPID病程較長,且容易反復發作。研究顯示,其與機體免疫-炎癥反應的異常改變密切相關,對女性生活造成嚴重影響[3]。西醫主要給予抗生素治療,以緩解盆腔疼痛,必要時采取手術措施來解除粘連狀態[4-5]。SPID歸屬于中醫“婦人腹痛”“經行腹痛”“不孕”等范疇,病機特點為“濕、熱、瘀、寒、虛”,治療以化瘀通絡、理氣化疏為主[6]。近年來,筆者以活血化瘀湯保留灌腸配合蒸熱療法治療SPID患者48例,臨床療效滿意,現報道如下:
1 資料與方法
1.1 臨床資料選取2017年6月至2018年6月在河北省民政總醫院收治的SPID患者96例,隨機分為觀察組和對照組,每組48例。兩組患者臨床資料比較,差異無統計學意義(P>0.05),具有可比性。見表1。
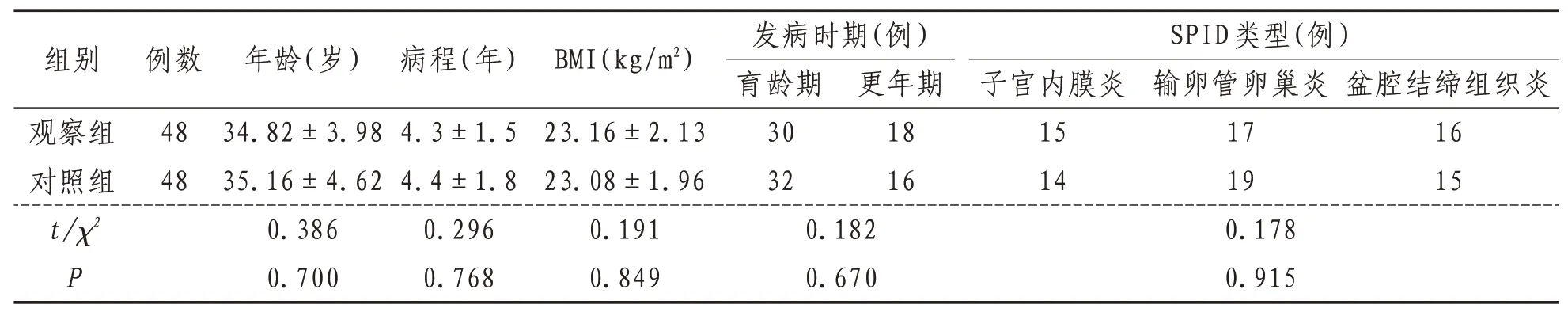
表1 兩組患者臨床資料比較
1.2 診斷標準
1.2.1 西醫診斷標準 參照《中藥新藥臨床研究指導原則(2002版)[7]》及普通高等教育“十一五”國家級規劃教材《婦產科學(2005版)》[8]中關于SPID的診斷標準:1)盆腔炎病史≥3個月。2)以下癥狀具備1項以上:(1)下腹部腫脹或疼痛且在勞累、性交及月經前后加重;(2)白帶異味明顯、異常增多,且呈現淡黃色至黃綠色水樣;(3)月經量多或經期延長;(4)不孕。3)輸卵管病變時在子宮一側或兩側觸及輸卵管呈條索狀增粗,卵巢囊腫時在盆腔一側或兩側觸及囊性腫物活動受限,盆腔結締組織病變時在子宮一側或兩側有片狀增厚,宮骸韌帶增粗、變硬,上述體征同時伴有子宮活動受限或粘連固定伴有壓痛。4)超聲檢查下無任何異常表現或伴有輸卵管增粗、積水或盆腔積液等,女性分泌物涂片檢出病原菌,白細胞或中性粒細胞總數增高,腹腔鏡檢查輸卵管表面明顯充血,輸卵管壁水腫。
1.2.2 中醫辨證診斷標準 參照《中醫婦產科學》[9]中SPID的診斷標準:1)中醫辨證為氣滯血瘀;2)主證為下腹脹痛或刺痛,痛處固定;3)次證為經前情志抑郁,乳房脹痛,腰骶脹痛,經量多或經期延長,或伴有陰道不規則少量出血,經血暗紅伴有血塊,白帶異常、量多、色白或黃,婚久不孕,舌質暗紅或見瘀斑,脈弦。
1.3 納入標準納入:1)符合上述SPID中西醫診斷標準者;2)年齡20~50歲,有性生活史者;3)本研究經醫院倫理委員會批準,且簽署知情同意書者。
1.4 排除標準排除:1)妊娠期或哺乳期婦女;2)伴有心、肝、腎等重要臟器嚴重功能性損害者;3)患婦科器質性病變者;4)無法配合治療者;5)入組前兩周內服用過同類藥物導致不能準確判斷療效者。
1.5 治療方法兩組患者均給予常規西藥抗感染治療:甲硝唑(華中藥業股份有限公司,批號:17021525,規格:0.2 g/片)每次0.4 g,口服,每日3次;左氧佛沙星[第一三共制藥(北京)有限公司,批號:17065662,規格:0.1 g/片]每次0.1 g,口服,每日2次。觀察組在此基礎上加用活血逐瘀類中藥保留灌腸聯合蒸熱療法進行治療,藥物組成:川芎12 g,丹參12 g,敗醬草10 g,蒲公英20 g,甘草10 g,山萸肉12 g,透骨草8 g,金銀花15 g,板藍根12 g,大青葉15 g。水煎2次得藥汁400 mL,分別導入2個250 mL藥瓶內,每日早晚兩次保留灌腸。操作方法:患者于灌腸前排空大小便,取側臥位,無菌輸液器插入藥瓶,12號尿管連接肛管,緩慢插入肛門內約15~18 cm處,采用靜脈輸液法排出氣體,藥液勻速滴入,每次灌藥200 mL,完全滴入后保留30 min。蒸熱療法:準備高度約為50 cm的容器,裝滿熱水,水溫控制在40~42℃左右,患者雙下肢均放入容器內,取坐位,蒸熱治療每次30 min。兩組均以治療10天為1個療程,連續治療3個療程。治療期間忌食辛辣生冷等刺激性食物,保持規律作息,避免性交。
1.6 觀察指標
1.6.1 證候評分 治療前及治療后10、20、30天參照《中藥新藥臨床研究指導原則(2002年版)》[7]評定兩組證候評分。評分項目主要有下腹墜脹疼痛或刺痛、腰骶脹痛、經行腹痛加重、經色紫黯,夾血塊、月經不調、胸脅或乳房脹痛及兩側附件區包塊大小,每項分值2~6分,分值越高說明癥狀越嚴重。
1.6.2 生活質量評分 采用諾丁漢健康調查表(nottingham health profile,NHP)[10]評估患者治療前后的生活質量評分,該量表包括疼痛、睡眠、情感、精力、身體活動及社交活動6個維度38個項目,得分越高說明生活質量越差。
1.6.3 ELISA法檢測血液炎性因子 采集患者清晨空腹靜脈血5 mL,置于含有乙二胺四乙酸抗凝管抗凝,剩余血漿經4°C,3000 r/min離心15 min收集血清,采用ELISA法檢測血清白細胞介素17(interleukin-17,IL-17)、轉化生長因子β(transforming growth factor-β,TGF-β)和白細胞介素10(interleukin-10,IL-10)水平。
1.6.4 RT-PCR法檢測外周血單核細胞RORγt、Foxp3的mRNA表達 治療前后,采集患者清晨外周血分離單核細胞,TRIzol試劑提取總RNA,用DNA/RNA測量儀測得RNA濃度。取符合要求的RNA樣本,采用半定量RT-PCR法擴增RORγt mRNA、Foxp3 mRNA。按照PrimeScrip反轉錄試劑盒進行反轉錄成cDNA,采用SYBR Premix Ex Taq說明書配置PCR反應體系,反應條件為:95℃預變性10 min,然后95℃10 s,60℃30 s,72℃10 s,40個循環;95℃5 s,60℃1 min,95℃30 s。擴增結束后,產物進行1.0%瓊脂糖凝膠電泳20 min,PUX Mix Marker作為分子量參照物同時電泳,以β-actin為內參,在凝膠成像分析儀在紫外光下采集圖像,采用Gepro 4.2軟件分析目的基因與同一條帶β-actin的光密度比值。引物序列見表2。
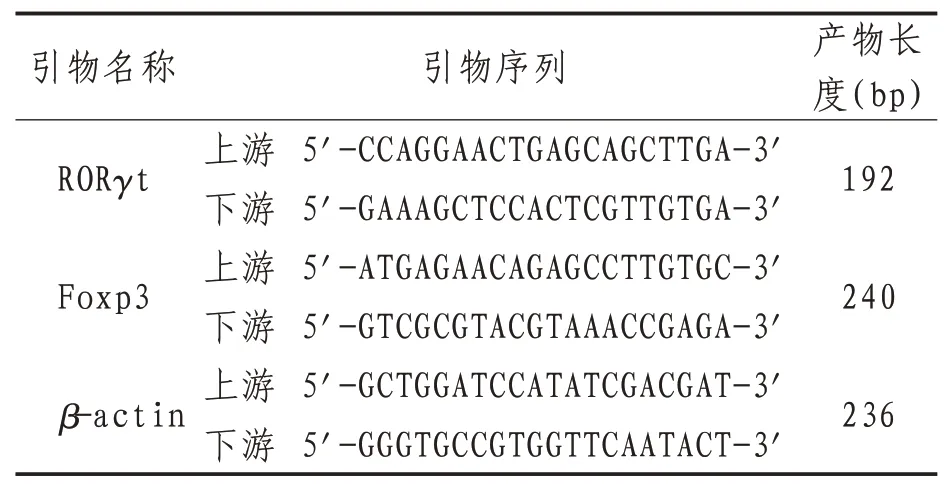
表2 引物序列
1.6.5 療效療效[11]治愈:臨床癥狀、體征基本消失,實驗室檢查相關指標(血常規、B超)恢復正常,證候評分減少≥95%,停藥1個月未現復發。顯效:臨床癥狀、體征明顯減輕,實驗室檢查相關指標明顯改善,癥狀評分減少60%~89%。有效:臨床癥狀、體征減輕,實驗室檢查相關指標改善,癥狀評分減少20%~59%。無效:臨床癥狀、體征無變化甚至惡化,實驗室檢查相關指標無改善,癥狀評分減少<20%。
1.7 統計學方法采用SPSS 16.0進行數據分析,計量資料以±s表示,采用t檢驗,計數資料以率表示,采用χ2檢驗或Fisher精確檢驗,P<0.05表示差異有統計學意義。
2 結果
2.1 臨床療效觀察組痊愈19例,顯效16例,有效8例,無效5例,總有效率89.58%(43/48);對照組基本痊愈16例,顯效11例,有效7例,無效14例,總有效率70.83%(34/48)。兩組總有效率比較,差異有統計學意義(P<0.05)。
2.2 不良反應兩組患者均未見腹瀉、皮疹、發熱等明顯藥物不良反應。
2.3 癥狀評分癥狀積分兩組治療前比較,差異無統計學意義(P>0.05);治療后10、20、30天后,兩組均低于治療前(P<0.05),且觀察組下降更為明顯,相同時間點兩組間比較,差異有統計學意義(P<0.05)。見表3。
表3 兩組治療前后癥狀評分比較(±s) 分

表3 兩組治療前后癥狀評分比較(±s) 分
?
2.4 NHP評分NHP各項評分兩組治療前比較,差異均無統計學意義(P>0.05);兩組治療后均明顯改善,且觀察組改善更為明顯,與對照組比較差異有統計學意義(P<0.05)。見表4。
表4 兩組治療前后NHP評分比較(±s) 分
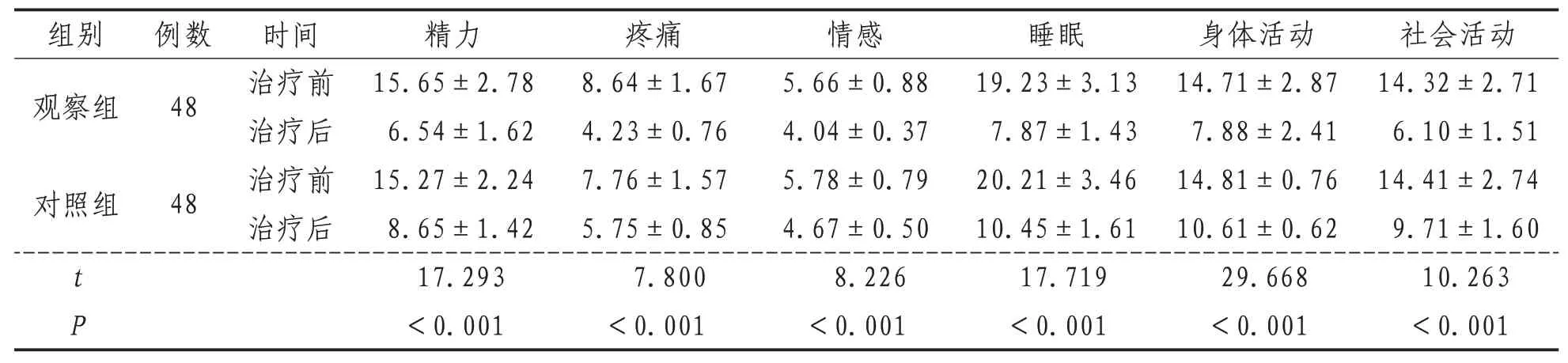
表4 兩組治療前后NHP評分比較(±s) 分
注:t、P為兩組間治療后比較統計值
?
2.5 血清炎性因子水平治療后兩組血清IL-17水平均明顯降低,IL-10、TGF-β水平均明顯升高,觀察組變化較對照組明顯(P<0.05)。見表5。
表5 兩組治療前后血清炎性因子水平比較(±s) pg/mL
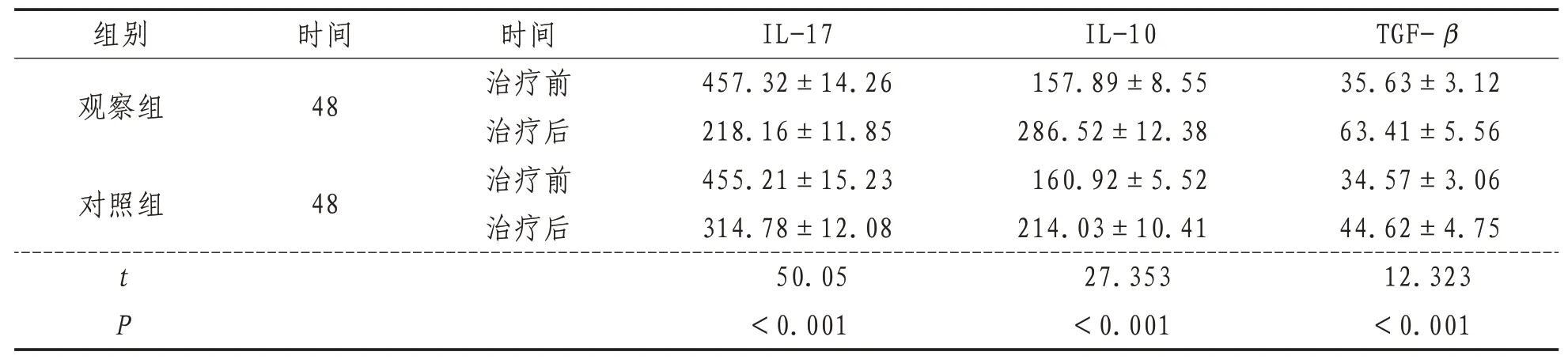
表5 兩組治療前后血清炎性因子水平比較(±s) pg/mL
注:t、P為兩組間治療后比較統計值
?
2.6 外周血單核細胞RORγt、Foxp3的mRNA表達兩組治療后RORγt mRNA表達水平及RORγt/Foxp3均明顯下降,Foxp3 mRNA表達水平明顯升高,觀察組較對照組變化更為明顯(P<0.05)。見表6、圖1。
表6 兩組治療前后RORγt mRNA、Foxp3 mRNA、RORγt/Foxp3水平比較(±s)
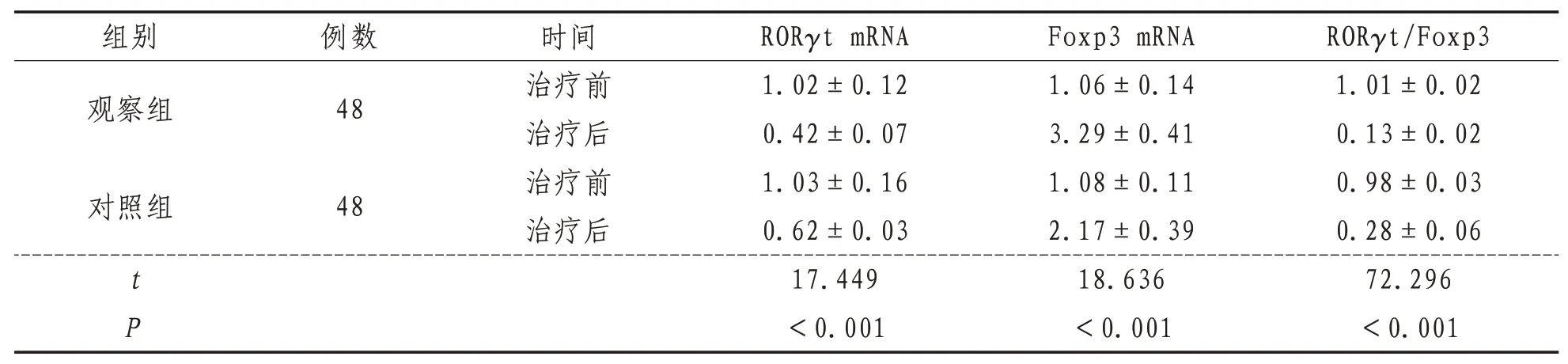
表6 兩組治療前后RORγt mRNA、Foxp3 mRNA、RORγt/Foxp3水平比較(±s)
注:t、P為兩組間治療后比較統計值
?
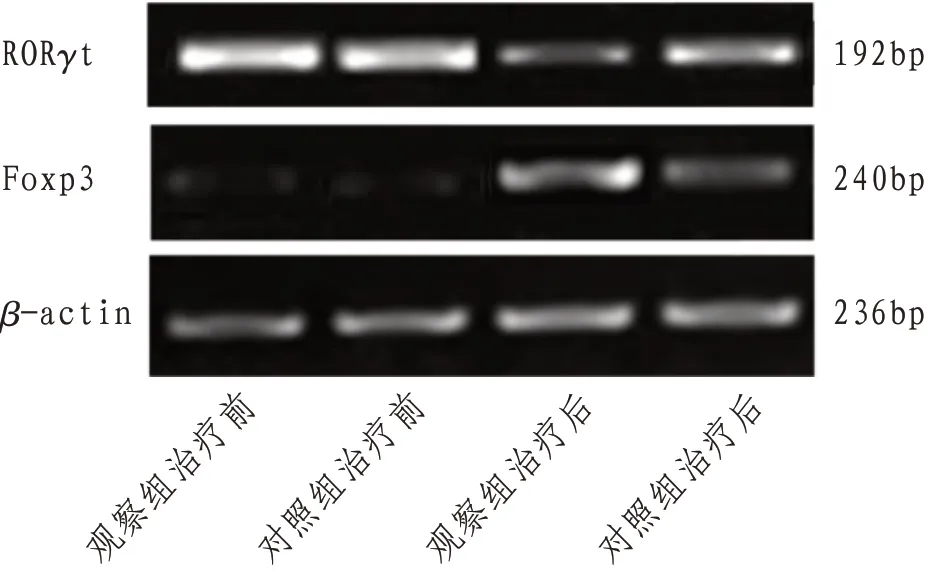
圖1 兩組治療前后RORγt mRNA、Foxp3 mRNA表達
3 討論
SPID的病理基礎為女性生殖道及周圍發生組織破壞、廣泛粘連及增生等組織病變導致輸卵管炎、子宮內膜炎及盆腔炎等疾病[12]。研究顯示,慢性炎性粘連的形成,與機體免疫力下降等多種因素相關[13]。有報道稱[14],SPID病理變化為免疫病理損傷,若沒有得到及時有效的治療,將對患者的生活質量造成嚴重影響。目前中西醫結合治療SPID已經在臨床中廣泛使用。研究表明[15],抗生素類西藥治療SPID主要是通過抑制病原菌生長,控制感染及炎癥狀態達到治療效果。中醫學認為SPID是因寒濕之邪內侵入體,導致濕熱、痰濁、血瘀之邪蘊結于胞宮,引起沖任帶脈功能失調。其病機為濕熱瘀阻及氣虛血瘀,所以中醫的治療策略為活血化瘀[16]。
本研究所用中藥組方中川芎、丹參活血化瘀通絡;敗醬草、蒲公英、甘草清熱解毒;山萸肉、透骨草抑菌殺菌。中藥保留灌腸法可使藥物在腸黏膜處吸收,快速到達盆腔并形成高濃度藥效[17]。蒸熱療法有助于藥物進入炎癥組織,具有改善局部新陳代謝的作用,在日常護理中被廣泛采用。本研究采用兩種療法配合常規口服西藥治療SPID,結果顯示,與對照組相比,觀察組病理改變更為明顯,證候積分降低更明顯,總有效率更高,治療后觀察組NHP評分明顯低于對照組。提示相比常規西藥治療,配合中藥保留灌腸聯合蒸熱法治療SPID效果更為顯著,更有利于改善患者生活質量。
金銀花、板藍根、大青葉可提高機體免疫功能[18-19]。SPID的發病機制是病原菌的直接侵害導致的免疫反應異常和慢性炎癥反應。Th17和Treg細胞屬于CD4+T細胞亞群,二者在生理功能上相互制約,共同參與調節機體免疫反應[20]。Th17細胞是新發現的輔助性淋巴細胞亞群,因分泌細胞因子IL-17而命名,在SPID的發病及黏膜組織修復過程中發揮重要作用。IL-17可誘導IL-6、GM-CSF等基因的表達從而增強TNF-α介導的炎癥反應,還可通過刺激巨噬細胞釋放促炎因子,加重SPID的炎性水平。在正常的盆腔內,Foxp3表達增強,T細胞趨于向Treg細胞方向分化,維持免疫耐受。當盆腔上皮出現障礙時,樹突狀細胞產生RORγt,誘導T細胞向Th17細胞分化,可誘導盆腔的炎癥反應[21]。因此Th17/Treg的免疫平衡在SPID發病過程中扮演重要角色。本研究發現,治療后兩組患者IL-17、RORγt mRNA及RORγt/Foxp3比值均明顯降低,IL-10、TGF-β、Foxp3 mRNA均明顯升高,觀察組明顯優于對照組。說明以中藥保留灌腸聯合蒸熱法治療SPID的機制可能是通過調節RORγt、Foxp3的表達及IL-17、IL-10和TGF-β的水平促進Th17/Treg的免疫平衡實現的。
綜上所述,中藥保留灌腸聯合蒸熱法可提高常規西藥治療SPID的療效,有助于改善患者預后及生活質量,且安全性高,治療機制可能與改善血液循環及促進機體Th17/Treg的免疫平衡有關。

