經皮撬拔閉合復位空心釘內固定術治療跟骨sandersⅡ、Ⅲ型骨折
陳昌斌, 龍丁柏, 陳興強
(瓊海市人民醫院創傷外科, 海南省瓊海市 571400)
跟骨骨折是骨科最常見的跗骨骨折類型,因跟骨解剖結構的特殊性及復雜性,目前跟骨骨折在分型、治療及預后評估方面難以達到統一標準[1]。特別對于骨SandersⅡ、Ⅲ型骨折,可能導致患者后期嚴重的足踝功能障礙[2]。隨著對跟骨骨折知識的不斷深入及影像學的不斷發展,骨SandersⅡ、Ⅲ型骨折患者多傾向于手術治療,但術式選擇尚無統一標準[3]。本文采用經皮撬撥閉合復位空心釘內固定術治療骨SandersⅡ、Ⅲ型骨折療效滿意,現報道如下。
1 資料和方法
1.1 研究對象
回顧性選取本院2017年4月—2018年10月住院手術的跟骨SandersⅡ、Ⅲ型骨折患者90例。根據手術方式不同分為兩組。對照組45例采用切開復位鋼板內固定治療,男27例,女18例,年齡22~69歲,平均(41.17±4.27)歲;受傷至醫院就診時間2~8 h,平均(4.16±0.35) h;致傷原因墜落傷13例,交通傷19例,摔傷4例,壓砸傷5例,其他原因4例;跟骨Sanders分型Ⅱ型28例,Ⅲ型17例。觀察組45例采用皮撬撥閉合復位空心釘內固定術治療,男29例,女16例,年齡22~70歲,平均(41.42±4.14)歲;受傷至醫院就診時間1~8 h,平均(4.08±0.46) h;致傷原因交通傷18例,墜落傷12例,摔傷4例,壓砸傷7例,其他原因4例;骨折Sanders分型Ⅱ型29例,Ⅲ型16例。
納入標準:①X線確診單側跟骨骨折Sanders分型SanderⅡ型和Ⅲ型;②新鮮閉合性骨折,受傷至手術時間≤1周;③性別不限,年齡22~70歲,病例資料完整;④無嚴重心臟、肺、肝腎等臟器損傷。排除標準:①存在嚴重精神疾病,治療過程中無法進行正常溝通;②合并傳染疾病、嚴重血液疾病、惡性腫瘤;③影像學檢查提示病理性骨折或者陳舊性骨折;④合并骨折周圍神經損傷;⑤嚴重骨質疏松;⑥既往有跟部手術史;⑦哺乳期或妊娠期特殊人群。
1.2 經皮撬拔閉合復位空心釘內固定術
觀察組患者取側臥位或者健側臥位,患肢常規術區消毒鋪巾,在C 型臂X線機透視下,于跟腱附著處內外側緣進針,用電鉆穿入1~2枚4.0斯氏針,進針方向與跟骨縱軸成50°~70°角,透視下見針進入距下關節面塌陷或者翻轉骨折塊中,進針深度不超過骨折線。術者一手握住撬撥針盡量向足鼎方向扳牽,一手握住前足盡量跖屈,由輕至重反復多次使塌陷的骨折板塊上抬以至恢復關節平面的平整及C型臂透視下Bohler角在20°~40°之間。隨后助手雙手交叉環抱,兩掌心相對用力擠壓跟骨兩側,糾正跟骨向外側膨隆移位,恢復跟骨高度39~44 mm、寬度25~34 mm及跟骨軸線。利用C型臂透視,如果Bohler角和Gissane角恢復,折端對位良好,則讓助手以跟骨結節為進針點,將1枚直徑3.5 mm斯氏針向距骨方向鉆入,但不能進入距下關節,再以跟骨上下結節中點為進針點,與跟骨縱軸向外側傾斜10°左右,鉆入第二枚導針,經骨折線,固定于跟骨前方關節面下。用C形臂線機攝片進行側位觀察,確認跟骨形態及關節面復位滿意后,空心釘內固定,手術完成后還需對傷口采取常規方式進行沖洗,逐層縫合切口,無菌包扎。
1.3 手術情況的觀察
術后所有患者均隨訪12月,定期復查,記錄兩組手術時間、術中失血量、術后24 h引流量、住院時間及骨折愈合時間[4]。
1.4 影像學評價指標
兩組患者術前、術后5天行標準正側位X線片、CT檢查,測量并記錄跟骨寬度和高度、Bolher角、Gissane角等指標,跟骨寬度正常25~34 mm,跟骨高度正常39~44 mm,Bolher角正常25°~40°,Gissane角正常120°~145°。
1.5 臨床療效評價指標
①術前、術后7天、1年疼痛評估,采用VAS疼痛視覺模擬評分標準[5]:紙上面劃一條10 cm長的橫線,橫線的一端開始到另外一段標記從0~10,0表示無痛,10表示劇痛;兩者之間部分用1~9作標記表示不同程度的疼痛。患者根據自我疼痛感覺在線上標記。②術前、術后1年足部功能評分,采用Maryland足踝功能評分[6],總分為100分,分為4個等級,即優為90~100分;良為75~90分;可為50~75分;差為<50分。
1.6 兩組并發癥發生情況
包括切口異常、創傷性關節炎、皮緣壞死、足跟痛等。
1.7 統計學方法
數據采用SPSS 21.0軟件進行分析,組間計量資料采用t檢驗,多個時間點之間的比較采用重復測量方差分析,計數資料采用χ2檢驗,P<0.05為差異具有統計學意義。
2 結 果
2.1 兩組手術情況比較
觀察組患者手術時間、住院時間較對照組明顯縮短,術中出血量、術后24 h引流量明顯減少(P<0.05;表1)。

表1 兩組手術情況比較
2.2 兩組影像學評價指標比較
兩組患者術后5天Bohler角、Gussane角、跟骨寬度、跟骨高度均較術前明顯改善(P<0.05);兩組患者術前、術后5天Bohler角、Gussane角、跟骨寬度、跟骨高度比較差異無顯著性(P>0.05;表2)。

表2 兩組影像學評價指標比較
2.3 兩組VAS評分比較
兩組患者術后7天、術后1年VAS評分較術前顯著降低,術后1年VAS較術后7天也明顯降低(P<0.05);術后隨訪1年發現觀察組VAS評分顯著低于對照組(P<0.05;表3)。

表3 兩組VAS評分比較 單位:分
2.4 兩組Maryland足踝功能評分比較
對照組Maryland足踝功能評分優良率較觀察組顯著升高(P<0.05;表4)。
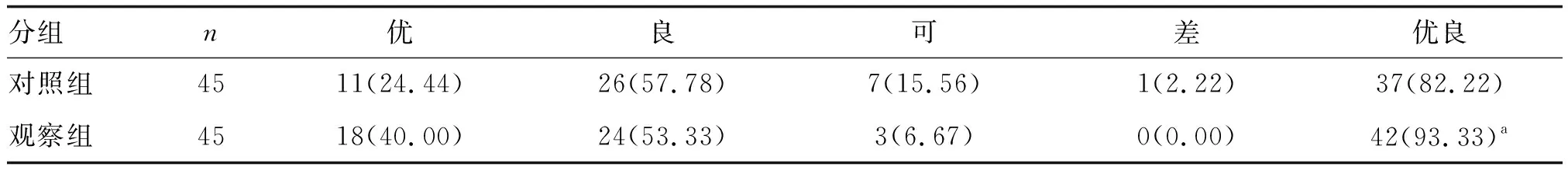
表4 兩組Maryland足踝功能評分比較 單位:例(%)
2.5 兩組并發癥發生率比較
隨訪期間對照組并發癥總發生率顯著高于觀察組(P<0.05;表5)。
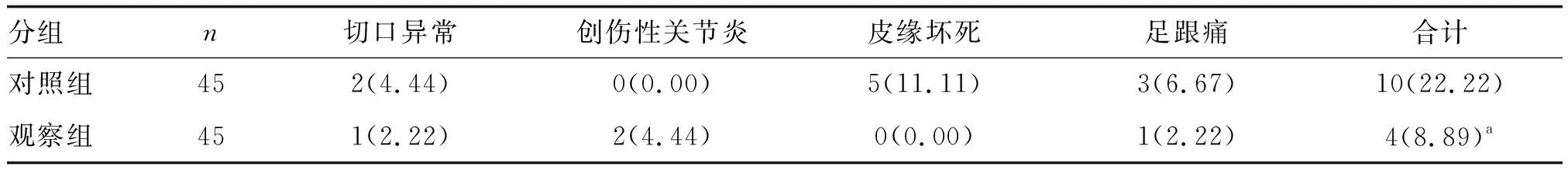
表5 兩組隨訪期間并發癥發生率比較 單位:例(%)
3 討 論
跟骨骨折多為高處墜落傷及高能量暴力損傷,因骨折部位解剖特點和損傷機制,復位及固定難度大,部分患者即使經過治療,依然出現持續的關節疼痛和功能障礙,是致殘的主要原因[7]。目前手術治療是骨sandersⅡ、Ⅲ型骨折治療的主要方法,手術重點在于恢復關節面平整和關節的對應關系,糾正跟骨內外翻畸形,主要的手術方式包括切開復位鋼板內固定、經皮閉合復位空心釘內固定術、外固定架及關節融合術等,其中經皮撬拔閉合復位空心釘內固定術應用最為廣泛,具有操作簡便、手術創傷小、術后恢復快等優勢[8]。
本研究結果發現,經皮撬拔閉合復位空心釘內固定術治療骨sandersⅡ、Ⅲ型骨折手術創傷更小,術中流血量更小,能夠最大程度保留骨折端周圍軟組織,術后恢復更快,跟骨活動性更好,縮短了住院時間;而切開復位鋼板內固定術對患者造成的創傷更大,術中失血量明顯增多,術后傷口愈合較差,時常出現比較多的滲血,延長了住院時間。此外,術后5天對所有患者復查正側位X線光片、CT檢查等相關檢查,評估骨折復位情況,結果發現,兩組患者術后5天Bohler角、Gussane角、跟骨寬度、跟骨高度均較術前明顯改善,說明經皮微創撬撥復位空心釘內固定術在骨折復位、矯正畸形方面效果穩定而且顯著,經皮微創撬撥復位空心釘內固定術對骨折端血運的破壞小,術中無需掀起皮瓣,保護了足部皮膚,降低了術后切口異常、皮緣壞死、足跟痛等并發癥發生率,說明經皮微創撬撥復位空心釘內固定術安全可靠[9]。本研究還發現兩組患者術后7天、術后1年VAS評分較術前顯著降低,術后1年VAS較術后7天也明顯降低;其原因是因為兩組患者術后7天內均介意臥床休息,疼痛程度并未表現出明顯差異。術后隨訪1年發現觀察組VAS評分顯著低于對照組,可能與術后關節活動延遲,關節面復位欠佳有關[10]。經皮撬拔閉合復位空心釘內固定術與切開復位鋼板內固定術干預跟骨骨折患者預后Maryland足踝功能評分優良率方面差異無顯著性。經皮撬拔閉合復位空心釘內固定術治療骨SandersⅡ、Ⅲ型骨折患者預后Maryland足踝功能評分優良率顯著高于傳統切口復位鋼板內固定術。結果表明,經皮撬拔閉合復位空心釘內固定術較切開復位鋼板內固定術更加微創和便利,有助于骨SandersⅡ、Ⅲ型骨折患者術后足踝功能的快速康復[11]。
綜上所述,在骨sandersⅡ、Ⅲ型骨折Bohler角、Gussane角、跟骨寬度、跟骨高度恢復方面,經皮撬拔閉合復位空心釘內固定術能達到切開復位鋼板內固定術相似的效果,不僅可以有效減少術中出血量、術后引流量、縮短住院時間等,且在改善遠期疼痛、足踝功能方面效果更顯著,安全可靠,具有較高的臨床應用價值,可在廣大基層醫院推廣應用。

