缺氧后適應(yīng)中HSP70對(duì)心肌細(xì)胞TLR4/NF-κB信號(hào)通路及免疫炎性損傷的影響
黃政,涂榮會(huì),鐘國(guó)強(qiáng),方存明,馬小林,胡學(xué)俊
(1.宣城市人民醫(yī)院 心血管內(nèi)科,宣城 242000;2.廣西醫(yī)科大學(xué)第一附屬醫(yī)院 心內(nèi)科,南寧 530022)
缺氧后適應(yīng)(hypoxic postconditioning,HPC)是減輕心肌缺血-再灌注損傷的有效方法,其機(jī)制可能與抑制免疫炎癥反應(yīng)有關(guān)[1]。近年來(lái)的研究發(fā)現(xiàn),TLR4/NF-κB信號(hào)通路在缺血-再灌注后的心肌免疫炎性損傷中發(fā)揮重要作用[2],積極干預(yù)TLR4/NF-κB信號(hào)通路可能是減輕心肌缺血-再灌注損傷的新靶點(diǎn)。熱休克蛋白70(heat shock protein 70,HSP70)對(duì)損傷的心肌細(xì)胞具有免疫調(diào)節(jié)作用,表現(xiàn)為細(xì)胞內(nèi)HSP70能夠與NF-κB結(jié)合,抑制NF-κB下游炎性蛋白基因的轉(zhuǎn)錄。另外,細(xì)胞內(nèi)HSP70也可對(duì)TLR4介導(dǎo)的炎癥反應(yīng)發(fā)揮負(fù)調(diào)節(jié)作用。缺血預(yù)適應(yīng)以及某些藥物可通過(guò)上調(diào)HSP70表達(dá)減輕心肌缺血-再灌注損傷[3-4]。HPC的心肌保護(hù)作用是否與TLR4/NF-κB信號(hào)通路以及HSP70表達(dá)有關(guān),目前鮮見(jiàn)報(bào)道。本研究通過(guò)建立心肌細(xì)胞缺氧/復(fù)氧(hypoxia/reoxygenation,H/R)損傷模型,實(shí)施HPC,體外模擬心肌HPC,從細(xì)胞水平探討HPC對(duì)HSP70、TLR4/NF-κB信號(hào)通路以及心肌細(xì)胞免疫炎性損傷的作用及其機(jī)制。
1 材料與方法
1.1 材料H9C2心肌細(xì)胞系購(gòu)自中國(guó)科學(xué)院上海細(xì)胞庫(kù)。DMEM培養(yǎng)液、FBS購(gòu)自Gibco公司,槲皮素(quercetin,Quer)購(gòu)自北京索萊寶科技公司,大鼠HSP70、TLR4、NF-κB p65、TNF-α、IL-1β、IL-6、、B淋巴細(xì)胞瘤2基因(B-cell lymphoma 2,Bcl-2)、Bcl-2相關(guān)蛋白(Bcl-2-associated X protein,Bax)、Caspase-3、β-actin抗體購(gòu)自北京博奧森生物科技有限公司,Hoechst 33242染色試劑盒購(gòu)自上海碧云天生物技術(shù)有限公司,Annexin Ⅴ-FITC細(xì)胞凋亡檢測(cè)試劑盒購(gòu)自江蘇凱基生物技術(shù)公司。
1.2 方法
1.2.1 細(xì)胞處理及分組 用含10%FBS的DMEM高糖培養(yǎng)液培養(yǎng)H9C2心肌細(xì)胞,置于37 ℃、5% CO2、95%空氣的培養(yǎng)箱中;細(xì)胞缺氧培養(yǎng)時(shí)更換為DMEM無(wú)糖培養(yǎng)液,置于含5% CO2、95% N2混合氣體的厭氧罐中;細(xì)胞復(fù)氧培養(yǎng)時(shí)再次更換為DMEM高糖培養(yǎng)液,置于37 ℃、5% CO2、95%空氣的培養(yǎng)箱中。按照不同處理方式將細(xì)胞分為4組:(1)對(duì)照組(常氧培養(yǎng)10 h);(2)H/R組(缺氧4 h后復(fù)氧6 h);(3) HPC組(缺氧4 h后行復(fù)氧5 min/缺氧5 min,共3次,再?gòu)?fù)氧6 h);(4)HPC+ Quer組(缺氧前1 h加50 μmol/L的HSP70抑制劑Quer后行HPC)。
1.2.2 Hoechst 33242染色觀察細(xì)胞形態(tài) 取處于對(duì)數(shù)生長(zhǎng)期的細(xì)胞接種于細(xì)胞爬片上,培養(yǎng)至約80%融合時(shí)進(jìn)行分組處理。處理結(jié)束后棄去培養(yǎng)液,用PBS漂洗后加入4%多聚甲醛,室溫固定10 min,再加入終濃度為10 μg/mL的Hoechst 33242染色液,避光染色5 min后加入抗熒光淬滅封片劑,在熒光顯微鏡下觀察細(xì)胞形態(tài)。
1.2.3 FACS檢測(cè)細(xì)胞凋亡情況 用胰蛋白酶消化各組細(xì)胞,離心后收集細(xì)胞,用預(yù)冷的PBS漂洗2次,加入適量的1×結(jié)合緩沖液輕輕吹打重懸細(xì)胞,調(diào)整細(xì)胞密度為1×109個(gè)/L,取100 μL細(xì)胞懸液加入5 μL Annexin Ⅴ-FITC,混勻,室溫孵育15 min。再加入5 μL 碘化丙啶(propidium iodide,PI)染色,用FACS檢測(cè)細(xì)胞的凋亡情況。
1.2.4 Western blotting檢測(cè)蛋白的表達(dá) 將各組細(xì)胞加至RIPA裂解液中冰上裂解30 min,以16 660×g離心10 min后取上清液。采用二喹啉甲酸(bicinchoninic acid,BCA)法測(cè)定蛋白濃度。取40 μg蛋白上樣,SDS-PAGE后將蛋白轉(zhuǎn)移至PVDF膜上,用5%脫脂牛奶室溫封閉2 h,加入一抗溶液(1∶1 000)4 ℃孵育過(guò)夜,再加入二抗溶液室溫孵育1 h。經(jīng)洗滌、顯影、灰度掃描后,用Odyssey 3.0軟件對(duì)蛋白條帶進(jìn)行灰度值測(cè)定。蛋白質(zhì)的表達(dá)量以目的條帶與β-actin的灰度比值表示。
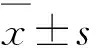
2 結(jié)果
2.1 HPC對(duì)心肌細(xì)胞HSP70表達(dá)的影響與對(duì)照組比較,H/R組HSP70表達(dá)水平顯著升高(P<0.05),HPC組HSP70表達(dá)水平較H/R組進(jìn)一步升高(P<0.05),而HPC+Quer組HSP70表達(dá)水平較HPC組顯著下降(P<0.05,圖1)。

注: A. Western blotting檢測(cè)HSP70蛋白的表達(dá);B.各組細(xì)胞HSP70蛋白相對(duì)表達(dá)量的比較。與對(duì)照組比較,* P<0.05;與H/R組比較,#P<0.05;與HPC組比較,△P<0.05。圖1 各組細(xì)胞HSP70蛋白表達(dá)水平的比較
2.2 HPC中HSP70對(duì)心肌細(xì)胞凋亡的影響Hoechst 33242染色結(jié)果顯示, 對(duì)照組細(xì)胞核形態(tài)正常,呈圓形或橢圓形,淡藍(lán)色,未見(jiàn)凋亡細(xì)胞;H/R組可見(jiàn)較多細(xì)胞核呈致密濃染或呈碎塊狀致密濃染、顏色發(fā)白的凋亡細(xì)胞;HPC組凋亡細(xì)胞較H/R組減少;HPC+Quer組凋亡細(xì)胞較HPC組增多(圖2)。

圖2 Hoechst 33242 染色觀察細(xì)胞形態(tài)變化(×200)
與Hoechst 33242染色結(jié)果一致,F(xiàn)ACS檢測(cè)結(jié)果顯示,H/R組細(xì)胞凋亡率[(61.9±1.8)%]較對(duì)照組[(8.6±0.2)%]顯著增加(P<0.05);HPC組細(xì)胞凋亡率[(26.6±1.3)%]較H/R組[(61.9±1.8)%]顯著減少(P<0.05);而HPC+Quer組細(xì)胞凋亡率[(54.8±1.4)%]較HPC組[(26.6±1.3)%]顯著增加(P<0.05,圖3)。

注: A.FACS檢測(cè)心肌細(xì)胞凋亡情況;B.各組心肌細(xì)胞凋亡率的比較。與對(duì)照組比較,*P<0.05;與H/R組比較,#P<0.05;與HPC組比較,△P<0.05。圖3 FACS檢測(cè)心肌細(xì)胞凋亡情況
2.3 HPC中HSP70對(duì)TLR4、NF-κB p65表達(dá)的影響H/R組TLR4、NF-κB p65表達(dá)水平較對(duì)照組顯著升高(P<0.05);HPC組TLR4、NF-κB p65表達(dá)水平較H/R組顯著下降(P<0.05);而HPC+Quer組TLR4、NF-κB p65表達(dá)水平較HPC組顯著升高(P<0.05,圖4)。
2.4 HPC中HSP70對(duì)炎性因子表達(dá)的影響H/R組TNF-α、IL-1β、IL-6 表達(dá)水平顯著高于對(duì)照組(P<0.05);HPC組TNF-α、IL-1β、IL-6表達(dá)水平顯著低于H/R組(P<0.05);而HPC+Quer組TNF-α、IL-1β、IL-6表達(dá)水平顯著高于HPC組(P<0.05,圖5)。

注: A. Western blotting檢測(cè)TNF-α、IL-1β、IL-6蛋白的表達(dá);B.各組TNF-α、IL-1β、IL-6蛋白相對(duì)表達(dá)量的比較;與對(duì)照組比較,*P<0.05;與H/R組比較,#P<0.05;與HPC組比較,△P<0.05。圖5 各組心肌細(xì)胞TNF-α、IL-1β、IL-6蛋白表達(dá)水平的比較
2.5 HPC中HSP70對(duì)凋亡相關(guān)蛋白表達(dá)的影響H/R組Bcl-2表達(dá)水平顯著低于對(duì)照組(P<0.05),Bax、Caspase-3表達(dá)水平顯著高于對(duì)照組(P<0.05)。HPC組Bcl-2表達(dá)水平顯著高于H/R組(P<0.05),Bax、Caspase-3表達(dá)水平顯著低于H/R組(P<0.05)。而HPC+Quer組Bcl-2表達(dá)水平顯著低于HPC組(P<0.05),Bax、Caspase-3表達(dá)水平顯著高于HPC組(P<0.05)。詳見(jiàn)圖6。
3 討論
本研究通過(guò)建立心肌細(xì)胞H/R損傷模型,并應(yīng)用HSP70抑制劑Quer干預(yù),從細(xì)胞水平探討HPC中HSP70對(duì)TLR4/NF-κB信號(hào)通路及炎性因子表達(dá)的影響。結(jié)果顯示,HPC在顯著上調(diào)心肌細(xì)胞HSP70表達(dá)的同時(shí),抑制TLR4、NF-κB p65及炎性因子TNF-α、IL-1β、IL-6表達(dá),減輕H/R誘導(dǎo)的心肌細(xì)胞損傷和凋亡,而應(yīng)用HSP70抑制劑Quer后上述效應(yīng)被減弱。本研究結(jié)果提示,HPC可能通過(guò)HSP70抑制TLR4/NF-κB信號(hào)通路,減輕H/R誘導(dǎo)的心肌細(xì)胞免疫炎癥損傷。
心肌缺血-再灌注損傷的發(fā)生并不少見(jiàn)。缺血心肌血流恢復(fù)后可產(chǎn)生不同程度的心肌結(jié)構(gòu)改變以及細(xì)胞凋亡、壞死加重,這些改變?cè)谂R床上難以被常規(guī)手段檢測(cè)到,容易被忽略。因此,預(yù)防和減輕缺血-再灌注損傷對(duì)進(jìn)一步改善再灌注治療患者的預(yù)后具有重要意義。
HSP是細(xì)胞在應(yīng)激狀態(tài)下新合成或合成增加的一組保護(hù)性蛋白,主要功能是協(xié)助蛋白質(zhì)的正確折疊、復(fù)性和移位,從而維持細(xì)胞結(jié)構(gòu)、功能穩(wěn)定。研究發(fā)現(xiàn),氧化應(yīng)激、鈣超載均可誘導(dǎo)HSP70表達(dá),后者通過(guò)其分子伴侶作用維護(hù)客戶蛋白的穩(wěn)定,維持細(xì)胞內(nèi)外鈣離子平衡,減輕細(xì)胞氧化應(yīng)激損傷[5-6]。HSP70也可通過(guò)Fas、JNK等信號(hào)轉(zhuǎn)導(dǎo)通路抑制凋亡相關(guān)蛋白(如AIF、eEF2等)的表達(dá),減少心肌細(xì)胞凋亡[7-9]。通過(guò)缺血預(yù)處理、藥物等手段誘導(dǎo)HSP70表達(dá)可減少缺血-再灌注動(dòng)物模型的心肌細(xì)胞凋亡,減小心肌梗死面積,改善心臟功能[6,10]。本研究發(fā)現(xiàn),HPC在上調(diào)HSP70的同時(shí)顯著抑制促凋亡蛋白Bax、Caspase-3的表達(dá),增加抗凋亡蛋白Bcl-2表達(dá),顯著減少H/R誘導(dǎo)的心肌細(xì)胞凋亡,而應(yīng)用HSP70抑制劑Quer后這種效應(yīng)被減弱,提示HPC抑制心肌細(xì)胞凋亡的機(jī)制可能與其上調(diào)HSP70表達(dá)有關(guān)。
需要指出的是,Quer是一種具有多種生物活性的化合物,其藥理作用包括抗脂質(zhì)過(guò)氧化、抑制腫瘤細(xì)胞增殖、抗菌、抗炎、抗過(guò)敏、降血壓、改善內(nèi)皮功能等。雖然Quer不是HSP70特異性抑制劑,但因其無(wú)細(xì)胞毒性而被作為HSP70抑制劑廣泛用于各種心血管疾病的研究[11-13]。Song等[14]在大鼠離體心肌細(xì)胞和在體心臟的研究中發(fā)現(xiàn),采用p38 MAPK抑制劑SB203580預(yù)處理可顯著減輕大鼠心肌細(xì)胞H/R和心肌缺血-再灌注損傷,采用shRNA敲除HSP70基因則顯著加重大鼠心肌細(xì)胞H/R和心肌缺血-再灌注損傷,而應(yīng)用Quer可以達(dá)到與敲除HSP70基因類似的效果。本研究同樣采用Quer作為抑制劑干預(yù)HSP70表達(dá),所得結(jié)果與文獻(xiàn)報(bào)道[11]一致。
目前已證實(shí),TLR在介導(dǎo)心、腦、腎等器官的缺血-再灌注損傷過(guò)程中發(fā)揮重要作用[15-17]。TLR4是重要的PRR,在心肌組織中高表達(dá)。心肌缺血-再灌注損傷時(shí)氧化應(yīng)激、鈣超載、炎癥反應(yīng)等導(dǎo)致心肌細(xì)胞結(jié)構(gòu)、功能受損,受損細(xì)胞釋放的損傷相關(guān)分子模式或內(nèi)源性配體可被TLR4識(shí)別,激活TLR4介導(dǎo)的免疫應(yīng)答,使心肌細(xì)胞成為自身免疫系統(tǒng)攻擊的靶標(biāo)。有研究發(fā)現(xiàn),TLR4通過(guò)上調(diào)Bax、Caspase-3表達(dá)并下調(diào)Bcl-2表達(dá),促進(jìn)新生大鼠H/R心肌細(xì)胞凋亡[18]。HSP70在TLR4介導(dǎo)的免疫應(yīng)答過(guò)程中發(fā)揮重要作用。細(xì)胞外HSP70可作為T(mén)LR4的配體,激活TLR4介導(dǎo)的免疫應(yīng)答,而細(xì)胞內(nèi)HSP70則通過(guò)TLR4、NF-κB等信號(hào)通路抑制免疫應(yīng)答[11,19]。本研究發(fā)現(xiàn),HPC在上調(diào)細(xì)胞內(nèi)HSP70的同時(shí)顯著抑制TLR4表達(dá),并減少H/R誘導(dǎo)的心肌細(xì)胞凋亡,而應(yīng)用HSP70抑制劑Quer后這種效應(yīng)被減弱,提示HPC中HSP70可能通過(guò)抑制TLR4活化參與對(duì)缺血-再灌注心肌細(xì)胞的保護(hù)。
炎癥反應(yīng)是心肌缺血-再灌注損傷發(fā)生的重要機(jī)制之一。TLR4/NF-κB是經(jīng)典的炎癥反應(yīng)信號(hào)轉(zhuǎn)導(dǎo)通路,其激活后可促進(jìn)下游炎性因子如TNF-α、IL-1、IL-6等表達(dá),而這些炎性因子又能誘導(dǎo)靶細(xì)胞凋亡、壞死、血管內(nèi)皮功能紊亂[20-22]。本研究發(fā)現(xiàn),HPC在上調(diào)HSP70并抑制TLR4表達(dá)的同時(shí),顯著減少NF-κB p65表達(dá),NF-κB的下游蛋白TNF-α、IL-1β、IL-6表達(dá)也顯著減少,提示HPC減輕炎癥反應(yīng)的機(jī)制可能與其抑制TLR4/NF-κB信號(hào)轉(zhuǎn)導(dǎo)通路有關(guān)。事實(shí)上,缺血-再灌注時(shí)TLR4/NF-κB信號(hào)通路激活的始動(dòng)因素是細(xì)胞結(jié)構(gòu)和功能的損傷,而HPC通過(guò)上調(diào) HS70表達(dá)以及其他機(jī)制減輕了細(xì)胞損傷和凋亡,從上游阻斷了TLR4/NF-κB信號(hào)通路的激活。
綜上所述,本研究顯示HPC通過(guò)上調(diào)HSP70表達(dá)減輕H/R誘導(dǎo)的TLR4/NF-κB信號(hào)通路活化,減輕心肌細(xì)胞免疫炎性損傷和凋亡。本研究結(jié)果是對(duì)HPC心肌保護(hù)作用機(jī)制的新補(bǔ)充。

