電化學耦合陰極二氧化碳還原與陽極氧化合成
葛睿,胡旭,董靈玉,李丹,郝廣平
(大連理工大學化工學院,精細化工國家重點實驗室,遼寧省低碳資源高值化利用重點實驗室,遼寧 大連 116024)
近年來,大氣中二氧化碳(CO2)濃度持續上升(目前已超過410cm3/m3),溫室效應問題引起廣泛關注,“碳中和”倡議得到全球各政府的響應。例如,我國提出CO2排放力爭2030年前達到“碳達峰”,2060 年前實現“碳中和”。電催化二氧化碳還原(CO2RR)得到高值化學品被認為是一種具有潛力的“碳中和”手段,既能滿足碳減排要求,又能以可持續的電能實現CO2的資源化[1]。然而,CO2是線性對稱型分子,化學性質穩定,標準摩爾生成焓為-394.4kJ/mol,因此要實現CO2活化,通常需要強電子供體、有效催化劑及高能量輸入[2-5]。此外,CO2RR反應是一個多質子耦合、多電子轉移的過程,反應路徑復雜,反應中間體及產物種類多樣,目標產物的選擇性較低[6-7]。雖然科研人員從催化劑的開發、電解液的篩選和電解池結構的設計三個方面對CO2RR 性能進行了優化[8-11],但較低的能量轉換效率仍然是限制電催化CO2RR 實際應用的技術壁壘。
通常,與陰極電催化CO2RR 對應的陽極反應是析氧反應(OER),由于動力學限制,起始電位較高,電解槽電壓較大(通常>3V),OER 能源消耗占總能量輸入的90%[12-13]。此外,OER 產物氧氣商業價值低,副產物活性氧(ROS)會降解電解槽膜,影響系統的穩定性[14]。因此采用熱力學上可行、動力學上有利的氧化反應取代OER,構建電催化CO2RR 與氧化合成反應耦合的電化學體系近年來成為研究熱點。目前與CO2RR 耦合的陽極反應主要有兩類:①氯陽極,革新氯堿工業;②有機物氧化陽極,生成高附加值化學品,或者用于降解污染物,修復生態環境。通過將CO2RR 與這些陽極電氧化反應耦合,電解體系可以實現低槽壓,同時在陰陽極得到高值化學品,達到更大的能量轉換效率[15]。基于此,本文首先介紹了近年來CO2RR耦合氧化合成體系在電解裝置和陰陽極催化劑這兩方面的最新進展,并總結比較了目前CO2RR 與氯堿過程、醇類和含氮有機物氧化等典型陽極氧化合成反應耦合的性能。最后,對當前面臨的挑戰和未來的研究趨勢進行了展望。希望對陰極電催化CO2RR與陽極電氧化合成耦合研究及應用起到一定的推動作用。
1 耦合電催化研究進展
1.1 耦合電催化電解裝置
1.1.1 電解池構型
目前,用于CO2RR 與陽極電氧化合成耦合體系的電解裝置主要有H型電解池和流動型電解池兩類。在H型電解池中,陰極側CO2以鼓泡的形式進入電解液,之后擴散至催化劑與電解液界面上發生反應。陰陽兩室之間通過離子交換膜或者多孔隔膜隔開,因而陰陽兩極所用的電解液種類及濃度可根據反應需求確定。此外,H型電解池結構簡單,設備成本低,操作方便,可實現長時間穩定運行。目前,H型電解池已用于CO2RR與陽極電氧化的耦合反應體系[15]。例如,Llorente 等[16]利用H 型電解池,將CO2RR 反應與丁香醛、鄰苯二胺縮合反應進行耦合,電解2h 后陰極法拉第效率(FE)達100%,丁香醛氧化縮合產物經分離純化后,收率為65%。Sabatino 等[17]將CO2RR 反應和陽極氧化2-萘酚偶氮對苯磺酸鈉(酸性橙7,AO7)進行耦合,陰極使用錫陰極將CO2RR 為甲酸,陽極利用摻硼金剛石實現AO7的氧化,結果表明產甲酸的最佳pH為4,降解AO7的最佳pH為3~7。
CO2本身在電解液中溶解度低,在液相中傳質速度較慢,導致反應電流密度較低,難以滿足工業化水平。因此,為實現CO2RR 耦合反應從實驗室到工業應用的跨越,需設計更為合理的電解池構型來滿足生產需要。為解決H型電解池中電流密度過低的問題,科研人員研發了流動型電解池。反應所需原料氣直接經催化劑背面的微孔層以氣態的形式擴散至催化劑與電解液相界面上發生反應,實現氣液傳質分離。原料氣供給充足,大大提高了反應速率,反應電流密度可由H型電解池中的毫安級提高至安級。這類電解池結構同樣有助于CO2RR 耦合實現大電流密度,以滿足工業化要求。常見的流動型電解池結構見圖1[18]。
單室微流控反應器陰陽兩極之間無隔膜,共用同一種電解液[圖1(a)]。與H 型電解池相比,電流密度明顯提升,但陰陽兩極產生的液相產物可能會擴散至另一極發生反應,對產物定量造成干擾,導致明顯的效率損失。因此,此類電解池并不適用于富產液相產物的電氧化反應。
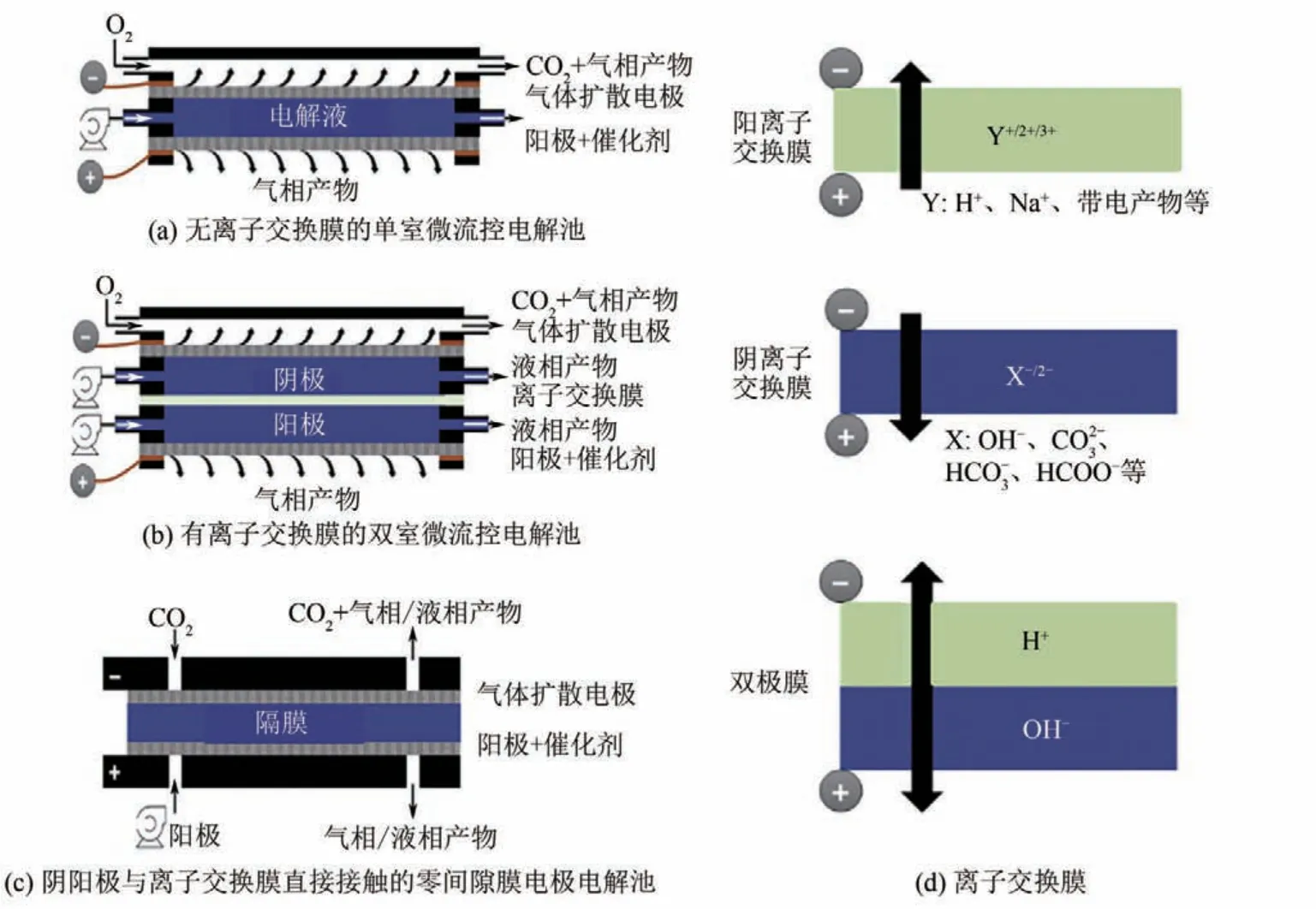
圖1 電解池類型[18]
圖1(b)中展示的電解池利用隔膜分隔形成獨立的陰極室和陽極室,一方面解決了部分產物被分解的問題;另一方面,研究人員可根據陰陽極反應選擇合適的電解液。目前,該類電解池應用更為廣泛,測試效果較為理想。例如,Guo 等[19]利用此類電解池,將CO2RR 反應與析氯反應進行耦合,當電流密度達到100mA/cm2時,槽電壓為3.8V。PéREZ-Gallent 等[20]將流動型電解池用于CO2RR 與1,2-丙二醇電氧化,其中CO2被還原為一氧化碳(CO),1,2-丙二醇被氧化為乳酸。當電流達到150mA 時,槽電壓為2.6V,減少了35%的能源消耗。但該類電解池結構更為復雜,測試難度大大提高。兩種電解質溶液和膜的存在增大了歐姆電勢降,降低了過程的能源效率。
零間隙膜電極(MEA)電解池[圖1(c)]具有陰陽兩極和離子交換膜直接接觸的結構優勢,有利于降低槽電壓,被認為是目前能量效率最高的電解裝置。例如,Xu 等[21]將銅基催化劑負載于聚四氟乙烯(PTFE)上制備膜電極,結合自清潔策略,單個電極能夠穩定運行157h(總持續時間236h),始終保持80%的C2產品選擇性和138mA/cm2的C2分電流密度。Bevilacqua等[22]利用膜電極電解池實現CO2轉化為有用燃料(甲烷、乙烯和甲酸鹽等)的陰極反應與乙醇氧化陽極反應耦合,與OER 相比,能耗降低了40.8%。然而,也正是由于陰陽極直接與離子交換膜接觸,催化劑的局部化學環境僅由膜和催化劑的化學反應以及具體的實驗操作條件決定。設計合理的幾何構型、優化膜電極制備工藝、調整合適的氣體流量、選擇合適的電解溫度及濕度等是電解池穩定運行的關鍵。
綜上所述,流動型電解池的引入,極大地提高了CO2RR 耦合電催化反應的性能,在從實驗室向工業化的過渡中起到了至關重要的推動作用。但目前流動型電解池依舊面臨眾多挑戰,例如,工作電極或催化劑表面疏水性不夠,無法實現裝置在高電流密度情況下長時間穩定運行;當以碳酸氫鹽或堿為電解液時,在高電流密度下進行CO2電解時易出現固體鹽沉積現象,限制了裝置運行的效果;當前CO2RR中CO2利用率很低,很難從實際意義上滿足碳轉化需求。因此,為進一步推進工業化水平,有必要開發更簡單、更節能高效的電解裝置并進行測試工藝條件探究。
1.1.2 高分子電解質膜(PEM)
在電解過程中,產物的分離十分重要。CO2RR耦合OER 時,產物氧氣分離較為容易,但陽極若采用富產液相產物的電氧化合成反應,則還需考慮產物分離問題。PEM 能夠根據反應需要,在陰陽兩極分別使用兩種組成、pH、離子強度均不同的電解質溶液進行CO2RR 耦合,提高目標產物的靈活性,協調離子在兩極間傳輸,減少產品交叉。目前電催化CO2RR 常用的三種離子交換膜[圖1(d)]為陽離子(質子)交換膜(CEMs)[23-24]、陰離子交換膜(AEMs)[25-26]和雙極膜(BPMs)[14,27],每一種膜都有不同的離子傳輸途徑,可以根據電解液的性質(pH、濃度、離子類型)篩選[28]。
CEM(如質子交換膜)促進陽離子從陽極擴散至陰極,使陰極偏酸性環境。特別是在MEA 反應器中,反應速率高,陰極的局部質子濃度很大,會加劇析氫競爭反應,這要求CO2RR 電催化劑在酸性條件下具有良好的活性。為了抑制CEM 的析氫問題,Newman 團隊[29]創造性地在陰極催化劑層和CEM膜之間加入了KHCO3液層,HCO-3 與擴散來的質子結合,調節陰極側化學環境,抑制了析氫競爭反應,CO 的分電流密度達到100mA/cm2,FE 為80%。雖然反應的選擇性得到了提高,但是電解體系穩定性較差,同時,液相產物會跨陽離子交換膜擴散至陽極,降低產率。隨后研究人員將目光轉向AEM。
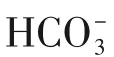
BPM 膜也在CO2RR 流動電解池中有所應用,BPM膜能夠促進水分解,使H+向陰極擴散,OH-向陽極擴散[31],這種機制能夠在電解池陰陽兩極維持恒定的pH,有助于篩選適宜的CO2RR耦合反應[32],但同理,BPM的使用會使陰極定向形成酸性環境,導致陰極析氫競爭加劇,需要陰極電解液緩沖層。2016 年,Mallouk 等[27]在MEA 中使用BPM,加濕的CO2作為原料氣直接與陰極催化劑接觸。BPM的使用提高了CO2RR 的反應活性,BPM 比AEM 或CEM具有更低的電阻(1.7Ω·cm2),且在80mA/cm2下能穩定運行14h。此外,他們還探究了陰極電解液層對CO2RR 的影響。研究表明,在氣相MEA 中,可以獲得高達200mA/cm2的電流密度,說明CO2與催化劑直接接觸可以緩解CO2RR 的質量傳輸限制,避免BPM/陰極界面酸堿中和導致的自由能損失。然而,BPM 膜在反向偏置的情況下,若陰陽極電解液pH 相近,膜電位會增大,從而提高驅動電解所需的電壓,降低了整體能量效率。
離子交換膜組合使用也是改善性能的重要因素。AEM 和CEM 結合使用能夠改變陰陽極的化學環境,對pH敏感的產物起到有效分離作用。例如,受析氫反應的影響,甲酸在高pH(8~11)下FE高,但甲酸多轉化為堿金屬甲酸鹽。為解決甲酸提純困難的問題,Yang等[33]設計了雙離子交換膜電解池,陰極電解產生的甲酸根離子穿過陰極側的AEM,與穿過陽極側CEM 的質子在中心室結合生成甲酸,避免了生產甲酸所需的二次酸化。因此利用離子交換膜的組合,可以實現對不同耦合反應的陰陽極環境調控,提高電解效率。然而CO2RR 耦合反應中兩種不同性質的電解質溶液和膜電阻會增加電解池的電阻,造成槽壓增大、能量效率降低。
1.2 耦合電催化劑
1.2.1 陰極催化劑
利用可再生能源在溫和可控的條件下電催化CO2RR 為有用燃料和化學品是能源化學的重要前沿,具有廣闊的應用前景。其核心挑戰是開發高性能電催化劑,提高目標產物產率和選擇性。CO2電催化材料主要包括以下幾類:①金屬(金、銀、銅、鋅等)[34];②金屬氧化物(氧化錫、氧化亞銅、四氧化三鈷、氧化銀等)[35-36];③共價有機骨架[37]與金屬有機骨架[38];④分子催化劑[39];⑤非貴金屬多孔炭基催化材料[40]。炭基催化材料由于導電性好、孔結構可控、比表面積大、穩定性突出等結構特色,被廣泛認為是一種穩定和豐富的金屬基替代催化材料,而且具有可調節的多孔結構和表面積,能夠調控CO2吸附能力,從而改變CO2RR的選擇性和電流密度[41-42]。與氧還原反應類似,多孔炭材料本身沒有催化CO2RR 活性,需要額外引入活性位點,常用策略是在炭基體中引入雜原子,從而改變相鄰碳原子的電荷分布和自旋密度。下文總結了炭基催化劑中的各種活性位點(圖2)并重點介紹非金屬雜原子摻雜、過渡金屬與氮原子共摻雜多孔炭基催化劑以及多孔炭負載配合物催化劑。
近年來,非金屬雜原子(N、B、S、F)摻雜多孔炭基(如碳纖維、碳納米管、石墨烯、金剛石、納米多孔炭、石墨烯量子點等)催化劑在CO2RR中得到了廣泛應用[43]。CO2RR的活性和選擇性與摻雜劑的類型密切相關,當N 原子與sp2碳骨架中的碳原子結合時,N有四種典型構型[44],即吡啶氮、吡咯氮、石墨氮和氧化氮。實驗和計算結果證明,吡啶氮是CO2RR 生成CO 的活性位點[圖2(a)]。圖2(a)概括了常見的氮摻雜炭基材料的活性位點及其CO2RR 性能,氮摻雜多壁碳納米管(NCNTs)是最早用于CO2RR 研究的非金屬雜原子摻雜多孔炭基催化劑之一,大量研究發現,NCNTs相比于貴金屬,具有較低的過電位和較好的穩定性[45]。Jhong等[46]報道的氮摻雜炭包覆多壁碳納米管納米復合材料在流動池中CO 選擇性達到98%,當電位為-1.46V(vs.Ag/AgCl)時,CO電流密度達到90mA/cm2,比Ag納米催化材料高3.5倍。除了N原子,其他雜原子,如B、S 等摻雜也可提高催化CO2RR活性。Sreekanth等[47]報道了B摻雜的氧化石墨烯(GO)催化CO2RR形成甲酸。當電位為-1.4V(vs.SCE) 時,B 摻 雜GO 生 成 甲 酸 的FE 達 到66%[48]。S摻雜的聚合物基納米多孔炭能夠在-0.6V(vs.RHE)時催化CO2RR,但對CO 的最大FE 僅為2%。基于此,研究者提出利用雙雜原子摻雜來調整氮-碳的局部電子環境。Li 等[49]研究發現,S、N雙摻雜納米孔炭的CO2RR 起始電位低,但在-0.99V(vs.RHE)時,對產物CO的選擇性僅為11.3%。為進一步提高CO 選擇性,Li 等[50]以SiO2為硬模板制備了N、S共摻雜的分級多孔炭,電催化結果表明,N、S 共摻雜有效提高了CO2的催化選擇性,CO 的最大FE為87.8%[51]。需要指出的是,大多數報道的非金屬雜原子摻雜的炭基催化劑樣品實際上在合成過程中引入了微量金屬雜質,一些早期的研究工作由于炭材料中金屬含量低于ICP或其他技術的檢測極限,將炭材料歸類為非金屬催化劑。然而越來越多的研究表明,痕量的殘余金屬具有催化CO2RR的顯著活性[52-53],雖然酸洗可以去除至少95%的金屬,但是被石墨炭殼保護或限制在炭孔內的金屬雜質很難除去。
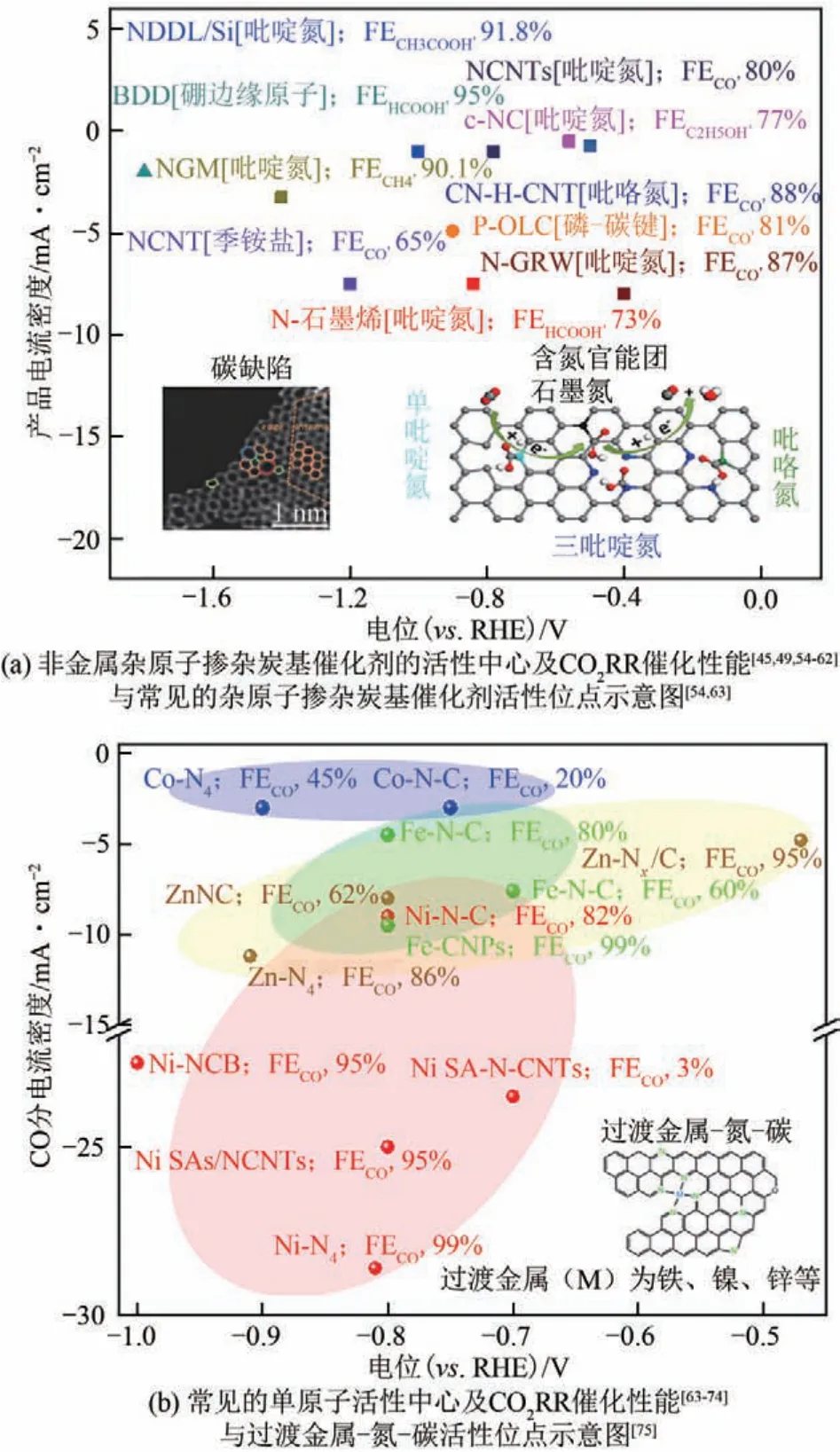
圖2 炭基催化劑中的各種活性位點
炭基催化劑的活性和選擇性還與炭基體的性質緊密相關。碳同素異形體(如無定形炭、金剛石、石墨等)摻雜水平相近,但結構不同,對CO2RR的活性和產物選擇性也不同。例如,氮摻雜石墨烯量子點可以實現CO2RR 生成乙烯,當電壓為-0.75V(vs.RHE)時,乙烯的最大FE達到31%,這是首次報道無金屬炭基催化劑生產乙烯的研究[76]。納米炭材料高溫制備過程中會發生坍塌產生缺陷,也可作為活性位點[圖2(a)]。Daiyan等[77]研究了溫度對氮摻雜介孔炭催化劑中氮含量的影響,觀察到炭化溫度越高,吡啶氮的含量越少,CO2RR的催化性能越好,提出氮物種的減少導致產生缺陷,有利于CO2RR 的設想。然而根據本文作者課題組的研究顯示,隨著溫度的升高,炭基催化劑的石墨化度升高,缺陷會減少,因此需要更多的研究來進一步證實溫度對缺陷位的影響。此外,近年來越來越多的研究人員發現,炭基催化劑的孔結構會明顯影響CO2RR的性能[58,76,78-79],這也是未來研究的一個重點內容。
隨后,單原子催化劑(SAC)因其金屬原子利用率高、催化活性好等優點在材料科學領域受到關注,在CO2RR中具有重要的應用前景。研究發現,過渡金屬與氮原子共摻雜的炭基催化劑(M-Nx-C)中,金屬離子與氮配位形成催化活性位點,可以顯著 提 高CO2RR 活 性[80-81]。圖2(b)概 括 了SAC 在CO2RR 時的活性位點及性能。Varela 等[80]采用聚苯胺衍生炭材料作為CO2RR 催化劑,在-0.55V(vs. RHE)時,CO 選擇性達到80%,還觀察到當在炭結構中引入金屬時,活性增加了8 倍。這表明,盡管含N官能團有一定的貢獻,但金屬中心的活性占主導地位。目前,實驗室中研究最多的、電解效率較好的材料是Ni-N-C,它能夠在低過電勢下高選擇性地將CO2還原為CO,并且CO的分電流密度可達223mA/cm2[64,67-68,82-84]。例如,Zheng 等[67]以商用炭黑顆粒為載體合成了鎳(Ni)單原子催化劑,僅2.7V 時電流密度就達到130mA/cm2,CO 的選擇性接近100%。通過進一步將電極放大到10cm×10cm,電流可以超過8A,CO 選擇性接近99%。此外,Cu-N-C 催化劑可以將CO2轉化為碳氫化合物或醇類,如甲烷、乙烯、乙醇、甲酸鹽等。Guan 等[85]通過氮配位策略合成了銅(Cu)、N摻雜碳納米片的Cu 單原子催化劑,實驗發現,改變熱解溫度可以調節Cu 摻雜濃度和Cu-Nx構型,當Cu 濃度達到4.9%(物質的量分數)時,相鄰Cu-Nx物種之間的距離足夠接近,可以C-C耦合產生C2H4。相反,在Cu 物質的量分數低于2.4%時,孤立分散的Cu-Nx物種有利于CH4的形成。DFT 計算進一步證實,生成C2H4的活性位點為兩個相鄰的Cu-N2位點,而孤立的Cu-N4、相鄰的Cu-N4和孤立的Cu-N2位點導致CH4的形成。然而,在高溫制備過程中單個原子易聚集成簇或納米顆粒,因此開發容易制備、成本低廉且單原子負載量高的SAC合成策略仍然具有挑戰性。
同時,研究人員還探索了采用均相催化劑與非均相催化劑融合的方式開發多孔炭負載配合物催化劑。例如,Wu 等[86]將酞菁鐵(FePc)、酞菁鈷(CoPc)和酞菁鎳(NiPc)大分子負載在碳納米管(CNTs)上,合成了配合物/炭催化劑。研究發現NiPc/CNT 和FePc/CNT 的H2選 擇 性 高 于CO,而CoPc/CNT 主要生成甲醇,FE 為44%,最大分電流密度為10mA/cm2,這一結果有望進一步推動研究者對陰極CO2RR 催化劑的探索,以實現CO2RR 高效生成液相產物。
1.2.2 陽極催化劑
近年來,與陰極電催化CO2RR 耦合的陽極反應相關的研究逐漸引起關注[16],在已經報道的耦合相關的研究工作中,陽極大多是發生氯氧化或者有機物氧化反應,其中有機物氧化反應按照反應物類型可以進一步分成醇類和含氮有機物的電氧化。其中,催化劑對產物法拉第效率與過電勢的改善起到關鍵性作用,本節主要對陽極反應所使用的催化劑進行總結。
目前在電催化CO2RR 耦合氯氧化反應體系中,陽極氯氧化最常使用的催化劑是形穩性陽極(DSA)。DSA 電極是一種釕鈦二元氧化物涂層電極,具有電催化活性高、耐腐蝕性強和穩定性好等優點,被廣泛應用于氯堿工業。DSA電極與電催化CO2RR 匹配性高,與陽極發生OER 相比,槽電壓顯著降低、能量效率和原子利用率提高,但貴金屬催化劑受到儲量和價格的制約,開發高性能非貴金屬催化劑仍是氯氧化陽極研究的重要內容[19,87-88]。
醇類有機物氧化反應與陰極電催化CO2RR 耦合研究也是目前研究較為廣泛的一個體系,醇類物質的氧化以貴金屬鉑(Pt)系催化劑為主。貴金屬穩定性好,耐腐蝕,能夠在大電流密度下承受更為苛刻的氧化條件[22,89-90]。貴金屬的種類、形態會影響產物的選擇性,既可以將醇直接氧化為酸[22],也可以抑制中間體反應,將醇類氧化為醛[89-90]。貴金屬雖然性能上具有吸引力,但是其儲量有限,價格昂貴,限制了規模化應用。研究人員一直致力于高效的非貴金屬催化劑的開發。材料優化表明,部分非貴金屬氧化物在有機物氧化反應中表現出優異的性能,非貴金屬氧化物導電性好,能夠促進反應過程中電子轉移,降低過電勢,對甘油氧化、含氮有機物氧化等反應均表現出較好的氧化能力[91-92]。此外,通過在貴金屬中摻雜過渡金屬,也能夠實現氧化反應高效進行,如鎳與釕均為親氧金屬,能夠在低過電位下高效吸附中間物(OHads),促進中間體的氧化解吸過程。因此,鎳作為促進劑,能夠在不影響催化性能的前提下降低貴金屬含量[93]。
2 與陰極二氧化碳還原反應耦合的陽極電合成反應
2.1 氯氧化反應
氯氣(Cl2)作為氯堿工業中最重要的化學產品之一,全球年生產能力約為7500 萬噸,廣泛應用于合成化學品、制藥、造紙、污水處理等行業,具有重要的經濟價值。將氯氧化反應作為陽極反應與CO2RR 耦合,能在生成氯氣和燒堿產品的基礎上,提高電能利用率、降低能耗,同時得到高值化學品。Lister等[87]提出了“氯氣-合成氣”工業,將陰極CO2RR 制備合成氣與陽極析氯反應耦合,以DSA 為陽極催化劑,Ag 為陰極催化劑,在氯化鉀和氯化氫電解液中首次利用流動型電解池實現氯堿過程與CO2RR 耦合。為進一步提高CO2的轉化效率,Sun 等[19]以卟啉鎳配合物為陰極催化劑、DSA為陽極催化劑,共電解CO2和KCl 溶液制備了Cl2、CO 和KHCO3,在100mA/cm2的電流密度下,槽電壓為3.8V,CO和Cl2的選擇性分別為98.5%和80%,體系能量效率達到89%。
除了Cl2,次氯酸鹽也是氯堿工業的重要產物。Quan 等[88]將陽極高效生產次氯酸鹽與陰極高效CO2RR耦合(圖3)。該反應體系沒有任何副產物,原子利用率達到100%。當陰極電位為-0.45V(vs. RHE)時,CO 和次氯酸鹽的法拉第效率均達到99%(圖4)。該催化劑在酸性條件下電解24h,能量效率維持在82%,陰、陽極的法拉第效率分別為99.63%、99.47%。此外,他們還采用了太陽電池作為能量輸入裝置,當電壓為2V 時,能量效率為71%。
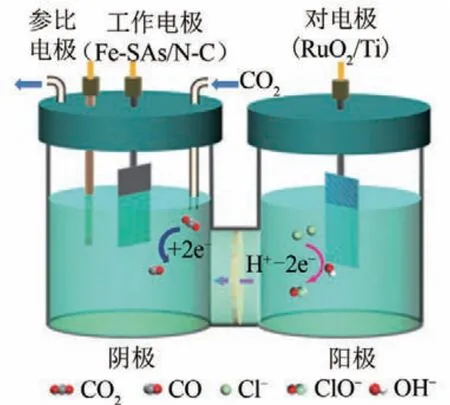
圖3 氯氧化陽極和CO2RR陰極H型電解池示意圖[88]

圖4 次氯酸鹽和CO的法拉第效率與陰極電位的關系[88]
氯氧化反應作為中間反應與CO2RR耦合生成高階產物也是最新發展前沿。Sargent課題組[94]利用電能將乙烯作為原料通入氯堿電化學體系反應得到環氧乙烷,為降低化學行業的碳排放提供了一條途徑(圖5)。他們在非均相-均相反應界面,使用氯為氧化還原介質促進電極和底物分子電子的間接交換,防止高電流密度下有機反應物在電極表面過氧化。使用這一策略,能夠在大電流密度(1A/cm2)、高FE(約70%)和高產物選擇性(約97%)下生產環氧乙烷。在300mA/cm2下電解100h,系統始終保持70%的FE。他們還將CO2RR與上述電化學系統串聯,將CO2RR產生的乙烯作為原料直接通入氯堿陽極,實現了碳的零排放。當電流密度為240mA/cm2、乙烯的流速為6mL/min時,環氧乙烷的FE達到了45%。
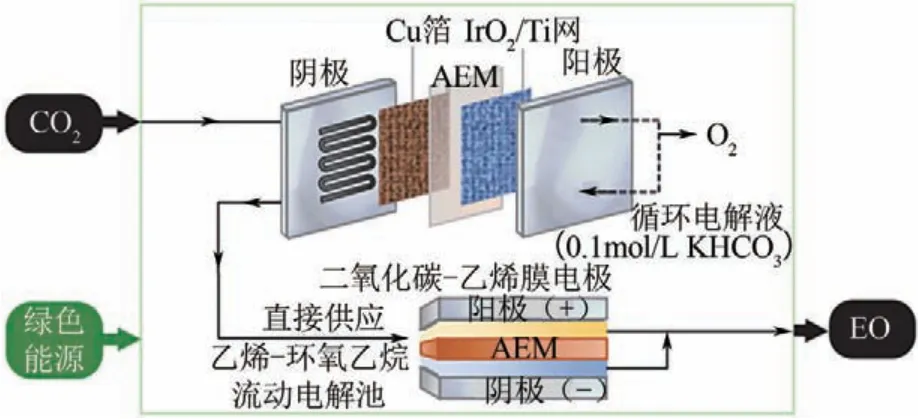
圖5 CO2RR串聯耦合氯堿氧化乙烯制備環氧乙烷(EO)過程示意圖[94]
因此,將氯堿工業與CO2RR 反應耦合,有利于生成高值產物,降低能耗,但目前報道的CO2RR與氯堿陽極的耦合大多仍聚焦于陰極CO2RR 催化劑的設計,而陽極材料的設計和電解池結構的優化仍未引起關注,耦合體系的穩定性難以與傳統氯堿工業匹敵。接下來的工作可以圍繞高效陽極催化劑設計進行,如采用儲量豐富、成本低廉的過渡金屬氧化物和配合物從而提高CO2RR 耦合氯氧化反應體系的經濟性以及穩定性。
2.2 有機物氧化反應
2.2.1 醇類有機物氧化
在電催化CO2RR 體系中,采用醇類有機物氧化替代OER 主要有兩個優勢:①醇類有機物氧化電位低,能夠顯著降低系統的槽電壓,提高能量效率;②醇類有機物的氧化產物為羰基或者羧基類化合物,是重要的化學產品中間體,經濟價值可觀。甲醇電氧化具有動力學優勢,平衡電勢僅0.103V(vs.RHE)(圖6),因此,低能耗電氧化甲醇生產甲酸或甲酸鹽具有很大的潛力。Shi等[95]分別采用1mol/L KHCO3中性電解液、1mol/L KOH 為陰陽極電解液,以泡沫銅上生長的氧化銅納米片(CuONS/CF)和碳布上生長的介孔二氧化錫(mSnO2/CC)為陰、陽極催化劑,實現了CO2RR 耦合甲醇氧化反應高效生產甲酸,陰、陽極甲酸鹽的FE 分別為91.3%和80.5%,在10mA/cm2的電流密度下,系統的槽電壓為0.93V。Bevilacqua等[22]設計了一種去極化陽極堿性膜CO2電解槽,采用酞氰銅與負載在燒結鈦網襯底上的鈀納米顆粒(Pd@Ti)為陰、陽極催化劑,在膜電極結構中研究了CO2RR耦合乙醇氧化反應。結果表明,在電流密度為12.5mA/cm2時,槽電壓降低到1.65V。與陽極發生OER相比,陰極用于合成碳氫化合物的凈能量輸入降低了53kW·h/kg。
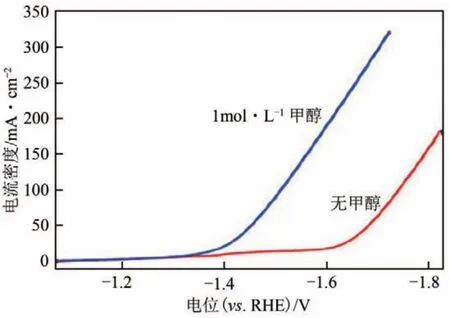
圖6 陽極發生OER和甲醇氧化電流密度差異[95]
甘油是一種生物質衍生化學物質,氧化電位低,可以極大地提高氧化還原過程的經濟性,Kenis等[96]選用流動型電解池及KOH水溶液電解質,分別考察了錫電極(圖7)、銅電極(圖8 和圖9)應用于陰極CO2RR 與陽極甘油氧化或者OER 耦合電解。作者發現,與陽極析氧反應耦合相比,陰極CO2RR 與甘油氧化反應耦合具有更低的起始電壓。此外,陰極CO2RR 產物的種類也會影響耦合體系電壓,其中,CO2RR生成甲酸鹽與甘油氧化耦合具有最低的起始電壓(0.9V)。Baranova等[97]設計了一種過渡金屬鎳摻雜的貴金屬催化劑用于陽極氧化甘油制備甲酸,同時陰極以商用Pt/C 為催化劑制備CO。在三種貴金屬Bi、Pd 和Au 中,Ni0.9Au0.1/C 具有最低的過電位(1.0V) 和最高的電流密度(6.0mA/cm2),該工作對發展非貴金屬基催化劑提供了一種新思路。CO2RR還可以與1,2-丙二醇氧化進行耦合,Gallent等[20]在流動電解池中,用金板或納米金負載的碳布作為陰極,碳布作為陽極,以TEMPO 衍生物介導1,2-丙二醇氧化制備乳酸,與陽極為OER 的CO2RR 電解體系相比,降低了約35%的能量消耗,提高了系統的產品價值,陰極和陽極FE之和達到160%。

圖7 CO2在錫上電還原為甲酸鹽耦合OER或甘油電氧化的電化學性能對比[96]

圖8 CO2在銅上電還原為乙烯耦合OER或甘油電氧化的電化學性能對比[96]
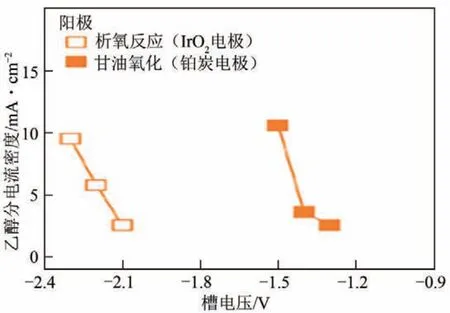
圖9 CO2在銅上電還原為乙醇耦合OER或甘油電氧化的電化學性能對比[96]
含有苯環的醇類也可以在陽極電氧化制備醛類,Meyer 等[90]在H 型電解池中,分別以0.5mol/L NaHCO3、含 有0.1mol/L C7H8O 的0.5mol/L CH3COOH與Na2SO4緩沖液混合物為陰陽極電解液,利用高活性和選擇性的Ru系分子催化劑在陰極制備合成氣,在陽極將苯甲醇氧化為苯甲醛。實驗表明,生成苯甲醛的FE 約為70%,耦合體系的最大能量效率為17.6%。Li 等[89]在用AEM 分隔的H 型電解池中,將CO2RR 生成CO 與醇類有機物氧化耦合。該電解槽采用鈦基上的銅銦化合物(Cu2In)作為陰極,Pt網作為陽極,0.5mol/L NaHCO3作為陰陽極的電解質。在陽極室中分別加入0.25mmol 伯、仲芐基和脂肪族醇(圖10),探究不同醇類作為反應物對耦合系統的影響。其中,苯乙醇氧化為乙酰苯的產率達到93%。
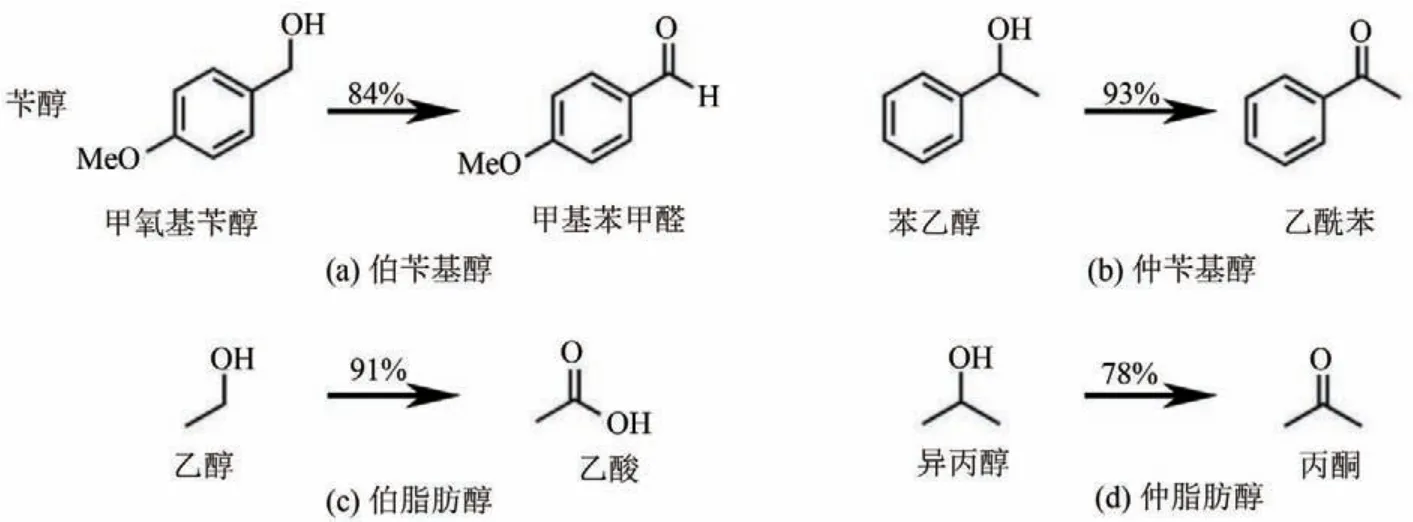
圖10 伯、仲芐基醇和伯、仲脂肪族醇的氧化[89]
綜上,替代OER的有機醇類物質陽極電氧化,既能降低體系槽電壓,提高系統能效,又具有經濟可行性。但是醇類氧化配對電解仍有以下問題亟待解決:①需要探索具有高穩定性和高催化活性的非貴金屬基催化劑;②研究仍處于早期階段,在工業規模上還不能與石油衍生氫經濟相提并論;③分離和純化易溶于水的產品需要復雜的程序和高成本的技術。
2.2.2 含氮有機物氧化反應
近年來由于化工、生物、制藥行業的快速發展,有機廢水的全球年產量達到3800 億立方米,廢水處理也日漸成為亟需解決的難題之一。傳統的處理方法通常成本高昂,且可能造成二次污染,利用電化學氧化法降解有機物是一種可替代的解決方法。
一些小分子含氮有機物(包括尿素或氨等)與CO2RR 耦合需要的槽電壓明顯低于CO2RR 與OER耦合電解過程,可顯著提升環境和能量效益。Klinkova 等[93]詳細比較了陰極電催化CO2RR 和CO2羧基化反應(ECR)與含氮有機物氧化反應耦合的理論槽電壓,由圖11 可知,與發生OER 的系統槽電壓(1.65V)相比,理論上電催化CO2RR 與尿素氧化(UOR)、氨氧化(AOR)耦合的槽電壓分別為1.45V、0.85V。研究人員在H型電解池中,采用泡沫鎳或Pt 網作UOR 電極、Pt/C 作AOR 電極、碳布負載Ag 納米粒子作CO2RR 陰極,在質子介質和非質子介質中分別進行CO2RR 耦合AOR 和UOR 過程。結果發現在相同電流密度下,耦合UOR 比AOR 表現出更低的槽電壓,而且UOR 不會產生毒化催化劑的含氮中間體,穩定性更高,與陽極發生OER相比,可將系統槽電壓降低210mV。
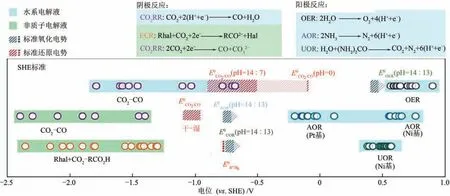
圖11 在質子和非質子介質中陰陽極半反應以及不同pH、電催化劑進行陰極反應(CO2RR到CO、ECR)和陽極反應(OER、AOR和UOR)的理論電位[93]
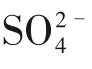
除了以上兩類有機物氧化反應之外,研究人員還探索了將有機物電催化合成精細化學品作為陽極的可能性。Moeller 等[16]將合成苯并咪唑衍生物與CO2RR生成CO耦合。該反應選用乙腈∶四氫呋喃∶甲醇為8∶3∶1的混合溶劑并加入0.8mol/L Et4NBF4作為電解質,利用Ce(Ⅳ/Ⅲ)介質促進木質素鋸末丁香醛與2-氨基苯胺的氧化縮合得到2-(3,5-二甲氧基-4-羥基苯基)-苯并咪唑。CO2RR到CO的選擇性接近100%,陽極產物的產率為65%。然而,陰陽極反應物的轉化率仍然較低,合理設計微流池反應器構型,優化電極面積與電解液流量比值等電解參數有助于提高全電解過程的轉化率,具有重要應用意義[98-99]。
3 結語
本文綜述了陰極CO2RR 與陽極氧化合成的電化學耦合的設計要求和最新研究成果,雖然該方向取得了一些重要進展,但是研究仍處于早期階段,在以下幾個方面還有待研究積累。
(1)陽極催化劑的設計與開發。目前耦合電解的陽極催化劑在活性、成本、穩定性等方面需要改進。有機物氧化合成反應存在催化劑中毒、催化劑浸出和電極載體降解等問題。利用結構工程手段,比如調控催化劑的形貌、摻雜狀態以及結構應變等方法,能優化電催化劑的局部固液界面,得到更加高效、穩定和低成本的陽極電催化劑,提升耦合電催化的效率。
(2)陰陽極耦合全電解產物的分離與工業化。目前CO2RR 耦合沿用了H 型和流動型電解池,初步實現了大電流密度下較高的法拉第效率和較低的槽電壓。然而對于CO2RR與電氧化陽極反應耦合,電解產物較為復雜,陽極(液相)產物的分離與檢測也是CO2RR 耦合全電解未來需要解決的關鍵問題。此外,耦合電催化研究仍處于早期階段,反應物轉化率低、電流密度、穩定性、反應裝置規模以及產品產量仍然不能達到工業級水平,今后的工作需要對電極結構以及電解裝置進行放大設計,以滿足工業化的要求。
(3)CO2RR 耦合體系的拓展。除CO2RR 與陽極電氧化合成的耦合外,CO2與N2等其他反應物陰極共還原、CO2RR串聯耦合等也可以構建經濟的電解體系,實現高級化學品轉化。此外,將微生物催化劑應用于CO2RR 的耦合也代表了化學生物交叉學科方向,細菌等微生物催化劑可將CO2RR 產物原位轉化為高值化學品,提高電解體系經濟性。

