肺移植手術患者的麻醉管理
唐菲,謝言虎,章敏,解明然,柯立
中國科學技術大學附屬第一醫院(安徽省立醫院),a 麻醉科,b 胸外科,合肥 230001
終末期肺病患者生活質量低、生存時間短,肺移植可明顯改善患者生活質量、提高生存期,是治療終末期肺部疾患的有效方法[1]。肺移植的成功開展依賴于多學科的共同協作,肺移植的麻醉面臨著一些的特殊要求與困難,如單肺通氣、體外膜肺氧合技術(ECMO)的選擇、精準的液體治療、血流動力學監測與維持以及血管活性藥物的合理應用等。中國科學技術大學附屬第一醫院2017年6月至2019年9月行肺移植手術麻醉共22例,現就相關臨床問題進行討論。
1 資料與方法
1.1 一般資料 選自中國科學技術大學附屬第一醫院2017年6月至2019年9月行肺移植手術麻醉共22例,美國麻醉醫師協會(ASA)Ⅲ~Ⅳ級;男性19例,女性3例;年齡范圍20~66歲,年齡(44.0±12.8)歲;身高范圍160~176 cm,身高(167.3±4.5)cm;體質量43~72 kg;體質指數(BMI)范圍14.37~24.80 kg/m2,BMI(19.9±3.1)kg/m2;行雙側肺移植8例、左側肺移植5例、右側肺移植9例,其中5例在體外膜肺氧合(ECMO)輔助下完成手術。
1.2 麻醉處理
1.2.1 麻醉方法 監測患者血壓(BP)、心電圖(ECG)和血氧飽和度(SpO2)和有創動脈壓。麻醉誘導方案為:咪達唑侖0.02 mg/kg、舒芬太尼0.4~0.8 μg/kg、依托咪酯0.2~0.3 mg/kg和羅庫溴銨0.8~1.0 mg/kg,待下頜松弛后行插管,所有患者均選擇左側雙腔氣管導管,纖維支氣管鏡協作定位,調節呼吸參數,選擇壓力控制模式,吸氣壓力設為18~35 cmH2O,呼吸頻率為12~18次/min。麻醉維持采用丙泊酚、順阿曲庫銨、舒芬太尼及七氟烷靜吸復合麻醉。
1.2.2 麻醉監測 常規監測BP、ECG、SpO2及有創動脈壓;支氣管麻醉后經左側股動脈穿刺置入脈搏指示連續心排量(PiCCO)專用帶溫度探頭的壓力監測導管并接監護儀(GE,Healthcare Finland Ov,型號:B650),同時監測中心靜脈壓(CVP),右側頸內靜脈放置Swan-Ganz導管,動態監測肺動脈壓(PA)。PiCCO監測心排出量(CO)、心臟指數(CI)、每搏量指數(SVI)、外周血管阻力(SVR)、舒張末期容積指數(GEDI)、胸腔內血容積指數(ITBI)和血管外肺水指數(EVLWI)等指標。
同時監測潮氣量、呼吸頻率、氣道壓及呼氣末二氧化碳(ETCO2)等,持續檢測尿量和體溫,間斷行血氣分析和電解質檢查。
1.2.3 麻醉觀察指標 記錄麻醉后5 min雙肺通氣時(T0)、手術開始后20 min單肺通氣時(T1)、肺動脈阻斷10 min時(T2)、肺動脈開放后20 min時(T3)、恢復雙肺通氣20 min后(T4)和手術結束平臥位10 min后(T5)共6個時間點的血流動力學參數,包括肺動脈壓(PAP)、中心靜脈壓(CVP)、平均動脈壓(MAP)、心率(HR),雙肺移植患者的T2、T3及T4值取2次的平均值。同時記錄各時間點的血氣分析結果,包括pH值、動脈血氧分壓(PaO2)、二氧化碳分壓(PaCO2)。
1.3 判斷標準 左室射血分數(LVEF)判斷標準:50%~75%為輕度降低,35%~49%為中度降低,34%以下為重度降低;肺動脈壓(PAP)判斷標準:26~35 mmHg為輕度升高,36~45 mmHg為中度升高,>45 mmHg為重度升高。

2 結果
2.1 一般資料 22例行肺移植手術麻醉患者中,行左肺移植術5例(22.7%),右肺移植術9例(40.9%),雙肺移植術8例(36.4%);ECMO輔助共5例(22.7%)。原發病為矽肺10例(45.5%);間質性肺炎合并肺纖維化6例(27.3%),包括支氣管擴張2例(9.1%)、慢性阻塞性肺疾病2例(9.1%)、肺淋巴管肌瘤病1例(4.5%)、呼吸道化學性損傷1例(4.5%)。
2.2 術前心臟射血分數、靜息肺動脈壓及氧合指數 LVEF降低:輕度17例,中度5例;PAP升高:中度5例,重度17例;氧合指數為200~300共4例,<200共18例。
2.3 術中各時點的血流動力學及血氣分析結果 T2時的PAP明顯高于其他各時點(P<0.05)、而T3、T4、T5時的PAP較T0時明顯降低(P<0.05);T1、T2時的CVP明顯高于其他時點(P<0.05)。見表1。
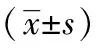
表1 22例行肺移植手術麻醉患者術中各時點的血流動力學及血氣結果
3 討論
行肺移植的患者大部分是終末期肺病患者,多表現為呼吸衰竭癥狀,同時合并有不同程度的肺動脈高壓[2]。肺移植手術創傷較大,術中需單肺呼吸、阻斷及開放肺動脈等,對患者的心肺功能影響較大。因此,在肺移植手術麻醉中,如何維持充分的氧合、維持血流動力學平穩是保證肺移植手術成功的前提之一。
3.1 麻醉監測 患者在麻醉誘導前監護BP、ECG、SpO2及有創動脈壓、頸內靜脈穿刺監測CVP,同時右側頸內靜脈放置Swan-Ganz導管,動態監測肺動脈壓PA,需要注意的是若決定或較大可能需ECMO輔助時應選用左側頸內靜脈穿刺,本研究中5例選擇左側頸內靜脈監測CVP,右側頸內靜脈近心端放置Swan-Ganz導管,遠心端放置ECMO頸內靜脈導管。22例患者均選用左側股動脈穿刺并置入PICCO專用帶溫度探頭的壓力監測管以監測CO、CI、SVI、SVR、GEDI和EVLWI等指標。其他監測指標包括有體溫、麻醉深度等。需要提醒的是,由于監測有創操作較多,可多人同時以縮短供肺的缺血時間。
3.2 呼吸管理 肺移植手術均需單肺通氣完成,本研究中所有患者均選擇左側雙腔氣管導管,左側相對右側對位更簡便、準確性更高且不易移位。麻醉過程中根據SpO2及血氣分析適當的調整呼吸參數,必要的時候需改手動控制呼吸。在肺移植手術中,由于患者術前肺功能損害一般較重,麻醉過程中允許高碳酸血癥進行通氣調節[3],在本研究中在單肺通氣過程中其PCO2均高于正常值。術中若出現進行性SpO2下降、動脈血氧分壓持續降低,經更改呼吸參數、調整支氣管導管位置、吸痰等處理無效時需及時行ECMO支持,因此,術前準確評估是否需ECMO支持顯得尤為重要。
在肺移植麻醉中,血氣分析結果PO2非常重要,單肺通氣對PO2的影響非常明顯。本研究中在單肺通氣過程中其明顯低于其他時間點,另本研究中在肺動脈夾閉和開放時PO2改善并不顯著,可能與其通氣/血流比值及缺血性肺血管收縮等代償有關[4]。
3.3 ECMO應用 肺移植麻醉過程中需要單肺通氣,嚴重低氧血癥及夾閉肺動脈都可能會進一步加重肺動脈高壓,嚴重會導致右心心力衰竭,ECMO對于糾正低氧血癥、降低肺動脈壓及維持血流動力學平穩均具有明顯的治療作用[5],但ECMO中肝素的使用會加重術中出血、增加手術時間、增加住院費用等缺點。目前關于是否在肺移植手術中常規使用ECMO尚存在爭論,有研究提示ECMO可減輕移植肺的損傷[6];一項回顧性研究提示:ECMO較體外循環在早期恢復更好、90 d死亡率也更低[7]。本研究中,術前綜合評估患者術前肺動脈高壓、心功能、氧合指數及單肺通氣后SpO2情況,有5例患者在ECMO輔助下完成手術麻醉的,其中一例術中出現進行性SpO2下降、動脈血氧分壓持續降低,經更改呼吸參數、調整支氣管導管位置、吸痰等處理無效后中轉行ECMO輔助。
3.4 循環管理及肺動脈高壓處理 肺移植麻醉中循環的管理面臨著很多挑戰,患者一般情況差,肺動脈高壓、出血、肺動脈夾閉和開放等均會對循環產生一定的影響。本研究中,發現在肺移植麻醉時,CVP在時間點T1、T2較基礎值升高,其主要原因可能是手術操作、單肺通氣等原因導致的異常升高,而PAP在T2時明顯升高,主要與肺動脈阻斷有關。因此,在肺移植麻醉中以CVP反映容量負荷存在明顯的局限性,需結合麻醉過程中實際情況,排除相關影響因素。研究表明GEDI 、ITBI在反映心臟前負荷的敏感性及特異性方面要明顯優于CVP及PAWP,且其不受機械通氣影響[8]。
本研究中輸液原則是以濃縮紅細胞、人工膠體、白蛋白或血漿為主,晶體為輔的原則,重點預防肺水腫的發生。EVLWI是目前反映肺水腫最為敏感的指標,對于早期發現肺水腫及早期治療均具有一定的指導意義[9-10]。本研究中EVLWI 維持在3.0~7.0 mL/kg,過低時加快補液,過高則減慢補液,必要時使用呋塞米脫水治療。在肺移植手術麻醉中,部分手術操作對循環影響較大,如肺動脈阻斷與開放以及肺靜脈左房袖吻合,有報道在阻斷肺動脈時發生心跳驟停[11];本研究中均采用了前列地爾肺動脈給藥以降低肺動脈壓,其對移植肺亦有明顯的保護作用[12],同時根據監測肺動脈壓變化情況及時調整用量,這與文獻報道[13]相符。另有研究報道小劑量NO吸入可以降低肺動脈壓,可提高肺移植術后肺氧合功能[14]。
本研究中22例圍術期間死亡2例,均為術后右心功能衰竭經ECMO輔助治療后仍不能改善;術后早期,胸腔出血2例,原因是胸腔內彌漫性粘連滲血;支氣管胸膜漏5例,經保守治療后好轉;12例出現不同程度的氣管狹窄,均發生于術后1~3個月,接受氣管鏡下球囊擴張治療后好轉;術后5例出現嚴重肺部感染,經氣管切開、機械通氣治療后治愈。由于肺移植手術創傷大,術后使用免疫抑制劑等原因,肺移植患者術后并發癥發生率相對較高,因此,肺移植手術的成功需要多學科的綜合治療。

