非紫紺型先天性心臟病嬰幼兒圍體外循環期腦血流動力學變化
錢晶晶,李曉英,俞 勁,劉清明,范 銘,葉菁菁
近年來先天性心臟病(congenital heart disease,CHD)的手術治療正朝著低齡化、復雜化的方向發展。 但嬰幼兒各器官發育尚不成熟,血管的通透性高,術后器官易出現滲出性和炎癥性改變。 人體貯氧量最低的腦組織耗氧量卻是最大的,于是就表現出腦組織對體外循環(extracorporeal circulation,ECC)的敏感性。 總體來說嬰幼兒心臟術后腦部并發癥較成人高30%左右,常見并發癥是彌漫性缺血缺氧性腦病[1]。 本研究應用經顱彩色多普勒超聲技術簡便、及時、動態、直觀地監測CHD 患兒圍術期腦血流動力學變化。
1 資料與方法
1.1 研究對象 選擇自2018 年1 月至2019 年12月間在本院門診體檢正常嬰幼兒26 例(正常組)和在本院住院治療的非紫紺型先天性心臟病患兒22例(CHD 組),年齡均為 6 月至 1 歲。 正常組嬰幼兒男 17 例,女 9 例,體重(8.33±1.42)kg。 入選標準:①無異常病史,臨床及超聲檢查未發現異常;②生長發育指標在正常范圍。 CHD 組患兒男12 例,女10例,體重(7.87±0.90)kg,病種包括室間隔缺損合并房間隔缺損6 例,室間隔缺損合并動脈導管未閉3例,室間隔缺損4 例,房間隔缺損8 例,肺動脈瓣狹窄合并房間隔缺損1 例。 排除標準:①合并可識別的非心臟畸形、染色體異常;②心律失常;③患有影響血流動力學的疾病,如糖尿病、甲狀腺疾病等。 本研究經醫院倫理委員會批準(批準文號2017-IR?BAL-034),患兒家屬知情同意。
1.2 手術方法 采用靜吸復合麻醉,氣管插管接呼吸機通氣,動脈有創血壓,血氧飽和度和心電圖監測,鼻溫、肛溫探頭置入測溫。 接受淺低溫全流量ECC 輔助下心臟根治手術,ECC 時間 38 ~88(57.1±16.7)min,主動脈阻斷時間 24~56(37.3±12.7)min。
1.3 TCCS 儀器與方法 使用 Philips iE33 彩色超聲診斷儀,S5-1 探頭,選擇經顱多普勒條件。 對不合作患兒以10%水合氯醛灌腸鎮靜。 首先進行超聲心動圖檢查,明確心臟有無畸形及類別。 然后經前囟分別通過冠狀切面及矢狀切面檢測腦實質內是否出現異常回聲,腦室內徑是否異常增寬或縮小。再經雙側顳窗行大腦中動脈(middle cerebral artery,MCA)的檢查,顯示患兒大腦 Willis 環(圖 1)。 將聲束平行于MCA,取樣容積(寬約2 ~3 mm)置于近場一側MCA 的起始段,超聲聲束與血流的夾角盡量接近 0,所有測量角度<20°(圖 2)。
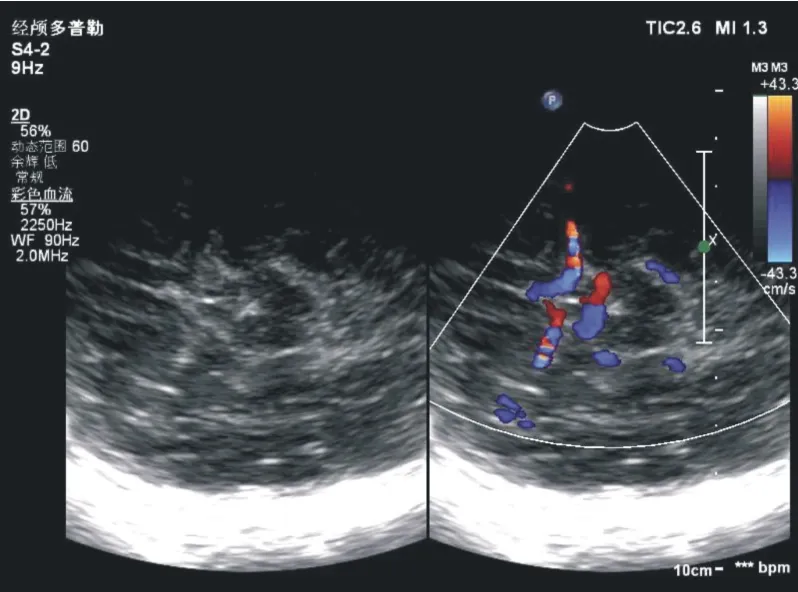
圖1 經雙側顳窗行MCA 的患兒大腦Willis 環
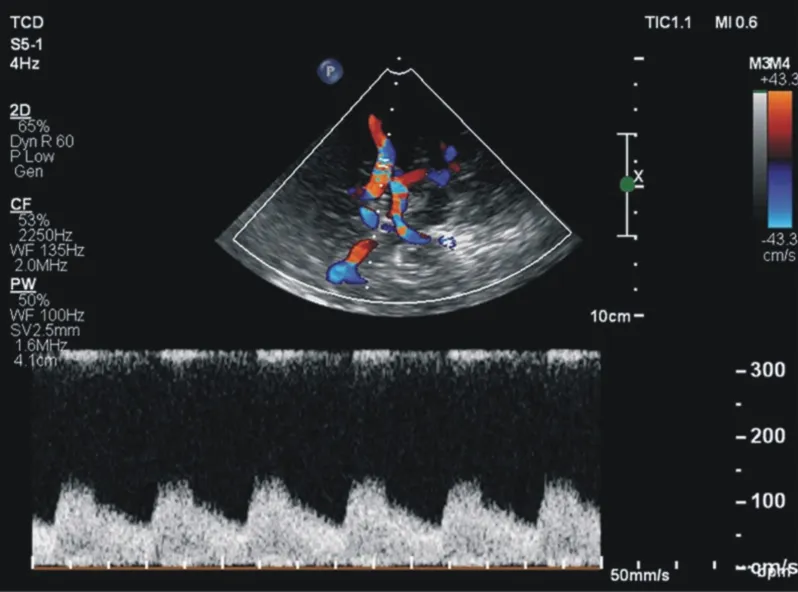
圖2 聲束平行于MCA 的起始段
正常組:獲取連續3 個以上形態一致、完整的頻譜,測量收縮期最大峰值血流速度(peak systolic blood flow velocity,PSV)、舒張末期血流速度(enddiastolic blood flow velocity,EDV)、平均血流速度(mean blood flow velocity,Vm)及搏動指數(pulsatili?ty index,PI),并取平均值。 同時記錄平均動脈壓。
CHD 組:分別于手術前(T0)、全流量 ECC 期(T1)、停 ECC 即刻(T2)、術后 1 d(T3)和術后 7 d(T4)等 5 個時間點,以及記錄 MCA 的 PSV、EDV、Vm、PI 和平均動脈壓。
1.4 統計學分析 采用 SPSS 17. 0 統計軟件包進行統計學分析。 計量資料以均數±標準差()表示。 對兩組大腦中動脈 PSV、EDV、Vm、PI 采用兩獨立樣本t檢驗,以P<0. 05 為差異有統計學意義。
2 結 果
2.1 二維超聲顯像和多普勒檢查 二維超聲顯像兩組患兒均未發現腦實質異常回聲,腦室內徑正常。
CHD 組 22 例患兒大腦中動脈 PSV、EDV、Vm、PI 在T0 及T4 時點與正常組嬰幼兒比較差異均無統計學意義(P>0.05)。 CHD 組患兒在 T2 時點PSV[右(104±27)cm/s、左(97±22)cm/s]和 Vm[右(59±14)cm/s、左(55±14)cm/s]較正常組嬰幼兒下降,差異有統計學意義(P<0.05)。 T3 時點 PI值[右(1.01±0.16)、左(1.00±0.15)]CHD 組較正常組嬰幼兒下降,差異有統計學意義(P<0.05)。 見表1。
表1 正常組嬰幼兒和CHD 組患兒各時期大腦中動脈血流值()
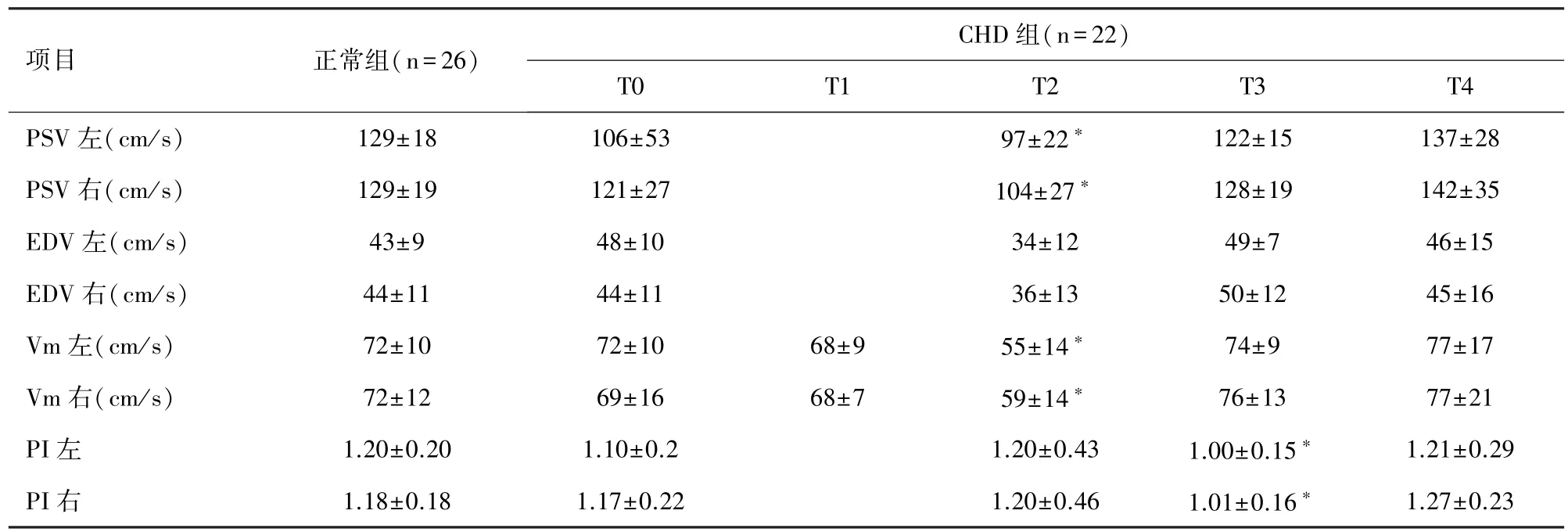
表1 正常組嬰幼兒和CHD 組患兒各時期大腦中動脈血流值()
注:PSV:收縮期最大峰值血流速度;EDV:舒張末期血流速度;Vm:平均血流速度;PI:搏動指數;*表示分別與正常組比較P <0.05
項目 正常組(n =26)CHD 組(n = 22)T0 T1 T2 T3 T4 PSV 左(cm/s) 129±18 106±53 97±22* 122±15 137±28 PSV 右(cm/s) 129±19 121±27 104±27* 128±19 142±35 EDV 左(cm/s) 43±9 48±10 34±12 49±7 46±15 EDV 右(cm/s) 44±11 44±11 36±13 50±12 45±16 Vm 左(cm/s) 72±10 72±10 68±9 55±14* 74±9 77±17 Vm 右(cm/s) 72±12 69±16 68±7 59±14* 76±13 77±21 PI 左 1.20±0.20 1.10±0.2 1.20±0.43 1.00±0.15* 1.21±0.29 PI 右 1.18±0.18 1.17±0.22 1.20±0.46 1.01±0.16* 1.27±0.23
CHD 組患兒在T1 時(平均動脈壓約48 mmHg)和T2 時(平均動脈壓約58 mmHg)血壓降低,最低為術前(平均動脈壓約67 mmHg)的71.6%,但是仍超過了生理所需要的最低灌注壓,此時MCA 的Vm 較術前降低不明顯(圖3)。
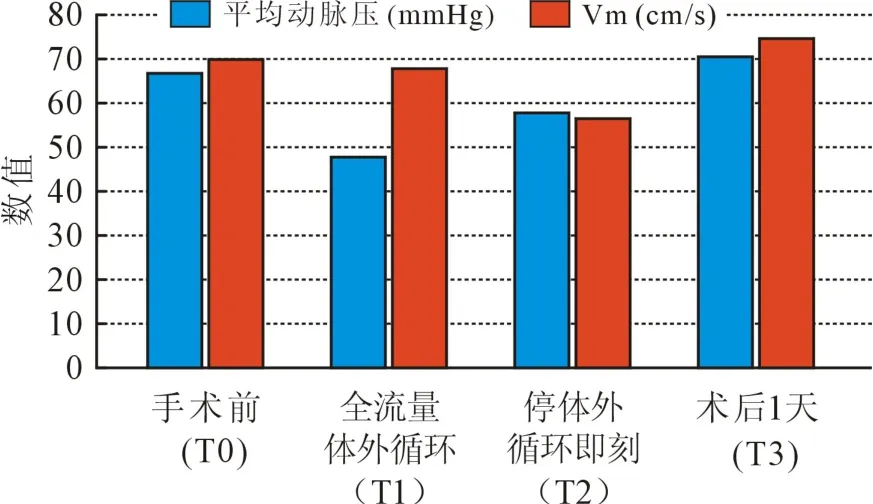
圖3 CHD 組患兒圍術期平均動脈壓和MCA 的Vm
2.2 臨床表現 CHD 組22 例患兒經手術治療康復出院,術后未出現神經系統異常體征和癥狀,未出現抽搐、驚厥、偏癱等嚴重神經系統后遺癥。
3 討 論
隨著理論研究和新設備及材料技術的不斷發展,已經使ECC 本身的非生理灌注、手術創傷的危險因素大為降低。 然而,腦損傷仍是ECC 下心臟手術后的主要并發癥之一[2-3]。 因此,CHD 治療的重點已由過去如何降低患兒的死亡率逐漸轉變為重視患兒術后的康復、發育、提高生活質量,對神經系統的保護在術中和術后都越來越得到重視[4],是心臟外科領域亟待解決的嚴重問題[5]。
TCCS 是利用低頻探頭,使聲束通過顱骨透聲窗(顳骨嶙部、枕骨大孔、眼眶、顱骨缺損區)而顯示顱內實質及血管結構,無創評價顱底血管血流動力學的檢查方法。 它把彩色多普勒、二維圖像及頻普多普勒結合在一起,在清晰顯示彩色血管的同時又能準確定位并測量其血流頻譜,豐富血管信息的同時極大地提高了診斷的準確性。 TCCS 較之經顱多普勒超聲(transcranial doppler,TCD)最主要的優勢是能夠比較清楚的顯示顱內大血管的結構,避免了與其他血管的混淆,并根據血管圖像的改變予以準確定位,而且能夠校正超聲束與血流之間的夾角,從而測得更加接近于真實值的血流速度值[6]。 目前TCCS 是檢測腦血流最敏感最直觀的工具[7-8],研究表明經顱彩色多普勒超聲與核磁共振血管成像有很高的一致性,MCA 的 PSV 的準確性最高[6]。 檢測MCA 的PSV、EDV、PI 能很好的反映腦血流的灌注。研究表明,MCA 近端的 PI 值低于中段及遠端,且MCA 近端血流指數的變異性最小[9],故本研究選用MCA 的起始段。 兒童雖可通過前囟探查到MCA 血流,但顳窗掃查取樣線與血流方向夾角小,獲得的血流數值準確性高。
腦血流隨著兒童年齡的變化而變化,本研究選取6 月至1 歲嬰幼兒作為研究對象,是因為該年齡段腦血流正常值國內外文獻欠缺報道,同時本院心臟ECC 手術最多見于該年齡段。
本研究發現非紫紺型CHD 患兒腦血流與正常嬰幼兒無明顯差異(表1)。 之前有學者對CHD 胎兒腦血流動力學進行研究發現CHD 胎兒存在積極的自動調節機制——腦保護效應,以盡量滿足胎兒發育過程中腦對氧氣的需求,同時不同類型CHD 所引起的腦血管代償反應程度不同[10-11]。 因此,對于紫紺CHD 患兒腦血流特點還有待進一步的研究。本研究還發現在停ECC 即刻會出現PSV 和Vm 一過性降低,術后 1 d 的 PI 值降低,PSV 和 Vm 恢復(表1),考慮是腦保護作用的結果,為保證足夠的腦血流量,防止腦損傷的發生。 術中合理的腦灌注壓可以保證足夠的腦血流供應,以往研究認為當腦血流低至生理流速30%~70%的范圍內都可能造成腦缺血損傷[12]。 因此,術中監測腦血流,使其在正常范圍內,可有效防止腦損傷的發生(圖3)。 因此,經顱彩色多普勒超聲作為腦損傷主動監測中的重要手段,可簡便、及時、直觀、動態監測CHD 嬰幼兒圍術期腦血流灌注情況,避免或減輕腦損傷的發生發展。

