AIHA患者血型血清學特征及輸注懸浮紅細胞療效分析
邸艷輝 管行 寇立舵 白薇 王新華
自身免疫性溶血性貧血(autoimmune hemolytic anemia,AIHA)是指由于自身紅細胞膜分子構象改變、免疫系統功能異常或某些遺傳因素等,產生自身抗體和(或)補體結合在紅細胞膜上,通過抗原抗體反應導致紅細胞破壞加速而引起的溶血性貧血。AIHA可根據抗體作用于紅細胞膜所需的最適溫度,分為溫抗體型和冷抗體型。給予有效的紅細胞輸注治療可以在短時間內迅速改善AIHA患者臨床貧血癥狀,是目前臨床上搶救重癥AIHA患者的重要措施之一[1]。本研究分析懸浮紅細胞輸注對AIHA患者治療效果及血型血清學特征及安全性,為臨床更好治療AIHA提供研究依據。
材料與方法
1 病例資料 選取我院2014年1月~2019年12月期間住院治療AIHA患者56例,其中8例患者采用藥物治療,為A組,年齡26~72歲,平均(48.9±8.2)歲;18例患者采用輸注洗滌紅細胞治療,為B組,年齡28~79歲,平均(48.2±8.9)歲;30例患者采用輸注懸浮紅細胞治療,為C組,年齡18~83歲,平均(47.5±9.1)歲。所有患者經診斷均符合AIHA臨床診斷標準[1]。3組患者性別、年齡等一般資料比較差異無統計學意義(P>0.05),具有可比性。
2 儀器與試劑 抗-A、抗-B血型定型試劑(批號:102182和204178)、RhD血型定型試劑(批號:517187)、ABO血型反定型細胞試劑(批號:115396C),均由美國Immucor公司提供;微柱凝膠抗人球蛋白卡(批號:20139.01.1)、低離子液(批號:20013.01)、專用孵育器(型號:DG THERM)、專用卡式離心機(型號:GRIFOLS DG SPIN),均由西班牙Diagnostic Grifols公司提供;紅細胞抗體篩查試劑(批號:8000451206)由荷蘭Sanquin Reagents B.V.公司提供;直接抗人球蛋白試驗分型卡(批號:202003001)由江陰力博醫藥生物技術公司提供;RBC、Hb、Ret檢測由邁瑞BC6900儀器提供,采用紅細胞阻抗法;TBIL檢測由貝克曼AU5811儀器提供,采用重氮比濁法;各種試劑均在有效期之內。
3 檢測方法 血型鑒定和直接抗人球蛋白試驗,應用全自動血型分析儀和配套試劑檢測血型;將患者紅細胞壓積稀釋1%紅細胞懸液,分別加50 μL到直接抗人球蛋白卡中,離心后看結果;將1%抗體篩查細胞(儀器操作)各50 μL分別加入微柱凝膠抗人球蛋白卡中,再將患者血漿25 μL依次加入,同時加自身對照,孵育15 min,離心后觀察結果。
4 評價指標
4.1 DAT分型與溶血嚴重程度的相關性:在DAT分型的同時檢測患者紅細胞、血紅蛋白和網織紅細胞作為溶血程度的參數。
4.2 DAT凝集強度與貧血程度的關系:通過檢測DAT凝集強度和Hb水平,分析其與溶血和貧血的關系。
4.3 DAT凝集強度與輸血療效的關系:對自身抗體和DAT凝集強度為W+~4+患者均選取與患者ABO同型懸浮紅細胞或O型洗滌紅細胞進行輸注。觀察治療前后的數值指標,判斷輸注療效。①有效:輸注后,患者血紅蛋白水平較輸注前增量至少為5(g/L)×60/患者體重(Kg);②部分有效:輸注后,患者血紅蛋白水平較輸注前明顯上升,但增量不足5(g/L)×60/患者體重(Kg);③無效:輸注后,患者血紅蛋白水平較輸注前無明顯上升甚至下降。總有效率=(有效+部分有效)例數/總例數×100%[2]。
4.4 紅細胞輸注:①對有自身抗體的患者,選取ABO同型懸浮紅細胞或O型洗滌紅細胞。②對有同種抗體+自身抗體的患者,選取沒有同種抗體對應抗原的ABO同型懸浮紅細胞或O型洗滌紅細胞。均用Liss/Coombs卡式做交叉配血,相合后輸注,如不相合用經典IAT法做交叉配血,相合后輸注。
5 統計學處理 采用SPSS 20.0軟件進行統計分析,計量資料以()表示,采用t檢驗。計數資料以百分率(%)表示,采用χ2檢驗。P<0.05為差異有統計學意義。
結 果
1 56例患者血型血清學特征分布、DAT分型與溶血程度的關系 單純型(IgG、C3d)和復合型(IgG+C3d)的溶血參數相比,有顯著性差異(P<0.05),見表1。
表1 56例血型血清學特征分布、DAT分型與溶血程度的關系()

表1 56例血型血清學特征分布、DAT分型與溶血程度的關系()
注:*:P<0.05
2 56例患者DAT凝集強度與貧血程度的關系 56例患者通過檢測DAT凝集強度與Hb水平,分析檢測結果,自身抗體和DAT凝集強度為W+~1+患者,其Hb水平集中在60 g/L以上,自身抗體和DAT強度為1+~2+患者,其Hb水平集中在60 g/L以下,自身抗體和DAT強度為2+~3+患者,其Hb水平集中在50 g/L以下,自身抗體和DAT強度為3+~4+患者,其Hb水平集中在40 g/L以下。DAT為2+凝集強度和2+以上凝集強度與溶血及貧血嚴重程度有統計學差異(P<0.05),見表2。
表2 56例患者DAT凝集強度與Hb水平的關系()

表2 56例患者DAT凝集強度與Hb水平的關系()
注:*:P<0.05,DAT凝集強度越強溶血程度越嚴重,而貧血程度隨之加重
3 治療前后實驗室指標變化比較 3組患者治療1天后,Hb、RBC水平較治療前明顯升高,Ret、TBIL水平較治療前明顯降低,差異具有統計學意義(P<0.05)。3組患者治療前Hb、RBC、Ret、TBIL水平之間的差異無統計學意義(P>0.05),3組患者治療后1天Hb、RBC、Ret、TBIL水平之間的差異無統計學意義(P>0.05),見表3。
表3 3組患者治療前后實驗室指標變化比較()
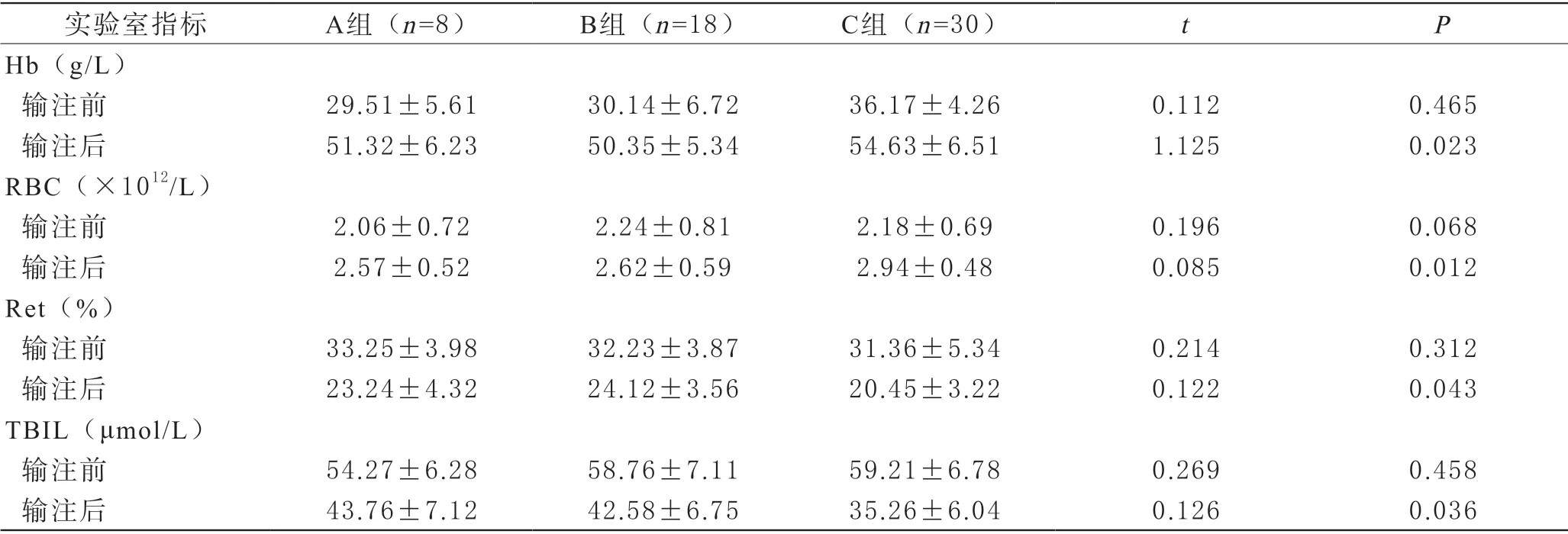
表3 3組患者治療前后實驗室指標變化比較()
4 治療后療效比較 3組患者治療后療效的差異無統計學意義(P>0.05),見表4。

表4 3組患者治療后療效比較
討 論
國外資料顯示AIHA的年發病率為(0.8~3.0/10萬)[3,4]。自身免疫性溶血性貧血(AIHA)是由于體內B淋巴細胞功能異常亢進,產生過多的自身紅細胞抗體和(或)補體吸附于紅細胞表面,從而加速紅細胞破壞而導致的一種較為常見的貧血[3]。臨床和實驗研究資料表明,自身免疫病的發生與病毒感染、惡性腫瘤、自身免疫疾病等相關,其可通過基因突變,改變紅細胞膜抗原等刺激機體產生抗紅細胞抗體,引起紅細胞脆性增加而發生溶血[5]。本研究中AIHA患者多見于自身免疫性疾病、白血病、淋巴瘤、惡性腫瘤及感染性疾病,可分為溫抗體型及冷抗體型[6]。AIHA以溫抗體型最為多見,其抗體類型主要為IgG及C3,其作用于紅細胞膜的最佳溫度為37℃,紅細胞被抗體吸附后,被單核-巨噬細胞系統識別吞噬,即發生血管外溶血[7]。冷抗體型在臨床上可分為陣發性冷性血紅蛋白尿(PCH)及冷凝集素綜合征(CAS)[8]。本研究中,56例AIHA患者自身抗體類型以IgG型最多,其次為IgG+C3型及C3型,各種類型AIHA溶血和貧血嚴重程度與DAT分型和凝集強度有關。單純型(IgG或C3d)和復合型(IgG+C3d)的溶血參數相比,有顯著性差異(P<0.05),且復合型溶血程度重于單純型,與楊國元等[9]報道相符。56例患者DAT結果均為陽性(凝集強度W+~4+),自身抗體和DAT凝集強度與溶血和貧血呈正相關(P<0.05),說明DAT凝集強度越高其溶血和貧血程度越嚴重。臨床工作中也發現DAT陽性的非AIHA病例,此患者DAT陽性可能是由于非紅細胞抗原特異性球蛋白非特異性黏附于紅細胞表面,這種結合與抗原抗體結合不同,不會引起抗體免疫球蛋白構象的改變,沒有補體參與,不會加速紅細胞破壞,因此不會產生溶血[10]。
本文研究表明3組治療前后比較Hb、RBC明顯升高,Ret、TBIL明顯降低,差異具有統計學意義(P<0.05);3組治療后比較,均能夠有效緩解患者的臨床癥狀,臨床治療效果明顯改善,未發生溶血及輸血不良反應,總有效率比較差異無統計學意義(P>0.05)。
本研究結果顯示,AIHA患者輸注懸浮紅細胞和洗滌紅細胞都可提高機體Hb水平,有效緩解貧血和機體缺氧狀況。但由于抗體陽性與自身免疫有關,常規輸血容易引起紅細胞脆性增加而發生溶血,從而發生輸血不良反應。因此,建議臨床以腎上腺皮質激素、免疫抑制劑、丙種球蛋白等藥物治療為主,對于貧血癥狀嚴重的患者,給予輸血治療可快速改善AIHA患者缺氧癥狀,但長期輸注可導致更多自身抗體產生,應選擇最小劑量的紅細胞進行輸注[11]。
由于洗滌紅細胞存在制備時間長、保存期短、紅細胞脆性大、庫存少等特點。本研究顯示,洗滌紅細胞相對懸浮紅細胞,并沒有給AIHA患者提供更為理想的輸注效果,過度使用洗滌紅細胞反而會對供血機構造成較大負擔[12]。經過臨床觀察,給予AIHA患者輸注懸浮紅細胞治療效果顯著,并且懸浮紅細胞保存期長,庫存充足,應用時很方便,能及時有效改善患者臨床癥狀,并且安全可靠,具有很重要的臨床意義。
綜上所述,由于AIHA免疫血清學十分復雜,在臨床輸血中,對AIHA輸血患者要嚴格掌握輸血適應癥,并以貧血的嚴重程度、發展速度及臨床癥狀為主要依據。選擇合適的輸血方法對于搶救患者生命、改善其預后等均具有重要意義。本研究中,輸注懸浮紅細胞治療AIHA的臨床療效十分確切,未出現輸血不良反應,具有安全有效性,且快捷方便,值得在臨床上廣泛推廣與運用。
利益沖突所有作者均聲明不存在利益沖突

