香菊片制備工藝的優化
韓立柱劉帝呈胡坤霞汪蕓蘭唐志書宋 逍
(陜西中醫藥大學藥學院,陜西 咸陽712046)
質量源于設計(QbD)理念是由美國FDA 于21 世紀初提出的應用于藥品管理的一種新觀念,在藥品監控系統中發揮重要作用[1],主要是通過對藥品處方的工藝設計來確定影響藥品關鍵質量屬性和關鍵工藝參數,并通過控制關鍵工藝參數的范圍以達到保障藥品安全、有效、質量可控的目的[2]。根據QbD 理念的要求,藥品質量應從研發開始時便把控,從輔料種類、工藝路線、工藝參數、物料控制等多個方面進行研究,在此過程中記錄關鍵數據并加以分析,最終確定藥品最佳處方組成和制備工藝[3],目前該理念已經逐漸應用于一些傳統劑型的制備工藝優化和處方組成的篩選中。
香菊片由化香樹果序、夏枯草、野菊花、黃芪、辛夷、防風、白芷、甘草、川芎組成,是應用于耳鼻喉科的純中藥制劑[4?5],具有抗過敏、抗炎、鎮痛效果,對急性、慢性鼻竇炎、鼻炎療效良好[6?8],但傳統制法并未過多考慮不同輔料以其用量對成片質量的影響。因此,本實驗將QbD 理念應用于香菊片生產過程中,并對其進行優化,以期為相關中藥處方片劑的制備工藝提供參考。
1 材料
1.1 儀器 UltiMate 3000 高效液相色譜儀(美國賽默飛世爾科技公司);BSA224S 電子天平[萬分之一,賽多利斯科學儀器(北京)有限公司];ZP?10 旋轉式壓片機(上海天和制藥機械有限公司);YPD?200C 片劑硬度儀(上海黃海藥檢儀器有限公司);FT?2000AE 脆碎度檢查儀(天津市天大天發科技有限公司);電熱鼓風干燥箱(北京科偉永鑫實驗儀器設備廠)。
1.2 試劑與藥物 糊精(天津大茂化學試劑廠,批號20181101);淀粉(天津北聯精細化學品開發有限公司,批號20190220);微晶纖維素(國藥集團化學試劑有限公司,批號20190404);α?乳糖(批號20160829)、蔗糖(批號20190116)(天津市科密歐化學試劑有限公司);羧甲基纖維素鈉(CMC?Na,天津市天力化學試劑有限公司,批號20190308);羧甲基淀粉鈉(CMS?Na,山東優索化工科技有限公司,批號20181107)。
2 方法與結果
2.1 風險評估 風險評估是質量管理的主要內容,包括識別、分析與評價[9],本實驗通過繪制魚骨圖來對香菊片制片過程中的影響因素進行相關分析,根據預試驗情況,將影響其成型以及成型后質量的風險因素分為工藝因素、處方因素、環境因素,結果見圖1。應用失效模式及效應分析(FMEA)對其風險因素作進一步分析,從失效后的嚴重程度(S)、失效發生的可能性程度(P)、失效的可檢測性(D)來評估,每個指標分值為1~4分[10],根據評估結果計算風險優先系數(RPN,S×P×D),結果見表1,RPN 不超過8 表明該風險因素影響較小,9~16 其影響中等,17 以上其影響較大。
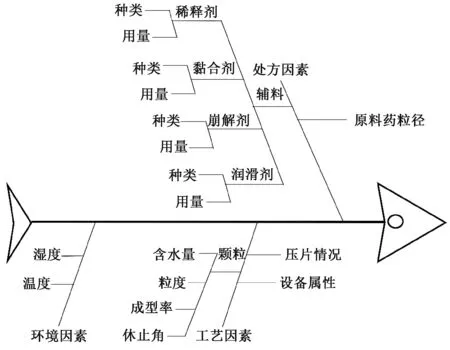
圖1 香菊片風險評估魚骨圖Fig.1 Fishbone diagram for risk assessment of Xiangju Tablets

表1 風險因素評估結果Tab.1 Results of risk factor evaluation
2.2 片劑制備
2.2.1 浸膏 將9 味中藥按處方比例加水煎煮2次,濾液合并,0.2 μm 陶瓷膜微濾、超濾,50 ℃下將其濃縮成浸膏,減壓干燥,粉碎,即得,密封保存。
2.2.2 素片 以每片片重0.30 g 為標準,采用濕法制粒法制備。將主藥置于研缽中研細,過80 目篩,稀釋劑過篩后通過等量遞增法加到主藥中繼續研磨,使其均勻混合,加入足夠黏合劑后手動制備軟材,16 目篩網制粒,將顆粒置于60 ℃電熱鼓風干燥箱中烘干,14 目篩整粒,加入潤滑劑(80目),壓片,即得。
2.3 處方工藝篩選
2.3.1 稀釋劑種類 本實驗選擇淀粉、糊精、乳糖、微晶纖維素作為稀釋劑,將提取出來的主藥在研缽中研細,加入過80 目篩的稀釋劑繼續研磨,使其均勻混合,加入一定量黏合劑制軟材,16 目篩制粒,60 ℃下烘干,14 目篩整粒,稱定質量,加入同一潤滑劑壓片,考察顆粒成型率、吸濕率、流動性、片劑成型性,結果見表2。由此可知,乳糖稀釋時顆粒成型率好,壓片后片面光潔無粉末,故確定其作為稀釋劑。

表2 稀釋劑種類考察結果Tab.2 Results of diluent type investigation
2.3.2 黏合劑種類 本實驗選擇水、10%淀粉漿、70%乙醇、50% 蔗糖溶液、2% CMC?Na 溶液作為黏合劑,主藥在研缽中研細后與同一稀釋劑均勻混合,加入黏合劑制軟材,16 目篩制粒,烘干,14 目篩整粒,同一潤滑劑壓片,考察制軟材難易程度、顆粒成型情況、壓片效果,結果見表3。由此可知,70%乙醇黏合時顆粒緊密,成型性好,壓片后藥片無缺損,故確定其作為黏合劑。

表3 黏合劑種類考察結果Tab.3 Results of binder type investigation
2.3.3 潤滑劑比例篩選 本實驗選擇硬脂酸鎂、滑石粉混合物作為潤滑劑,前者具有良好的附著性、潤滑性、抗粘附性,但助流性不理想,故選擇與助流性較好的后者合用,兩者比例通常為1∶6~1∶7,用量為0.5%~2%。本實驗選擇用量為1%,將滑石粉、硬脂酸鎂按1∶6、1∶7 比例混合后與顆粒混勻壓片,固定漏斗法測定休止角,發現比例為1∶6 時顆粒流動性更好,休止角為27.72°,壓片后片劑外觀光潔,硬度為4.15 kg/cm2,崩解時限為6 min,故確定其作為潤滑劑比例。
2.4 關鍵質量屬性、關鍵工藝參數確定 基于香菊片制備工藝風險評估及特性,結合上述實驗結果,綜合考慮當前條件下所有可控的、對實驗結果可能造成影響的因素。最終確定,稀釋劑用量、黏合劑用量、潤滑劑用量為關鍵工藝參數,片劑成型率、硬度、有效成分含量為關鍵質量屬性。
2.5 含量測定 參考文獻[11]報道。
2.5.1 色譜條件 十八烷基硅烷鍵合硅膠色譜柱(250 mm×4.6 mm,5 μm);流動相甲醇?0.035%磷酸(5∶95);體積流量1.0 mL/min;柱溫30 ℃;檢測波長270 nm;進樣量10 μL。
2.5.2 對照品溶液制備 精密稱取沒食子酸對照品7.80 mg,置于50 mL 量瓶中,50%甲醇溶解稀釋至刻度,輕微振蕩搖勻,即得(質量濃度為0.156 mg/mL)。
2.5.3 供試品溶液制備 取素片10 片,研細,精密稱取1.5 g 粉末至錐形瓶中,50% 甲醇溶解,40 ℃下超聲(360 W、50 Hz)處理60 min 后取出,室溫下放冷,濾過,置于25 mL 量瓶中,50%甲醇定容至刻度,輕輕搖勻,即得。
2.5.4 線性關系考察 精密吸取同體積對照品溶液,50%甲醇逐倍稀釋后,在“2.5.1”項色譜條件下進樣測定,以峰面積為縱坐標(Y),進樣量為橫坐標(X)進行回歸,得方程為Y=18.932X-0.054 9(R2=0.999 8),在0.24~1.56 μg/mL 范圍內線性關系良好。色譜圖見圖2。
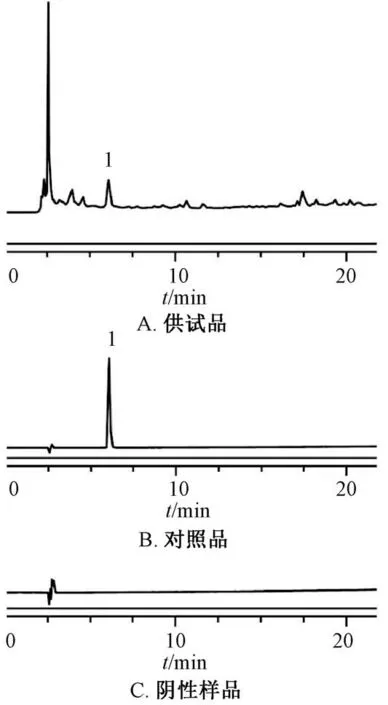
圖2 沒食子酸HPLC 色譜圖Fig.2 HPLC chromatograms of gallic acid
2.6 Box?Behnken 響應面法優化 在單因素試驗基礎上,以乳糖用量(A)、70% 乙醇用量(B)、硬脂酸鎂、滑石粉混合物用量(C)為影響因素,沒食子酸含量(Y1)、成型率(Y2)、硬度(Y3)為評價指標,Box?Behnken 響應面法優化制備工藝[12?13],結果見表4。
通過Design?Expert 10.0 軟件對表4 數據進行擬合,得方程分別為Y1=-0.626+0.042 5A+0.057 2B+1.157C- 0.000 969A2- 0.004 10B2-0.353C2-0.000 353AB-0.005 30AC-0.009 1BC、Y2=- 0.061+0.017 79A+0.064 0B+0.971C-0.000 477A2-0.003 83B2-0.296 9C2+0.000 675AB-0.000 06AC-0.027 08BC、Y3=-14.98+0.401A+1.710B+17.06C-0.009 37A2-0.118 4B2-4.82C2+0.008 87AB-0.060 2AC-0.471BC,方差分析見表5。
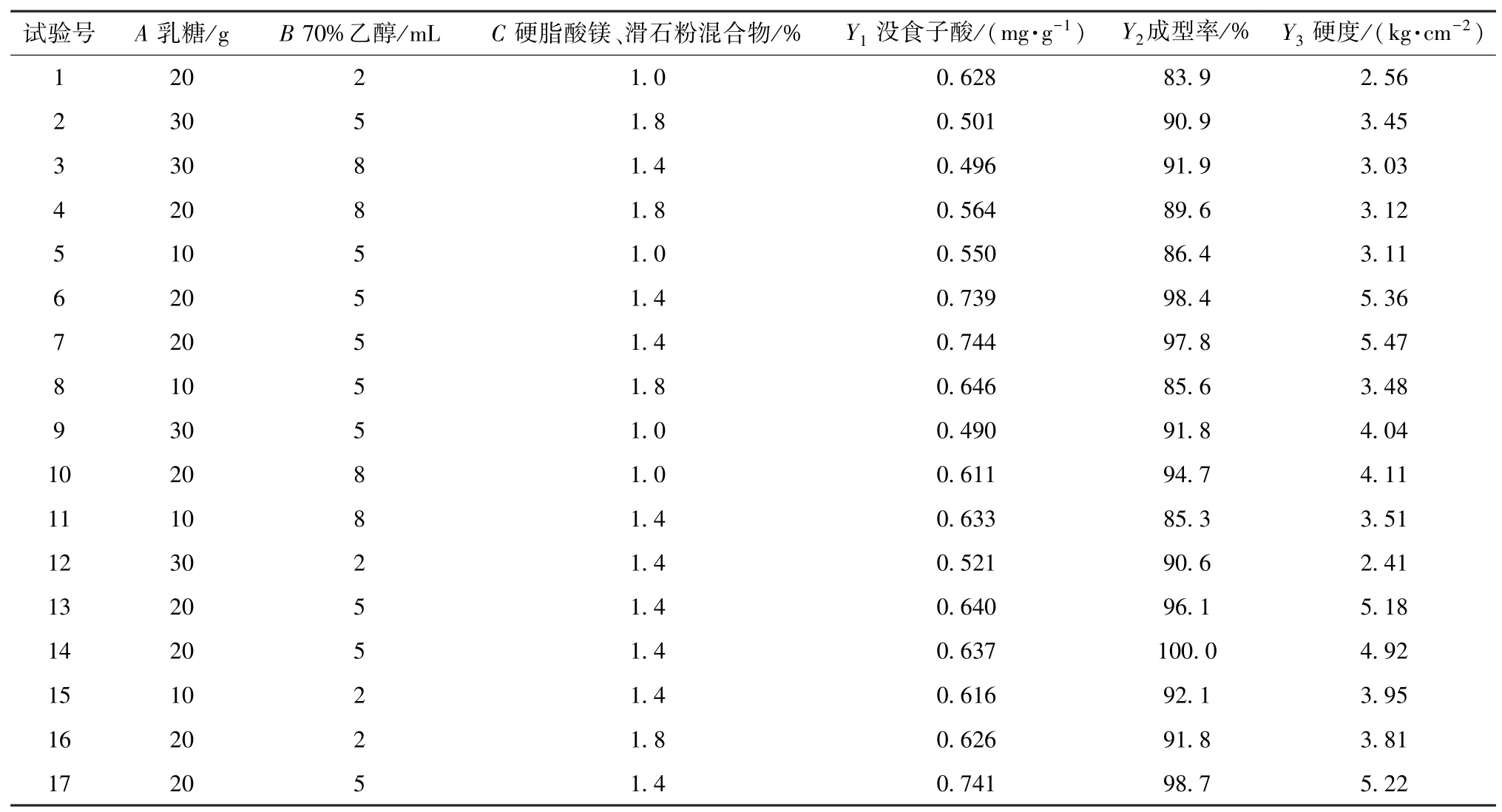
表4 試驗設計與結果Tab.4 Design and results of tests
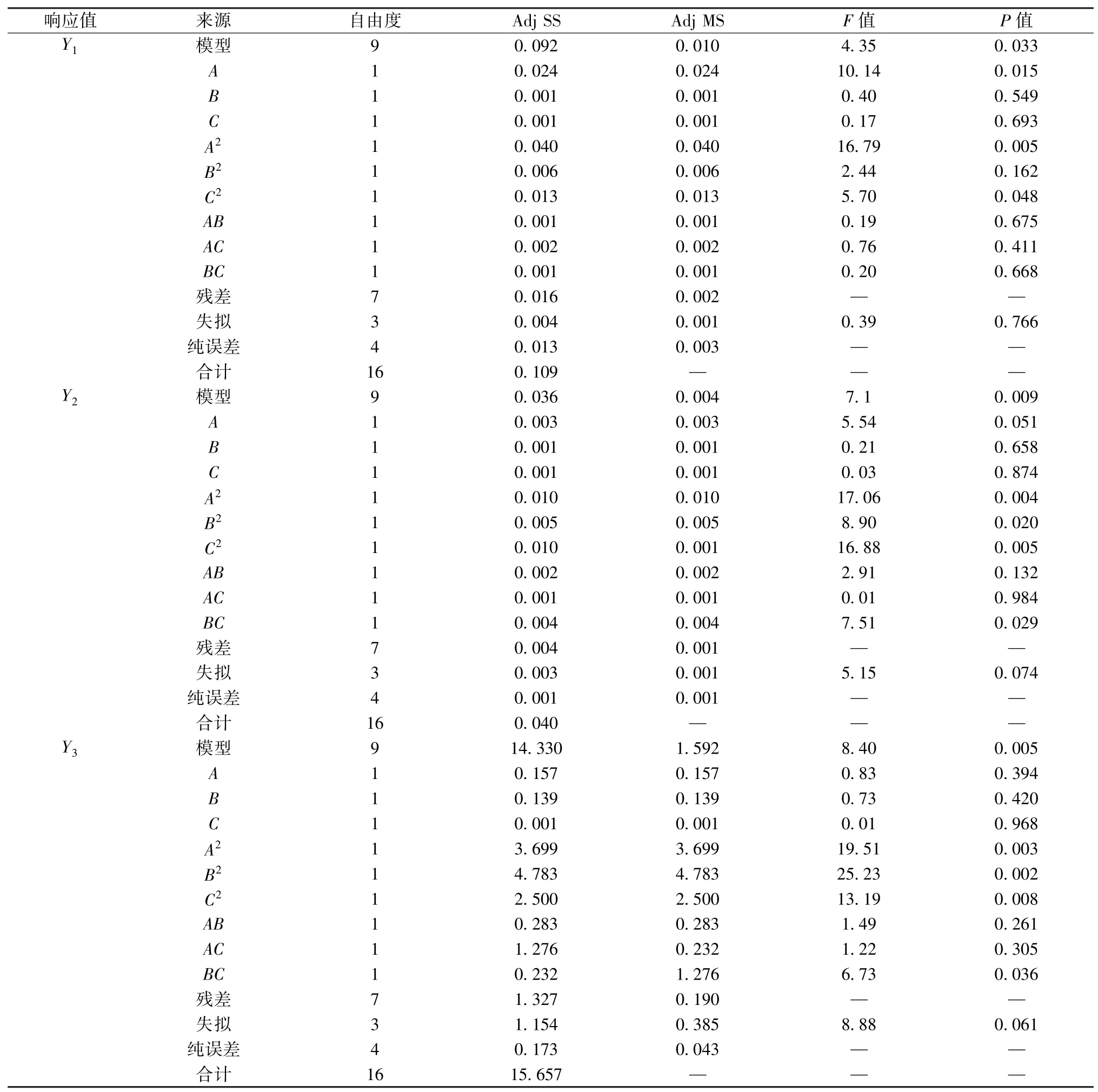
表5 方差分析Tab.5 Analysis of variance
由此可知,3個方程P<0.05,失擬值P>0.05,表明模型顯著,誤差和未知因素影響小,能很好地反映各因素與響應值之間的關系,適用性良好;方程Y1中因素A、A2、C2有顯著影響(P<0.05),AB、AC、BC無顯著影響(P>0.05),影響程度依次為A>B>C;方程Y2中因素A2、B2、C2、BC有顯著影響(P<0.05),AB、AC無顯著影響(P>0.05),影響程度依次為A>B>C;方程Y3中A2、B2、C2、BC有顯著影響(P<0.05),AB、AC無顯著影響(P>0.05),影響程度依次為A>B>C。
響應面分析見圖3~5。由圖3 可知,AB、AC、BC的交互作用影響較小,與方差分析一致;由圖4 可知,成型率隨硬脂酸鎂、滑石粉混合物用量增加呈先升后降的趨勢,響應面陡峭,其原因可能是兩者都是以固態加入,壓片時用量過多或過少均會導致松片或粘沖,從而影響成型率;由圖5 可知,70%乙醇用量有顯著影響,響應面陡峭,其原因可能是粘合劑加入量對藥材粉末粘合程度影響不同,壓片時片劑硬度會有明顯變化。采用Design?Expert 10.0 軟件進行分析,確定最優工藝為乳糖用量19.29 g,70%乙醇用量5 mL,硬脂酸鎂、滑石粉混合物用量1.41%。
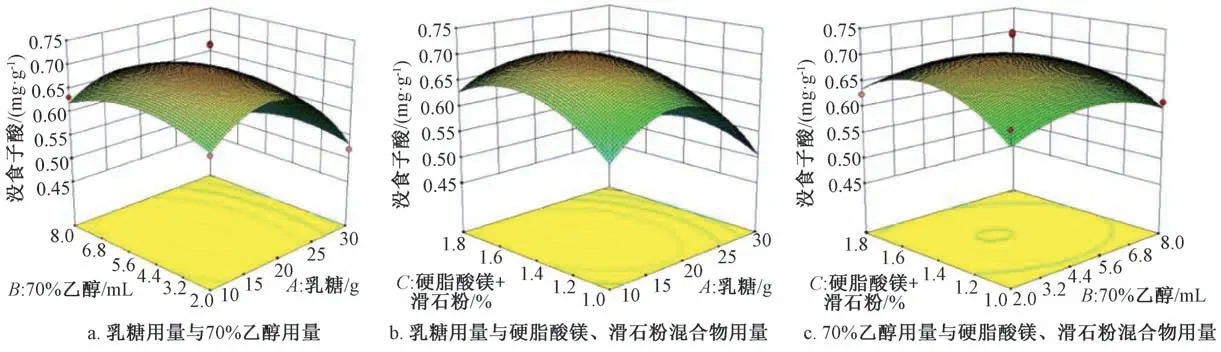
圖3 沒食子酸含量響應面圖Fig.3 Response surface plots for gallic acid content
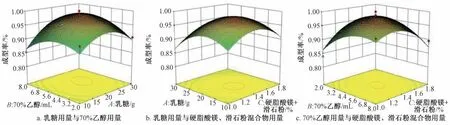
圖4 成型率響應面圖Fig.4 Response surface plots for molding rate
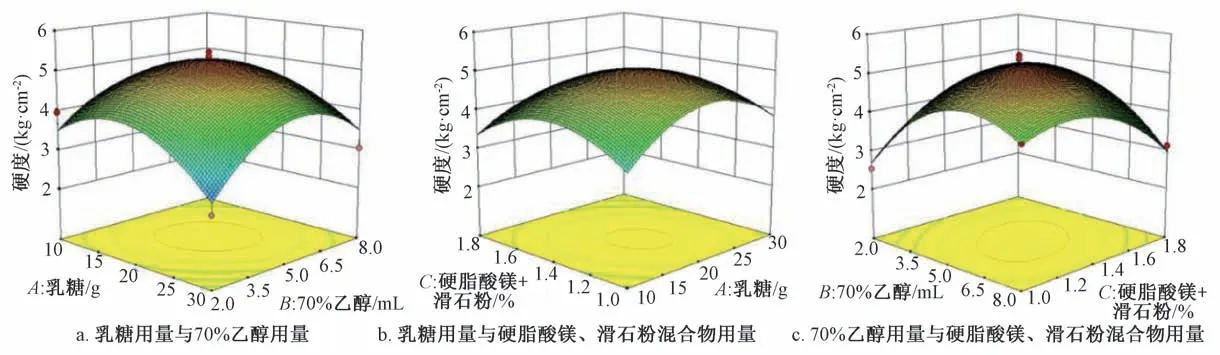
圖5 硬度響應面圖Fig.5 Response surface plots for hardness
通過Design?Expert 10.0 軟件建立設計空間,設定Y1>90%,Y2>95%,Y33~5.5,置信水平α =0.05,結果采用Overlay plot 可視化,見圖6。由此可知,乳糖用量為A1~A2(14.95~21.75 g),70%乙醇用量為B1~B2(3.16~6.42 mL);當硬脂酸鎂、滑石粉混合物用量為1.41% 時,能達到沒食子酸質量分數0.63~0.74 mg/g、成型率大于95%、硬度3~5.5 kg/cm2的目標要求。
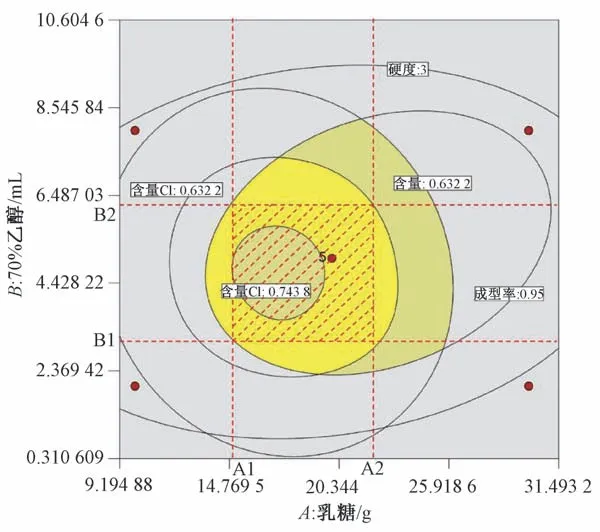
圖6 香菊片設計空間Fig.6 Design space of Xiangju Tablets
根據Box?Behnken 響應面法、設計空間結果,確定主藥、乳糖、70%乙醇用量比例為5∶19∶5,16 目藥篩制粒,60 ℃下烘干,14 目藥篩整粒,硬脂酸鎂、滑石粉混合物比例為1∶ 6,用量為1.41%,混勻后壓制成片。
2.7 驗證試驗
2.7.1 沒食子酸含量 隨機取3 批片劑,每批2份,測得沒食子酸質量分數為0.72 mg/g,RSD 為1.52%,表明各批片劑之間該成分含量均一穩定,制備工藝可靠。
2.7.2 成型率 統計3 批片劑中每批片數總量N1,觀察出現裂片、松片、掉粉、表面粗糙等現象的成品,其總數計為N2,計算成型率,公式為成型率=[(N1-N2)/N1]×100%。結果,每批片劑成型率均大于95%,符合相關標準。
2.7.3 片重差異 根據2020年版《中國藥典》規定的重量差異檢查法,從3 批片劑中各取20 片,精密稱定總質量,計算平均值,再單獨稱定質量,計算其片重差異,范圍在-1.09%~1.86% 之間。結果,3 批片劑的片重差異均在規定的±5.0%范圍內,符合相關要求。
2.7.4 硬度 從3 批片劑中任取6 片,采用硬度測試儀測定其徑向硬度,發現均在3~4.5 kg/cm2范圍內,平均值約為3.9 kg/cm2,表明其硬度適宜。
2.7.5 脆碎度 從3 批片劑中取總片重為6.5 g左右的成品,除掉表面脫落的粉末,精密稱定總質量,再將其依次放入脆碎度檢查儀圓筒中旋轉100次,除去表面細粉,精密稱定質量,計算減失質量。結果,3 批片劑減失質量分別為0.29%、0.31%、0.23%,均未超過規定的1%,同時無斷裂、破碎出現,符合相關標準。
2.7.6 崩解時限 從3 批片劑中各取6 片,采用吊籃法進行檢測,其間需在每管內加入1 塊擋板。結果,所有片劑均在12 min 內崩解,不超過15 min,符合在1 h 內全部崩解的要求。
3 討論
本實驗將QbD 理念運用到香菊片制備工藝中,篩選具有顯著性影響的因素,并對相關數據建立二次多項式回歸模型[14?15],得到設計空間,確定最優工藝,從而明確制備工藝參數與質量屬性之間的關系。
片劑輔料組成和用量對其成型率、操作難度、崩解時限都會產生較大的影響,本實驗以成型性為評價指標,考察不同稀釋劑、粘合劑、潤滑劑對制片的影響,發現以70%乙醇為粘合劑制備的顆粒更緊密,成型性更好,壓片后無缺損,而水、淀粉漿粉末較多;在稀釋劑考察中,α?乳糖顆粒成型率為93.74%,優于淀粉、糊精、微晶纖維素,吸濕率為1.42%。設計空間可直觀展示香菊片在制備過程中關鍵質量屬性達到目標要求時相應關鍵工藝參數的設定值,結果乳糖用量14.95~21.75 g、乙醇用量3.16~6.42 mL 能滿足預定目標。
4 結論
經過QbD 理念優化后,香菊片成型率、脆碎度、崩解時限等均符合2020年版《中國藥典》 要求。本實驗將風險管理、關鍵工藝參數、關鍵質量屬性、設計空間等與香菊片制備工藝優化相結合,展現了研究的主動性與設計的科學性[16],以期在一定程度上控制該制劑質量,提高其穩定性,并為其他中藥復方片劑制備工藝的優化提供參考。

