電絮凝法與電氧化法處理壓裂返排液對比研究*
童志明 吳 達 江 南 陳 武
(1.長江大學化學與環境工程學院 2.中石油HSE重點實驗室(長江大學) 3.中國石油大學(華東)石油工程學院)
0 引 言
壓裂是非常規油氣開發和增產穩產的重要技術手段[1],但是壓裂作業完成后會產生大量返排液,其組分復雜、穩定性強,礦化度、化學需氧量(COD)及總懸浮物(TSS)均較高,毒性大[2]。為避免水資源浪費及環境污染,國內外對壓裂返排液主要處置方式是處理達標后回注地層、排放或回用[3-4]。目前,壓裂返排液主要通過絮凝沉降、氣浮選及水力旋流等方法進行油水初級分離,然后進行化學處理后回注,存在工藝復雜、處理周期長、處理成本高及二次污染嚴重等問題[5]。
與上述幾種常規方法相比,電化學方法具有效率高、反應條件溫和、操作方便及綠色環保等優點[6]。因此,相關學者采用多種形式的電化學方法開展了處理壓裂返排液的研究。牛會娟等[7]采用微電解法對壓裂返排液進行處理,COD去除率達60%。王燕等[8]利用三維電化學氧化工藝處理壓裂返排液,使COD從606.4 mg/L降至68.5 mg/L,含油質量分數從153.7 mg/L降至9.1 mg/L。孟宣宇等[9]對壓裂返排液進行電絮凝處理,COD去除率達92.8%,濁度去除率達97.8%。上述研究所采用的電化學方法不同,效果也不同,但污染物的去除都是電氧化還原及電絮凝氣浮中的一種或多種協同作用的結果。
電絮凝技術主要通過陽極板溶出金屬離子形成高活性、多形態絮凝劑,以網捕、壓縮雙電層、吸附架橋和電中和等作用使廢水中的污染物通過凝聚沉淀或氣浮而分離[10],同時可能有少量有機物在陽極被氧化,分解為小分子而易于被絮凝體吸附,重金屬離子則在陰極被還原或被絮體吸附而去除[11-12]。電氧化技術是通過陽極對有機物進行直接或間接氧化去除污染物[13]。其中,直接電氧化中有機物與電極表面直接發生電子轉移,使有機物被氧化分解為小分子以及N2、CO2等氣體[14-15];而間接氧化中水在陽極表面生成氧化媒介·OH,氧化媒介·OH與有機物發生氧化作用,使其分解[16-17]。因此,電絮凝與電氧化去除污染物的途徑及機理均不同。
針對廢液處理的不同目標,為了選擇出最具針對性及效果最好的電化學方法,有必要弄清電絮凝與電氧化在處理廢液過程的不同點及其原因,但是目前鮮見將電絮凝與電氧化方法進行對比研究的報道。為了探討電絮凝與電氧化方法在處理壓裂返排液表現不同的原因,本文開展了電絮凝氣浮與電氧化處理壓裂返排液對比試驗研究。
1 試驗準備
1.1 試驗儀器與裝置
1.1.1 電解裝置
采用自制的連續監測電解處理廢液電解過程產氣的成套裝置開展試驗,該裝置主要包括:可收集電解產氣的電解槽(有效容積1 200 mL),直流穩壓電源、電極極板、氣體干燥塔、氣體累積流量計及氣體分析儀。

1—直流穩壓電源;2—電解槽;3—電極極板;4—氣體干燥塔;5—氣體累積流量計;6—氣體分析儀。
1.1.2 試驗儀器
儀器主要包括:WYK-60V30A程控型直流電源穩壓器、MFM氣體流量計及MFM610累積量計量器、GT-2000 泵吸式混合氣體分析儀、Thermo AQ2010數字式濁度儀、Vario TOC總有機碳分析儀、7890A/5975C氣質聯用儀(GC-MS)、670型傅里葉紅外光譜儀(FTIR)及CS350H電化學工作站。
1.2 試驗水樣
本試驗所用壓裂返排液水樣取自涪陵工區某井,該水樣pH值為8,色度為499.53,濁度為246 NTU,COD(Cr)為1 620 mg/L,總有機碳(TOC)質量濃度為350.73 mg/L,Cl-質量濃度為19 464.88 mg/L。
1.3 試驗方法
在室溫條件下,量取一定體積的壓裂返排液水樣倒入電解槽中,分別選擇電絮凝氣浮電極體系Al(+)-Al(-)、Al(+)-Ti/RuO2/IrO2(-) 和電催化氧化電極體系Ti/RuO2/IrO2(+)-Ti/RuO2/IrO2(-)、Ti/RuO2/IrO2(+)-Al(-)共4種電極組合,在不同條件下對酸化壓裂返排液進行處理。處理過程中產生的氣體經電解槽的導氣管進入氣體干燥塔干燥,隨后進入氣體累積流量計記錄產氣總量,最后進入泵吸式混合氣體分析儀進行組分及含量分析,并自動記錄、儲存各組分數據。試驗結束后,靜置30 min,再分別收集處理后的壓裂返排液以及裝置底部殘渣。
2 電絮凝與電氧化處理返排液試驗結果對比分析
2.1 處理效果對比
為了對比電絮凝與電氧化對壓裂返排液的處理效果,在電極間距d=4.0 cm、電解時間t=30.0 min、電解電流I=0.5 A、面體比S/V(陰極有效面積與處理壓裂返排液體積的比值)=0.11 cm2/mL的條件下,分別開展電絮凝與電氧化處理壓裂返排液試驗研究,結果如表1所示。

表1 不同組合處理返排液效果對比 %
由表1可知:兩種方法對COD(Cr)去除率都在80%以上;二者相比較,電絮凝法對返排液處理效果更好,壓裂返排液處理后的脫色率達92.92%,去濁率達95.93%,TOC去除率達89.52%,COD(Cr)去除率最高達到90.12%。這是因為電氧化主要依靠氧化作用,在電流較低時,直接和間接氧化作用都不強,而電絮凝卻以其本體為主并輔以電氧化,電極溶解產生的活性絮凝劑與壓裂返排液中帶負電荷的膠體顆粒物(如黏土等)及帶顏色的有機物產生網捕吸附,通過沉降或與氣浮協同作用除去所含污染物;同時絮凝體對大分子的有機物也有一定的吸附能力,使有機物被氧化和被絮凝同時去除,所以電絮凝法的TOC去除率高于電氧化法。
2.2 處理中產氣對比
為了探究電絮凝與電氧化在處理壓裂返排液過程中產生氣體類型及氣體量的差異,在d=4.0 cm、t=30.0 min、I=0.5 A的條件下,采用上述兩類4種電極組合進行對比試驗,研究了不同面積比時,兩類電極體系處理廢液產生的氣體差異,結果如圖2所示。

圖2 電絮凝與電氧化過程產氣對比分析Fig.2 Comparative analysis of gas production between electrocoagulation and electrooxidation
由圖2可見:試驗中檢測到H2、CO2及H2S三種氣體,電絮凝和電氧化方法產氣情況相差顯著,同種處理方法中的兩組電極組合產氣量差別不大。電絮凝與電氧化處理壓裂返排液時產生氣體中以H2(產生的O2量理論上為H2量的)為主,CO2和H2S產量較少。處理壓裂返排液時,當面體比相同時,電絮凝產生的H2量遠高于電氧化,其中電絮凝法中的Al(+)-Al(-)組合H2產量最高;電絮凝和電氧化法處理壓裂返排液都產生H2S和CO2,但后者產氣量均高于前者,表明兩種處理方法中都存在氧化作用,能把壓裂返排液中的有機物氧化成H2S、CO2和H2O等小分子,但電絮凝的氧化作用弱于電氧化;根據H2S和CO2產量可以判斷不同電極組合的氧化性順序為:Ti/RuO2/IrO2(+)-Ti/RuO2/IrO2(-)>Ti/RuO2/IrO2(+)-Al(-)>Al(+)-Ti/RuO2/IrO2(-)>Al(+)-Al(-)。
2.3 處理中陽極消耗對比
通過對不同電極組合在處理廢液過程中陽極消耗的測試,可以判斷電極組合是否有電絮凝作用發生。因此,在試驗前分別對兩類4種電極組合的陽極進行稱量記錄,在d=4.0 cm、t=30.0 min、I=0.5 A、面體比=0.11 cm2/mL的條件下,分別開展兩類4種電極組合處理壓裂返排液試驗,對試驗后的陽極干燥至恒質量,得到4種電極組合的陽極消耗率,結果如圖3所示。

圖3 電絮凝與電氧化陽極極板消耗率對比Fig.3 Comparison of anode plate consumption rate between electroflocculation and electrooxidation
由圖3可知:電絮凝Al(+)-Al(-)、Al(+)-Ti/RuO2/IrO2(-)電極組合的陽極消耗率為17~25 g/(m2·h),隨著面體比的增加而降低;而電氧化Ti/RuO2/IrO2(+)-Ti/RuO2/IrO2(-)、Ti/RuO2/IrO2(+)-Al(-)兩種組合在處理壓裂返排液過程中陽極消耗率為0。分析結果表明:在處理壓裂返排液時,Al(+)-Al(-)、Al(+)-Ti/RuO2/IrO2(-)兩種電極組合可以產生對污染物有絮凝作用的溶解性Al3+離子,而Ti/RuO2/IrO2(+)-Ti/RuO2/IrO2(-)、Ti/RuO2/IrO2(+)-Al(-)兩種電極組合只發生氧化作用,不會發生絮凝作用。
3 電絮凝與電氧化處理返排液機理研究
3.1 電絮凝與電氧化處理后殘渣FTIR分析
為了研究電絮凝及電氧化去除污染物的成分差異,分別取電絮凝及電氧化4種電極組合處理后產生的殘渣,在50 ℃的真空干燥箱中烘干至恒質量,得到待測樣品。采用Nicolet Nexus670型傅里葉紅外光譜儀對樣品進行表征分析,結果如圖4所示。

圖4 4種不同電極組合處理后殘渣的FTIR圖Fig.4 FTIR image of residue after treatment with 4 different electrode combinations
由圖4可知,Ti/RuO2/IrO2(+)-Ti/RuO2/IrO2(-)電極組合處理后的殘渣與原廢液沉淀成分最為相似,而Al(+)-Ti/RuO2/IrO2(-)和Al(+)-Al(-)兩種電極組合處理后的殘渣紅外圖譜中出現很多較小的雜峰,這是因為電氧化過程幾乎不產生有機殘渣,而電絮凝過程產生的絮凝體可以吸附部分有機物,使有機物被絮凝沉淀。
對比光譜的特征峰發現:3 122和1 400 cm-1附近可能是有機酸O-H吸收峰,由于返排液中有機酸吸附在帶正電荷的固體顆粒上并沉降,故可以檢測到有機酸O-H吸收峰;經過電絮凝與電氧化處理后有機酸被氧化分解,處理后的殘渣中有機酸吸收峰減弱或消失,表明電絮凝與電氧化都有氧化作用;765 cm-1附近可能是芳烴C-H吸收峰,在Al(+)-Ti/RuO2/IrO2(-)、Al(+)-Al(-)兩種組合處理后的殘渣里可以檢測到,表明電絮凝可以對返排液中難降解的芳烴進行吸附絮凝并去除。紅外分析表明,電氧化法處理壓裂返排液過程中,主要以氧化的方式降解有機物。電絮凝法是憑借絮凝和氧化的共同作用來去除有機酸以及芳香烴類物質。
3.2 處理前、后主要有機物GC-MS圖譜分析
為了進一步驗證壓裂返排液在電絮凝和電氧化過程中有機物是否發生降解,采用GC-MS分析處理前、后的壓裂返排液。用50 mL CH2Cl2分次萃取一定量的電化學處理前、后的污水樣,收集有機層,濃縮至溶劑完全揮發后,加入30 μL內標物D10-蒽(0.124 mg/mL)和30 μL內標物nC24D50(0.465 mg/mL),混合均勻后上機檢測,得到處理前、后返排液中有機物GC-MS圖,分別如圖5及圖6所示,其中有機物豐度變化如表2及表3所示。

圖5 處理前壓裂返排液中有機物的GC-MS圖Fig.5 GC-MS diagram of organic matter in fracturing backflow fluid before treatment

圖6 四種組合處理后壓裂返排液中有機物GC-MS圖譜Fig.6 GC-MS spectrum of organic matter in fracturing backflow fluid after four combined treatments
壓裂液本身是由清水及各種添加劑(增稠劑、降阻劑、破膠劑、表面活性劑及殺菌劑等)組成的復雜體系,壓裂返排液相比壓裂液更加復雜。根據文獻報道,在壓裂液和返排液中檢測出的有機物已超過80種,主要包括烯類、烷類和芳香類等有機物[18]。因此,在做GC-MS檢測時,盡管添加了內標,仍無法定性定量,只能判別主要有機物的豐度及其變化。從圖5及表2可以看出,壓裂返排液中有12種主要有機物質被檢測出來,這些物質主要為各種添加劑以及從地層中攜帶出來的石油烴類物質。
從表2和表3可以看出,電絮凝和電氧化法都對有機物進行了不同程度的氧化分解,都出現了新的氧化產物。

表2 處理前、后壓裂返排液中有機物豐度變化Table 2 Changes of organic matter abundance in fracturing backflow fluid before and after treatment

表3 壓裂返排液處理后由于降解新增的有機物豐度Table 3 New organic abundance due to degradation after treatment of fracturing backflow fluid
由圖5和圖6可知,電絮凝和電氧化法在處理壓裂返排液時對有機物5和10的處理效果都很好,對其他有機物也有不同程度降解。
表3中序號1~9為電絮凝及電氧化法處理過程中因氧化降解新產生的有機物的豐度,比較新產生的有機物(序號1~9),電絮凝Al(+)-Al(-)組合,氧化產物種類和豐度都比較高。電氧化Ti/RuO2/IrO2(+)-Al(-)組合,對有機污染物去除率高,氧化產物少、豐度低。這是因為電氧化對有機物的氧化徹底,殘留的有機物量少或有機物已經徹底氧化分解為CO2等氣體小分子,這也與前述產氣試驗結果相符合。因此,電絮凝及電氧化工藝可以有效地降解壓裂返排液廢水中的主要有機污染物,而且電氧化法比電絮凝對有機物有更強的氧化降解能力。
3.3 電絮凝與電氧化法處理壓裂返排液活性中間產物分析
為了探究電絮凝和電氧化法處理壓裂返排液過程中的間接氧化作用,有必要對處理過程中產生的活性物質進行檢測。文獻報道,電化學處理廢液過程中會產生H2O2和O3等活性物質,但在廢液中僅存在痕量H2O2和O3等,常規方法難以準確、定量地檢測[19]。因此本試驗H2O2的測定采用Ti(IV)-5-Br-PADAP法測定[6],O3的測定采用靛藍鉀比色法[19]。在最佳條件下電解處理20~70 min,分別測定4種不同電極組合處理壓裂返排液過程中O3和H2O2的質量濃度,結果如圖7所示。
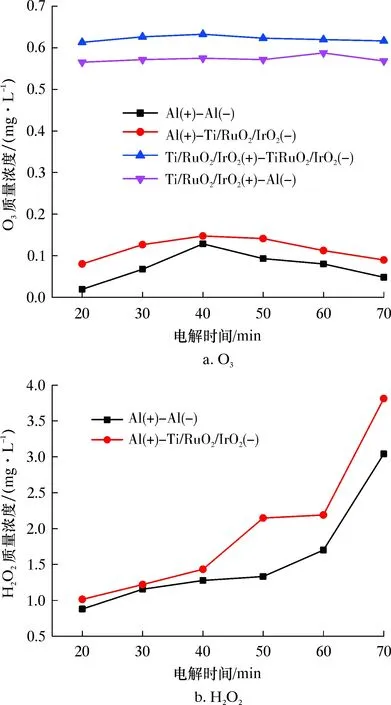
圖7 電絮凝與電氧化過程活性中間物對比分析Fig.7 Comparative analysis of active intermediates in electrocoagulation and electrooxidation processes
由圖7a可知:電絮凝和電氧化處理的壓裂返排液中都可以檢測到O3,Al(+)-Al(-)和Al(+)-Ti/RuO2/IrO2(-)兩種電絮凝電極組合處理過程產生的O3質量濃度隨電解時間的延長先上升后下降,在40 min時質量濃度達到最大,分別為0.128和0.147 mg/L;Ti/RuO2/IrO2(+)-Ti/RuO2/IrO2(-)和Ti/RuO2/IrO2(+)-Al(-)兩種電氧化電極組合處理壓裂返排液產生的O3質量濃度較高,且隨時間變化較小,最高時分別為0.633和0.588 mg/L。這可能是因為電絮凝兩種組合產生的溶解Al3+阻止了氧原子和氧分子的有效碰撞,而Ti/RuO2/IrO2電極不產生金屬離子,不影響氧原子和氧分子的有效碰撞,因此以Ti/RuO2/IrO2為陽極的電氧化法產生的O3較多。
由圖7b可知:電絮凝Al(+)-Al(-)和Al(+)-Ti/RuO2/IrO2(-)兩種電極組合在處理過程中檢測到較多H2O2,而且質量濃度隨電解時間的延長而增大;而電氧化Ti/RuO2/IrO2(+)-Ti/RuO2/IrO2(-)和Ti/RuO2/IrO2(+)-Al(-)兩種電極組合都無法檢測到H2O2。這可能是因為發生了如下反應。
陽極:
H2O-4e→4H++O2
(1)
H2O2→HO2·+H++e
(2)
HO2·→O2+H++e
(3)
陰極:
O2+2e+2H+→H2O2
(4)
溶液中:
2H2O2→2H2O+ O2
(5)
電氧化過程中陽極發生電解水反應,為陰極產生H2O2提供所需的氧氣,而H2O2因不穩定性而存在分解過程,即一方面H2O2會在溶液中發生化學分解和生成;另一方面H2O2會在陽極表面發生氧化,導致H2O2含量較少或無法被檢測到[20]。
3.4 電極電化學性能分析
從電絮凝與電氧化法在處理壓裂返排液過程中產生的氣體類型及氣體量的對比結果來看,兩者產生氣體都以H2為主,H2S和CO2產量都較少,因此氣體量的差異性主要體現在H2產量的不同。不同的陽極在溶液中的溶解速率不同,H2在陰極的產生速率和產量也不同。
為了研究不同電極材料對H2產量的影響,探索電氧化和電絮凝法產氣差異的原因,本文通過穩定電位測試法、Tafel曲線測試法及析氫過電位曲線測試法來研究Al電極和普通Ti/RuO2/IrO2電極的電化學性能與產氣的關系。試驗中將電極置于涪陵壓裂返排液中,工作電極(板狀Al電極和板狀普通Ti/RuO2/IrO2電極)、輔助電極(鉑電極)及參比電極(飽和甘汞電極)構成三電極體系, 利用CS350H電化學工作站對兩種不同材料的穩定電位和極化曲線進行測定,將電極置于常溫下濃度為1 mol/L的NaOH溶液中[21],利用CS350H電化學工作站對試驗中的兩種電極的析氫過電位進行測定,結果如表4所示。

表4 電化學性能測試數據Table 4 Electrochemical performance test data
由表4可知:不同電極的穩定電位和塔菲爾斜率不同。板狀Al電極屬于活潑性電極,在涪陵返排液中的穩定電位低,塔菲爾斜率小;普通Ti/RuO2/IrO2電極屬于惰性電極,穩定電位相對較高,塔菲爾斜率大。當陽極和陰極材料惰性都很強時,H2產量偏低;陽極材料穩定電位低時,H2產量偏高;電極的塔菲爾斜率越小,在極板電極上發生析氫反應的阻力也越小,反應速度相對就快[4]。電絮凝的兩種電極組合都以鋁極板為陽極,因此H2產量相對較高。
對比表4中析氫過電位可知,板狀Al電極析氫過電位遠低于板狀Ti/RuO2/IrO2電極,表明Al陰極析氫更容易。同時,根據文獻[21]對析氧電位和析氯電位的研究結果,采用惰性電極作為陽極,易產生O2和Cl2,Cl2可以溶解在水溶液中形成HClO,解離后形成ClO-,ClO-可以從陰極與H+競爭獲得電子(ClO-+ H2O + 2e → 2Cl-+ 2OH-)[4],從而降低陰極的H2產量。
在相同條件下,板狀Al電極穩定電位低,極化曲線塔菲爾斜率小,析氫過電位低,析氫反應的阻力小,析氫更容易,且電絮凝都采用較為活潑的鋁極板作為陽極,受到HCIO影響小,所以H2產量更高。
4 結論及建議
(1)電絮凝和電氧化法對壓裂返排液COD(Cr)的去除效果都表現出很強的能力,但電絮凝法處理能力更好,其脫色率達92.92%,去濁率達95.93%,TOC去除率達89.52%,陽極消耗達25 g/(m2·h),電氧化陽極消耗為0。
(2)FTIR與GC-MS分析和對活性物的檢測結果表明,電絮凝法在處理壓裂返排液時,絮凝和氧化同時起作用,氧化階段產生的中間活性物質以H2O2為主,絮凝過程可以有效去除壓裂返排液中的顆粒物和芳香烴類有機物。電氧化法在處理過程中,中間活性物質O3產量較多,主要以氧化的方式降解有機物。
(3)電絮凝與電氧化處理壓裂返排液時產生氣體都以H2為主, H2S和CO2產量較少。絮凝法所用的鋁電極穩定、電位低,塔菲爾斜率小,析氫電位低,析氫電位阻力小,因此H2產量較高。而電氧化法對有機物氧化更徹底,所以H2S和CO2的產量均高于電絮凝法。
(4)建議在處理壓裂返排液時,優先選擇電絮凝法,并對電絮凝過程的產氣潛在風險與危害采取通風或去除等措施進行防范,重點關注產H2(O2)的爆炸風險及H2S的健康危害等。

