模擬失重對大鼠聽功能及耳蝸帶狀突觸的影響
李元超,吳 瑋,3*,王 剛,屈昌北,王 磊,李保衛,韓浩倫,李 丹,劉 鋼
(1北京大學解放軍306醫院教學醫院耳鼻咽喉科,北京 100101;2中國人民解放軍戰略支援部隊特色醫學中心耳鼻咽喉科;3國家環境保護環境感官應激與健康重點實驗室;4首都醫科大學公共衛生學院;*通訊作者,E-mail:ent306ww@126.com;#共同通訊作者,E-mail:wanggang306yy@126.com)
內毛細胞帶狀突觸(ribbon synapses,RS),即內毛細胞(inner hair cell,IHC)與Ⅰ型螺旋神經元(spiral ganglion neurons,SGNs)形成的突觸,因前膜活化區內錨定有含C末端結合蛋白2(C-terminal binding protein 2,CtBP2)的特定結構——帶狀體得名,每個IHC可通過帶狀體與多個SGNs形成RS,由其負責完成聲信號的機械-電換能過程并向中樞方向傳導,對聲音的編碼具有決定性作用[1]。RS對多種理化因素都非常敏感,易受噪聲、耳毒性藥物以及衰老等影響發生損傷且難以恢復[2]。失重可導致航天性聽損傷,表現為聽性腦干反應(auditory brainstem response,ABR)閾值暫時性、甚至永久性閾移,嚴重時可增加宇航員執行任務的失敗風險、縮短職業壽命[3,4]。有學者在模擬失重大鼠海馬組織中觀察到突觸活動區范圍明顯減少[5]。但耳蝸RS是否會受到失重影響而發生改變尚不明確。因此,本研究通過觀察模擬失重后大鼠聽功能及突觸帶狀體數量的變化,探討失重對聽覺器官的損傷機制。
1 材料與方法
1.1 實驗動物及分組
48只8周齡雄性SD大鼠(購自斯貝福公司)隨機均分為模擬失重組和空白對照組,每組24只;再依據暴露時間隨機分為1周、4周組,每組12只24耳。模擬失重組大鼠暴露期間始終保持模擬失重狀態;空白對照組常規飼養。在暴露前(B0)、暴露結束后即刻(P0)和脫離暴露環境7 d(P7)進行雙耳ABR閾值和畸變產物耳聲發射(distortion product otoacoustic emission,DPOAE)檢測,并在P0和P7測聽結束后分別處死每組6只大鼠,再解剖分離雙側耳蝸。P7時各組測聽耳數減半,為12耳。實驗前所有大鼠均無噪聲及耳毒性藥物接觸史,雙側耳廓、外耳道及鼓膜未見異常。
1.2 模擬失重方法
采用經典的頭低位模擬失重法(Morey Holton法)[6]:大鼠頭低位、前肢承受部分重量,后肢離地,身體縱軸與水平面成-30°。懸吊期間大鼠可以自由進食水,頭部可自由活動。
1.3 聽力學檢測
1.3.1 ABR閾值檢測 分別于B0、P0、P7時,采用10%水合氯醛溶液4 ml/kg腹腔注射麻醉大鼠,置于37 ℃恒溫電熱毯上,使用聽性腦干反應儀(ICS Chartr EP,Medsen)在隔聲靜電屏蔽室內檢測雙耳ABR閾值。刺激聲為短聲(click),強度為80-5 dB連續測定,衰減間隔10 dB,接近閾值時改為5 dB,以可以重復的Ⅲ波的最低強度為閾值。
1.3.2 DPOAE檢測 選擇初始純音的頻率f1和f2,頻率比f2/f1=1.21;初始音強度L1和L2,強度差L1-L2=10 dB聲壓級(sound pressure level,SPL)。以兩個初始音頻率的幾何均數f0為測試頻率,疊加1 024次,取2f1-f2處聲信號幅值與本底噪聲差值>6為DPOAE引出,選擇f0分別為2,4,8 kHz,測試耳在所有測試頻率上的DPOAE全部引出時方可記為DPOAE通過。
1.4 RS免疫熒光染色檢測
分離的耳蝸采用4%多聚甲醛固定、10%EDTA脫鈣處理后,在解剖顯微鏡下剝離基底膜。于10%山羊血清37 ℃封閉后,采用兔CtBP2抗體(Abcam公司,稀釋比例1 ∶400)4 ℃孵育過夜,山羊抗兔IgG二抗(Abcam公司,稀釋比例1 ∶400)室溫孵育1 h;DAPI染色,在體視顯微鏡下鋪片,抗熒光猝滅封片劑封片。激光共聚焦顯微鏡(Leica TCS-SP8)下觀察并對突觸帶狀體進行計數,評估RS損傷情況。
1.5 耳蝸RS計數
參考Viberg的方法,在計數時以頂回為0%,底回為100%,整個基底膜從頂回至底回分段計數,按照距頂端平均距離共取10個計數段。每個計數段用40倍(oil)物鏡拍攝,然后在其中選取邊長145 μm的正方形為計數視野,每個視野計數13-18個相連的IHC細胞核及RS數量,最后依據整個基底膜樣本觀察到的突觸總數和IHC總數計算整個基底膜上平均每個IHC的帶狀體數量(個/IHC)[7]。
1.6 統計學方法
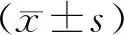
2 結果
2.1 ABR閾值結果
各實驗組在B0、P0、P7時的ABR閾值見表1。B0時空白對照1周組、模擬失重1周組、空白對照4周組和模擬失重4周組間ABR閾值差異無統計學意義;空白對照1周組和空白對照4周組內在B0、P0、P7時ABR閾值差異均無統計學意義(P>0.05)。模擬失重1周和模擬失重4周組在P0時的ABR閾值較B0時顯著升高(P=0.001,P<0.001),且模擬失重4周組ABR閾值高于模擬失重1周組(P=0.001)。模擬失重1周和4周組大鼠在P7時的ABR閾值較B0時差異均無統計學意義(P分別為0.833,0.955)。

表1 各組暴露前(B0)、暴露結束后即刻(P0)及脫離暴露環境7 d(P7)ABR閾值
2.2 DPOAE結果
各組間大鼠在B0、P0和P7時的DPOAE引出率差異無統計學意義(P>0.05,見表2)。

表2 各組暴露前(B0)、暴露結束后即刻(P0)及脫離暴露環境7 d(P7)DPOAE引出情況
2.3 免疫熒光結果
模擬失重后大鼠耳蝸IHC細胞核移位、排列散亂,至P7時有所恢復(見圖1)。各組大鼠突觸計數結果見表3。模擬失重1周組在P0時帶狀體數量較空白對照1周組下降53.23%,到P7時該組帶狀體數量仍比空白對照1周組低31.61%;而模擬失重4周組在P0時的帶狀體數量較空白對照4周組下降了61.19%,到P7時該組的帶狀體數量比空白對照4周組低39.12%。空白對照1周組在P0和P7時的帶狀體數量差異無統計學意義(P=0.074);空白對照4周組在P0和P7時的帶狀體數量差異也無統計學意義(P=0.295)。在P0時,模擬失重1周組較空白對照1周組、模擬失重4周組較空白對照4周組的突觸帶狀體數量均明顯減少(P<0.001),且模擬失重4周組大鼠P0時突觸帶狀體數量減少較失重1周組更明顯(P<0.001);模擬失重1周組和模擬失重4周組在P7時突觸帶狀體數量均較P0時數量增多,且差異有統計學意義(P<0.001),但仍分別低于空白對照1周組和空白對照4周組(P<0.001),且模擬失重4周組低于模擬失重1周組(P<0.001)。

白色短箭頭所示為IHC細胞核,白色長箭頭表示CtBP2標記的突觸帶狀體,黃色長箭頭表示移位的IHC細胞核圖1 各組大鼠免疫熒光染色結果Figure 1 Immunofluorescence staining results of rats in each group

表3 各實驗組P0、P7內毛細胞突觸帶狀體計數
2.4 帶狀體數與ABR閾值相關性分析
對大鼠RS帶狀體數量與ABR閾值進行相關性分析,結果顯示RS帶狀體數量與ABR閾值負相關(r=-0.759,P=0.029,見圖2)。失重組大鼠ABR閾值在暴露結束后即刻最高,脫離暴露環境7 d后恢復至暴露前水平,而突觸帶狀體數量在暴露結束后即刻到達最低水平,脫離暴露環境7 d后部分恢復。

圖2 突觸帶狀體數量與ABR閾值相關性分析結果Figure 2 Correlation analysis between RS ribbon count and ABR threshold
3 討論
天宮二號在軌飛行30 d任務圓滿完成標志著中國人在太空的駐留時間記錄刷新,較長時間太空飛行潛在的健康問題也受到更多關注。既往研究[8,9]表明模擬失重可引發聽覺損傷,表現為ABR閾值升高;而損傷機制的研究主要集中于耳蝸毛細胞纖毛紊亂、凋亡和缺失等形態結構和數量的改變。本研究中模擬失重4周內大鼠ABR閾值隨暴露時間延長而提高,且耳蝸IHC表現為核移位、排列散亂,但這些變化均可逆。在以上可逆性損傷之外是否存在聽覺傳入通路上其他敏感部位的損傷,是本研究重點關注的內容。
耳蝸RS因前膜活化區內錨定有含CtBP2的帶狀體得名。含神經遞質谷氨酸的突觸囊泡大量栓系在帶狀體表面,突觸后膜上表達相應受體[1]。外界聲音信號經過機械-電轉化使突觸前膜發生去極化,引起活化區CaV1.3L型鈣通道開放、Ca2+內流觸發谷氨酸釋放,作用于突觸后膜上的受體,引起突觸后膜去極化,聲信號開始在聽神經上傳導[10]。任何導致RS病變的因素均可造成其后的聽神經纖維無法興奮,損傷聽功能。自Liberman等[11]提出噪聲暴露原發性損傷耳蝸RS,而毛細胞缺失和SGNs退行性改變繼發于RS損傷的觀點以來,越來越多的研究[12-14]表明RS是聽覺系統中對各種理化因素作用非常敏感的部位,其損傷或丟失常早于內、外毛細胞的損傷。鄧子宣等[5]研究表明模擬失重2周大鼠CA1海馬神經元的突觸間隙和神經元活動區長度顯著減少;王婷梅等[15]在尾吊4周大鼠的海馬組織中發現突觸后膜興奮性離子型谷氨酸受體的表達明顯下調。這些研究均表明失重對神經中樞突觸造成損傷,而失重環境對耳蝸RS是否產生損傷及具體損傷表現缺乏報道。
本研究使用免疫熒光染色法,以CtBP2抗體標記耳蝸突觸帶狀體并進行計數,評估模擬失重后的帶狀突觸損傷。結果表明模擬失重可導致RS數量減少:模擬失重1周組突觸帶狀體數量較空白對照組下降53.23%,模擬失重4周組帶狀體數量進一步減少,較空白對照組下降61.19%。目前認為各種理化因素損傷RS的機制可能有內耳缺血、活性氧、自由基損傷以及突觸后Ca2+超載等[2,16]。模擬失重導致RS數量減少可能的機制主要有兩方面;一方面,失重引起的體液頭向分布可導致顱內壓升高、內耳淋巴液容積增大[17],到達一定程度后血流減少,影響氧供和代謝,打破機體正常的氧化與抗氧化的平衡體系[18],在內耳可表現為大量的氧自由基蓄積造成損傷;另一方面,失重也會引起機體內多種細胞Ca2+濃度變化,導致細胞內鈣穩態失衡,鈣信號異常[19,20]。而耳蝸IHC的L型鈣離子通道(CaV1.3)和Ca2+穩態對IHC發育和RS突觸前膜的活躍必不可少,內毛細胞RS突觸前膜CaV1.3開放、Ca2+內流是誘發突觸囊泡與細胞膜融合、神經遞質Glu釋放的關鍵步驟[10]。若失重狀態下IHC內的Ca2+濃度以及Ca2+通道電流改變,也可能導致RS數量變化。
脫離暴露環境7 d后突觸帶狀體計數顯示,模擬失重1周組和模擬失重4周組的帶狀體數量在P7時均有所恢復,但仍與空白對照組差異有統計學意義,提示模擬失重4周內可能已對RS造成了部分不可逆損傷。目前關于帶狀突觸損傷的研究結果因暴露條件和研究對象而有差異,但均表明耳蝸內毛細胞RS是易損傷、難恢復的敏感結構[11-14,21]。哈佛大學的Liberman等[11]發現成年小鼠單次100 dB SPL噪聲暴露2 h導致的ABR閾移雖然可以完全恢復,但帶狀突觸數量卻僅能恢復50%,并存在SGN的慢性退行性死亡;Furman等[21]研究表明106 dB SPL白噪聲暴露2 h后的豚鼠,2周后ABR和DPOAE閾值完全恢復正常,但內毛細胞上有多達30%的突觸缺失。這提示我們失重后RS損傷短期內雖然不伴有ABR閾值的永久性閾移,但其有限的自我修復能力可能對聽覺系統造成繼發性損傷。本研究顯示模擬失重4周內的ABR閾移在脫離失重環境7 d后完全恢復,但RS數量仍存在39.12%的缺失,若RS數量不能隨著恢復時間延長進一步增多,可能在遠期造成繼發性聽損傷。
本研究對模擬失重環境后大鼠RS帶狀體數量變化進行了初步觀察研究,明確了模擬失重會導致其數量減少,且脫離暴露環境后RS有一定程度的恢復,但恢復期設定較短,有必要在今后的研究中延長恢復期,明確遠期的RS恢復程度及聽功能水平。模擬失重導致的RS損傷對聽功能影響的具體特點尚不明確,還需在下一步研究中結合反映RS功能的復合動作電位以及ABRⅠ波振幅、潛伏期等檢測指標來確定。

