同卵雙生單人表型眼-耳-脊柱綜合征1例
代佳秋 朱琳 王思霽 陳子琦 向長超 歐陽曦 康厚墉
重慶醫科大學附屬第一醫院耳鼻咽喉科(重慶 400000)
1 病例資料
患者,女,9歲,漢族。自幼右耳耳廓畸形并外耳道閉鎖。5歲時因腹痛就診于當地醫院,腹部超聲檢查發現右側腎缺如,患兒發育較同齡人一致,智力正常,言語發育好。患兒為第一胎,同卵雙胎之一,孕38周足月生產,出生時體重2.55kg,出生無缺氧史,無明顯黃疸等。其孿生姐姐無耳廓畸形及腎缺如。母親孕5月有感染史,無特殊用藥,無糖尿病等代謝疾病史。父親左足第四、第五趾并趾畸形,簡單查體未發現聽力障礙及顏面部畸形,未行相關聽力學檢查。否認耳廓畸形、耳聾及腎缺如家族史。
體檢:生命體征正常,表情自然,神清,查體及對答配合,視力正常,面部對稱,無唇裂、眼球皮樣囊腫。右耳原耳廓處多數結構無法辨認,殘耳呈臘腸狀,Marx分度Ⅱ度,外耳道閉鎖,殘耳前方有一細小瘺口(見圖1),左耳耳廓發育正常,耳道通暢,鼓膜完整。面部發育稍不對稱,右側口角較左側稍高,雙側肋脊角區無叩擊痛。

圖1 患兒術前外貌特征A.正面觀;B.側面觀Fig.1 Appearance of Patient before operation.A.front view;B.lateral view
輔助檢查:①純音測聽:純音聽力測試右耳傳導性聾,語言頻率平均聽閾氣導70dB,骨導10dB,左耳聽力正常。②顳骨高分辨CT右側外耳道狹窄,右鼓室腔小、聽骨鏈、耳蝸、半規管及前庭骨性結構正常,左側正常(見圖2)。③肋軟骨三維重建可見胸3-胸4椎間隙變窄,胸6椎體形態失常,呈蝴蝶椎改變,胸5、6椎體融合,胸6-7間隙變窄,左側第8-9后肋聯合,右側第6、7后肋及腋段融合,前段呈分叉狀改變(見圖3)。
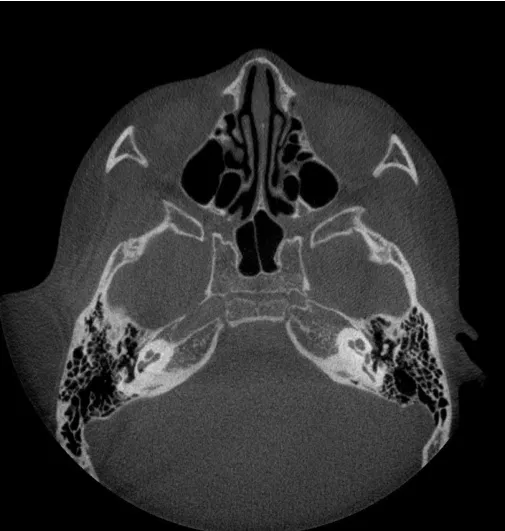
圖2 患兒顳骨CT圖像,右側耳廓畸形外耳道狹窄,內耳及中耳結構正常,左側正常Fig.2 CT image of temporal bone.Right auricle abnormality and stenosis of external auditory canal;normal structure of in‐ner ear and middle ear;normal left side
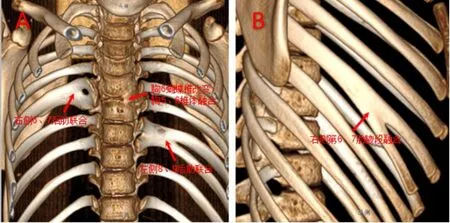
圖3 椎體及肋骨畸形A.正面觀;B.側面觀Fig.3 Deformity of vertebrae and ribs;A.front view;B.lat‐eral view
2 討論
OAVS是一種累及多器官系統的嚴重先天畸形,臨床表現復雜多樣,目前報道的其發病率約為1:45000[1,2],其典型表現為眼、耳、脊椎異常,其中眼部異常可表現為眼球角膜緣皮樣囊腫、皮脂瘤、眼瞼缺損、小眼或無眼等;耳部異常表現為小頜、小耳、附耳、耳前瘺管、感音神經性聾、傳導性聾、外耳道閉鎖、面神經異常等[3]。除此之外,OAVS還經常合并其他系統發育異常。顱面部畸形可表現為半面短小、面部不對稱、巨口、牙齒發育異常等;心血管系統畸形可表現為先天性心臟病(法洛四聯癥,間隔缺損,大血管移位,主動脈弓形異位、右位心);泌尿生殖系統異常表現為單側腎發育不全,雙輸尿管,腎異位,腎積水,輸尿管積水;中樞神經系統異常表現為胼胝體脂肪瘤,小頭畸形,腦膨出,脊椎畸形,Arnold-Chiari畸形,其他系統出現畸形的概率約為50%。研究表明典型表現(眼、耳、脊椎)越嚴重,其出現其他系統異常的概率越高[4]。目前,OAVS尚無統一的診斷標準,目前普遍認為副耳是此類疾病的共同表型,耳廓畸形或副耳合并半面短小是診斷OAVS的最輕標準[5]。普遍接受的診斷標準是包括以下兩種或兩種以上的異常:耳畸形(包括小耳畸形和副耳屏)、半面發育不良(包括小頜畸形)、眼球皮樣囊腫或脂皮樣囊腫或椎體異常(融合或半椎體)。在本病例中,患兒未表現出眼睛發育異常,但同時出現了耳廓畸形及椎體發育異常,并出現累積其他系統的情況(單側腎缺如)。OAVS正確完善的診斷是治療的前提。對于疑似OAVS患者,應完善其他系統評估以發現其他系統缺陷,盡早于相關科室就診。而頜面部畸形嚴重影響患者的外貌和心理健康,應盡早手術矯治。對于耳廓畸形,目前公認的手術時間為8歲左右,年齡過小肋軟骨尚未發育完全,而年齡過大擇肋軟骨出現鈣化,影響雕刻效果[6,7]。近年來也出現了一些人工材料用以代替肋軟骨,如medpor支架,其優點在于不需要術者術中雕刻,對手術技巧要求不高,其次肋軟骨支架對血供要求較高,而人工材料擇對血供無依耐性,同時也適用于肋軟骨鈣化的患者[8]。OAVS多為傳導性聾,根據畸形程度選擇助聽器或手術治療均能提高患耳聽力。其中Frenzel等在2013年根據高分辨CT的結果提出了一個術前評價標準,致力于更好的評估手術治療的可行性,納入的評價指標有乳突和中耳的氣化情況、前庭窗、面神經走行等,總分是16分,16~13分是簡單組、12~9分是中等組、8~5分是困難組、4~0分是高風險組,簡單組通過手術獲得良好聽力的可能性大,而困難組則不建議行中外耳成形術[9]。對于不符合手術條件的患者,可行BAHA、人工耳蝸植入術[10]。本例中患兒已于我院完成Ⅰ期及Ⅱ期耳廓成形術(見圖4-5),顳骨CT發現其中耳結構完整,聽骨鏈分化好,行中外耳成形術有很高的機會獲得較好聽力,本例患兒計劃二期術后軟骨支架穩定存活后再行外耳道及鼓室成形術以改善聽力。
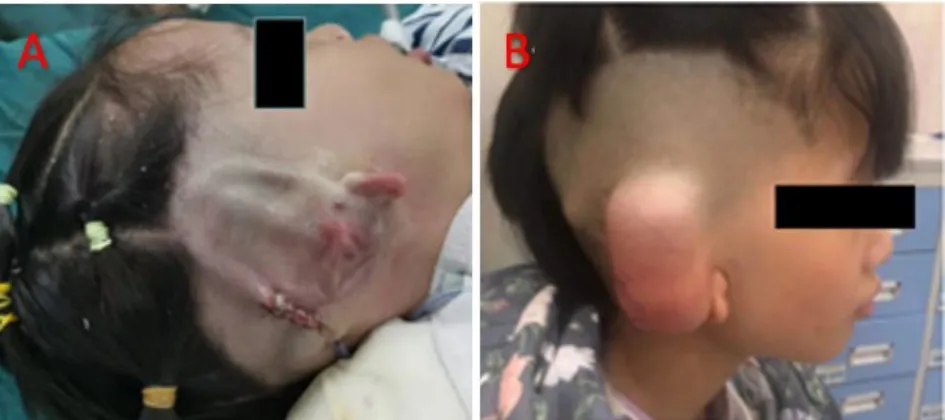
圖4 一期術后側面觀。A.術后即刻;B.水囊注水后Fig.4 Lateral view after the first stage.A.Immediately after operation;B.After water injection
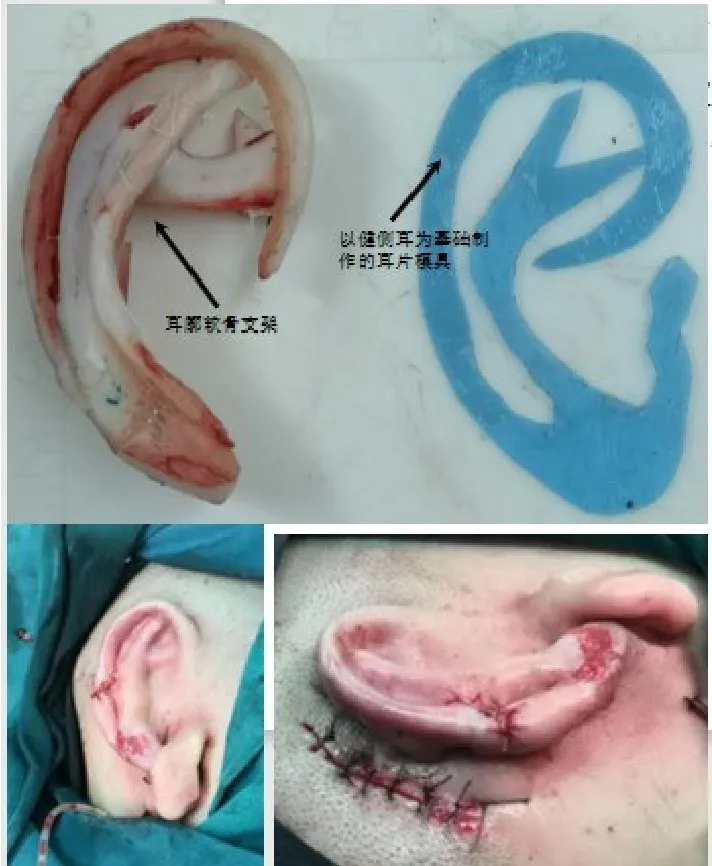
圖5 Ⅱ期術后形態Fig.5 The view after the second stage
OAVS發病機制目前尚不清楚,目前認為是環境及遺傳多種因素共同作用的結果。咽弓在胚胎第4周開始發育,由間充質細胞組成,而顱面發育的一個重要特征是腦神經嵴細胞的形成。因此該過程中某些基因及蛋白質的表達可能決定了OAV的表型特征及嚴重程度。目前研究認為妊娠期糖尿病、血管活性藥物,吸煙和多胎妊娠等環境因素均會影響該病的發生[3]。近年來遺傳因素越發受到學者的關注,也提出了一些遺傳學證據及模式。對于有明顯家系的患者,能觀察到常染色體顯性遺傳特征。而大多數患者為散發病例,也發現了一些基因突變或染色體異常。比如涉及WNT5B基因的5p13.3-pter區域缺失。22q區域異常也多次被觀察到,其一般表現為部分區域缺失或者22三體。而Lopez E的研究則第一次確定了一個致病基因MYT1。其研究認為突變型MYT1無法調控全反式維A酸受體而導致OAVS發生,但擁有該突變的病例比例較低[11]。值得一提的是,本例患兒為孿生兒,其孿生姐姐頜面部外觀正常,亦未發現相關系統異常。此前已有研究指出,多胎出現OAVS概率較單胎更高。K.Lawson等調查的調查結果表明雙胎及多胎妊娠OAVS患病率高于一般人群,他們認為導致這種現象的原因是在分化過程中雙胎之一出現血管出血或梗塞導致組織供血不足進而分化異常[12]。但其研究僅認為環境因素導致發病,未對遺傳因素進一步評估。本例中患兒父親存在并趾畸形,雖然暫未發現其家族存在相似的病例,但我們認為仍不能排除遺傳因素,其家系遺傳信息將于后續研究中進一步報道。
OAVS是一種復雜的臨床綜合征,臨床表現復雜多樣,但只要抓住其特征性表現即能作出該綜合征的診斷。在治療上應該多學科協助進行,其發病率較低,在多胎妊娠中發病率較一般人群高,目前大部分觀點認為其發病是環境及遺傳共同作用的結果,但仍有待更深入的研究,為該疾病的早期診斷及防治提供理論依據。

