嗜酸性中耳炎1例
唐一萍陳明林柳瑋華龔樹生王國鵬*
1首都醫科大學附屬北京友誼醫院耳鼻咽喉頭頸外科(北京 100050)
2四川省南充市中心醫院耳鼻咽喉頭頸外科(南充市 637000)
3首都醫科大學附屬北京友誼醫院病理科(北京 100050)
嗜酸性粒細胞性中耳炎(Eosinophilic otitis media,EOM)是一種罕見的、難治性慢性中耳炎,以中耳充滿大量黏稠分泌物和/或息肉組織、伴支氣管哮喘或鼻息肉為主要臨床特征[1]。本病發生率較低,對中耳炎的常規治療(如抗生素、鼓膜穿刺或鼓膜切開置管等)效果不佳或易復發。本文中我們報道了1例EOM患者的臨床資料及診療經過。
1 臨床資料
患者,女,57歲,因“雙耳流膿伴聽力下降10年”入院。患者10年前因感冒后出現雙耳悶塞感,伴雙耳聽力下降,曾于外院行雙耳鼓膜穿刺3次,鼓膜切開1次,鼓膜置管1次。鼓膜置管后因雙耳出現流膿癥狀,于當月取出置管,并行抗生素滴耳液治療,流膿癥狀無明顯好轉。病程中無眩暈、無耳痛、無頭痛、無惡心嘔吐、無胸痛、無心悸、無嚴重腹痛腹瀉等其他不適。大小便基本正常。
既往史:有“支氣管哮喘”和“過敏性鼻炎”病史20余年,長期口服西替利嗪、孟魯司特及局部噴用信必可及內舒拿,近兩年未再發作哮喘;因“鼻竇炎、鼻息肉”于2006年、2008年和2011年在外院先后行三次鼻內鏡手術;確診阿司匹林不耐受三聯征4年。
查體:心、肺、腹部和神經系統查體均未見明顯異常。專科查體示雙側鼓膜緊張部大穿孔,可見粉紅色息肉樣新生物突入外耳道,表面附著淡黃色黏稠分泌物(圖1A和圖1B);外鼻無異常,雙中鼻道呈術后改變,黏膜水腫,可見少許半透明息肉樣組織。

圖1 耳內鏡下可見雙耳鼓膜穿孔,鼓室內粉紅色息肉樣新生物突入外耳道,附著黏稠分泌物。A,左耳;B,右耳。Fig.1 The endotoscopic examination reveals that both tym‐panic membranes are perforated,and the pink polypoid neo‐plasm in the tympanum protrudes into the external auditory canal with viscous secretion(A:the left ear;B:the right ear).
輔助檢查:心電圖未見明顯異常;肺CT示雙側支氣管壁多發增厚,雙肺多發索條及磨玻璃密度影,慢性炎癥或陳舊性病變可能。純音測聽示左耳為混合型耳聾,骨導平均聽閾為35dB HL(500、1000、2000Hz聽閾的平均值,下同),氣導平均聽閾為60dB HL,骨氣導差25dB HL;右耳為傳導性耳聾,骨導平均聽閾為20dB HL,氣導平均聽閾為60dB HL,骨氣導差40dB HL。顳骨CT示乳突呈氣化型,乳突蜂房及鼓室內可見軟組織密度影,鼓室內軟組織突入外耳道(圖2A),聽小骨未見明顯骨質破壞(圖2B)。雙側竇口鼻道復合體擴大,部分篩竇及鼻甲結構未見明確顯示(呈術后改變)。血常規示嗜酸粒細胞計數0.89×109/L(正常參考范圍0.02-0.52×109/L),嗜酸粒細胞百分比為13.5%(正常值0.5%-8%)。血清免疫球蛋白E(IgE)檢查:410 IU/ml(正常值為<100IU/ml)。抗中性粒細胞胞漿抗體譜和抗ENA抗體均為陰性,肝腎功能和尿常規均未見異常。

圖2 顳骨高分辨CT示雙耳乳突呈氣化型,乳突蜂房及鼓室內可見軟組織密度影,突入外耳道(圖A白色箭頭),聽小骨未見明顯破壞(圖B黑色箭頭)。Fig.2 A temporal bone high-resolution CT image(axial view)shows that the pneumatic mastoid and the tympanic cavity are fulfilled with soft tissue,which protrudes into the external auditory canal(white arrows in Fig.A).There is no evident damage to the ossicular chain(black arrows in Fig.B).
診斷:嗜酸性中耳炎(雙),過敏性鼻炎,鼻竇炎,支氣管哮喘,阿司匹林不耐受三聯征。
診療經過:術前1周開始雙耳滴用激素抗生素滴耳液(地塞米松磷酸鈉注射液以1:10加入氧氟沙星滴耳液中,5滴/次,3次/天);口服潑尼松龍30mg,晨起頓服,每日一次,連續用7天;一周后,在全麻下行雙耳鼓室探查及鼓室病變切除術。術中見雙耳鼓室內充滿黃色黏稠分泌物和粉紅色質軟息肉樣新生物,鼓室黏膜腫脹。切除新生物送病檢,并清除鼓室內分泌物后,鼓室內填塞地塞米松浸潤的明膠海綿。術后病理蘇木精-伊紅染色示:送檢組織可見大量嗜酸性粒細胞(圖3)。術后給予鼓室內地塞米松浸潤的明膠海綿換藥,每日兩次,5日后清除明膠海綿,開始滴用地塞米松氧氟沙星滴耳液。術后2周復查耳內鏡,見雙側鼓膜大穿孔,未見息肉及黏稠分泌物(圖4A和圖4B)。術后2月隨訪患者,訴雙耳無流膿癥狀。
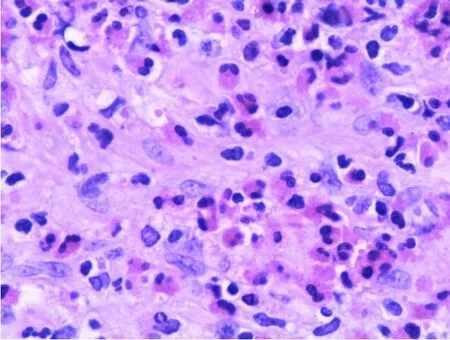
圖3 鼓室息肉石蠟切片,鏡下見大量嗜酸粒細胞聚集(HE染色,X400)。Fig.3 Paraffin section of the tympanic polyp reveals a number of eo‐sinophils in the tissue(HE staining,X400).
2 討論
EOM是一種罕見的難治性慢性中耳炎,其特征是耳內溢液高度黏稠,常與支氣管哮喘和鼻息肉伴發。此病發病年齡多在50-60歲,62%的患者為女性,男女比例約為1:2,多數為雙側發病。其臨床特征:中耳內大量黃色黏稠分泌物,亦可見息肉組織,分泌物病理學和細胞學檢查可見大量嗜酸粒細胞浸潤[2-4]。EOM在CT上可見到鼓室和乳突氣房內充滿大量的軟組織影,但多無聽骨鏈、骨質侵蝕,且常伴有明顯擴張的咽鼓管及雙側鼻竇炎。
2011年,Iion等人提出了EOM的診斷標準[3],主要診斷依據:分泌物或者病理檢查中有嗜酸性粒細胞浸潤的分泌性中耳炎或慢性中耳炎。次要診斷依據:1、極為黏稠的中耳分泌物;2、常規中耳炎治療無效;3、合并有支氣管哮喘;4、合并有鼻息肉。確診條件:主要診斷依據陽性+兩條或者兩條以上的次要診斷依據。同時需排除嗜酸性肉芽腫性血管炎(Eosinophilic granulomatosis polyangiitis,EG‐PA)、嗜酸粒細胞增多癥。EGPA又稱為Churg-Strauss綜合征,是一種系統性血管炎性疾病,其主要特點為壞死性血管炎、組織器官嗜酸粒細胞浸潤和血管外肉芽腫形成,患者往往還伴有難治性的哮喘、外周血嗜酸粒細胞增多、慢性鼻竇炎和過敏性鼻炎等癥狀,多有心臟及神經系統等器官病變,少部分患者可以出現分泌性中耳炎、感音神經性聽力下降等癥狀。在出現血管炎之前,EGPA相關的中耳炎與EOM的表型特征非常相似。因此單純從耳鼻喉專科檢查來區分這兩種疾病有困難,需要進行全身系統檢查[5]。本病例符合EOM的診斷標準,且無心臟和神經系統癥狀和體征,心電圖、肝腎功能、尿常規和自身免疫性抗體檢測未見明顯異常,故不考慮EGPA。此外,EOM還應與肉芽腫性多血管炎(原名Wegener肉芽腫)鑒別。肉芽腫性多血管炎是一種壞死性肉芽腫性血管炎,主要侵犯上、下呼吸道和腎臟。當鼻腔、鼻竇和耳部受累時,可出現鼻竇炎和中耳炎的癥狀,抗生素治療效果欠佳。肉芽腫性多血管炎患者通常有鞍鼻、腎功能不全和自身免疫性抗體的異常,無哮喘癥狀及嗜酸粒細胞升高。本病例外周血和術后病理均有嗜酸粒細胞增多,無外鼻異常,無腎功能不全和自身免疫性抗體的異常,故可排除肉芽腫性多血管炎的可能。
EOM的治療應根據中耳病變的嚴重程度來選擇合適的治療方式[6]。EOM可分為兩個類型三個級別:鼓膜完整時為分泌性中耳炎(Otitis media with effusion,OME)型,鼓膜穿孔時為慢性中耳炎(Chronic otitis media,COM)型;OME型和中耳黏膜無明顯增厚的COM型為G1級,中耳黏膜增厚伴息肉形成且位于鼓室內的COM型為G2級,中耳黏膜增厚伴息肉形成且突入外耳道的COM型為G3級。G1和G2級患者對局部激素治療有效,但當病情明顯加重,出現聽力明顯下降及眩暈癥狀時,應該全身給予激素沖擊治療;G3級患者,對于單純激素治療效果較差,需手術切除外耳道和鼓室內息肉組織,然后鼓室內放置激素浸潤的明膠海綿,并輔以抗生素和全身激素治療。
因EOM極易復發,EOM患者行鼓室成形術前須仔細評估中耳病變的嚴重程度[7]。手術效果與術前中耳病變狀態密切相關,若中耳黏膜病變輕微,可嘗試行鼓室成形術,圍手術期輔以激素治療,術后可獲得良好效果[4,7];而如果中耳出現了嚴重的肉芽組織增生性病變,行鼓室成形術后復發率高[2]。此類患者通常行分期手術,一期手術切除外耳道和鼓室內息肉組織,并輔以抗生素和全身激素治療,保證較長一段時間的干耳后再考慮行鼓室成形術。對伴有雙側重度感音神經性聾的EOM患者,可行人工耳蝸植入術[6]。本患者屬于COM型G3級,屬于最難治療的類型,我們在術中清除了鼓室內分泌物及息肉組織后,術后繼續用地塞米松氧氟沙星滴耳液滴耳,效果良好,目前仍在嚴密隨訪中。
綜上,嗜酸性中耳炎是一種特殊類型的中耳炎。臨床上對于有雙耳閉塞感、雙耳流膿、聽力下降等癥狀,行抗生素治療、咽鼓管吹張、鼓膜穿刺或鼓膜切開置管等治療后效果不明顯或易復發,同時伴支氣管哮喘或鼻息肉的患者,如果查體見鼓室內有黏稠黃色分泌物和/或息肉組織,應考慮EOM的可能。EOM診斷時須與EGPA和肉芽腫性多血管炎鑒別。EOM患者治療上應給予以糖皮質激素為主的綜合性治療,并根據中耳病變的嚴重程度來選擇合適的治療方式。

