乳腺神經內分泌腫瘤一例
周武琳,陳銳,程曉明,劉勝珊,王云,趙青青
遵義醫科大學附屬醫院甲狀腺乳腺外科,貴州 遵義 563000
原發性乳腺神經內分泌癌(neuroendocrine breast cancer,NEBC)十分罕見,占所有乳腺癌發生率的不足0.1%。腫瘤通常表現為ER和PgR陽性和HER-2陰性[1]。2003年,世界衛生組織(WHO)把神經內分泌乳腺癌定義為至少50%的腫瘤細胞中一種或多種神經內分泌標記物呈陽性染色的上皮源性腫瘤[2]。然而,在2012年修訂的WHO分類中刪除了50%的診斷臨界值,因此目前診斷NEBC無需特定的腫瘤細胞表達閾值。本文報道1例我院2020年7月收治的NEBC患者,并對既往文獻進行綜述,旨在提高對NEBC的認識,指導臨床經驗,以便提高對NEBC的診治水平。
1 病例簡介
患者女性,48歲,于2020年7月6日因“發現左側乳腺腫塊3 d”入院。左乳腫塊大小5 cm×4 cm,無壓痛,無乳頭溢血及溢液,局部皮膚無破潰、流膿,門診以“左乳腺腫塊”收住入院。體查:左乳外上象限觸及5 cm大小腫塊,質韌,活動尚可,與周圍組織邊界清楚,雙側腋窩及鎖骨上、下未捫及腫大淋巴結。彩超+超聲造影:左側乳腺12~3點鐘方位距乳頭約13 mm處探及大小約54 mm×26 mm實性低回聲腫塊,邊界不清,形態不規則,呈分葉狀,見毛刺征,內部回聲不均,結合超聲造影診斷為乳腺癌,BI-RADS 5類(圖1)。乳腺鉬靶顯示左乳外上象限腫塊影伴左側腋下淋巴結影(BI-RADS分類:0類),見圖2。
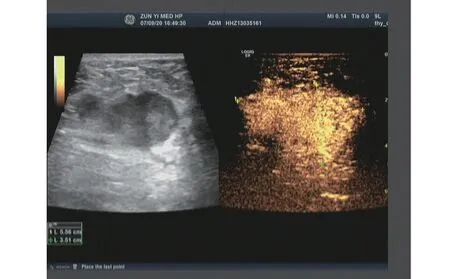
圖1 乳腺彩超及超聲造影

圖2 左乳外上象限腫塊影伴左側腋下淋巴結影
于2020年7月7日在局麻下行“左乳腫塊穿刺活檢術”,術后病理:(左乳腺)浸潤性癌。免疫組化報告:(左)乳腺浸潤性癌2級(腺管形成3分,核異型2分,核分裂2分)。免疫組化染色示腫瘤細胞:CK(+)、GATA3(+)、GCDFP-15(-)、E-Ca(+)、P120(+)、CgA(+)、Syn(+)、CD56(+)、Ki-67(60%+)、ER(-)、PR(-)、HER2(0),結合組織形態及免疫表型,考慮伴神經內分泌特征的浸潤性癌。于2020年7月15日予以TEC(多柔比星脂質體40 mg+環磷酰胺800 mg+白蛋白紫杉醇400 mg,每3周為一個療程,共6個療程)方案化療,于2020年11月10日行“左癌改良根治術”,術后病理:眼觀,(左側乳腺1)距乳頭1.5 cm、皮下3 cm見一灰白質硬區,8 cm×6 cm×4 cm,切面灰白,質中,大部分區域壞死,(左側乳腺2)大小6 cm×6 cm×4 cm,切面灰白,質硬,大部分區域壞死;鏡下,(左側乳腺1、2)伴神經內分泌特征的浸潤性癌,乳頭見惡性腫瘤累及,基底未見腫瘤組織累及。免疫組化:組織內腫瘤細胞CK(++)、P120(膜+++)、Syn(+++)、CD56(++)、E-Cadherin(+)、CgA(弱+)、GATA3(偶見弱+),P63、TTF1、SMA、Vimentin、GCDFP-15、ER、PR、HER2均陰性,Ki-67增殖指數約60%(見圖3、圖4)。術后予以卡培他濱輔助化療。
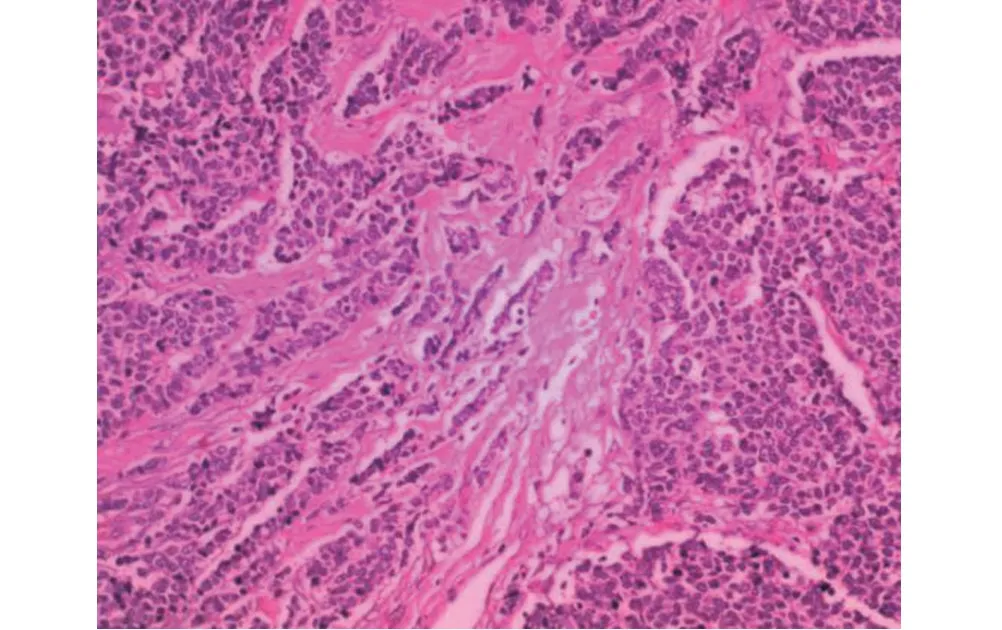
圖3 光鏡下見腫瘤細胞排列成腺泡狀、索梁狀,局部可見浸潤性導管癌成分,乳頭可見惡性腫瘤浸潤(HE×100)
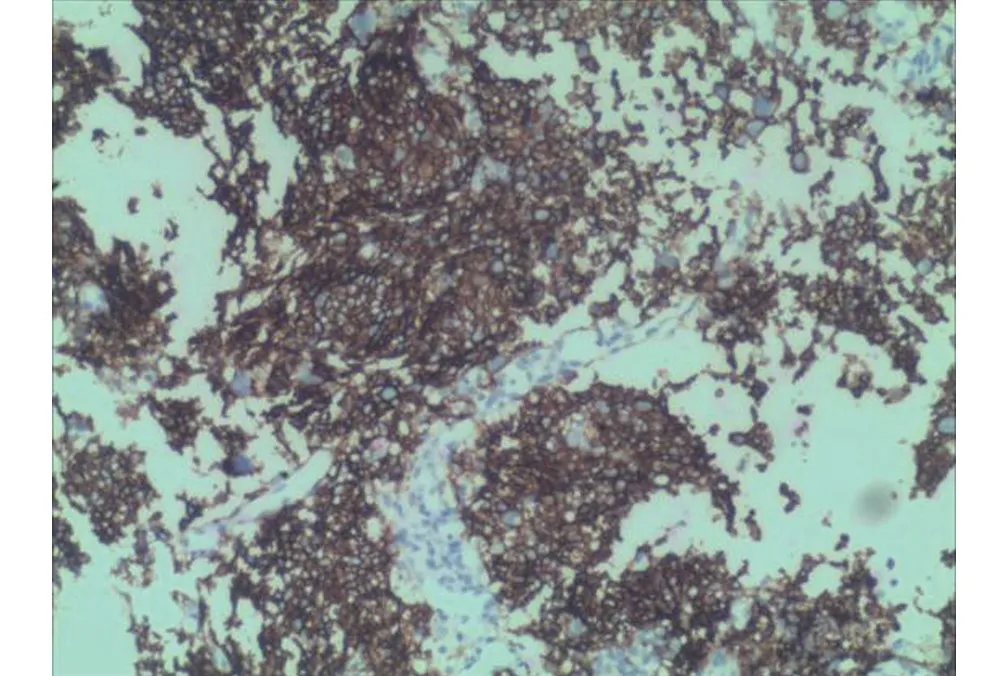
圖4 Syn(膜+)彌漫強陽;CD56強陽;CgA(膜弱+)(IHC×100)
2 討論
NEBC的概念在1963年由Feyrter和Hartmann首次提出,他們將NEBC定義為鏡下形態類似腸道類癌的浸潤性乳腺癌[3]。1977年CUBILLA等[4]報道了8例NEBC,并對NEBC的病理學分類與預后作出了相關描述,但其診斷標準未達成共識。直至2003年,WHO將其定義為至少50%的腫瘤細胞中一種或多種神經內分泌標記物呈陽性染色的上皮源性腫瘤,并且將其列為乳腺癌的一個獨立亞型[2]。由于NEBC發病率低、神經內分泌標志物在乳腺癌診斷中尚未常規應用,且NEBC在臨床上或在基礎免疫組織化學上難以識別,因此在臨床工作中應當嚴格按照診斷標準進行診斷以降低漏診率。
細胞起源和分類乳腺神經內分泌癌的機制尚不清楚。通常認為NEBC起源于腫瘤干細胞在上皮細胞和神經內分泌細胞中的分化。另一個假設是它來自遷移到乳房的神經嵴細胞或來自乳房組織中的神經內分泌細胞。總而言之,就NEBC細胞來源目前尚無研究闡明其機制,今后可進行更多相關研究來證實。為了更為有效地判斷預后和指導臨床治療,2003年WHO將其分為4個亞型:實性神經內分泌癌、非典型類癌、小細胞/燕麥細胞癌和大細胞神經內分泌癌[2]。2012年WHO腫瘤分類又對NEBC進行了重分類[5],將伴神經內分泌癌特征的癌分為3個類別:高分化神經內分泌腫瘤、低分化神經內分泌癌/小細胞癌、伴有神經內分泌分化的浸潤性乳腺癌。本病例中患者的術后病理提示具有神經內分泌特征,局部見浸潤性導管癌成分,因此屬于伴有神經內分泌分化的浸潤性乳腺癌。
臨床特征及診斷NEBC臨床表現與非特殊類型的乳腺癌相比沒有明顯區別,常表現為乳房無痛性腫塊,質硬,邊界欠清,可伴或不伴乳頭溢血溢液,極少數患者因異位激素分泌過多而出現類癌綜合征的相關表現。通過乳腺彩超、鉬靶或MRI來確診NEBC非常困難,NEBC在彩超或超聲造影中常表現為形狀不規則的腫塊,容易誤診為乳腺纖維腺瘤或其他良性病變。在鉬靶中NEBC呈不均勻、邊界不清的圓形或橢圓形腫塊,部分見毛刺征、鈣化,因此診斷NEBC時影像學檢查均缺乏特異性。NEBC的診斷基于形態特征和神經內分泌標志物,因此組織病理學檢查仍然是診斷NEBC的金標準,神經內分泌標志物檢測可協助診斷NEBC,如突觸素(synaptophysin,Syn)、嗜鉻粒蛋白A/B(chromogranin,CgA/B)。
治療NEBC最佳初始治療方法的先決條件是明確診斷和分期[6]。手術是早期NEBC治療的基石,腫瘤的位置及臨床分期決定了手術方式,類似于非特殊組織學的原始乳腺癌,但由于NEBC的罕見性,目前對于手術切除范圍尚未達成共識。查閱相關文獻發現對于浸潤性Ⅰ~Ⅱ期患者可行保乳手術,后期進行殘余乳腺放療或乳房切除術。在T4腫瘤和炎性癌中未能找到前哨淋巴結的情況下,如果懷疑有淋巴結轉移,則應行腋窩淋巴結清掃術,且至少要切除10個淋巴結。對于≤cT2和cN0的乳腺癌前哨淋巴結微轉移患者,可不進行腋窩淋巴結清掃[7]。針對高危NEBC患者,放療可降低其復發轉移率,然而HARE等[8]研究發現,乳腺小細胞癌在放療并中不能獲益。由于HER-2在NEBC的表達率低,因此針對HER-2的分子靶向治療在NEBC中的研究報道極少。輔助全身治療應基于個體化治療的精準治療,需考慮到患者的年齡、分期和復發風險等疾病生物學特征[9]。對于激素受體陽性患者推薦使用內分泌治療,對于HER2陽性的NEBC患者推薦使用抗HER2靶向治療,對于高復發風險患者,如三陰型患者可考慮進行化療,局部晚期或不宜手術者可行新輔助治療。此外,對于HER2陰性的NEBC患者,可以進行多基因檢測:如Oncotype、Endopredict等。通過評估相關基因的差異性表達,計算其復發評分(RS),從而預測10年內遠處復發的風險。本例患者屬于三陰型乳腺癌,Ki-67增殖水平高,考慮復發轉移風險高,術前行新輔助化療,術后使用卡培他濱輔助化療,以期進一步降低患者的復發轉移率。
在NEBC的預后判斷方面,由于缺乏相關研究的大樣本數據,已發表的報道相關數據存在很大差異。學者們普遍認為,影響NEBC預后的因素應包括患者年齡、分級、腋窩淋巴結狀態、激素受體、HER2、Ki-67增殖指數和腫瘤浸潤淋巴細胞等。毛勤香等[10]研究發現激素依賴型腫瘤預后較好,多發灶患者預后較差,黏液分化的NEBC預后較好,小細胞NEBC等同于未分化癌,提示預后差。本例患者ER、PR陽性率低,Ki-67增殖指數高,提示惡性腫瘤分化程度低,預后較差。
綜上所述,NEBC是一種少見的乳腺腫瘤疾病,由于其罕見性及相關研究報道較少,目前對NEBC的診斷和治療方案與非特殊型浸潤性乳腺癌相似,大多采用以手術為主的綜合治療。隨著對其認識的不斷深入,越來越多的研究將會為NEBC的治療及預后提供參考依據,指導臨床決策。

