肺移植術后尖端賽多孢子菌致肺部感染一例
強燕飛
尖端賽多孢子菌是一種罕見且致死率高的真菌,本文通過復習1例肺移植術后患者因尖端賽多孢子菌導致肺部感染的治療過程,旨在提高對免疫功能低下的患者真菌病原學的快速診斷,為臨床治療提供經驗。
1 病例
患者,男,69歲,退休。因“雙肺移植術后6年,反復畏寒發熱1個月”入院。患者6年前因塵肺行雙肺移植,術后長期規律口服他克莫司和嗎替麥考酚酯抗免疫排異,6年來生活習慣良好,規律復查肺CT,未見明顯肺部感染。1個月前出現畏寒發熱,最高40℃,體溫無明顯變化規律,當地衛生院予阿莫西林克拉維酸鉀2.4 g靜脈滴注bid抗感染治療5 d無明顯好轉轉診至本院。入院后查體:體溫39.7℃,脈搏108次/min,呼吸20次/min,血壓168/96 mmHg(1 mmHg≈0.133 kPa)。神志清,精神軟,表淺淋巴結未觸及,頸軟,頸靜脈無怒張,甲狀腺不大,雙肺呼吸音粗,未聞及干濕啰音,心率108次/min,律齊,未聞及明顯病理性雜音,腹軟,肝脾肋下未及,全腹無明顯反跳痛,腎區無叩擊痛,臉頰及雙下肢輕度浮腫,四肢肌力V級,病理征未引出,雙足背動脈搏動存在。輔助檢查:血常規:C反應蛋白(CRP)51 mg/L,白細胞(WBC)8.8×109/L,中性粒細胞比例(N%)82%,紅細胞(Hb)123 g/L,血小板計數(PLT)159×1012/L,腦鈉肽(BNP)89.7pg/ml。生化:白蛋白31.8g/L。血氣分析:pH 7.55,二氧化碳分壓(PaCO2)26 mmHg,氧分壓(PaO2)72 mmHg,氧飽和度92%,血沉8 mm/h,降鈣素原(PCT)0.15 ng/ml,自身抗體陰性,二便常規無殊。腫瘤標志物:CA-199 114 U/ml,CA-125 294 U/ml,余無殊。痰培養:未見細菌生長。G試驗、GM試驗及隱球菌試驗均陰性。入院后第2天行肺CT提示右下肺感染,兩側胸腔積液(封四彩圖8)。予頭孢哌酮舒巴坦針2.0靜脈滴注q8 h抗感染治療,1周后仍有畏寒發熱,抗感染效果不佳。于入院后第8天完善氣管鏡檢查,提示右中間支氣管狹窄,中間支氣管炎性改變,予灌洗、刷檢術,真菌培養,同時對肺泡灌洗液行NGS檢測。5 d后NGS檢測結果提示尖端賽多孢子菌。改用伏立康唑針0.2 g靜脈滴注q12 h抗真菌治療,5 d后伏立康唑針改成伏立康唑片0.2 g bid口服序貫治療,1周后肺泡灌洗液真菌培養結果提示尖端賽多孢子菌生長(封四彩圖9~10)。1個月后復查肺CT提示肺部感染較前明顯好轉(封四彩圖11),次日予伏立康唑片0.2 g口服bid帶藥出院。
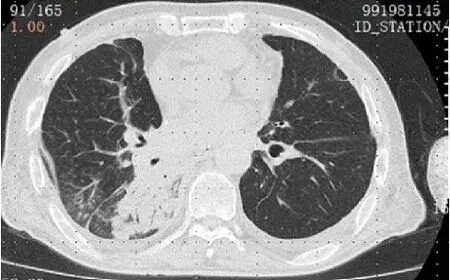
圖8 患者入院第2天查肺CT檢查示右下肺大片感染
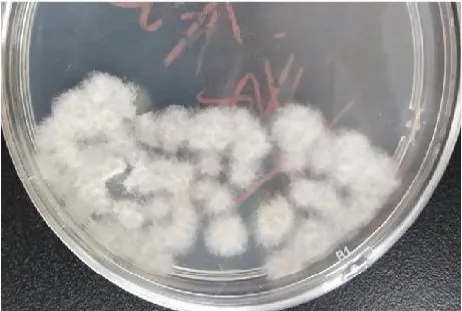
圖9 SDA培養1周見鼠毛樣灰色菌落
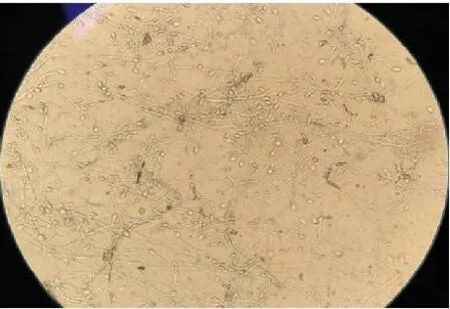
圖10 鏡下見倒卵形分生孢子,環痕產孢(乳酸酚棉蘭染色,油鏡×100)
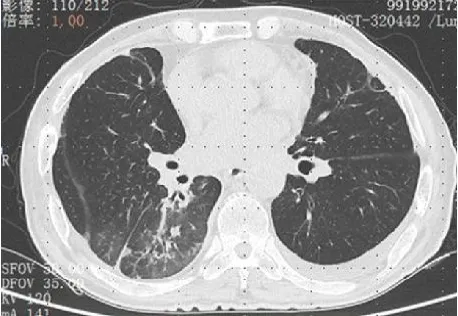
圖11 患者入院1月后復查肺CT示右下肺感染明顯吸收
2 討論
尖端賽多孢子菌是波氏假阿利什菌的無性型,是一種罕見且病死率高的機會性真菌感染,普遍存在于污水、土壤、腐敗物質等受污染環境中。多發生于肺囊性纖維化、艾滋病、器官移植、白血病及長期使用激素或免疫抑制劑等人群中,偶可發生在免疫功能正常者,如創傷、溺水者[1]。它可在肺部疾病患者的鼻竇和氣道定居,在肺移植后長期服用免疫抑制劑者可發展為侵襲性感染[2]。因尖端賽多胞子菌感染的影像學不典型,且組織病理與曲霉菌等菌種難鑒別,雖然以菌落形成的真菌培養是診斷的金標準,但真菌培養耗時長,易出現陰性結果且需多次培養才能確診,因而早期診斷很困難[3-4]。而下一代測序技術(NGS)作為研究病原體特征的一個新手段,具有通量高、準確性好等優勢,在了解病原體的毒力特征、預測疾病嚴重程度及疾病早期發病期進行風險評估等方面起著重要作用[5]。NGS在真菌檢測的突出優勢不僅在于檢測出多種真菌,還可以檢測出耐多藥菌株突變的耐藥基因并分析其耐藥機制,為臨床治療提供重要線索[6]。因尖端賽多孢子菌對兩性霉素B、伊曲康唑等抗真菌藥物的耐藥性使其死亡率在60%左右,因而治療比較棘手。而伏立康唑對其有較高的生物敏感性,具有很好的抗菌作用,已被FDA批準用于尖端賽多孢子菌感染的治療[7]。近年來,聯合使用抗真菌藥物是一個熱點。在一項多中心研究中,Schwarz等[8]發現,在尖端賽孢子菌引起的肺部感染患者中,使用口服唑類(伏立康唑或泊沙康唑或伊曲康唑)聯合一種靜脈用棘白菌素(卡泊芬凈或米卡芬凈)可以使患者獲得更好的療效。本例患者雙肺移植術后,6年來長期規律服用免疫抑制劑,免疫功能受損,為真菌的定植及播散提供了條件。通過及時行氣管鏡檢查,對其肺泡灌洗液早期進行NGS檢測及病原菌培養,準確且快速檢測出致病菌,為及時正確的診斷和治療提供了條件,且治療效果滿意。
綜上所述,對于免疫功能異常病人懷疑肺部真菌感染且不確定病原菌時,要及早進行病原學培養及NGS檢測,盡快找到病原菌,做到早診斷,早治療,早康復。

