宮頸LEEP錐切術治療宮頸高級別病變臨床療效分析
李永琴,陳貴芹
子宮頸癌是女性常見的惡性腫瘤之一,嚴重威脅著女性的生命,2018年數據顯示其發(fā)病率和病死率居全球第四位[1]。隨著宮頸普查及宮頸癌前病變的有效干預,可以有效降低子宮頸癌發(fā)病率及病死率[2]。子宮頸鱗狀上皮內病變(SIL) 是一組與宮頸癌密切相關的癌前病變的統稱,之前稱為宮頸上皮內瘤變(CIN) ,它是宮頸癌發(fā)生發(fā)展過程中的重要環(huán)節(jié)。2014年WHO對女性生殖器腫瘤分類采用二級分類法,將SIL分為 LSIL 和高級別病變(HSIL),LSIL 等同 CIN1,HSIL 包括 CIN3 及絕大多數的 CIN2[3]。2012 年的美國陰道鏡和子宮頸病理學會(ASCCP)指南建議子宮頸環(huán)形電切術(LEEP)是治療 HSIL 的主要方式。經陰道鏡組織病理學確診為 HSIL 的非妊娠患者,應進行干預,行診斷性和治療性宮頸錐切術[4-5]。宮頸錐切術包括LEEP和冷刀錐切術(CKC),術后切除部位仍存在病變持續(xù)存在或復發(fā)的風險。LEEP 術在宮頸HSIL治療方面已經日漸成熟,具有創(chuàng)傷小、手術時間短、術中出血少、術后康復快、術后HPV轉陰率高及并發(fā)癥發(fā)生率低等優(yōu)點。本研究進行回顧性分析了我院100例宮頸HSIL患者,比較LEEP和CKC治療宮頸HSIL的臨床療效。
1 資料與方法
1.1 資料來源:選取2018年6月-2019年6月漯河市召陵區(qū)人民醫(yī)院收治的100例宮頸HSIL患者,分為2組,A組50例,行LEEP;B組50例,行CKC。A組患者年齡29~57歲,平均(31.27±8.29)歲,其中CINⅡ級22例,CINⅢ級28例; B組患者年齡26~52歲,平均(27.8±7.36歲),其中CINⅡ級21例,CINⅢ級29例。
1.2 納入標準:非妊娠患者,術前具備HPV、TCT檢查結果、陰道鏡檢查結果及陰道鏡指導下宮頸活檢病理確診宮頸HSIL患者。
1.3 排除標準:正處于月經期、妊娠期和哺乳期的患者;患有急性生殖道炎癥,檢查前48 h 內有性生活史或經陰道及宮腔操作的患者;患有嚴重心腦血管疾病、血液系統疾病、急性或慢性肝腎功能嚴重損傷、嚴重感染性或代謝性疾病等不能耐受手術者。2組患者臨床資料比較差異無統計學意義(P>0.05)。
1.4 治療方法
1.4.1 儀器設備:選用德國萊斯康(Leisegang)陰道鏡鏡器械和設備,LEEP使用江蘇同人醫(yī)療生產的婦科LEEP手術吸煙凈化系統,CKC則選用常規(guī)手術器械。
1.4.2 手術方法:A組患者LEEP全程在陰道鏡下操作,采用局部麻醉患者取膀胱截石位,常規(guī)外陰、陰道及宮頸消毒鋪巾,絕緣窺器充分暴露宮頸,陰道鏡下再次評估病變區(qū)。宮頸上涂抹復方碘染色,標記宮頸病灶,宮頸3、9點利多卡因局部麻醉,采用金科威高頻電刀,連接電源,負極板固定于患者大腿內側,電切功率55 W,電凝功率45 W。根據患者病灶大小,用環(huán)形電極切刀,在染色區(qū)外3~5 mm進刀,對宮頸進行環(huán)形、椎形切除。根據轉化區(qū)類型選擇切除深度在1.0~2.5 cm,手術不要停頓,切除后創(chuàng)面出血點電球狀或針狀電極電凝進行止血,切除標本大頭針固定宮頸12點處送病理檢查。如果患者Ⅲ型轉化區(qū),需要頸管補切,加做“牛仔帽”,必要時行殘余頸管組織搔刮送病理檢查。依照個人習慣,也可以使用不同型號的三角形電切環(huán)或者“魚嘴”型進行螺旋式切割,術后創(chuàng)面填塞紗布止血。術后予抗生素口服預防感染,術畢24 h 取出陰道內紗布,1個月內禁止性生活及盆浴。B組患者CKC均住院實施,積極完善術前檢查后,月經干凈3 ~7 d 后實施手術。全身麻醉,患者取膀胱截石位,常規(guī)外陰、陰道會陰區(qū)消毒鋪巾;再次消毒陰道宮頸,宮頸3、6、9、12點分別注射稀釋后腎上腺素,用碘液進行標記;在未著色區(qū)域外3~5 mm進刀,沿著宮頸進行環(huán)形切除,切除深度為1.5~2.5 cm。切除完成后對創(chuàng)面進行縫合止血,陰道填塞紗布后24 h 取出,標本送病理科進行檢查。
1.5 觀察指標:手術時間、術中出血量、術后出血時間、宮頸恢復正常時間(術后開始到宮頸無瘢痕時間);術后感染、出血、宮頸粘連發(fā)生率,切緣陽性率、CIN復發(fā)率、HPV清除率。
2 結果
2.1 2組患者圍手術期平均手術時間、出血量、切口愈合時間比較:A組患者平均手術時間(9.21±2.71)min,B組(25.86±4.83)min;A組術中出血量(8.81±2.47)mL,B組(31.59±5.66)mL;A組切口愈合時間(37.31±4.37)d,B組(56.78±5.24)d,見表1。

表1 2組患者手術情況比較
2.2 2組患者術后并發(fā)癥比較:術后出血A組患者1例,B組2例;術后感染A組2例,B組6例;術后宮頸粘連A組1例,B組6例。A組患者術后并發(fā)癥(出血、感染、宮頸粘連)發(fā)生率均小于B組(χ2=10.19,P<0.05),見表2。

表2 2組患者術后并發(fā)癥比較[n(%)]
2.3 2組患者術后隨訪情況比較:A組患者7例(14%)切緣陽性,B組有2例(4%)切緣陽性。在6個月的隨訪期間,A組患者有4例(8%)復發(fā),B組有1例(2%)復發(fā)。A組患者6個月內HPV病毒清除的有43例(86%),B組患者6個月內HPV病毒清除的有46例(92%),見表3。
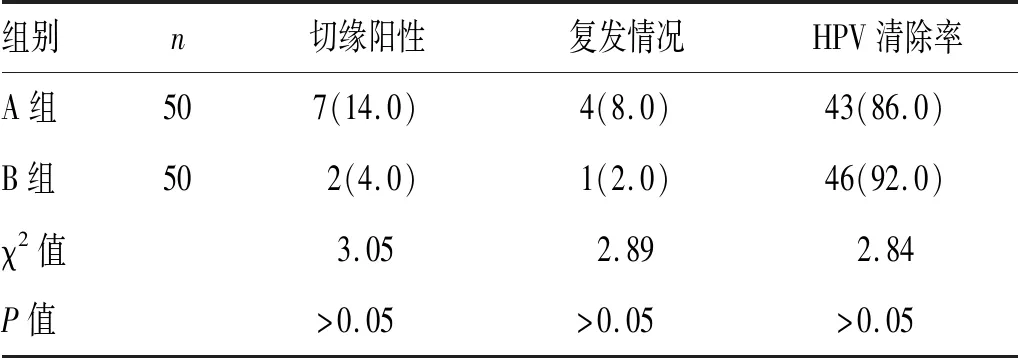
表3 2組患者隨訪情況比較[n(%)]
3 討論
在全球女性惡性腫瘤死亡原因中,宮頸癌排名第三位。由于越來越普及的宮頸細胞學篩查及宮頸癌前病變的治療,宮頸癌的發(fā)病率下降多達75%[6]。宮頸癌前病變的常見治療方式包括CKC、LEEP、激光消融和冷凍治療。 LEEP和CKC是首選的方法,因為它們在治療的同時,可以收集標本,以便進行進一步的組織病理學、診斷和對疾病殘留的預測[7]。CKC近年來在治療宮頸上皮內瘤變取得了一定的療效,其實采用冷刀直接對病灶進行切除,需要手術醫(yī)師充分掌握切除深度,如深度過深會影響宮頸組織的功能。有研究證實宮頸冷刀錐切由于切除宮頸范圍較廣,可致宮頸管短等宮頸機能不全,導致不良妊娠相關并發(fā)癥早產、流產等不良妊娠結局[8]。如切除不足易引起復發(fā),并且手術時間長,過程復雜、繁瑣,出血量多,宮頸愈合時間較長。LEEP術是采用環(huán)形電極切除, 治療原理是經利用高頻交流電借助金屬絲結構傳導并作用于活體組織,依靠電子傳導利用高熱達到切除病變組織目的,具有操作簡便等優(yōu)點[9-10]。在陰道鏡下,在切除病灶的同時電凝止血,環(huán)形電極有多種形狀,便于掌握手術切口深度,因此具有時間短、操作簡單、并發(fā)癥少等優(yōu)點,是更加方便、快捷的治療方法;并且LEEP是對于未來有妊娠需求的年輕患者首選的治療方法,相比LEEP、CKC有較高的早產率。因此,對于患有CIN的年輕女性,特別是那些想懷孕的女性,LEEP是首選的治療方法。LEEP術治療CIN患者,有效縮短了患者術后傷口愈合恢復時間,顯著降低了相關并發(fā)癥的發(fā)生率,且同時減少患者住院,可在門診完成,節(jié)省醫(yī)療資源,減輕患者及醫(yī)保經濟負擔。
結合本研究數據,在手術時間、術中出血量、切口愈合時間上,LEEP組顯著少于CKC組,2組數據差異有統計學意義(P<0.05)。在并發(fā)癥發(fā)病率上,LEEP組低于CKC組,2組差異有統計學意義(P<0.05)。這表明與LEEP相比,CKC可能會增加感染、出血、宮頸粘連的機會。在切緣陽性、復發(fā)、HPV清除率方面,CKC組稍高于LEEP組,但2組差異無統計學意義。由此可見,與CKC相比,LEEP治療HSIL的優(yōu)勢更加明顯,值得臨床選擇。

