預氧化HP40合金表面催化結焦的研究
顏磊,劉京雷,王志遠,徐宏
(華東理工大學機械與動力工程學院化學工程聯合國家重點實驗室,上海200237)
預氧化HP40合金表面催化結焦的研究
顏磊,劉京雷,王志遠,徐宏
(華東理工大學機械與動力工程學院化學工程聯合國家重點實驗室,上海200237)
為研究不同的表面狀態對HP40合金表面催化結焦的影響,分別以水蒸氣、空氣為預氧化氣氛,對HP40合金試樣進行了不同溫度的氧化處理以及氧化后結焦實驗.利用XRD,SEM,TEM對氧化層和焦炭的形貌進行了表征,采用元素分析儀和拉曼(Raman)光譜儀對焦炭的碳氫比和結構進行了分析.結果表明:合金試樣經水蒸氣氧化后,表面形成了針狀、富鐵氧化物;經空氣氧化后,表面形成顆粒狀、致密的富鉻氧化物,隨氧化溫度升高部分試樣的氧化層出現了剝落,剝落后的疏松、多孔表面對催化結焦有強烈的促進作用.焦炭主要為典型的催化絲狀焦,焦絲的直徑約80 nm,還含有少量的熱裂解焦;焦炭縮合度較高,由有序狀炭和無序狀炭共同構成,且石墨化程度低.不同的預氧化氣氛對合金表面氧化狀態影響較大,但是對后續結焦過程,焦炭的形貌和結構無明顯影響.
HP40合金預氧化催化結焦焦炭形貌
蒸汽裂解爐管內表面的結焦和滲碳是制約乙烯裝置長周期正常運行的主要因素.裂解爐管的結焦會導致爐管傳熱效率降低,能耗增加,爐管內徑減小,流體壓降增加,造成乙烯的產量下降.周期性的清焦則引起爐管內表面產生熱疲勞,加速滲碳,最終導致爐管使用壽命縮短[1].
目前,國內外采用的主要抑制結焦方法有:優化爐管結構、添加結焦抑制劑[1-4]、裂解原料預處理[5]和表面涂層技術[6].但無論何種方法,都需要對合金表面的結焦過程進行研究,為開發更為有效的抑焦技術提供理論支持.Grabke等[7-9]研究了爐管內表面催化結焦機理,認為鐵和鎳及其氧化物粒子促進了催化結焦,絲狀焦是催化結焦的典型形貌.在結焦初始階段,催化結焦速率較快,后期速率較慢,結焦也從催化結焦轉化為熱裂解結焦.周建新[10]研究了HP40合金表面的催化結焦過程,結果表明:合金表面的催化結焦經歷了由焦炭形核到焦炭粒子生長,并最終形成絲狀的過程.
合金表面元素組成對結焦過程有很大影響,裂解爐的清焦主要采用空氣、水蒸氣或其混合氣體對爐管進行燒焦.基于此,本課題主要研究預氧化氣氛分別為水蒸氣和空氣時對HP40合金試樣表面氧化層的影響,以及對后續結焦過程及焦炭結構的影響,為今后系統地研究HP40合金表面狀態對催化結焦的影響進行探索.
1 實驗方法
1.1 預氧化實驗與結焦實驗
實驗所用HP40合金試樣尺寸為20 mmX 10 mmX2 mm,其主要元素含量見表1.

表1 HP40蒸汽裂解爐管組成 w,%
預氧實驗在OTF-1200管式爐中進行,結焦在自制的管式電加熱爐中進行.氧化實驗條件:氧化溫度600~900℃,保溫2 h,空氣流量30 L/h;水蒸氣流量0.12 L/h.
裂解原料輕石腦油購置于上海閃爍化工有限公司,密度(20℃)669.8 kg/m3,餾程68~120℃,烴族組成數據見表2.裂解溫度為850℃,輕石腦油流量150 mL/h,稀釋比0.5,裂解時間1 h.

表2 石腦油烴族成分數據 w,%
1.2 試驗儀器
用X-射線衍射儀對氧化層表面進行物相分析;采用掃描電鏡(SEM)和透射電鏡(TEM)對氧化層和焦炭的微觀形貌進行表征;采用德國Elementar Vario EL III元素分析儀分析焦炭的碳氫比;采用激光拉曼光譜儀分析焦炭的化學結構(氬離子激光器波長為512 nm,光譜收集范圍100~2 000 cm-1).
2 結果與討論
2.1 氧化氣氛和氧化溫度對氧化層形貌的影響
圖1為試樣以水蒸氣為預氧化氣氛,氧化溫度分別為600,700,800,900℃條件下,試樣表面氧化層的SEM照片,以及900℃氧化后的試樣表面EDS能譜.圖2為相應條件下氧化后試樣表面的XRD圖譜.
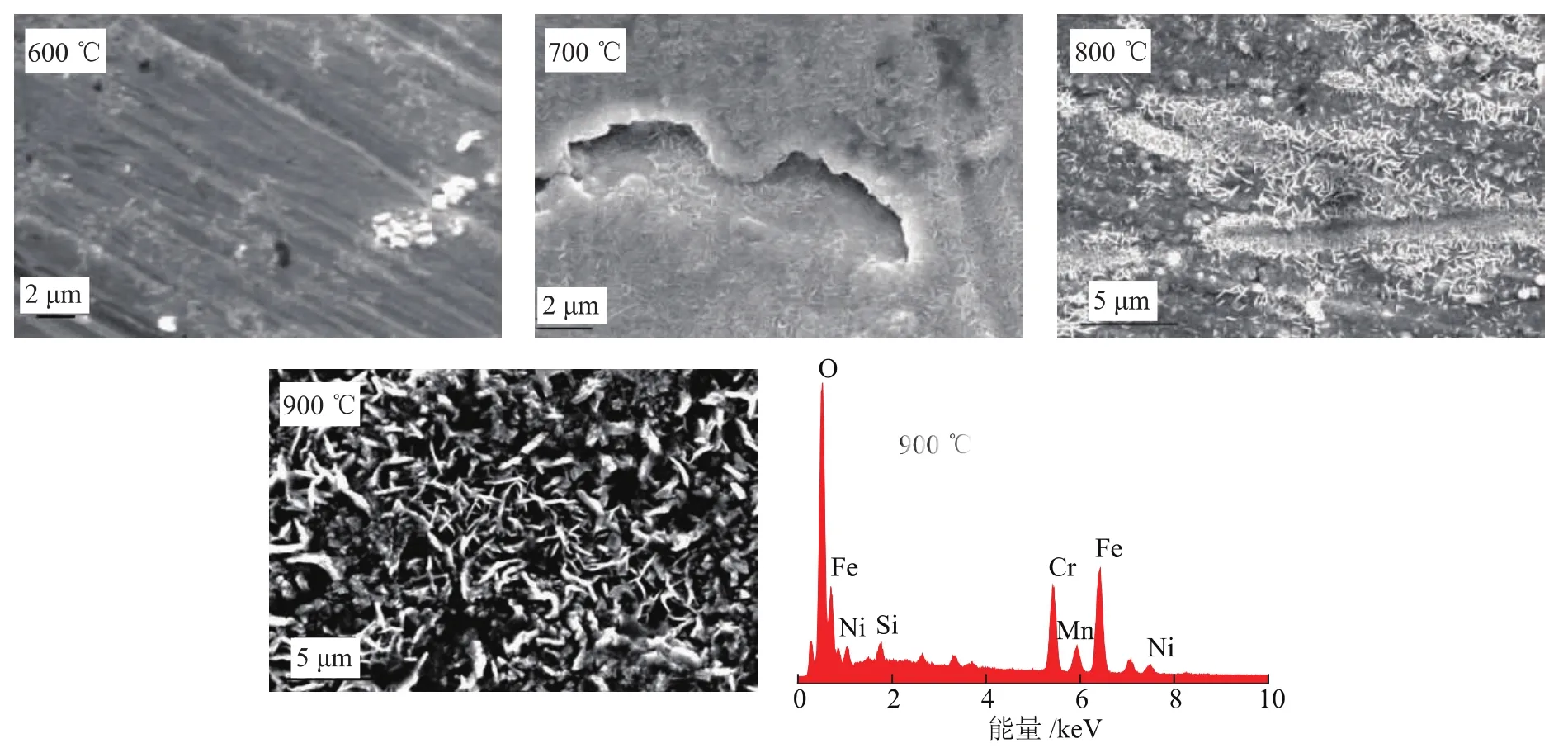
圖1 以水蒸氣為氧化氣氛、不同氧化溫度下氧化層表面的SEM照片和900℃下能譜

圖2 以水蒸氣為氧化氣氛、不同氧化溫度下試樣表面XRD圖譜
由圖1可知:當氧化溫度為600℃時,表面氧化層較平整、光滑;當氧化溫度為700℃時,試樣表面出現了針狀氧化物;隨著氧化溫度的升高,針狀物數量逐漸增多,最終布滿試樣表面.這種針狀氧化物主要是一種富鐵氧化物[11-12].氧化溫度為900℃時,合金試樣表面的EDS能譜也證實了這個結論.由圖2可知,隨著溫度的升高,合金表面氧化層中(Cr,Fe)2O3與FeCr2O4的含量逐漸增加,這兩種氧化物在高溫下具有較好的穩定性和抗氧化性能[12].
圖3為試樣以空氣為預氧化氣氛,氧化溫度分別為600,700,800,900℃條件下,試樣表面的SEM照片以及900℃氧化后的試樣表面能譜.圖4為相應條件下氧化后試樣表面的XRD圖譜.
由圖3可知:氧化溫度為600℃時,試樣表面主要為針狀氧化物;隨著氧化溫度的提高,針狀氧化物逐漸轉變為顆粒狀;當溫度為900℃時,氧化物完全轉變為顆粒狀,但此溫度下,氧化層發生了剝落,由其放大圖可以看出,剝落后表面為一層疏松、多孔組織,結合其XRD圖譜(圖4)可知,未剝落層表面氧化層主要是顆粒狀、致密的富鉻氧化物.顆粒的尺寸較為均勻,在2 μm左右.Luan等[13]利用空氣為預氧化氣氛,在950℃條件下對Incoloy 800合金進行氧化試驗,分析結果表明:經氧化處理后,合金試樣表面的Cr、Mn元素含量增加,Fe、Ni元素含量降低,合金表面形成了一層厚度為1~3 μm的富Cr貧Fe的氧化層,由于具有催化作用的Fe、Ni粒子的減少,因此這種富Cr貧Fe的氧化層對催化結焦有一定的抑制作用.
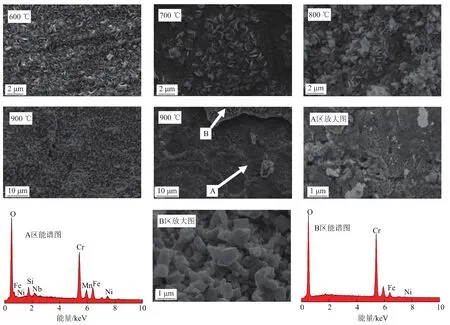
圖3 以空氣為氧化氣氛、不同氧化溫度下氧化層表面SEM照片和900℃下能譜
2.2 焦層的形貌

圖5 HP40合金試樣表面結焦增重圖
圖5為不同氣氛、不同溫度條件下,氧化后的HP40合金試樣結焦增重圖.由圖5可以看出:由水蒸氣和空氣氧化的試樣,表面焦炭的量在一個數量級;在溫度低于800℃時,隨著溫度的升高,焦炭的量均無明顯變化,說明在這兩種氧化氣氛下氧化后,試樣表面狀態對后續的結焦影響不大.空氣氧化的試樣表面焦炭在900℃時急劇增加,其主要原因可能是,試樣表面氧化層剝落后的區域為疏松、多孔的表面,有利于形成焦炭的前軀體的吸附與沉積;另外此區域富含Fe、Ni催化粒子,從而加劇了催化結焦,導致焦炭的增加.
圖6為不同氧化氣氛,氧化溫度分別為800℃和900℃時,HP40合金結焦后表面焦炭的SEM照片.由圖6可知,不同預氧化氣氛下,試樣結焦后表面的焦炭均主要由絲狀焦和少量的粒狀焦組成,焦絲的直徑與形貌并無太大差異.可見在本實驗中,無論是以水蒸氣還是空氣為預氧化氣氛,所形成的表面狀態對結焦過程基本沒有影響,主要為催化結焦.

圖6 氧化后HP40合金試樣結焦后焦炭SEM照片
圖7為不同氧化氣氛、800℃條件下氧化后, HP40合金試樣結焦后表面焦炭的TEM圖.由圖7可以看出,焦絲的直徑在80 nm左右,外表面粗糙不平,為典型的催化焦形貌.圖中焦絲尖端的黑色顆粒為具有催化結焦性能的金屬粒子.

圖7 800℃時HP40合金試樣焦炭的TEM照片
可見,不同表面狀態對催化焦形貌沒有明顯的影響,焦炭為典型絲狀的催化焦.在石腦油裂解過程中,烴類裂解形成的中間體首先沉積在試樣表面,在具有催化作用的金屬粒子作用下分解成碳原子或原子團,這些碳原子溶解并擴散到這些金屬粒子的內部,在金屬顆粒冷端面析出,并將這些金屬粒子頂出試樣表面,上述過程不斷重復,導致金屬粒子冷端面析出的焦炭不斷增長,最終導致絲狀焦炭的形成[7-9].氣相中的結焦前軀體通過自由基反應并入絲狀焦表面,造成絲狀焦的徑向生長[14-15],導致絲狀焦的外表面粗糙不平.

圖8 800℃時焦炭的Raman光譜
2.3 焦炭的結構
采用德國Elementar Vario EL III元素分析儀分析焦炭的碳氫比.結果表明,在水蒸氣和空氣氣氛下氧化后,HP40表面結焦的焦炭樣品中,C元素質量分數均在95%以上.說明在這兩種表面氧化狀態下,焦炭以縮合度較高的結構為主[16-17].這是由于裂解溫度較高,導致結焦過程不斷釋放出氫,焦炭氫含量降低,焦炭的縮合度增加.石腦油裂解過程中,焦炭的生成主要來自于兩方面[18-19]:一方面是通過乙炔聚合反應生成聚乙炔,并最終脫氫、縮合成焦;另一方面是芳烴發生縮合反應的結果:結焦母體首先通過環化反應生成單環芳烴,單環芳烴進一步聚合成多環芳烴,最后脫氫、縮合生成稠環的焦炭.
圖8為氧化溫度為800℃、經不同氣氛下氧化后,試樣結焦后焦炭的Raman光譜圖.由圖8可知,不同氧化氣氛下都顯示了非晶碳材料的兩個典型峰值:G峰(位于1 580 cm-1)和D峰(位于1 350 cm-1).G峰是石墨狀sp2雜化C-C鍵散射的結果,來源于sp2鍵的所有伸縮振動模式(芳香環和烯烴結構).D峰是所有無序狀炭所共有的特征,僅源于芳香環式結構的伸縮振動模式[20-21].2種樣品中的焦炭主要由有序狀炭和無序狀炭組成,是由sp2和sp3組成的混合結構.
D峰與G峰的相對強度比IDG可以作為材料石墨化程度的衡量標準[22].對圖8中2條譜線的1 000~2 000 cm-1區域進行洛倫茲擬合,結果如圖9所示.由圖9可知,2條譜線的G峰與D峰峰位穩定,ID/IG在2.0~2.3的范圍內,變化不大,焦炭的石墨化程度較低(ID/IG>2).

圖9 800℃焦炭的Raman光譜洛倫茲擬合圖
3 結論
(1)HP40合金試樣在水蒸氣氣氛下氧化2 h后,表面形成了針狀的氧化物,隨著氧化溫度的升高,針狀氧化物逐漸增多,氧化層主要是富鐵氧化物,且氧化層中出現了(Cr,Fe)2O3和FeCr2O4兩種氧化物;在空氣氣氛下氧化2 h后,隨著氧化溫度的升高,試樣表面的針狀氧化物逐漸轉變為顆粒狀,氧化溫度為900℃時,試樣表面的氧化層出現了剝落,剝落后的表面是一層疏松、多孔的覆蓋層,促進了催化結焦,而未剝落的氧化層主要是顆粒狀、致密的富鉻氧化物.
(2)以水蒸氣和空氣作為氧化氣氛,氧化后的不同表面狀態的結焦過程主要為催化結焦,焦炭的形貌和結構無明顯差異.焦炭主要是在具有催化性能的Fe、Ni及其氧化物粒子作用下形成的絲狀催化焦,焦絲的直徑大約是80 nm;焦炭中還含有少量的熱裂解焦.焦炭的縮合度較高,由有序狀炭和無序狀炭共同構成,且石墨化程度低.
[1] Wang Zhiyuan,Xu Hong,Luan Xiaojian,et al.Effect of potassium acetate on coke growth during light naphtha thermal cracking [J].Ind Eng Chem Res,2011,50:10292-10297
[2] Wang J D,Reyniers M-F S G,Martin G B.Influence of dimethyl disulfide on coke formation during steam cracking of hydrocarbons[J].Ind Eng Chem Res,2007,46(12):4134-4148
[3] Niaei A,Salari D,Towfighi J,et al.Effect of organophosphorous compounds as coke inhibitors on coking rate in the pyrolysis of naphtha[J].Petroleum Science and Technology,2008,26(18): 2170-2181
[4] 欒小建,徐宏,王志遠,等.SiO2/S涂層與硫磷抑制劑的結焦性能研究[J].石油煉制與化工,2011,42(5):75-80
[5] 王松漢.乙烯裝置技術[M].北京:中國石化出版社,1993: 178-187
[6] Zhou Jianxin,Xu Hong,Liu Jinglei,et al.Study of anti-coking property of SiO2/S composite coatings deposited by atmospheric pressure chemical vapor deposition[J].Materials Letters,2007, 61(29):5087-5090
[7] Grabke H J.Thermodynamics mechanisms and kinetics of metal dusting[J].Materials and Corrosion,1988,49:303-308
[8] 吳欣強,楊院生,詹倩,等.25Cr35Ni耐熱合金表面結焦機制[J].腐蝕科學與防護技術,1999,11(5):274-278
[9] Cai Haiyong,Andrzej Krzywichi,Oballa M C.Coke formation in steam cracker for ethylene production[J].chemical Engineering and Processing,2002,41:199-214
[10] 周建新,徐宏,馬秋林,等.HP40合金氧化表面的催化結焦[J].石油學報(石油加工),2010,26(3):419-424
[11] Mthiazhagan P.Effect of water vapor on the oxidzation behavior of modified low alloy steels at high temperatures[J].The Arabian Journal for Science and Engineering,2009,34(2C):159-178
[12] Pujilaksono B,Jonsson T,Heidari H.Oxidzation of binary FeCr alloy(Fe-2.25Cr,Fe-10Cr,Fe-18Cr and Fe-25Cr)in O2and in O2+H2O environment at 600℃[J].Oxid Met,2011,75: 183-207
[13] Luan Ta-Chi,Roger E E,Lyle F A.Gaseous pretreatment of highalloy steels used in ethylene furnaces:Pretreatment of incoloy 800 [J].Ind Eng Chem Res,2003,42(20):4741-4747
[14] Reyniers M-F S G,Froment G F.Influence of metal surface and sulfur addition on coke deposition in the thermal cracking of hydrocarbons[J].Ind Eng Chem Res,1995,34(3):773-785
[15] Mohamadalizadeh A,Towfighi J,Karimzadeh R.Modeling of catalytic coke formation in thermal cracking reactors[J].Journal of Analytical and Applied Pyrolysis,2008,82:134-139
[16] 陳桂梅,李子木,張香文,等.溫度對USY催化模型吸熱燃料甲苯超臨界裂解結焦及前軀體的影響[J].含能材料,2007, 15(4):305-309
[17] Ren Y,Mahinpey N,Freiting N.Kinetic model for the combustion of coke derived at different coking temperatures[J].Energy and Fuels,2007,21(1):82-87
[18]Reyniers G C,Froment G F,Kopinke F D,et al.Coke formation in the thermal cracking of hydrocarbons.4.Modeling of coke formation in naphtha cracking[J].Ind Eng Chem Res,1994,33 (11):2584-2590
[19] Lee J H,Kim K M,Kim S H,et al.Effects of steam on coking in the non-catalytic pyrolysis of naphtha components[J].Korean Journal of Chemical Engineering,2004,21(1):252-256
[20] Robertson J.Diamond-like amorphous carbon[J].Material Science and Engineering R,2002,37(4/5/6):129-281
[21] Shroder R E,Nemarnich R J,Glass J T.Analysis of the composite structures in diamond thin films by Raman spectroscopy[J]. Physical Review B,1990,41:3738-3745
[22] Reshetenko T V,Avdeeva L B,Ismagilov Z R,et al.Catalytic filamentous carbon structure and textural properties[J].Carbon, 2003,41:1605-1615
Abstract:To study the effect of various HP40 alloy surface status on the catalytic coke formation,HP40 alloy samples were oxidized by steam and air respectively at different temperatures,followed by coking tests.The oxidized surfaces of the samples and the morphology of coke were characterized by SEM,EDS and XRD,furthermore,the C/H ratio and the structure of coke were analyzed by elemental analysis and Raman spectroscopy.Test results showed that when alloy sample was oxidized under steam,a layer of needle type Fe rich oxide was formed on the surface;oxidation under air,Cr rich oxide particles were well dispersed on the alloy surface,with the increase of oxidation temperature,spalling of oxide layer from the alloy surface might happen,in this case,the exposed porous surface could be an ideal area for forming catalytic coke.The coke formed was mainly catalytic filamentous coke with a diameter of about 80 nm,minor thermal cracking coke might exist too.The coke having a very condensed structure consisted of both ordered and amorphous types,and with low graphitization degree. However,the atmosphere of pre-oxidation had more influence on the oxidized surface of alloy,yet just little on the followed coking process,coke morphology and structure.
Key Words:HP40 alloy;pre-oxidation;catalytic coke;coke morphology
A RESEARCH OF CATALYTIC COKE FORMATION ON THE PRE-OXIDATION SURFACE OF HP40 ALLOY
Yan Lei,Liu Jinglei,Wang Zhiyuan,Xu Hong
(State-Key Laboratory of Chemical Engineering,School of Mechanical and Power Engineering, East China University of Science and Technology,Shanghai 200237)
2011-10-31;修改稿收到日期:2012-04-02.
顏磊(1987-),男,碩士研究生,主要從事抑制裂解結焦技術研究工作.
徐宏,E-mail:hxu@ecust.edu.cn.
教育部博士點基金項目(20110074110009),上海市教委曙光跟蹤計劃項目.

