精準肝切除理念在腹腔鏡下Ⅰ型肝血管瘤剝除術中的應用*
郭志唐,龍 奎,王 琳,滕毅山,孫 敏,雷學芬,李世思,陳章彬
(昆明醫科大學第二附屬醫院肝膽外科 650101)
肝血管瘤為肝膽胰外科常見肝臟良性腫瘤,其大多數不需要外科手術治療,原則上以隨訪觀察為主,僅血管瘤較大破裂出血風險較高、明顯進行性增大、診斷不明確或合并明顯臨床表現時才需手術治療[1]。其治療方式多樣、包括外科手術(半肝切除、肝葉切除、血管瘤剝除)、射頻消融、介入栓塞等多種手術方式,肝血管瘤射頻消融雖然一定程度上降低了手術的創傷,但存在消融不全、血管瘤殘留、消融不徹底的問題[2],介入栓塞存在較高的復發率[3]。外科手術切除是肝血管瘤最確切的治療手段,但是半肝切除或者肝葉切除常需連同部分肝組織切除,導致部分肝組織無辜性切除的同時也增加了手術相關并發癥發生率。肝血管瘤剝除術則具有保證血管瘤完整、徹底切除的同時不連同無辜性肝臟切除的優勢[4],也正是董家鴻院士所提出的21世紀肝臟外科新理念:精準肝切除理念在肝血管手術治療上的臨床應用。本研究回顧分析本院因肝血管瘤采用腹腔鏡下肝血管瘤剝除術治療的54例Ⅰ型肝血管瘤病例,現總結報道如下。
1 資料與方法
1.1 一般資料
采用描述性病例研究方法,回顧分析2017年1月至2020年3月因肝血管瘤收住本院采用腹腔鏡下肝血管瘤剝除術治療的54例Ⅰ型肝血管瘤患者的病例資料,其中男15例、女39例,年齡24~70歲,平均(48.09±11.96)歲。所有患者均無上腹部手術史、均不合并肝硬化。臨床表現為上腹部腹脹不適者26例,其余患者為體檢發現,無腹部疼痛等特殊不適。血管瘤位于Ⅱ段5例、Ⅲ段者8例、Ⅳ段者7例,Ⅴ段者11例、Ⅵ段者13例、Ⅶ段者7例、Ⅷ段者3例,血管瘤直徑5.1~10.4 cm,平均(7.01±1.42)cm。術后均經病理學檢查確診:肝海綿狀血管瘤。
1.2 方法
麻醉成功后,患者取平臥“人”字位,常規碘伏消毒手術區皮膚,鋪無菌巾、單。于臍上建立氣腹,氣腹壓力控制在12~14 mm Hg后置入腹腔鏡探查腹腔,根據肝血管瘤大小、位置及肝臟與重要脈管結構關系決定戳卡的位置、數量并依次建立各操作孔。
探查腹腔明確肝血管瘤位置及與周圍毗鄰關系,根據肝血管瘤的位置決定游離肝臟的范圍,除位于肝臟膈面與臟面交界處易于暴露的血管瘤外,其他部位血管瘤均常規使用超聲刀離斷肝圓韌帶和鐮狀韌帶、進而離斷雙側冠狀韌帶及三角韌帶,將肝臟適度下移以利于肝血管瘤暴露。適度解剖第一肝門,第一肝門處過一根棉線作為預阻斷帶。充分暴露血管瘤后,用電鉤在肝血管瘤邊緣標記處預切線,第一肝門阻斷后找到肝血管瘤與正常肝組織之間的纖維鞘間隙,采用超聲刀沿此間隙逐步解剖切除血管瘤,并配合良好的負壓吸引以清楚顯露肝血管瘤毗連脈管結構,所遇直徑大于2 mm的膽管及血管均予5-0 Prolene線縫閉或一次性康基結扎夾閉后離斷,注意準確計時,肝門阻斷時間每次小于15 min,間歇時間每次大于5 min,總阻斷時間小于120 min。切除完畢后取下第一肝門阻斷棉線,檢查肝臟顏色及質地有無變化。沖洗術野,徹底止血,檢查術野無明顯活動性出血后取出切下的肝血管瘤組織。在肝斷面下放置乳膠引流管一根、負壓引流管一根分別于腹壁戳卡孔引出縫線固定妥當。清點器械、紗布無誤后逐層關閉手術切口。
1.3 觀察指標
觀察患者手術時間、術中出血量、住院時間、總住院費用、術后并發癥發生情況及隨訪患者術后恢復情況。
1.4 統計學處理
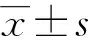
2 結 果
全組54例患者均順利完成手術,4例合并膽囊結石、1例合并膽囊息肉同時行腹腔鏡下膽囊切除術。手術時間(137.50±17.26)min,術中出血量(157.04±40.22)mL。術后出現膽漏3例,2例經腹腔引流管引流及加強營養支持后痊愈,1例因腹腔引流管引流欠佳,復查B超發現肝周包裹性積液后行超聲引導下經皮腹腔穿刺置管引流術引流痊愈。術后出現胸腔積液繼發肺部感染4例,行超聲引導下胸腔積液穿刺引流及加強抗感染治療后治愈出院。無術后出血、肝衰竭、腹腔感染、切口感染等并發癥發生。術后住院時間(11.24±2.11)d,總住院費用(2.31±0.34)萬元。所有患者均采用門診或電話隨訪,其中6例失訪,其余48例患者隨訪無異常,隨訪時間3~38個月,中位隨訪時間16個月。
3 討 論
肝血管瘤是肝膽外科常見病,其通常被認為是胚胎發育過程中血管過度發育或分化異常導致的血管畸形。其發病率為1.5%[5]。隨著人們生活水平及自我體檢意識地提高,大多數肝血管瘤被體檢發現,因肝血管瘤為肝臟外科常見良性疾病,多以隨訪為主[6-7]。對于存在較大破裂出血風險或伴發臨床癥狀者才需要手術治療。2019版肝血管瘤診斷和治療專家共識[5]中提出肝血管瘤治療指征為:(1)伴發癥狀或出現嚴重并發癥者;(2)進行性增大者(增長速度大于2厘米/年);(3)診斷不明確尤其是伴有肝炎、肝硬化、肝癌或其他惡性腫瘤者;(4)伴有嚴重焦慮等精神癥狀者;(5)需預防性治療者。
在肝血管瘤住院患者中僅44.23%具有臨床癥狀,且在有臨床癥狀的患者中約71.87%表現為輕癥[5]。其治療方法多樣,包括射頻消融、介入治療、外科手術(開腹/腹腔鏡下肝葉切除、開腹/腹腔鏡下肝血管瘤剝除術)[8],射頻消融治療因消融電極一次毀損肝腫瘤體積有限及熱傳導致周圍組織熱損傷不足存在消融不徹底,腫瘤殘留后并發周圍組織損傷等不足。肝血管瘤為肝動脈及門靜脈雙重供血,介入治療僅可栓塞肝動脈、因此介入治療很難完全阻斷肝血管瘤血供、介入治療后僅少數患者可保持腫瘤長期縮小狀態,大部分患者表現出腫瘤繼續增大或短期內縮小后再次繼續增大的狀態,治療效果有限。半肝或肝葉切除常需連同腫瘤周邊部分無辜性肝組織一同切除,增加了手術的創傷及手術風險。而肝血管瘤剝除術既能徹底切除血管瘤又可避免無辜性肝臟切除、降低手術并發癥發生率,具有良好治療效果,也正是董家鴻院士精準肝切除理念及加速康復外科理念的體現與臨床應用[9]。
筆者結合臨床實踐及手術體會總結以下幾點,(1)精確的術前評估及手術規劃。術前完善肝臟血管CT檢查是必不可少的,通過術前CT檢查明確腫瘤的位置及其周圍管系結構。術前完善肝儲備功能檢驗,檢查患者心、肺、肝功能及凝血、血細胞分析等相關檢驗,術前精確評估患者肝血管瘤大小及位置、周圍毗鄰關系、滋養血管來源與走形、手術的耐受性及安全性、必要時結合3D虛擬重建技術,行可視化精確術前評估[10]。在術前精確評估的基礎之上進一步進行手術入路、術中處理要點、可能出現的情況及應對措施等的精致規劃,條件允許的情況下充分利用術前3D虛擬重建技術及模擬肝切除軟件反復推敲與琢磨,做到胸有成竹、心中有數。(2)良好的肝臟游離、暴露及預置阻斷。根據肝血管瘤的位置及手術規劃,游離肝圓韌帶、肝鐮狀韌帶、左右三角韌帶、冠狀韌帶及肝腎韌帶,對位于肝右后葉及肝Ⅷ段血管瘤在充分游離右半肝后于右側肝腎間隙置入水囊使肝臟上移充分暴露肝臟的同時人為創造更大的肝腎間隙以提高手術的安全性。充分游離暴露肝臟第一肝門預置阻斷帶后行血管瘤剝除,第一肝門預置阻斷帶可阻斷肝臟入肝血流使肝血管瘤質地變軟,同時在保證循環穩定的前提下使用各種方法維持低中心靜脈壓(中心靜脈壓控制在0~5 cm H2O)降低肝血管瘤張力便于手術操作,此操作還可減少術中出血、降低術后并發癥發生率、縮短住院時間并且對肝腎功能無明顯影響[11]。但應注意準確計時,肝門阻斷時間每次需小于15 min,間歇時間每次大于5 min,總阻斷時間小于120 min。良好的肝臟游離、暴露及預置阻斷是成功實施手術的關鍵,即使局部粘連,需花費一定的時間也在所不惜。(3)精細的手術操作。精細的手術操作是手術的核心,肝血管瘤與正常肝組織之間實際存在完整的纖維鞘[12],手術中應正確找到此間隙,沿腫瘤邊緣采用超聲刀小口鉗夾,精細分離,避免分離層次過深或者過淺導致手術創面滲血不止而增加手術的被動性,另外肝血管瘤一般都存在滋養血管,術中正確有效處理其滋養血管后瘤體就會變軟、萎縮從而降低手術的難度[13]。直徑小于2 mm的脈管結構超聲刀基本可以凝閉,但對于大于2 mm的脈管結構術中必須采用Hem-o-lok夾可靠夾閉或Prolene線縫閉后凝斷,此種處理可使肝血管瘤切除后的肝臟創面基本不需再次縫合處理。(4)精良的術后管理。肝臟切除術后出血基本在48 h內發生,術后48 h內應嚴密觀察患者引流量、顏色變化及生命體征、尿量、血色素等變化。對于患者出現膽漏在保證引流充分、無明顯腹腔內積液潴留的情況下常不需要特殊處理,若存在肝周膽汁淤積引流不暢的情況應果斷行超聲引導下穿刺引流術[14]。術后給予充分的鎮痛并鼓勵患者早期下床活動及恢復飲食,患者術后24 h后即可下床活動及進食流質飲食,早期恢復胃腸道功能可降低胸腔積液、肺部感染及體靜脈血栓等相關并發癥的發生率[15]。其次肝切除術后必要清蛋白、足夠熱卡的補給及維生素、電解質的補充是非常必要的,低清蛋白血癥是術后膽漏的獨立危險因素。但同時應注意液體量的控制,遵循“偏干”的原則避免大量輸液導致肝臟水腫、加重肝臟負荷[16]。
綜上所述,筆者認為在董家鴻院士提出的精準肝切除理念指導下精確的術前評估及手術規劃、良好的肝臟游離暴露及預置阻斷、精細的手術操作、精良的術后管理,腹腔鏡下肝血管瘤剝除術在位于肝臟邊緣的Ⅰ型肝血管瘤治療上安全可行并具有良好治療效果,值得臨床推廣應用。

