早期宮頸癌手術后IMRT和3D-CRT治療的對比分析
朱偉華 韋德華 王麗娜
宮頸癌是臨床上常見惡性腫瘤,發病率居婦科惡性腫瘤首位,早期宮頸癌術后復發高危因素有淋巴結陽性、切緣陽性、腫瘤侵犯及肌層等,術后放療能降低局部復發率、提高無瘤生存期、降低遠處轉移率。3D-CRT是利用CT掃描獲得三維立體重建圖像,在三維方向上保證照射野形狀和靶區一致,由放射物理師根據靶區形狀,設計射線入射方向、形狀,調整其劑量。保證腫瘤組織受到均勻足量照射。IMRT是在三維適形放療基礎上發展的一種精準治療技術,優勢在于其能夠增加腫瘤放射的劑量,減少正常組織受照射體積與劑量,降低患者的不良反應,并提高局部控制率。臨床上對IMRT和3D-CRT放療效果報道[1-2]不一,爭議性大。本次研究就通過對比早期宮頸癌術后IMRT和3D-CRT治療的影響性,以期選擇最佳方法,提高放療后患者的生存質量,同時降低了不良反應率,現將結果進行如下報告。
1 資料與方法
1.1 臨床資料
收集我院2018年4月至2020年4月收治的早期宮頸癌患者共110例作為受試者,按受試順序平均分成2組。對照組55例,年齡最小34歲、最大62歲,平均年齡(45.8±3.7)歲;FIGO臨床分期:ⅡA期36例、ⅡB期13例、ⅢA期6例;病理類型:腺癌3例,鱗癌52例。研究組55例,年齡最小32歲、最大60歲,平均年齡(45.6±3.5)歲;FIGO臨床分期:ⅡA期38例、ⅡB期12例、ⅢA期5例;病理類型:腺癌4例,鱗癌51例。2組患者在年齡、病理類型、臨床分期等方面具有組間可比性(P>0.05)。
納入標準[3]:①均行手術治療,術后病理組織切片為早期宮頸癌;②均同意接受放療,且簽署知情同意書,征得醫院倫理委員會同意批準;③預計生存時間在6個月以上;④受試前檢查均能耐受方案。
排除標準:①未行手術治療,且術后病理診斷非宮頸癌;②未簽署知情同意書,未征得醫院倫理委員會同意批準;③生存時間在6個月內;④有嚴重肝腎功能損害。
1.2 治療方案
IMRT組先進行CT模擬定位,所有受試者保持膀胱自然充盈位,掃描前用熱塑體膜固定盆腔,然后采用飛利浦大孔徑CT模擬機進行定位,定位同時向體內注射優維顯90 ml進行增強掃描,掃描范圍從第2腰椎上緣至坐骨結節下5 cm,掃描層厚、間隔均為5 mm,經局域網傳輸至放療計劃設計系統中。在進行勾畫靶區時,依據CT勾畫的情況,勾畫出大體腫瘤和周圍淋巴結,即GVTnd,大體腫瘤范圍上至腹主動脈分叉處,下到閉孔下緣,確切以陰道受侵情況向下緣沿,主要有髂總、髂外及閉孔淋巴結引流區等等。計劃靶體積則在掃描范圍上向外擴張0.5 cm,勾畫出正常組織,如直腸、膀胱、股骨頭等,照射劑量為50~60 Gy,腔內后裝治療適度充盈膀胱,在陰道填塞紗布時,要盡量推開膀胱與直腸,減少受量,危及器官直腸、膀胱均為50%以下,股骨頭V50在5%以下、小腸V50在10%以下。
3D-CRT定位同IMRT組,采用四野箱式照射技術,劑量為45~50.4 Gy,后裝治療同IMRT組,單次劑量為6~7 Gy,總劑量為30~42 Gy,外照射加后裝治療劑量為80~87 Gy。
所有受試者均每3個月進行門診或電話隨訪,主要項目有患者的生存情況、影像學情況、液基細胞學檢查、血尿常規、放射學損傷評價,對出現不良反應的則及時對癥處理。
1.3 觀察指標和判斷標準
觀察放射性損傷、復發率和有效率,生活質量。生活質量評定標準采用宮頸癌患者生命質量測評量表進行,分別對比放療前和放療1年后生活質量變化情況。指標包括生理維度、社會家庭維度、情感維度、功能維度、宮頸癌特意維度。急性放射性損傷指血小板下降、血紅蛋白下降、白細胞下降、消化系統損傷、泌尿系統損傷,慢性放射性損傷則為放療結束后6~8個月進行,指標為放射性直腸炎、放射性膀胱炎,分為0級、Ⅰ級、Ⅱ級、Ⅲ級。根據WHO療效評價標準,包括完全緩解(CR)、部分緩解(PR)、疾病穩定(SD)、疾病進展(PD),總有效為CR+PR。復發率為局部復發和遠處淋巴結轉移率,分別對比術后1年復發率情況。
1.4 統計學處理
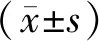
2 結果
2.1 2組治療后不良反應情況比較
研究組治療后在血小板下降、血紅蛋白下降、白細胞下降、消化系統損傷、泌尿系統損傷、放射性直腸炎及放射性膀胱炎等0級上發生率上顯著高于對照組,而在Ⅲ級發生率上則顯著低于對照組,具有統計學差異(P<0.05),見表1。
2.2 2組療效和復發情況比較
對照組總有效率61.82%、研究組為65.45%,差異無統計學意義(P>0.05);對照組局部復發率16.36%、遠處轉移率7.27%,研究組局部復發率7.27%、遠處轉移率3.64%,2組比較差異顯著(P<0.05),見表2。

表1 2組治療后不良反應情況比較/例

表2 2組療效和復發情況比較(例,%)
2.3 2組治療前后生活質量比較
2組治療前生理維度、社會家庭維度、情感維度、功能維度、宮頸癌特意維度評分比較,差異均不顯著(P>0.05),治療后均較治療前顯著提高(P<0.05),且研究組顯著優于對照組(P<0.05),見表3。
3 討論
宮頸癌發病率和死亡率僅次于乳腺癌,雖然手術能切除病根,但為減少復發,術后需結合放療或化療,但化療有腹瀉、腹痛、出血、腸梗阻和粒細胞減少等不良反應,這不僅會降低患者生活質量,且部分患者因嚴重不良反應被迫停止治療,故很多早期宮頸癌患者會選擇放療。
根據2009年NCCG指南提出建議,早期宮頸癌術后高危因素有淋巴結陽性、侵犯深層肌層、脈管陽性、腫瘤直徑在4 cm以上患者需補充放療治療,而對存在淋巴結轉移患者則還需同步接受化療治療[5]。放療范圍是瘤床、陰道殘端和盆腔淋巴結引流區等。目前放射治療對正常組織器官損傷程度主要是放療總劑量、單次劑量和受照射體積。報道[6-7]稱,3D-CRT技術照射范圍大,放療后患者直腸炎、膀胱炎和骨髓抑制等不良反應大,會嚴重影響患者生活質量和放療進程。

表3 2組治療前后生活質量比較分)
而IMRT則能在保證靶區放射劑量同時將周圍正常組織受量減至最低。研究[8-10]稱,IMRT適形指數為(0.76±0.06),顯著優于3D-CRT的(0.36±0.04),在相同30 Gy照射劑量下降,膀胱直腸IMRT受照射面積為(67.34±4.52)和(80.23±5.45),顯著低于3D-CRT的(90.24±5.23)和(96.45±6.14),這說明IMRT在相同劑量下,能顯著減少高劑量照射膀胱和直腸體積。此外,放療副作用屬于累積性,隨著照射時間推移,其優勢性體現越明顯。研究[11-12]稱,IMRT在減少危及器官受照體積、照射野內上均顯著下降。放療劑量學表面,3D-CRT小腸照射劑量為300 cm2,而IMRT照射劑量僅為33 cm2,且沒有顯著增加小腸接受20 Gy受照射體積,其能明顯降低直腸、膀胱照射劑量。結果顯示,采用IMRT放療后,患者在不良反應程度上顯著下降,這說明IMRT能顯著減少放療后不良反應。
早期宮頸癌中,腸管和膀胱等正常組織器官放射性損傷是降低生活質量、造成患者死亡的重要因素[13-14]。有研究指出[15-16],IMRT在保證安全范圍內提高靶區劑量,提高腫瘤局部控制率,且在保護正常組織器官和改善生存質量上優勢性顯著。其通過對比3D-CRT在膀胱直腸不良反應上比率為8.5%和12.6%,遠高于IMRT的2.4%和6.3%。而減少不良反應和提高生活質量存在協同性,在本次結果中可見采用IMRT能顯著提高生活質量。
雖然IMRT有顯著作用,但IMRT治療分次間擺體位,重復精確性難保證,因IMRT劑量分布適形度和靶區基本一致,治療靶區劑量波動大,適形度高,微小差異則會造成靶區劑量不足,影響放療療效和周圍正常組織器官的超量,會增加放射性損傷可能[17-18]。另外,因宮頸癌術后盆腔解剖結構改變,腸管位置下移和粘連,放療時腸道蠕動,正常組織器官充盈程度均會造成劑量增加,故放療前要盡量充盈膀胱,擺位準確,最大程度減少擺位誤差,保證治療安全性。

