不同極性溶劑的草果提取物抗氧化活性研究
3陸海峰
(1. 右江民族醫學院藥學院,廣西 百色 533000;2. 右江民族醫學院基礎醫學院,廣西 百色 533000;3. 右江民族醫學院科學實驗中心,廣西高校右江流域特色民族藥研究重點實驗室,廣西 百色 533000)
草果[1]【別名】:草果仁、草果子(AmomumtsaokoCrevostetLemarie)為姜科植物的干燥成熟果實,也是豆蔻屬多年生草本植物,莖叢生,高可達3米,全株有辛香氣,秋季果實成熟時采收,除去雜質,曬干或低溫干燥,分布于中國云南、廣西、貴州等省區,栽培或野生于疏林下,海拔1100~1800米。草果是藥食兩用中藥材大宗品種之一,草果作調味香料;全株可提取芳香油。果實入藥,具有燥濕健脾,除痰截瘧的功能。許多中成藥的配方都含有草果,如透骨搜風丸、益腎丸、開郁舒肝丸、寬胸利膈丸、潔白丸等。草果味辛,性溫;歸脾、胃經;芳烈燥散;臨床上主治脘腹脹滿、反胃嘔吐、食積瘧疾、胸膈痞滿、脘腹冷痛、惡心嘔吐、泄瀉下痢、食積不消、霍亂、瘟疫、瘴瘧等癥。抗氧化活性研究已成為評價保健食品、藥品開發的重要內容。研究表明[2],草果具有調節胃腸功能、減肥降脂、降血糖、抗氧化、抗腫瘤、防霉和抗炎鎮痛等藥理作用。本文為草果的進一步深入研究開發及應用提供理論依據。
1 材料與儀器
1.1 材料 粉碎后的草果、95%乙醇、蒸餾水、石油醚、乙酸乙酯、正丁醇、無水乙醇、甲醇、BHT(2 ,6-二叔丁基-4-甲基苯酚)、ABTS[2 ,2-聯氮-二(3-乙基-苯并噻唑-6-磺酸)二銨鹽]、K2S2O8、FeSO4·7H2O、水楊酸、H2O2、菲啰嗪、FeCl2:均為國產分析純。
1.2 儀器 紫外可見分光光度計(N4S型,棱光牌,上海儀電分析儀器有限公司生產);分析天平(FA1204B型,上海天美天平儀器有限公司生產);循環水式多用真空泵(SHB-B88型,鄭州長城科工貿有限公司生產);真空干燥箱(DZF-6020型,廣州市星爍儀器有限公司生產);旋轉蒸發器(RE-3000A型,上海亞榮生化儀器廠生產);數顯恒溫水浴鍋(HH-Z4型,金壇市城東光芒儀器廠生產)。
1.3 方法 稱取粉碎后的草果5 kg,放入圓底燒瓶中, 加入適量95%乙醇進行加熱回流2 h,反復提取3次,合并每次得到濾液,并用紗布進行過濾,過濾好的液體經旋轉蒸發儀蒸發濃縮,再經水浴鍋蒸發至無乙醇味膏狀。取適量的提取物浸膏,用少量蒸餾水溶解后,按照1∶1比例先后順序放入有機溶劑石油醚、乙酸乙酯、正丁醇分別萃取3次;最后,得到4個極性部位,對其進行蒸發濃縮干燥,低溫下保存。分別精密稱量4個極性部位的浸膏0.05 g,并用甲醇定容至50 ml,濃度都為1 g/L,然后分別配制成0.5 μg/ml、1.0 μg/ml、2.0 μg/ml、3.0 μg/ml、4.0 μg/ml,封口放置在低溫下冷藏(4℃)備用。
1.4 草果提取物抗氧化活性的測定
1.4.1 ABTS+自由基清除能力的測定 配置ABTS+溶液:稱取0.384 g ABTS用蒸餾水溶解后,定容至100 ml,使ABTS溶液濃度為7 mmol/L。稱取0.1514 g的過硫酸鉀用蒸餾水溶解,定容至10 ml,K2S2O8溶液濃度為2.45 mmol/L。取100 ml ABTS+溶液和4.6 ml K2S2O8溶液混合,室溫下避光保存 16 h,使用前用無水乙醇稀釋,作為工作液備用。往具塞試管加入6 ml ABTS+溶液和0.6 ml不同濃度提取液,進行均勻混合后,避光反應1 h,測定在波長λ=734 nm處的吸光度A1;同樣操作下,測定 6 ml無水乙醇和0.6 ml不同濃度提取液的吸光度A2;同時測定6 ml ABTS+溶液和0.6 ml無水乙醇吸光度A0,把BHT作為陽性對照品,計算ABTS+自由基清除率(%)=[1-(A1-A2)]/A0×100%。
1.4.2 羥自由基清除能力的測定 事先配制好需要用的提取物溶液濃度,分次加1 ml 9 mmoL/L FeSO4溶液和1 ml 9 mmoL/L水楊酸-乙醇溶液于試管中,再向具塞量筒加入不同濃度提取物溶液3 ml和8.8 mmoL/L H2O2溶液1 ml,并在溫度37℃下反應40 min,用蒸餾水作為空白調零,用BHT做陽性對照品,測其吸光度在510 nm處,按以下公式計算清除率。羥自由基清除率(%)=[1-( A0-A1) /A0]×100%,式中A0:0.5 ml FeSO4溶液+0.5 ml水楊酸-乙醇溶液+蒸餾水定容到10 ml+0.5 ml H2O2溶液;A1:0.5 ml FeSO4溶液+0.5 ml水楊酸-乙醇溶液+3 ml樣品溶液+蒸餾水定容到10 ml +0.5 ml H2O2溶液。
1.4.3 金屬離子(Fe2+)螯合能力的測定 用分析天平稱取0.04 g FeCl2,用蒸餾水溶解,并定容至100 ml,得到2 mmol/L FeCl2溶液,同時稱取0.1255 g菲洛嗪,用蒸餾水溶解,并定容至50 ml,得到5 mmol/L菲啰嗪溶液。然后分別用移液槍量取不同濃度樣品2 ml加入到有濃度為2 mmol/L FeCl2溶液0.1 ml的具塞試管中,經室溫孵育后,加入0.2 ml的5 mmol/L菲洛嗪試劑,最后加入3 ml蒸餾水,反應10 min后,在562 nm處讀取吸光值。金屬離子(Fe2+)螯合清除率(%)=[(A0-A1)/A0]×100%。A0:2 ml蒸餾水+0.1 ml FeCl2+0.2 ml 5 mmol/L菲啰嗪+3 ml蒸餾水的吸光度值;A1:2 ml樣品+0.1 ml FeCl2+0.2 ml 5 mmol/L菲啰嗪+3 ml蒸餾水的吸光度值。
2 結果
2.1 ABTS+自由基清除能力的結果分析 提取物溶液加入ABTS+溶液后,ABTS+會與提取物的抗氧化成分發生反應,生成穩定化合物,使溶液褪色,由此,說明清除率越高抗氧化能力越高。從圖1可知,不同極性溶劑的草果提取物對ABTS+自由基清除率中BHT陽性對照品的清除率最強,高達90.56%,說明其抗氧化能力最好。提取物對ABTS+自由基的清除能力大小為BHT>乙酸乙酯部位>正丁醇部位>水部位>石油醚。
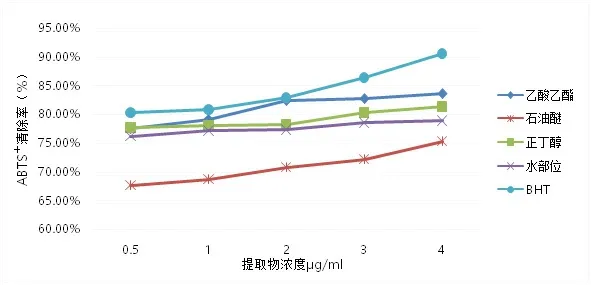
圖1 不同提取物濃度對ABTS+自由基清除率的影響
2.2 羥自由基清除能力的結果分析 羥自由基能力是測定抗氧化活性的常用指標之一,羥自由基的清除率越高說明其抗氧化能力越高。從圖2可知,草果提取物對羥自由基表現出了不同的清除能力,正丁醇部位清除率最高,但整體清除率比ABTS+自由基清除率低很多,在相同提取物濃度中,正丁醇部位對羥自由基清除能力最強,其次是BHT,而且不同極性部位之間的清除率較為接近,均在0%~25%范圍內,特別是乙酸乙酯和石油醚部位清除率很相近。羥自由基清除能力大小為:正丁醇部位>BHT>石油醚部位>乙酸乙酯部位>水部位。
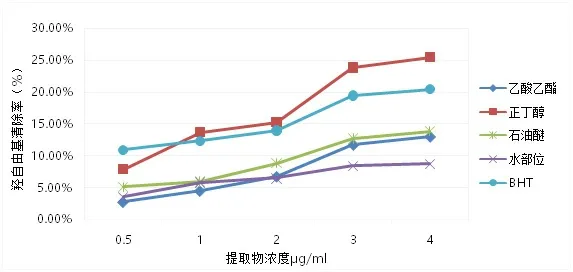
圖2 不同提取物濃度對羥自由基清除率的影響
2.3 金屬離子(Fe2+)螯合清除能力的結果分析 從圖3可知,草果提取物都具有對Fe2+螯合的清除能力,其濃度越高清除率越強,極性不同清除率也不一樣。其中以陽性對照品BHT對其清除能力影響較大,對金屬離子(Fe2+)螯合清除率從8%大幅度的增加到30%。在提取物濃度為4 μg/ml時,BHT清除率接近最高點30%。而其他極性部位清除率均穩定上升,但不同極性部位的草果提取物清除能力相差不大,上升幅度在10%之間。金屬離子(Fe2+)螯合清除能力大小為:正丁醇部位>BHT>水部位>乙酸乙酯部位>石油醚部位。
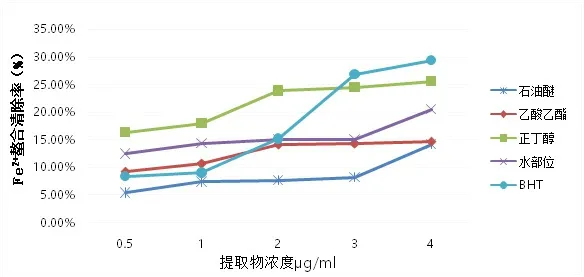
圖3 不同提取物濃度對Fe2+螯合清除率的影響
3 討論
草果含有抗氧化成分,具有抗氧化活性,但抗氧化活性能力并不一樣。實驗圖表的曲線均呈現上升趨勢,并且清除能力隨濃度增加而不斷增強。三個數據圖表結果表明,在BHT部位清除能力最好,有很好的抗氧化活性,其次是正丁醇部位體現了強的穩定的抗氧化活性能力。因此,為研究草果在抗氧化活性方面奠定了堅實的基礎。
本論文使用有機溶劑醇提取法,并對草果進行體外抗氧化活性的測定,測定草果提取物對ABTS+自由基、羥自由基的清除能力以及金屬離子(Fe2+)螯合清除能力,發現草果對ABTS+自由基清除能力最強,抗氧化活性最好,以BHT清除能力最好,高達90%;正丁醇部位對清除羥自由基的清除能力效果較好;螯合Fe2+的能力在提取物濃度為4μg/ml時BHT最強,草果在一定濃度范圍內隨提取物濃度的增加而增強。綜上所述,表明了不同極性溶劑的草果提取物具有良好的抗氧化活性和抗自由基清除能力。

