惡性腫瘤合并心房顫動對抗凝治療后患者血栓栓塞和出血發生的影響
王 霞 蔡 蕾 張小麗
心房顫動是臨床上一種常見的房性心律失常,心跳頻率往往快而且不規則,心房失去有效的收縮功能,患者可能出現心悸、眩暈、胸部不適、氣短等癥狀,研究表明其有可能引發心力衰竭,增加缺血性卒中風險以及心腦血管疾病病死率[1-2]。據報道房顫的發病率與年齡、精神緊張、水電解質紊亂、嚴重感染、高血壓等多種因素有密切關系[3-4]。隨著現代社會腫瘤患者生存率的明顯提高和生存期的逐漸延長,腫瘤合并心房顫動的患者也有所增加,有研究提示腫瘤本身和抗腫瘤藥物均可增加心房顫動風險[5]。相對于單獨的心房顫動患者,腫瘤合并心房顫動無論在發生血栓栓塞和出血風險上還是在治療方案上,都更具特殊性,值得臨床關注[6]。本研究探討惡性腫瘤合并心房顫動對抗凝治療后患者血栓栓塞和出血發生的影響,現總結報告如下。
1 資料與方法
1.1 一般資料
選取2018年1月至2019年5月在我院診治的39例惡性腫瘤合并心房顫動患者作為觀察組,入選標準:①性別、年齡不限;②房顫血栓危險度評分CHADS2≥2分且HAS-BLED<3分能夠進行正常抗凝治療;③腫瘤均經病理組織學確診;④患者和/或家屬知情同意研究內容并配合研究進行。排除標準:①嚴重肝腎功能或凝血功能異常患者;②其他抗凝治療禁忌證患者;③近一年內消化道、泌尿道等出血患者;④近一年內外傷或手術史患者。入組患者中男性20例,女性19例;年齡37~79歲,平均(56.3±4.9)歲;食管癌5例,胃癌7例,腸癌11例,肝癌5例,肺癌6例,其他5例;陣發性心房顫動25例,持續性心房顫動14例。同期40例心房顫動患者作為對照組,其中,男性23例,女性17例;年齡35~78歲,平均(56.1±5.0)歲;陣發性心房顫動24例,持續性心房顫動16例。2組性別、年齡、心房顫動類型比較,差異均無統計學意義(P>0.05),均衡可比。研究符合醫學倫理要求。
1.2 方法
2組患者均進行CHADS2房顫血栓危險度評分及HAS-BLED出血風險評分,并給予華法林抗凝治療。CHADS2評分中C代表充血性心衰(1分),H代表高血壓(1分),A代表年齡>75歲(1分),D代表糖尿病(1分),S2代表既往卒中或短暫性腦出血發作(各1分)。入選研究的患者CHADS2評分均≥2分,2~3分中危,4~6分高危。HAS-BLED評分中H代表高血壓(1分),A代表腎功或肝功異常(各1分),S代表卒中(1分),B代表出血(1分),L代表異常國標標準化比值(international normalized ratio,INR)(1分),E代表>65歲(1分),D代表藥物或飲酒(各1分)。所有患者均給予華法林抗凝治療,起始劑量2.5 mg/d,每日1次,每隔3 d復查INR值,根據INR值調整藥物劑量,每次可加量0.5 mg,至維持INR值2.0~3.0,根據患者個體情況維持此時用藥劑量3個月以上。
1.3 觀察項目
所有患者完成12個月隨訪工作,觀察比較2組抗凝治療后患者血栓栓塞和出血發生情況及藥物不良反應。血栓栓塞事件包括心肌梗死、下肢靜脈栓塞、肺栓塞等。出血事件包括消化道出血、皮膚出血點/瘀斑、血尿、咳血、齒齦滲血等。不良反應包括惡心嘔吐、頭痛、呼吸困難、眩暈等。
1.4 統計學分析
2 結果
2.1 2組血栓栓塞事件發生率比較
觀察組CHADS2評分為(3.02±0.71),略高于對照組的(2.89±0.65),但差異無統計學意義(t=0.849,P>0.05);2組的血栓中危、高危患者比例差異亦無統計學意義(P>0.05),見表1。觀察組心肌梗死、下肢靜脈栓塞、肺栓塞發生率略高于對照組,但差異無統計學意義(P>0.05),見表1。

表1 2組患者血栓栓塞風險及發生情況比較(例,%)
2.2 2組出血事件發生率比較
觀察組、對照組HAS-BLED評分進行比較,前者略高于后者,但差異無統計學意義(P>0.05),2組患者均為出血低危風險,無HAS-BLED評分≥3分的高危患者,見表2。觀察組的皮膚出血點/瘀斑、齒齦滲血發生率顯著高于對照組,組間差異有統計學意義(P<0.05),組間其他出血事件發生率差異無統計學意義(P>0.05),見表3。

表2 2組患者出血風險比較
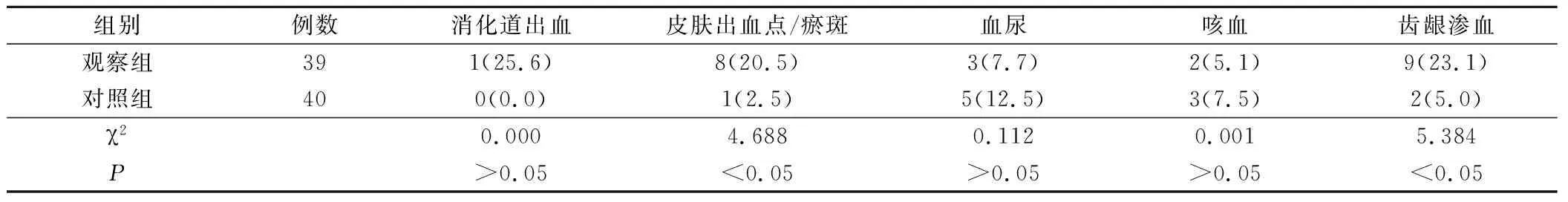
表3 2組患者出血事件發生情況比較(例,%)
2.3 2組不良反應發生率比較
觀察組不良反應發生率為38.5%(15/39),顯著高于對照組的17.5%(7/40),組間差異有統計學意義(χ2=4.318,P<0.05),見表4。2組患者出現不良反應較多,但均為輕微癥狀,無需特殊處理可自行緩解。
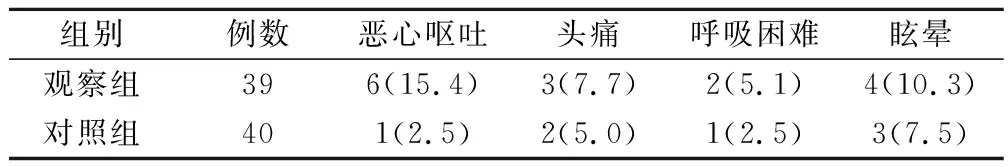
表4 2組患者不良反應發生情況比較(例,%)
3 討論
心房顫動是由心房主導折返環引起許多小折返環導致的房律紊亂,其發生時心房喪失收縮功能,血液容易在心房內淤滯而形成血栓,血栓脫落后可隨著血液至全身各處,導致腦栓塞、肢體動脈栓塞等,多給予抗凝治療,而長期應用抗凝藥物容易增加出血風險,因此一直以來血栓栓塞風險評估、抗凝治療是心房顫動診療的重點[7-9]。
據流行病學資料顯示腫瘤患者心房顫動發生率高,并且2種疾病發病過程均與血栓形成前狀態有關,栓塞發生風險更高[10]。研究中觀察組血栓栓塞風險CHADS2評分略高于對照組,心肌梗死、下肢靜脈栓塞、肺栓塞發生率略高于對照組,但是差異并未體現出統計學意義。多項研究提示惡性腫瘤患者普遍存在高凝狀態,腫瘤發生、局部浸潤、遠處轉移過程中的基因突變或分子表達異常會對機體中血液高凝起到了促進作用,使得機體血管內皮細胞損傷,凝血、纖溶以及體內抗凝系統等功能失調,易發生下肢靜脈血栓栓塞、肺栓塞等[11-13]。這些研究內容支持了本研究結果中惡性腫瘤合并心房顫動患者的血栓栓塞風險評分及不良事件發生率高于單獨心房顫動患者,可能因為病例樣本量較少、個體差異等原因數據分析結果無統計學差異。
合理抗凝是預防、減少心房顫動所致血栓栓塞的有效治療手段,但同時增加了出血風險,腫瘤合并心房顫動患者再加上腫瘤本身的復雜性及其相關的血小板減少癥會進一步增加出血風險,故需要確定患者的出血風險并盡力平衡血栓與出血風險,選擇合適的用藥方案[14-15]。本研究中所有研究對象均為出血風險HAS-BLED評分<3分適合抗凝治療的患者,評估結果還顯示腫瘤合并心房顫動患者的評分略高于對照組,經過治療觀察組的皮膚出血點/瘀斑、齒齦滲血發生率顯著高于對照組并且體現了統計學差異,其他出血事件的發生率無明顯差異,表明腫瘤合并心房顫動患者的出血風險更高,在治療用藥上面臨更大的困難和挑戰[16]。
臨床調查顯示已有多種新型口服抗凝藥應用于臨床,例如,利伐沙班預防性抗凝可抑制外源性、內源性兩大凝血途徑而降低血栓風險[17],阿哌沙班可有效改善患者血流循環狀態而起到明顯的抗凝效果[18],均提示新型抗凝藥物的有效性和安全性不劣于以往應用的低分子肝素、華法林等抗凝藥物。但新型口服抗凝藥的應用受到費用、遠期療效、不良反應等方面的因素影響并未得到廣泛的應用和推廣[19]。目前階段對于腫瘤合并心房顫動患者的抗凝用藥方案并未明確規范,本研究考慮到新型抗凝藥物會通過肝臟細胞色素代謝進而影響血藥濃度,干擾到抗凝效果可能引起血栓栓塞和出血等[20],而且新型口服抗凝藥在臨床應用時間較短,見諸報道的最主要不良反應為出血[21],因此堅持了華法林治療方案,但用藥過程中需要高度注意對患者定期進行凝血和INR監測,以保證用藥安全性。
綜合以上所述可見,惡性腫瘤合并心房顫動一定程度上增加了血栓栓塞和出血風險,需要根據患者具體情況選擇合理的治療方案以提高抗凝療效,減少血栓栓塞和出血不良事件的發生。

