改良PCH方案對(duì)HER-2陽(yáng)性乳腺癌的療效及與ER、PR水平的關(guān)系
解婷婷 樊 曉
近年來(lái)女性承受的社會(huì)壓力增加,生存環(huán)境的改變使得乳腺癌的臨床發(fā)病率不斷增加,乳腺癌也成為女性惡性腫瘤中發(fā)病較高的疾病[1]。既往臨床研究顯示,人表皮生長(zhǎng)因子受體-2(HER-2)陽(yáng)性乳腺癌患者約占乳腺癌患者總數(shù)的30%,通常發(fā)生于乳腺癌中晚期,其惡性程度高、侵襲性強(qiáng),對(duì)該類疾病需要進(jìn)行針對(duì)性治療[2]。目前研究指出對(duì)于HER-2陽(yáng)性乳腺癌患者需采用曲妥珠單抗+紫杉醇+卡鉑(PCH)方案,而白蛋白結(jié)合型紫杉醇在臨床的普及可逐漸代替PCH方案中傳統(tǒng)的溶劑型紫杉醇[3]。乳腺癌屬于激素依賴型的惡性腫瘤,其生長(zhǎng)、調(diào)節(jié)均依賴于體內(nèi)的雌激素受體(ER)、孕激素受體(PR),因而這兩種指標(biāo)的表達(dá)可能對(duì)乳腺癌的化療療效產(chǎn)生一定影響[4]。本研究選取近年來(lái)我院接受治療的患者作為研究對(duì)象,探討改良PCH方案用于HER-2陽(yáng)性乳腺癌后的療效及其與ER、PR水平的關(guān)系,現(xiàn)將結(jié)果報(bào)告如下。
1 資料與方法
1.1 基礎(chǔ)資料
選取2018年3月到2020年3月來(lái)我院接受治療的100例HER-2陽(yáng)性乳腺癌患者作為研究對(duì)象,按照隨機(jī)數(shù)字表法將其隨機(jī)分為改良PCH組和對(duì)照組,每組50例,其中改良PCH組:年齡36~59歲,平均(47.28±5.34)歲;腫瘤直徑2~8cm,平均(4.64±1.18)cm;腫瘤類型包括小葉癌17例,浸潤(rùn)性導(dǎo)管癌33例;TNM分期[5]包括Ⅱ期24例,Ⅲ期26例;對(duì)照組:年齡37~58歲,平均(48.31±5.28)歲;腫瘤直徑2~8cm,平均(4.51±1.21)cm;腫瘤類型包括小葉癌15例,浸潤(rùn)性導(dǎo)管癌35例;TNM分期包括Ⅱ期22例,Ⅲ期28例;比較兩組一般資料,差異無(wú)統(tǒng)計(jì)學(xué)意義(P>0.05),具有可比性,本研究經(jīng)我院倫理委員會(huì)審核并批準(zhǔn)實(shí)行。
1.2 納入標(biāo)準(zhǔn)
①參照《中國(guó)抗癌協(xié)會(huì)乳腺癌診治指南與規(guī)范》[6]有關(guān)標(biāo)準(zhǔn),所有患者均被確診為乳腺癌,且病理組織學(xué)證實(shí)為HER-2陽(yáng)性;②年齡36~59歲;③美國(guó)東部腫瘤協(xié)作組(ECOG)評(píng)分[7]<2分且TNM分期Ⅱ~Ⅲ期;④患者及家屬知情并簽署知情同意書(shū)。
1.3 排除標(biāo)準(zhǔn)
①預(yù)計(jì)生存期>3個(gè)月;②心、肝、腎功能經(jīng)檢查存在明顯異常;③合并其它類型腫瘤或腫瘤已發(fā)生遠(yuǎn)處轉(zhuǎn)移;④雙側(cè)乳腺癌患者或因其它原因不能耐受化療;⑤參與研究前已接受其它類型治療,或因?yàn)榫窦膊o(wú)法配合治療。
1.4 方法
(1)改良PCH組:采用改良PCH方案對(duì)患者進(jìn)行治療,分被于開(kāi)始治療后的第1、8、15d采用100 mg/m2白蛋白結(jié)合型紫杉醇(石藥集團(tuán)歐意藥業(yè)有限公司,國(guó)藥準(zhǔn)字H20183044)靜脈注射+卡鉑(齊魯制藥有限公司,國(guó)藥準(zhǔn)字H10920028)AUC-2靜脈注射,21 d為1個(gè)周期;化療6個(gè)周期后可評(píng)價(jià)療效,期間持續(xù)采用曲妥珠(上海羅氏制藥有限公司,國(guó)藥準(zhǔn)字J201600033)單抗治療,首次負(fù)荷劑量為4 mg/kg,維持劑量2 mg/kg,每周1次。(2)對(duì)照組:采用常規(guī)PCH方案,分別于開(kāi)始治療后的1、8、15 d采用80 mg/m2紫杉醇(哈藥集團(tuán)生物工程有限公司,國(guó)藥準(zhǔn)字H20059962)靜脈注射+卡鉑AUC-2靜脈注射,28 d為1個(gè)周期;化療6個(gè)周期后可評(píng)價(jià)療效,期間持續(xù)采用曲妥珠單抗治療,用量與改良PCH組相同。
1.5 觀察指標(biāo)
(1)療效評(píng)價(jià):參照WHO實(shí)體瘤療效評(píng)價(jià)標(biāo)準(zhǔn)[8],分別于治療6個(gè)周期后對(duì)兩組臨床療效進(jìn)行評(píng)價(jià);分為完全緩解(CR)、部分緩解(PR)、疾病穩(wěn)定(SD)、疾病進(jìn)展(PD);客觀緩解率(ORR)=(CR+PR)/總例數(shù)×100%。(2)病理學(xué)檢測(cè):分別于化療前后通過(guò)穿刺獲取活檢標(biāo)本,采用40g/L甲醛溶液進(jìn)行固定,通過(guò)石蠟包埋后切成厚度約3μm的切片,采用免疫組化法對(duì)組織中雌激素受體(ER)、孕激素受體(PR)、人表皮生長(zhǎng)因子受體-2(HER-2)水平,比較兩組患者化療前及化療6個(gè)周期后的ER、PR、HER-2水平。(3)不良反應(yīng):比較兩組化療期間不良反應(yīng)發(fā)生情況。(4)不同療效ER、PR、HER-2水平:將改良PCH組按照療效不同分為CR、PR、SD、PD四組,比較各組間ER、PR、HER-2水平。(5)生存時(shí)間隨訪:在兩組患者結(jié)束化療治療后分別對(duì)其進(jìn)行為期1年的隨訪,每2個(gè)月對(duì)患者進(jìn)行一次實(shí)地,同時(shí)采用Kaplan-Meier法繪制生存曲線。
1.6 統(tǒng)計(jì)學(xué)方法
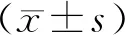
2 結(jié)果
2.1 兩組療效情況評(píng)價(jià)
改良PCH組化療后ORR為78.00%,顯著高于對(duì)照組(58.00%),差異有統(tǒng)計(jì)學(xué)意義(P<0.05),見(jiàn)表1。

表1 兩組療效情況評(píng)價(jià)(例,%)
2.2 化療前后病灶組織ER、PR、HER-2水平變化比較
改良PCH組化療后ER、PR水平顯著高于化療前及對(duì)照組,HER-2水平顯著低于化療前及對(duì)照組,差異有統(tǒng)計(jì)學(xué)意義(P<0.05)。見(jiàn)表2。
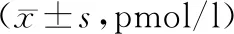
表2 化療前后病灶組織ER、PR、HER-2水平變化比較
2.3 兩組化療期間不良反應(yīng)情況比較
改良PCH組不良反應(yīng)總發(fā)生率為34.00%,與對(duì)照組(42.00%)比較,差異無(wú)統(tǒng)計(jì)學(xué)意義(χ2=0.679,P=0.410),見(jiàn)表3。

表3 兩組化療期間不良反應(yīng)情況比較(例,%)
2.4 改良PCH組不同療效患者化療前ER、PR、HER-2水平比較
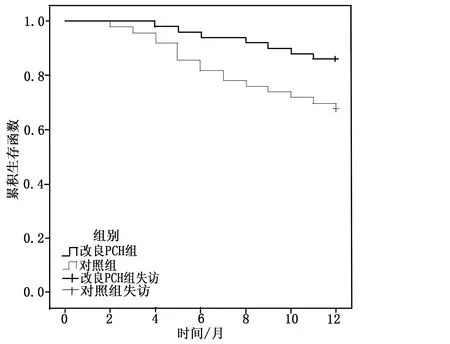
不同療效患者ER、PR水平:CR組>PR組>SD組、PD組,HER-2水平:CR組 表4 改良PCH組不同療效患者化療前ER、PR、HER-2水平比較 2.5 兩組化療后1年內(nèi)生存情況分析 對(duì)所有患者實(shí)行為期1年的生存情況隨訪,改良PCH組1年內(nèi)無(wú)失訪,死亡7例,生存率為86.00%(43/50);對(duì)照組1年內(nèi)無(wú)失訪,死亡16例,生存率為68.00%(34/50);兩組患者化療后1年內(nèi)隨訪生存情況采取Log-Rank檢驗(yàn),改良PCH組生存率顯著高于對(duì)照組,差異有統(tǒng)計(jì)學(xué)意義(Log-Rank=4.779,P=0.029),見(jiàn)圖1。 圖1 兩組化療后1年內(nèi)生存情況分析 目前,對(duì)于晚期年輕乳腺癌患者治療策略為新輔助治療后綜合決策模式,可先通過(guò)新輔助方案進(jìn)行化療,降低腫瘤臨床分期,從而提高未來(lái)乳腺癌手術(shù)切除成功率及保乳機(jī)會(huì)[9]。PCH方案作為臨床常用的治療HER-2陽(yáng)性乳腺癌的化療手段,有良好效果,但傳統(tǒng)的紫杉醇類藥物極難溶于水,需以無(wú)水乙醇或蓖麻油作為溶劑進(jìn)行靜脈注射,影響臨床療效,且可能增加患者藥物反應(yīng)[10]。白蛋白結(jié)合型紫杉醇,采用納米技術(shù)制成,不需要額外使用溶劑,避免了溶劑所增加的額外反應(yīng),因而可用來(lái)替代PCH方案中的溶劑型紫杉醇[11]。 本研究結(jié)果顯示,改良PCH組化療后ORR為78.00%顯著高于對(duì)照組58.00%,提示改良PCH方案治療HER-2陽(yáng)性乳腺癌具有更高的臨床療效。卡鉑作為第二代鉑類化合物,其生化物征與順鉑相似,但與順鉑相比其神經(jīng)毒性、腎毒性明顯更低,作為一種廣譜抗腫瘤藥物,它能與DNA結(jié)合,形成交叉鍵,破壞DNA功能,使其不能再?gòu)?fù)制合成,進(jìn)而對(duì)生長(zhǎng)各期的腫瘤細(xì)胞產(chǎn)生殺傷作用。曲妥珠單抗作為一種針對(duì)HER-2陽(yáng)性的單克隆抗體,可通過(guò)將自己附著于HER-2來(lái)阻止人體表皮生長(zhǎng)因子在HER-2上的附著,從而阻斷癌細(xì)胞的生長(zhǎng),同時(shí)刺激自身免疫細(xì)胞來(lái)摧毀癌細(xì)胞,臨床上通常將其與紫杉醇進(jìn)行聯(lián)合治療[12]。紫杉醇是從植物紫杉樹(shù)的樹(shù)皮中提取的一種紫杉烷類化合物,自上世紀(jì)90年代開(kāi)始便大量應(yīng)用于臨床惡性腫瘤的臨床化療,可通過(guò)誘導(dǎo)和促進(jìn)細(xì)胞周期中微管蛋白的聚合,促進(jìn)其維持穩(wěn)定,可抑制細(xì)胞有絲分裂中紡錘體和紡錘絲的形成,導(dǎo)致有絲分裂的異常停止,誘導(dǎo)細(xì)胞凋亡從而發(fā)揮其抗腫瘤作用,但傳統(tǒng)溶劑型紫杉醇選擇性較差,靶向作用更弱[13]。白蛋白結(jié)合型紫杉醇以人體內(nèi)固有的溶脂性白蛋白為載體,無(wú)需溶劑的靶向藥物,可直接經(jīng)胞吞轉(zhuǎn)運(yùn)運(yùn)輸,更快速地穿過(guò)內(nèi)皮細(xì)胞層,表現(xiàn)出強(qiáng)大的組織穿透力,也因?yàn)槠涓鼜?qiáng)的靶向性,改良PCH方案治療HER-2陽(yáng)性乳腺癌擁有更好的抑瘤效果[14]。 改良PCH組化療后ER、PR水平顯著高于化療前及對(duì)照組,HER-2水平顯著低于化療前及對(duì)照組,提示改良PCH方案治療HER-2陽(yáng)性乳腺癌對(duì)于改善ER、PR、HER-2水平擁有更良好的效果。原癌基因的異常活躍可誘導(dǎo)細(xì)胞表面受體增多,從而引起細(xì)胞癌變。改良PCH方案中白蛋白結(jié)合型紫杉醇的使用使得其可以以藥物為載體做成納米微粒,改變體內(nèi)吞噬細(xì)胞對(duì)于藥物的吞噬能力,延長(zhǎng)藥物在血液中的存在時(shí)間,通過(guò)獨(dú)特的白蛋白結(jié)合轉(zhuǎn)運(yùn)同理與富含半胱氨酸酸性分泌性蛋白的結(jié)合提高局部藥物濃度,增加療效,而腫瘤細(xì)胞的減滅使得患者內(nèi)分泌水平可以得到改善,從而改善ER、PR等指標(biāo)的表達(dá)[15]。 改良PCH組不良反應(yīng)總發(fā)生率為34.00%,與對(duì)照組42.00%比較無(wú)明顯差異,提示改良PCH不會(huì)增加傳統(tǒng)PCH方案引起的不良反應(yīng)。溶劑型紫杉醇藥物轉(zhuǎn)運(yùn)效率低,組織利用率低,聚氧乙烯蓖麻油的存在可引起過(guò)敏、腎毒性、神經(jīng)毒性等,引起不良反應(yīng),而白蛋白結(jié)合型紫杉醇可將藥物濃度靶向聚集于腫瘤細(xì)胞,使得其具有更高的腫瘤選擇性,減少正常組織中的藥物暴露,從而不會(huì)明顯增加紫杉醇引起的藥物毒性[16]。 比較不同療效患者ER、PR水平CR組>PR組>SD組、PD組,比較不同療效患者HER-2水平CR組 綜上,改良PCH方案用于HER-2陽(yáng)性乳腺癌可明顯提高其臨床療效,改善患者體內(nèi)ER、PR、HER-2分泌,延長(zhǎng)患者生存時(shí)間,且其療效可能受患者化療前ER、PR、HER-2影響。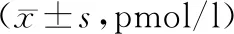
3 討論

