EZH2表位肽在多發(fā)性骨髓瘤中的預(yù)測(cè)和驗(yàn)證
鐘 赟 劉 哲
多發(fā)性骨髓瘤(multiple myeloma,MM)是一類源自于B細(xì)胞的血液系統(tǒng)惡性腫瘤,它占所有惡性腫瘤的1%,占到了血液系統(tǒng)惡性腫瘤的13.4%,是血液系統(tǒng)惡性腫瘤發(fā)病率第二的惡性腫瘤[1]。MM是由漿細(xì)胞單克隆性增殖引起,最終導(dǎo)致靶器官受損。目前,盡管部分患者通過化療、靶向治療、造血干細(xì)胞移植能得到暫時(shí)緩解,但是最后發(fā)現(xiàn)大部分患者仍會(huì)復(fù)發(fā)[2],進(jìn)而出現(xiàn)大多數(shù)患者仍無法治愈的結(jié)果。因此我們亟待尋求一種確實(shí)有效的治療方法,以期望能治愈多發(fā)性骨髓瘤。
染色質(zhì)水平的修飾是基因表達(dá)調(diào)控的重要途徑,(PcG)蛋白介導(dǎo)的基因轉(zhuǎn)錄抑制是目前在基因表達(dá)調(diào)控方面的研究熱點(diǎn)[3]。近階段的研究發(fā)現(xiàn),PcG蛋白與X 染色體的失活、干細(xì)胞分化、細(xì)胞癌變等存在密切的關(guān)系,而EZH2蛋白是PcG蛋白核心復(fù)合體的重要構(gòu)成部分。研究者在多種實(shí)體瘤及血液系統(tǒng)腫瘤中均發(fā)現(xiàn)EZH2蛋白的高表達(dá),如前列腺癌、乳腺癌、MDS及淋巴瘤等,并且發(fā)現(xiàn) EZH2 蛋白的高表達(dá)常與預(yù)后相關(guān),它預(yù)示腫瘤惡性程度高且有發(fā)生廣泛轉(zhuǎn)移的傾向[4]。一般認(rèn)為 EZH2 蛋白通過其甲基轉(zhuǎn)移酶活性在染色體水平抑制基因轉(zhuǎn)錄。正常的骨髓漿細(xì)胞不表達(dá) EZH2,當(dāng)發(fā)生漿細(xì)胞腫瘤時(shí),EZH2會(huì)隨著疾病進(jìn)展逐步上調(diào)表達(dá)。在過去的的研究中,有學(xué)者用 siRNA的方法將細(xì)胞株中的EZH2表達(dá)沉默,發(fā)現(xiàn)EZH2表達(dá)水平下調(diào)的腫瘤細(xì)胞株停止生長(zhǎng)[5]。 因此,我們基于上述研究成果,初步可預(yù)測(cè)在腫瘤中大量表達(dá)的EZH2蛋白,實(shí)際上在腫瘤細(xì)胞分化、生長(zhǎng)、發(fā)展過程中起到了抗凋亡分子的某些作用,因此可認(rèn)為EZH2蛋白是一種較為理想的惡性腫瘤包括多發(fā)性骨髓瘤的免疫治療假想靶點(diǎn)。
本研究應(yīng)用生物信息學(xué)軟件對(duì)EZH2蛋白進(jìn)行HIA-A0201限制性CTL抗原表位的初步預(yù)測(cè),驗(yàn)證該表位肽是生理和病理情況下都存在的,為多發(fā)性骨髓瘤免疫治療奠定基礎(chǔ)。
1 材料與方法
1.1 臨床資料
選取2018年1月至2018年12月的初診且按NCCN診斷標(biāo)準(zhǔn)確診為多發(fā)性骨髓瘤的患者30例作為MM組,取同期健康體檢者30例作為健康對(duì)照組,本實(shí)驗(yàn)研究中的相關(guān)部分已獲得所在醫(yī)院的倫理委員會(huì)的批準(zhǔn),并與患者、家屬均簽署了相關(guān)知情等告知性同意書。
1.2 試劑和儀器
人TAP-缺陷型細(xì)胞株T2(HLA-A0201)(上海復(fù)祥生物科技有限公司提供);流感病毒基質(zhì)蛋白肽段(上海波泰生物科技有限公司);PBS緩沖液(上海生工生物工程有限公司提供),RPMI1640培養(yǎng)液、FBS(GIBCO公司);胞外布雷菲德菌素(上海同田生物技術(shù)有限公司)HIV-l pol肽段、FITC標(biāo)記小鼠抗人HLA-A02單克隆抗體(北京表源生物技術(shù)有限公司);BB7.2與PE標(biāo)記的aa27及aa670肽段四聚體(北京表源生物技術(shù)有限公司);β2微球蛋白(Raybiotech公司)。
主要儀器和設(shè)備:流式細(xì)胞儀(Beckman Coulter公司);96孔板(丹麥NUNC公司);二氧化碳恒溫細(xì)胞培養(yǎng)箱(日本SANYO公司生產(chǎn));無菌超凈工作臺(tái)(吳江市凈化設(shè)備總廠生產(chǎn));電熱恒溫水浴鍋(上海醫(yī)療器械一廠生產(chǎn));IMT-2型倒置顯微鏡(日本olympus公司生產(chǎn))。
1.3 生物信息軟件
本研究采用以下生物信息學(xué)軟件NCBI NP-00309(http:// www.ncbi.nlm.nih.gov/genbank/);BIMAS(http://www-bimas.cit.nih.gov/ molbio/hla_bind);SYFPEITHI(http://www.syfpeithi.de/ Scripts/ MHCScrver.dll/ EpitopePrediction.htm)。
1.4 主要方法
1.4.1 HLA-A0201限制性EZH2蛋白CTL表位肽預(yù)測(cè) 根據(jù)在Genbank中登記的相關(guān)數(shù)據(jù),查找出EZH2蛋白的信息,從而確定好EZH2的蛋白氨基酸序列,并由NIH/BIMAS系統(tǒng)預(yù)測(cè)出數(shù)個(gè)EZH2蛋白相關(guān)的HLA-A0201限制性的CTL表位肽構(gòu)成,再通過SYFPEITHI系統(tǒng)對(duì)上述表位肽進(jìn)行驗(yàn)證,選取累計(jì)積分最高的肽片段。使用超基序方案對(duì)已預(yù)測(cè)出的CTL表位肽片段進(jìn)行修飾以進(jìn)一步提高積分。我們通過NIH/BIMAS提供表位肽預(yù)測(cè)的網(wǎng)絡(luò)服務(wù)站點(diǎn),將EZH2蛋白序列檢測(cè)出分別獨(dú)立預(yù)測(cè)得分值較高的抗原多肽,預(yù)測(cè)出多條表位肽,并通過量化基序方案以及超基序方案進(jìn)一步篩選出最合適的2條表位肽。
1.4.2 多肽的合成與驗(yàn)證 在研究中所使用的全部肽段均由上海波泰生物科技公司合成并驗(yàn)證。結(jié)合文獻(xiàn)報(bào)道及相關(guān)預(yù)測(cè),我們?cè)趯?shí)驗(yàn)中預(yù)測(cè)并選取分別合成出了2條HLA A0201陽性肽(HIV-1 pol肽段,序列:ILKEPVHGV;流感病毒基質(zhì)蛋白肽段,序列:GILGFVFTL;)作為本實(shí)驗(yàn)的陽性對(duì)照。
在線篩選出2條EZH2高積分肽段,同時(shí)使用HLA-A0201+T2雜交瘤細(xì)胞驗(yàn)證肽段的親和力、穩(wěn)定性,在此基礎(chǔ)上篩選出具備高親和力和穩(wěn)定性的一條肽段。
1.4.3 T2細(xì)胞表位肽結(jié)合親和實(shí)驗(yàn) 將細(xì)胞密度為2×105/孔T2細(xì)胞混懸液制備備用,并分別依次接種于24孔細(xì)胞培養(yǎng)板中備用;實(shí)驗(yàn)中按方案設(shè)立分組為實(shí)驗(yàn)組、陽性對(duì)照組、空白對(duì)照組,并在實(shí)驗(yàn)中每個(gè)實(shí)驗(yàn)組設(shè)3個(gè)副孔,通過調(diào)整后每孔含2.5 μg/mL β2微球蛋白。實(shí)驗(yàn)中每孔加入相應(yīng)的候選肽段作為實(shí)驗(yàn)組,其余部分孔位中加入對(duì)照肽段的為陽性對(duì)照組,剩余的未加肽段的T2細(xì)胞孔位作為空白對(duì)照。后將所有細(xì)胞孵育18 h,完成后分別收集細(xì)胞,洗滌3次,再分別加入FITC標(biāo)記的HLA-A0201單克隆抗體,并通過流式細(xì)胞儀檢測(cè)平均熒光強(qiáng)度。
試驗(yàn)中使用熒光系數(shù)(FI)作為衡量親和力的指標(biāo),熒光系數(shù)>1的表位肽被認(rèn)為HLA-A0201的分子具有高親和力,熒光系數(shù)由以下公式計(jì)算得到:熒光系數(shù)(FI)=(樣本平均熒光強(qiáng)度-空白對(duì)照平均熒光強(qiáng)度)/空白對(duì)照平均熒光強(qiáng)度。
1.4.4 T2細(xì)胞表位肽結(jié)合穩(wěn)定性實(shí)驗(yàn) 分別將密度為1×105/孔的混懸液接種到96孔細(xì)胞培養(yǎng)板中備用,再分別依次加入β2微球蛋白,分組為無血清1640培養(yǎng)基以及對(duì)照肽段和相應(yīng)的候選肽段,并共同孵育18 h后,再次洗滌細(xì)胞后孵育1 h,并預(yù)設(shè)不同的時(shí)間點(diǎn)(0,2,4,8,12,24 h)按計(jì)劃分次收集細(xì)胞。每一個(gè)實(shí)驗(yàn)組設(shè)置3個(gè)副孔,分別加入FITC標(biāo)記的HLA-A0201單克隆抗體,并盡早使用流式細(xì)胞儀檢測(cè)平均熒光強(qiáng)度。
1.4.5 檢測(cè)患者、健康對(duì)照者所篩選肽段相對(duì)應(yīng)五聚體陽性細(xì)胞毒性T細(xì)胞 分別按分組情況,收集多發(fā)性骨髓瘤患者及健康對(duì)照者的外周血5 ml,并提取外周血單個(gè)核細(xì)胞,并將1×106個(gè)單個(gè)核細(xì)胞加入2 μL同型對(duì)照和所篩選表位肽對(duì)應(yīng)的五聚體,孵育40 min,加入FITC標(biāo)記的CD8+單克隆抗體,取出后進(jìn)行流式細(xì)胞儀檢測(cè)。
1.5 統(tǒng)計(jì)學(xué)分析
數(shù)據(jù)采用Graphpad Prism6軟件進(jìn)行統(tǒng)計(jì)學(xué)分析。
2 結(jié)果
2.1 HLA-A0201限制性EZH2蛋白CTL表位肽預(yù)測(cè)
EZH2蛋白氨基酸序列的確定:我們?cè)贕enbank中登記的數(shù)據(jù)中查找到了EZH2蛋白,它由746個(gè)氨基酸殘基組成,Genbank登錄號(hào)為:AAC51520.1,其編碼的蛋白質(zhì)序列如下:mgqtgkksek gpvcwrkrvk seymrlrqlk rfrradevks mfssnrqkil erteilnqew kqrriqpvhi ltsvsslrgt recsvtsdld fptqviplkt lnavasvpim yswsplqqnf mvedetvlhn ipymgdevld qdgtfieeli knydgkvhgd recgfindei fvelvnalgq yndddddddg ddpeereekq kdledhrddk esrpprkfps dkifeaissm fpdkgtaeel kekykelteq qlpgalppec tpnidgpnak svqreqslhs fhtlfcrrcf kydcflhpfh atpntykrkn tetaldnkpc gpqcyqhleg akefaaalta eriktppkrp ggrrrgrlpn nssrpstpti nvleskdtds dreagtetgg enndkeeeek kdetssssea nsrcqtpikm kpnieppenv ewsgaeasmf rvligtyydn fcaiarligt ktcrqvyefr vkessiiapa paedvdtppr kkkrkhrlwa ahcrkiqlkk dgssnhvyny qpcdhprqpc dsscpcviaq nfcekfcqcs secqnrfpgc rckaqcntkq cpcylavrec dpdlcltcga adhwdsknvs ckncsiqrgs kkhlllapsd vagwgifikd pvqknefise ycgeiisqde adrrgkvydk ymcsflfnln ndfvvdatrk gnkirfanhs vnpncyakvm mvngdhrigi fakraiqtge elffdyrysq adalkyvgie remeip。通過CTL表位肽在線預(yù)測(cè)網(wǎng)站預(yù)測(cè)出積分較高的肽段:YMCSFLFNL 及 SQADALKYV。如表1。
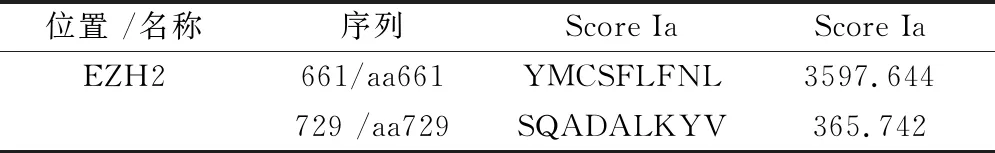
表1 CTL表位肽對(duì)EZH2積分較高肽段的預(yù)測(cè)
完成 EZH2-HLA0201 特異性肽段篩選,篩選出“YMCSFLFNL”肽段進(jìn)行下一步功能實(shí)驗(yàn),實(shí)驗(yàn)結(jié)果表明“YMCSFLFNL”肽段與HLA-A020結(jié)合是穩(wěn)定的。見圖1、2。
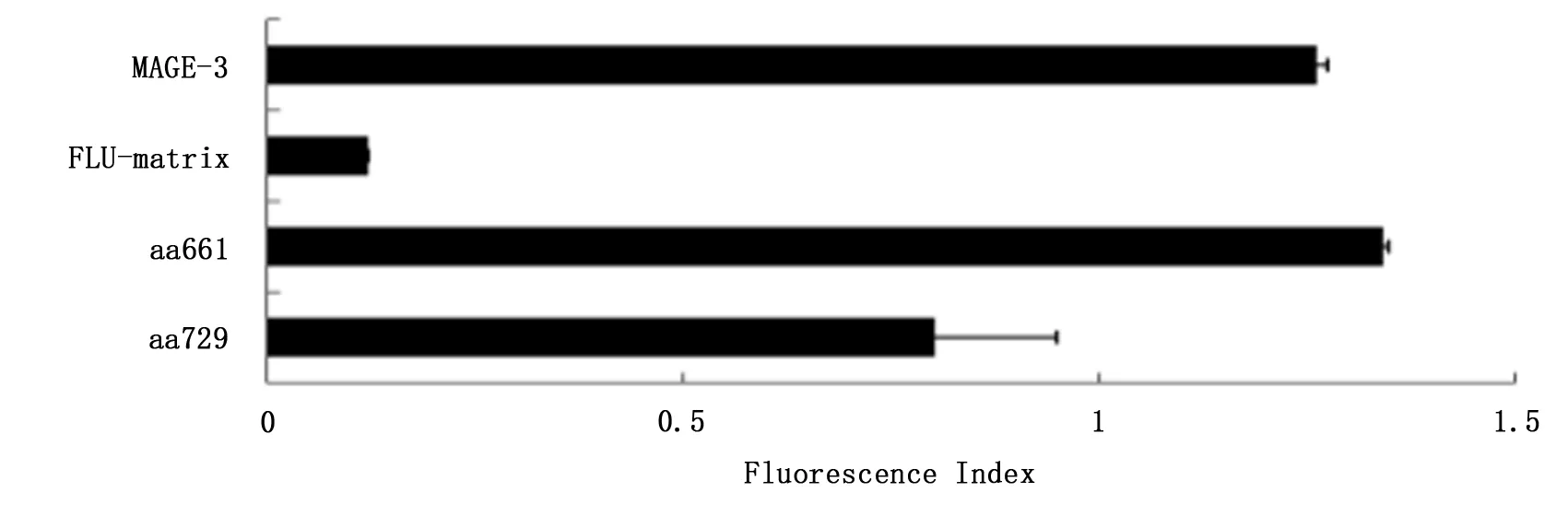
圖1 EZH2 肽段與T2細(xì)胞結(jié)合力實(shí)驗(yàn)結(jié)果
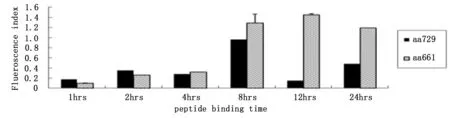
圖2 EZH2 肽段與T2細(xì)胞結(jié)合穩(wěn)定性實(shí)驗(yàn)結(jié)果
2.2 HLA-A0201限制性EZH2蛋白CTL表位肽驗(yàn)證
初步證明合成的EZH2-CTLS五聚體在健康供者及患者中都存在,并發(fā)現(xiàn)多發(fā)性骨髓瘤患者體內(nèi) EZH2-CTLS水平顯著高于健康對(duì)照者。見圖3。
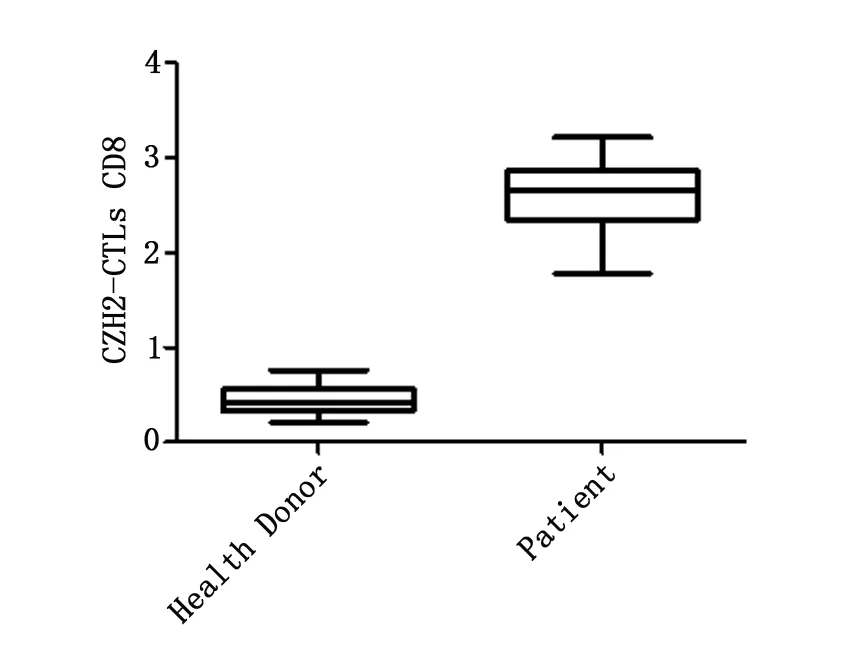
圖3 患者和健康對(duì)照者EZH2-CTLs水平測(cè)定
3 討論
多發(fā)性骨髓瘤是血液系統(tǒng)惡性腫瘤第二高發(fā)的,目前治療中大部分患者仍不能治愈。多發(fā)性骨髓瘤的疾病特點(diǎn)是單克隆的漿細(xì)胞呈惡性增殖,從而導(dǎo)致多發(fā)骨質(zhì)破壞、并進(jìn)一步導(dǎo)致腎功能衰竭等在內(nèi)的各個(gè)靶器官的功能性損害。我們希望設(shè)計(jì)出一種全新的治療方式來達(dá)到穩(wěn)定甚至起到清除那些已經(jīng)通過自體造血干細(xì)胞移植來達(dá)到緩解的或者穩(wěn)定的患者體內(nèi)的可能存在的微小殘留病灶。
免疫治療一直是醫(yī)學(xué)研究的熱點(diǎn),免疫治療或許可以成為治愈MM的一種新的選擇。研究者一直積極探索了許多MM的靶點(diǎn),比如未折疊蛋白(XBP1)[6]、熱休克蛋白(HSP)[7]及 CD138+[8]等,但上述靶點(diǎn)均存在相當(dāng)?shù)木窒扌訹9]。近來的研究發(fā)現(xiàn)免疫治療就是這樣一個(gè)無極接近設(shè)想的治療效果的理想的選擇,免疫治療可以有效清除骨髓瘤患者體內(nèi)存在的微小殘留病灶,甚至可以達(dá)到替代常規(guī)化療鞏固療效的作用。今年來已經(jīng)有少數(shù)學(xué)者通過使用來自患者血清的獨(dú)特型免疫球蛋白作為疫苗進(jìn)行免疫治療,但是結(jié)果并不理想,因?yàn)檠芯堪l(fā)現(xiàn)在體內(nèi)這種多發(fā)性骨髓瘤特異性T細(xì)胞被清除了,而且這種獨(dú)特型免疫球蛋白肽段也不是所有骨髓瘤患者的共同腫瘤抗原[10]。為了能提供更有效的免疫治療策略,我們需要找到一種骨髓瘤患者共有的腫瘤特異性抗原。EZH2具有理想腫瘤抗原的特性,在很多腫瘤中高表達(dá),最重要的是EZH2對(duì)于腫瘤細(xì)胞的生存至關(guān)重要,下調(diào)或者抑制EZH2的表達(dá)會(huì)使腫瘤細(xì)胞顯著凋亡[11-12]。
本研究通過在線篩選出EZH2高積分肽段,同時(shí)通過 T2細(xì)胞實(shí)驗(yàn)進(jìn)一步篩選出具備高親和力及穩(wěn)定性的一條肽段,合成五聚體后已分別在健康供者及患者外周血中檢測(cè)到不同水平的EZH2-CTLs,證明該表位肽是在生理及病理情況下自然存在的,為后續(xù)EZH2表位肽作為MM治療的靶點(diǎn)運(yùn)用于臨床奠定了基礎(chǔ)。

