乙型肝炎病毒相關慢加急性肝衰竭患者IL-6的表達及其對預后的影響
周超 張寧 何婷婷 王焱 余思邈 付雙楠 張晶晶 王宣 李昕 梁肖肖 李筠 宮嫚
乙型肝炎病毒相關慢加急性肝衰竭是臨床常見的肝病危重癥候群,短期病死率為50%~90%[1,2]。有研究顯示炎癥反應、免疫損傷、組織穩態失衡參與了疾病的進展[3-5]。慢加急性肝衰竭人群同時存在系統性炎癥反應和免疫抑制的雙重特征[6]。當機體遭受感染或非感染因素打擊時,立即啟動宿主應答,釋放促炎癥細胞因子,促炎介質和抗炎介質參與調節機體的應答能力[7]。損傷較為局限時,機體可及時組織修復而痊愈;當釋放的促炎介質超過局部到達全身時,引起全身炎癥反應綜合征,繼而導致抗炎反應同時并存的狀態[8];在炎癥與抗炎癥相互拮抗過程中,抗炎反應可能會減少過量炎癥反應的毒性作用,但也可能減弱宿主對抗感染的自我保護作用,導致肝功能的惡化以及器官功能衰竭[9,10]。白細胞介素6(IL-6)具有多種生物效應,涉及促炎癥反應、組織損傷、肝細胞再生、脂質代謝等多個方面[11]。本研究分析乙型肝炎病毒相關慢加急性肝衰竭人群中IL-6的表達特征及其對于疾病轉歸的影響。
資料與方法
一、研究對象
分析“十二五”重大專項課題入組的乙型肝炎病毒相關慢加急性肝衰竭患者的數據資料。所有病例來自解放軍總醫院第五醫學中心(原解放軍第三〇二醫院)、湖南中醫藥大學第一附屬醫院、華中科技大學附屬同濟醫院、湖北省中醫院、首都醫科大學附屬北京佑安醫院、中山大學附屬第三醫院、福州市傳染病醫院(孟超肝膽病醫院)、成都市公共衛生臨床醫療中心、深圳市中醫院、廣西中醫藥大學第一附屬醫院、杭州市西溪醫院、上海中醫藥大學附屬曙光醫院、首都醫科大學附屬北京地壇醫院、深圳市第三人民醫院、上海公共衛生臨床中心、天津市第二人民醫院、吉林省肝膽病醫院及沈陽市第六人民醫院18家單位。慢加急性肝衰竭診斷符合《肝衰竭診療指南(2012年版)》[12]。慢加急性肝衰竭的器官衰竭定義參照2013年歐洲肝病學會指南[13]。腎功能衰竭:肌酐≥2 mg/dL或需要進行血液凈化治療;肝功能衰竭:總膽紅素≥12 mg/dL;凝血功能衰竭:國際標準化比值≥1.5或血小板計數≤20×109/L;循環功能衰竭:使用血管活性藥物維持血壓;肺功能衰竭:氧分壓/吸入氧濃度≤200,或氧飽和度/吸入氧濃度≤214;腦功能衰竭:肝性腦病Ⅲ或Ⅳ期。
二、納入及排除標準
納入標準:①符合ACLF診斷標準的住院患者;②有HBV慢性感染基礎者;③自愿參加本研究并簽署知情同意書者。排除標準:①急性肝衰竭、亞急性肝衰竭、慢性肝衰竭;②其他病因(包括酒精性、藥物性、自身免疫性等)導致的ACLF;③妊娠或哺乳期婦女;④原發性肝癌患者;⑤合并其他嚴重的全身性疾病和精神病患者;⑥抗HIV陽性者;⑦近3 個月內曾參加其他臨床試驗者;⑧不愿合作者;⑨入組時已合并腦水腫、嚴重感染(包括感染性休克、深部真菌感染、2個部位以上感染和二重感染等)、Ⅰ型肝腎綜合征和消化道大出血者。
三、研究方法
采集入組病例的基線資料,包括性別、年齡、疾病分期、并發癥、器官衰竭等;檢測血常規、生化、病毒載量以及IL-6等指標;觀察4周、48周病死率。
四、統計學方法

結 果
一、人群基線特征
754例乙型肝炎病毒相關慢加急性肝衰竭患者的年齡為(42.7±10.9)歲,男性664例。疾病早、中、晚期分別為227例(30.1%)、337例(44.7%)、190例(25.2%);合并單一器官衰竭197例(26.1%),兩個及以上器官衰竭291例(38.6%),無器官衰竭457例(60.6%);179例有吸煙史(23.7%),77例有飲酒史(10.2%),合并糖尿病病史30例(4.0%),高血壓病28例(3.7%)。總膽紅素為(19.6±7.3)mg/dL,凝血酶原活動度為(31.9±6.9)%,國際標準化比值為2.3±0.6,MELD評分為24.1±5.5,IL-6為9.7(4.7,22.3)pg/mL。
二、IL-6與肝損傷指標和病毒載量的相關性
IL-6與國際標準化比值、總膽紅素、MELD評分呈正相關,相關系數分別為0.108、0.143、0.173;與血小板計數、ALT、AST、白蛋白呈負相關,相關系數依次是-0.160、-0.151、-0.129、-0.126;差異均有統計學意義(均P<0.01)。IL-6與白細胞計數、病毒載量無顯著相關性,相關系數分別為0.038,-0.044(均P>0.05)。
三、IL-6與疾病分期、器官衰竭、感染與否及HBeAg狀態的相關性
乙肝相關慢加急性肝衰竭早期患者的IL-6水平為7.25(3.95,16.36)pg/mL,中期為9.88(5.39,22.95)pg/mL、晚期為13.64(5.11,30.40)pg/mL,差異有統計學意義(P<0.01)。無器官衰竭患者的IL-6水平為8.82(3.91,18.81)pg/mL,乙肝相關慢加急性肝衰竭合并2個及以上器官衰竭患者的IL-6水平高于合并1個器官衰竭患者,差異有統計學意義(P=0.014)。IL-6等細胞因子水平在HBeAg(+)和HBeAg(-)、是否合并感染的乙肝相關慢加急性肝衰竭人群中的差異無統計學意義(P>0.05)。見表1。
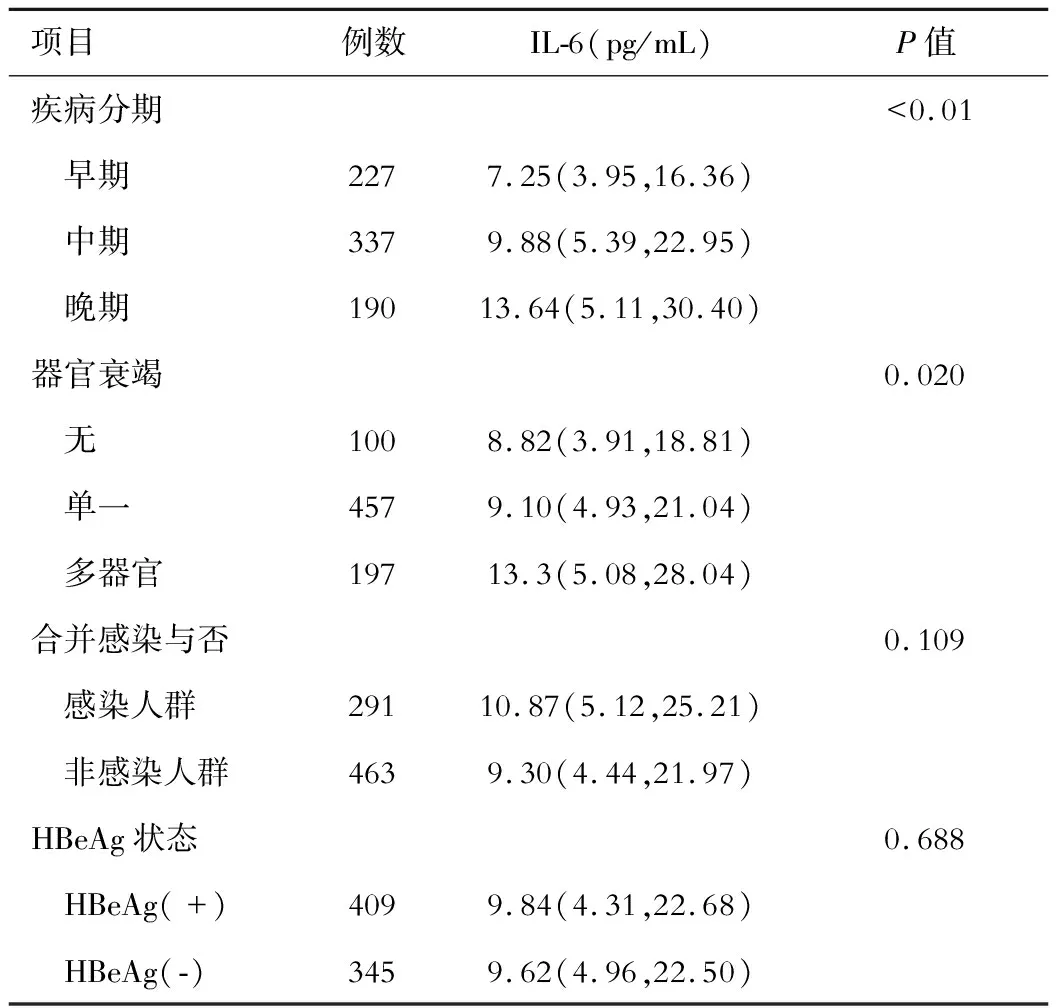
表1 IL-6在不同人群中的表達差異
四、IL-6對預后的影響
754例患者中,IL-6>9.78 pg/mL 377例,IL-6≤9.78 pg/mL 377例。IL-6高水平組4周、48周病死率高于IL-6低水平組;IL-6高水平組4周死亡風險是低水平組的2.20倍(P<0.01),經校正年齡、MELD評分后死亡風險為1.93(P=0.003);IL-6高水平組48周死亡風險是低水平組的1.74倍(P<0.01),經校正年齡、MELD評分后死亡風險為1.47(P=0.008)。見表2。

表2 IL-6對4周、48周病死率的影響
討 論
本研究結果顯示,IL-6與乙型肝炎病毒相關慢加急性肝衰竭肝損傷的程度有關,是疾病預后的獨立影響因素;患者基線時IL-6升高與疾病晚期、多器官衰竭、高死亡風險密切相關;預示IL-6可以作為反映肝損傷程度和評估預后的潛在指標。
IL-6是由成纖維細胞、單核細胞、巨核細胞、T細胞以及內皮細胞合成和分泌,具有多重功能,在生理條件下,可以維持適度的肝組織穩態,肝臟再生能力,感染防御和調節代謝功能[14,15]。當機體出現組織損傷或炎癥感染時,IL-6迅速合成,通過刺激急性免疫反應和造血系統促進機體的防御功能;而當組織穩態恢復時,IL-6中止合成[16]。但IL-6通路的持續激活與肝臟損傷、肝癌發生有關[17]。動物模型證實,IL-6可誘導慢性肝病的穩定狀態出現急性肝損傷[18]。IL-6在體內發揮不同功能與調控的傳導通路有關,IL-6經典通路主要與急性炎癥反應密切相關,而IL-6信號轉導與肝細胞再生有關[11,19]。在慢加急性肝衰竭人群中檢測到IL-6水平顯著高于慢性肝病或肝硬化人群[20-23]。本研究發現疾病晚期或多器官衰竭人群中的IL-6水平顯著升高,表明IL-6可能與乙型肝炎病毒相關慢加急性肝衰竭的疾病損傷程度有關;但在感染與否人群未呈現差異,這可能是受到人群感染時限的影響,通常在早期急性炎癥反應階段(24~48 h)IL-6升高。同時,本研究發現IL-6升高與高死亡風險相關。當機體出現早期炎癥反應,大量促炎癥介質的釋放,機體代償性啟動抗炎反應,最終導致免疫病理損傷,這一過程與慢加急性肝衰竭出現器官衰竭、不良預后密切相關[9,10]。IL-6作為促炎性因子參與早期炎癥反應,但在慢加急性肝衰竭疾病進展過程中的作用仍需通過進一步的研究進行闡述。
近年來,關于IL-6在維持肝臟生理和病理方面作用的研究取得了很大的進展。動物實驗證實IL-6促進肝臟再生能力主要與反信號通路有關[19],但IL-6應用于肝病的臨床治療仍在進一步的研究中,精確選擇或調控IL-6的信號通路可能成為肝病治療的新手段。因此,IL-6可作為一種輔助指標用于臨床判斷乙型肝炎病毒相關慢加急性肝衰竭肝損傷程度和轉歸。