醫療器械生產企業質量檢驗信息化系統的研發和應用
林定余,郭永兵,朱清,
1 寧波戴維醫療器械股份有限公司,寧波市,315700
2 浙江醫藥高等專科學校,寧波市,315100
0 引言
中國醫療器械產業發展迅速,已成為全球第二大醫療器械市場[1],然而國內眾多醫療器械企業的質量管理體系依舊存在諸多不足[2]。質量管理體系的良好運行是產品質量與安全的保障[3]。國內法規要求醫療器械生產企業應按照《醫療器械生產質量管理規范》的要求,建立健全與所生產醫療器械相適應的質量管理體系并保證其有效運行[4]。隨著國內外監管從上市前監管轉向產品全生命周期的監管[5-6],對生產企業的質量管理體系提出了更高的要求。新時代的醫療器械監管更加注重過程控制,包括對產品、過程和檢驗設備等方面的控制,而不單純只強調檢測。產品檢測內容方面,包括對原材料、過程、成品質量的檢驗。要求工廠產品檢驗(或驗證)應符合“技術要求”的全部項目[7]。
2016-2017年,原國家食品藥品監督管理局在國內醫療器械生產企業飛行檢查中發現,生產企業質量管理體系缺陷主要存在于文件和記錄控制、生產管理、采購等環節中[8-9]。其中,文件管理不當的缺陷項是監管部門日常監督檢查或飛行檢查中發現的高頻問題之一。這類問題部分是由于企業管理層對質量管理體系理解不到位,沒有妥善保管質檢文件;或由于企業跨部門間溝通效率低,沒有及時記錄檢驗數據、更新倉儲數據;或由于一線檢驗人員對法規、標準理解不到位等原因造成的[10]。為了解決上述問題,本公司研發了一套質量管理檢驗信息化系統,并應用到企業管理中,用以提高企業的質量體系管理水平。
1 系統設計
1.1 系統框架
質量管理檢驗信息化系統分為用戶界面層、應用服務層、數據接口層和數據庫等四層。用戶界面層包含檢驗人員的移動客戶端操作界面和PC客戶端操作界面。應用服務層為產品生產檢驗業務流程模塊的構建。數據接口層負責連接檢驗數據和ERP數據,以及信息化系統業務模塊之間的數據交互。數據庫包括檢驗標準化數據儲存和ERP系統數據庫,兩個數據庫的數據動態鏈接,實時更新產品檢驗過程數據,如圖1所示。

圖1 質量管理檢驗信息化系統總體結構圖Fig.1 Structure chart of quality inspection information system
1.2 用戶界面層
用戶界面層面向檢驗人員、復檢人員、審核人員、產品放行審批人和倉儲管理人員五類人員。
(1)檢驗人員:采用移動終端掃描采購件、中間品或成品二維碼,通過電子檢驗登記單輸入檢驗結果。對于定量檢驗,檢驗人員只需要輸入檢驗結果,系統將自動將檢驗結果與該檢驗項目指標的標準進行比較。如果檢驗結果在標準值允許的范圍內,系統自動判斷為合格;如果檢驗結果不符合標準值,系統自動判斷為不合格,并自動產生一條復檢記錄。
(2)復檢人員:查看產品的不合格項目指標,并對采購件、中間品或成品的不合格項進一步復查,給出復檢結果和復檢結論,并做好復查記錄。
(3)審核人員:需要根據檢驗人員的檢驗記錄單和復檢人員的復檢記錄單,審核產品是否全部符合檢驗和試驗規范要求,并給出產品檢驗的最終結論。
(4)產品放行審批人:成品由制造部發起產品放行審批單,采購物資由采購部門發起產品放行審批單。系統根據預先流程設置,相關部門分別在流程中對產品放行的必要條件逐一進行確認,最終由公司制定的產品放行審批人進行最終審批。
(5)倉儲管理人員:接收到放行審批單后,采用移動終端掃描產品二維碼并確認產品實物,系統會自動在ERP系統中生成入庫單,對產品庫存數據實施自動更新,倉儲管理人員按法規要求在倉儲區域進行分類放置、標識和管理。
1.3 應用服務層
應用服務層根據業務流程設計開發,整體上可分為基礎性業務工作和常規性業務工作兩類。
基礎性業務工作包括建立產品數據庫、導入產品質檢方案和關聯產品檢驗項目指標等三個步驟。首先,依照企業內產品品種或型號建立標準化的產品數據庫;然后,根據產品的品種或型號導入對應的產品質檢方案;最后,根據產品質檢方案,梳理對應產品項目指標清單、檢驗操作流程/規范和檢驗合格的標準值范圍。基礎性業務工作如無變更,一般只需填報一次。
常規性業務工作包括產品檢驗登記、檢測數據結果、復檢、放行審核和產品入庫等工作環節。常規性業務工作可直接調用基礎性業務工作的相關數據庫。
第一步,檢驗人員掃描每批/臺的產品二維碼,系統根據基礎性業務工作中的產品數據庫,生成該產品的電子檢驗記錄表。如該產品品種或型號不在產品數據庫中,則需要在基礎性業務工作中對該產品的數據進行補充。
第二步,檢驗人員核對系統生成的檢驗方案,并根據該方案的項目指標完成對應的采購物料、中間品和/或成品的所有檢驗項目。檢驗人員將完成檢驗的該臺/批產品檢驗記錄單提交至最終審核人。審核人員對檢驗內容和項目進行核查,如出現復檢項,還要對復檢結果進行核查。經核查所有檢驗項目全部符合檢驗和試驗規范要求后,方能通過審核。
第三步,產品放行審批人根據產品的檢驗登記表和檢驗報告單,判斷產品是否符合放行條件。倉儲管理人員根據產品的最終放行審批單,按法規要求在倉儲區域進行分類放置、標識和管理。
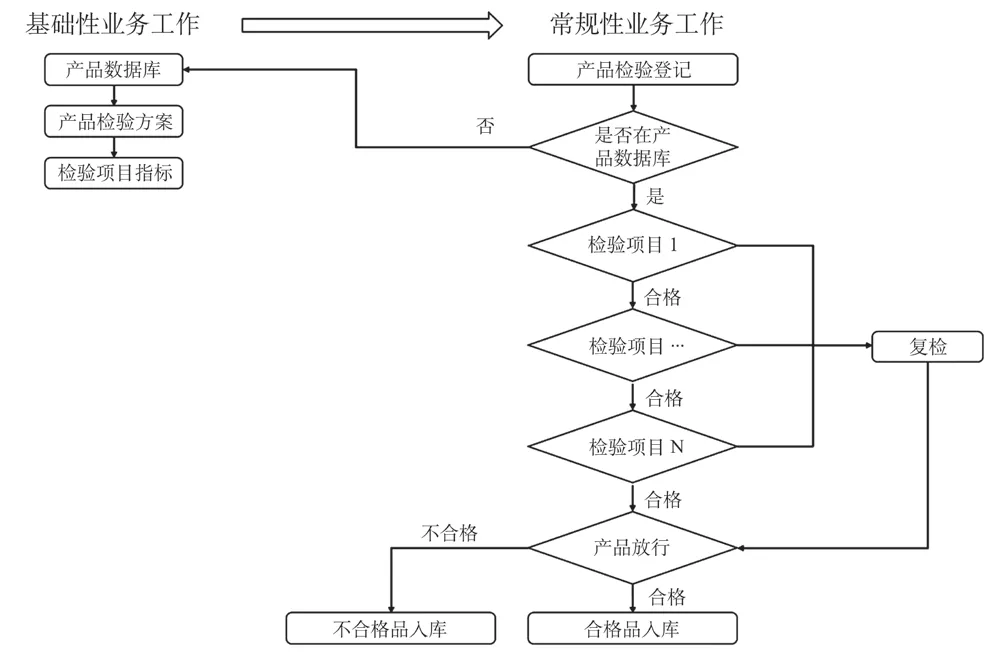
圖2 質量管理檢驗信息化系統業務流程圖Fig.2 Business flow chart of quality inspection information system
1.4 數據庫層
數據庫包括檢驗數據庫和ERP系統數據庫。檢驗數據庫的物料領用和產品檢驗信息,與ERP數據庫的進存銷數據保持動態連接,以保證物料和成品庫存數據可隨生產和檢驗過程實時更新。
檢驗數據庫層包括產品信息、基礎數據檔案、質檢方案、檢驗項目指標、關鍵元器件和檢驗裝置,以及每批/臺設備的檢驗信息、復檢信息和放行信息等。產品信息包括產品類型型號等,該信息與產品實物之間通過二維碼實現關聯。每個產品一旦進入生產環節,將生產一個二維碼作為該產品的“身份證”,保證產品和二維碼之間唯一對應。通過掃描產品的二維碼,能夠關聯產品生產和檢驗的所有信息,包括產品的生產日期、檢驗項目、檢驗人員、檢驗數據和結果等信息。基礎數據檔案包括檢驗用的儀器、設備的狀態、校準日期等信息;質檢方案包括文件版本號、方案內容、生效日期和檢驗操作指導書等;項目指標包括產品出廠檢驗需要檢測的項目清單、技術要求等。
調用的ERP系統數據庫包括物料采購信息、物料庫存、庫存等信息。ERP系統數據庫與檢驗系統數據庫之間存在數據的流向如下:通過ERP系統從供應商處采購物料,檢驗人員完成進貨檢驗并上傳檢驗系統。合格的物料進入ERP物料庫存,不合格的進行退貨或銷毀。當生產車間開始產品生產時,從倉庫領用物料,ERP系統對應核減。在產品生產中或生產完后,對中間品或產成品進行檢驗和復檢。管理人員對合格產品放行進入倉庫,不合格產品放置于不合格區,同時在ERP系統中生成記錄,如圖3所示。
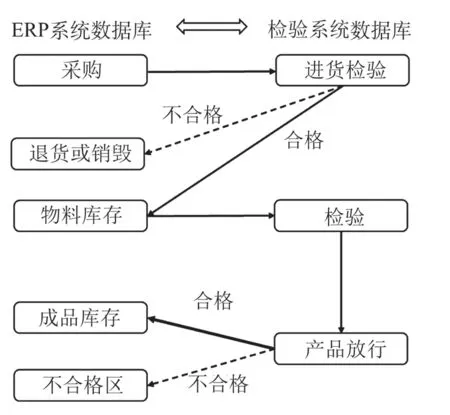
圖3 ERP系統數據庫與檢驗系統數據庫的數據交換示意圖Fig.3 Sketch map of data exchange between ERP system database and inspection system database
1.5 系統研發
質量管理信息化系統采用C/S架構,由SQL Server數據庫、服務端和客戶端組成,適用于Win7/Win10操作系統。
根據業務流程,管理人員和檢驗人員PC端界面的菜單欄包含基礎數據檔案維護、項目指標總清單、質檢方案檔案、質檢項目登記、產品檢驗登記、產品檢驗審核、復檢記錄保持、質檢報告打印和查詢、質檢數據搜索和統計分析等功能,各功能視實際需求開放給所需人員。具體操作界面,如圖4所示。
圖4 管理人員和檢驗人員的操作界面,包括產品檢驗登記、檢驗復核、復檢記錄等Fig.4 Operation interface of management personnel and inspection personnel,including product inspection registration,inspection review,re-inspection records,etc.
2 應用成效
質量檢驗信息化系統的研發始于2018年3月,并于2020年4月在本公司中實際投入使用,覆蓋企業全部的醫療器械產品,共計16類品種、78個型號。質量檢驗信息化系統的應用不僅實現所有產品檢測過程信息化和可視化,而且與ERP系統實時聯動,從而保證物料、中間品和成品數據的準確性。
2.1 凸顯質量管理的重要性
醫療器械生產企業質量管理檢驗系統研發的最大難點,往往并不僅僅在于系統開發硬件上的難點,還在于企業思想上的“軟件”問題[10]。信息化系統的研發過程,需要打破企業傳統的工作模式和工作習慣。在短期內增加企業員工的工作量,必然引起一部分企業工作人員對于信息化系統的抵觸。因此,要推進信息化系統的研發和應用,需要改變生產企業過往的“重理論、輕質量”“重生產、輕質檢”的理念,要重新激發企業的內在創新動力。信息化系統研發的過程,幫助企業管理層重新認識產品質量管理對于企業發展的重要性,提高了企業的技術研發人員、生產車間人員等對質檢作用的重視,督促企業投入資金和技術用以加強產品質量體系建設,最終在企業內形成產品生產和質檢“兩手都要抓,兩手都要硬”的新氛圍。
2.2 完善質量管理的追溯體系
質量管理檢驗信息化系統實現了質檢方案、檢驗記錄等數據的電子化,有利于企業發現產品質量管理中可能存在的問題或漏洞,幫助企業追溯問題產品的根源。
質檢方案是企業產品檢驗的“憲法”,是質量體系的基石,是保障產品安全有效的重要組成。大部分生產企業的質檢方案一般采用紙質文件的形式保存。紙質文件會因為保存時間跨度過長、原保管人員的離職、企業生產地址搬遷等眾多因素而損壞或遺失。質檢方案電子化后可將其保存在企業云端,從而打破空間和時間的局限性,可供企業和監管部門隨時隨地調取、檢索和翻閱,提高工作效率。而且,電子化的質檢方案即使經過多個版本的變更或修訂,歷史的版本都可以進行有效追溯,方便企業對質量體系建設過程和歷史進行總結和回顧性的評價。
檢驗記錄的電子化,將所涉及檢驗的人員、檢測時間地點、使用的檢驗儀器、檢測原始數據等重要信息均保存在云端。一方面,如果產品出現故障或不良事件,可快速追溯、重現該設備的生產、檢驗的過程,有利于分析和排查導致不良事件發生的原因。另一方面,電子化檢驗數據有利于企業從時間軸上分析比較各批次產品的檢驗數據,查找趨勢性變化,通過專家會診或大數據分析的方法,排查質量體系中可能存在的不足。
2.3 提高產品質檢效率和準確性
以往產品檢驗采用紙質記錄方式,不同的檢驗項目會有多份紙質檢驗登記表。如果多品種、多型號、多批次的產品同時需要檢驗,容易造成登記表混淆,且不方便登記表的管理。隨著信息化系統的應用,產品的種類、型號、批次信息可通過掃描產品的二維碼直接生成。因此提高了檢驗工作效率和準確率。既避免了同一產品多個項目的重復填寫,也保證實際檢驗的產品和檢驗登記表相一致。
掃描產品的二維碼,不僅能獲得對應產品的基本信息,還能提供產品的質檢方案和項目清單。檢驗人員根據移動終端的提示,開展項目檢測并填寫檢驗數據。系統根據檢驗結果和項目清單自動判斷該項目是否合格,從而減少人為判定的誤差。這使得檢驗人員可更專注于檢驗的過程,提高檢驗效率。
2.4 順應新時代醫療器械數字化監管的趨勢
一方面,隨著人民的生活水平提高和對醫療服務需求的多樣化,國內藥械化企業發展迅速,企業數量和產品種類日益增加,使得藥監部門的監管壓力不斷增加。因此,通過打造智能監管系統,提高監管效能,已經成為國家藥械化監管的大趨勢[11]。多個省市的監管部門已加快推進“數字藥監”的建設和應用。生產企業的基本數據監管和生產業務數據是構建“數字藥監”的一個重要組成部分,為“數字藥監”風險預警模型提供所需的數據源,增強風險預警系統的預判性[12]。
另一方面,監管部門的檢查人員到企業現場檢查的過程中,有不少精力和時間浪費在質量體系文檔、產品生產檢驗原始記錄和倉儲文檔等紙質文件上查找和比對信息。信息化系統整合ERP和檢驗數據庫,可以為檢查人員提供便捷的搜索功能。通過關鍵詞搜索,找到對應的文檔進行核對和數據校驗;當檢查員到車間檢查產品生產和檢驗過程時,檢查人員可通過移動終端掃描產品的二維碼,立即獲得產品的所有檢驗信息。這提高了現場檢查的效率和有效性。
3 總結和展望
醫療器械生產企業質量檢驗信息化系統能夠將生產質檢過程透明化,有利于企業扁平化管理,明確職責,提高企業內部協同效率。然而,一套系統是否能順利運作,不僅僅靠系統本身,還與企業內參與系統使用者息息相關。企業需要統一思想,做好系統使用培訓,切實將質量控制從線下轉到線上線下相結合的模式,讓信息化系統發揮真正的作用。未來,隨著工業4.0智能制造設備和5G物聯網的推進應用,檢驗設備能夠自動完成檢驗和數據上網[13],將進一步提高檢驗效率,減少人為誤差以及人為篡改數據的可能性。

