基于網絡藥理學、分子對接和實驗驗證探討朱茯苓用于失眠的作用機制
周 揚,郭冷秋,劉 遜,談如藍,鐘其新,曾 峰
1蘇州衛生職業技術學院 蘇州檢驗醫學生物技術重點實驗室,蘇州 215009;2廣州中醫藥大學青蒿研究中心,廣州 510445;3廣州中醫藥大學深圳醫院(福田),深圳 518034
失眠通常指患者對睡眠時間和(或)質量不滿足并影響白天社會功能的一種主觀體驗,是一種常見的生理心理疾患[1],其發病率約為20%[2],已日益成為涉及范圍甚廣的社會熱點,引起人們的廣泛重視。失眠在中醫中亦稱“不寐”,指由于外感或內傷等原因,造成陰陽氣血及心、肺、脾、腎等臟腑功能失調而引起的無法正常睡眠為特征的一種病癥[3],輕者入睡困難、睡后易醒、醒后不能再寐或時寐時醒等。重者整夜徹夜難眠,長期失眠會給人的正常生活和工作帶來嚴重的不利影響。目前臨床治療失眠的西藥以苯二氮卓、非苯二氮卓類為主,此類藥物主要作用于神經遞質γ-氨基丁酸(GABA)[4],但副作用大、依賴性強、有成癮風險。而中醫藥治療失眠主要以補虛瀉實、調整臟腑陰陽為治則,在治療失眠方面具有副作用小、無依賴性和成癮性等優勢,越來越受到重視,在臨床應用廣泛并取得良好的療效。
茯苓味甘性平,歸心、肺、脾和腎經,有利水滲濕、健脾寧心的功效[5]。茯苓的主要有效成分為茯苓多糖和三萜類物質,相關研究表明茯苓特有的四環三萜化合物茯苓酸具有鎮靜催眠作用且茯苓酸的催眠效果與調節腦內GABA的A型受體(GABA-A)表達水平有關[6]。朱砂為硫化物類礦物辰砂族辰砂,主含硫化汞(HgS),朱砂味甘性微寒,歸心經,有清心鎮驚、安神、明目、解毒的功效,相關研究表明,朱砂能夠延長大鼠的慢波睡眠,有效改善大鼠的睡眠[7]。拌衣炮制是一種傳統炮制工藝,朱茯苓即為采用此工藝制成,取茯苓塊以清水噴淋,稍悶潤后加水飛朱砂細粉撒布均勻,反復翻動,使其外表粘滿朱砂粉末,然后晾干而成(每50 g茯苓配用水飛朱砂細粉1 g)[8]。《本草綱目》中記載:“茯苓,本草言利小便,伐腎邪……同朱砂能秘真元”。因此理論上,茯苓拌染朱砂后,可共奏鎮靜安神、祛邪寧心之效,多用于失眠、驚悸、健忘諸癥。然而,目前關于朱茯苓治療失眠的研究和機制探討的文章尚不多見。
網絡藥理學緊緊圍繞系統生物學、生物網絡構建和分析等進行藥物有效性、代謝特性的揭示,是建立在高通量組學數據分析、計算機虛擬計算及網絡數據庫檢索基礎上的生物信息網絡構建及網絡拓撲結構分析策略和技術基礎上的科學思想和研究策略。利用網絡藥理學技術構建多層次網絡模型,從整體角度對中藥進行研究,已成為一種科學解釋中藥有效性和科學性的新策略,在多方面的中藥研究中已具備了成功應用的經驗[9]。
本研究以朱茯苓鎮靜安神的功效為切入點,遵循網絡藥理學理論與技術,篩選朱茯苓活性成分及潛在靶點,構建活性成分-靶點網絡,對交集靶點進行器官定位,并進行GO功能和KEGG通路的富集分析以及分子對接驗證,通過免疫印跡實驗(Western blot)驗證朱茯苓對GABA受體α1亞基基因(Gamma-aminobutyric acid receptor subunit alpha-1,GABRA1)和γ2亞基基因(Gamma-aminobutyric acid receptor subunit gamma-2,GABRG2)兩種受體蛋白水平的影響,以期從分子層面初步闡述朱茯苓治療失眠的可能的分子作用機制,為朱茯苓進行后續深入研究提供新思路和新方法。
1 材料與方法
1.1 朱茯苓的活性成分篩選
朱茯苓活性成分的篩選,基于TCMSP平臺(http://tcmspw.com/index.php)、TCMID數據庫(http://www.megabionet.org/tcmid/)和BATMAN-TCM數據庫(http://bionet.ncpsb.org/batman-tcm/)以及文獻查閱,收集茯苓和朱砂的活性成分,以口服生物利用度(oral bioavailability,OB)和類藥性(drug-likeness,DL)篩選區符合條件的候選活性成分和對應靶點,將OB≥30%和DL≥0.18設為篩選條件,針對某些成分雖然OD值和DL值較低但仍具有較強活性這一情況,結合相關活性成分的文獻記載,得到最終篩選得到的活性成分,使用Pubchem數據庫(https://pubchem.ncbi.nlm.nih.gov/)驗證活性成分并獲取其分子結構及PubChem CID等信息。
1.2 靶點的預測與篩選
運用TCMSP平臺、BATMAN-TCM數據庫和STITCH數據庫(http://stitch.embl.de/)預測活性成分的靶點。在OMIM數據庫(https://omim.org/)、TTD數據庫(http://db.idrblab.net/ttd/)、CTD數據庫(http://ctdbase.org/)和GeneCards數據庫(https://www.genecards.org/)上篩選失眠相關靶點。將活性成分和疾病靶點導入Uniprot數據庫(http://www.uniprot.org/),篩除非人類靶點并校正靶點名稱。
1.3 化合物-靶點相互作用網絡及靶點間相互作用網絡的構建與分析
將活性成分及其靶點信息導入Cytoscape_v3.7.2軟件(http://www.cytoscape.org/),構建化合物-靶點相互作用網絡。基于String數據庫(https://string-db.org/)獲取活性成分和疾病的交集靶點的高置信度PPI網絡信息,在Cytoscape軟件中構建靶點間相互作用網絡,使用“NetworkAnalyzer”工具對網絡進行拓撲分析,根據拓撲參數篩選核心化合物和核心靶點。
1.4 器官定位
將朱茯苓治療失眠的潛在靶點上傳至BioGps數據庫(http://biogps.org/)進行器官定位分析,并繪制靶點的器官定位圖。
1.5 GO功能和KEGG通路富集分析及化合物-靶點-通路網絡的構建
將朱茯苓治療失眠的潛在靶點上傳至David6.8數據庫(https://david.ncifcrf.gov/),選擇物種和背景為人(Homo sapiens),進行GO功能富集分析及KEGG通路富集分析并在Cytoseape軟件中構建化合物-靶點-通路網絡。
1.6 分子對接驗證
根據上述篩選出的活性成分和核心靶點,從PDB數據庫(http://www.rcsb.org/)獲取相應靶點的蛋白結構,使用Autodock_vina軟件(http://vina.scripps.edu/)對靶點與核心活性成分和陽性對照藥物艾司唑侖(estazolam)進行分子對接驗證。
1.7 Western blot檢測小鼠腦組織中GABRA1及GABRG2的表達
1.7.1 藥材、試劑和儀器
艾司唑侖片(20180710,常州四藥制藥有限公司);朱砂拌白茯苓飲片(2017101808,上海余天成中藥飲片有限公司);戊巴比妥鈉(626Y9216,美國Sigma公司);GABRA1單克隆抗體、GABRG2單克隆抗體、β肌動蛋白(β-actin)(AH01126063,AC072366,AH11279138,北京博奧森生物技術有限公司);Allegra 64R臺式高速冷凍離心機(美國Beckman Coulter公司);PowerPac Basic 型蛋白電泳儀(美國Bio-Rad公司)。
1.7.2 動物
健康SPF級ICR雄性小鼠,體重<15 g,購于上海斯萊克實驗動物有限責任公司,實驗動物許可證號:SCXK(滬)2017-0005。
1.7.3 實驗方法
將30只健康SPF級雄性ICR小鼠適應性飼養7天后,隨機分為生理鹽水組、艾司唑侖組、朱茯苓水煎液低、中、高劑量組,分別灌胃相應濃度的藥液(艾司唑侖藥液劑量為0.15 mg/kg,朱茯苓水煎液低中高劑量分別為1.14、2.28和4.55 g/kg),給藥體積20 mL/kg,每天1次,連續灌胃7天,于末次給藥50 min后腹腔注射戊巴比妥鈉閾劑量并禁食12 h,脫頸椎處死小鼠,于冰浴皿上快速取出大腦,剝去腦膜,用預冷的生理鹽水洗凈,濾紙吸干后,然后取腦組織加入裂解液,冰上裂解1 h后高速離心取上清,測定組織蛋白濃度,以PAGE凝膠電泳分離蛋白樣品。按照說明書提供的分子量條帶選定切膠范圍,濕法轉膜,用封閉液封閉1 h(含5%脫脂奶粉的TBS-T緩沖液)。室溫孵育后棄去封閉液,加入一抗在4 ℃孵育過夜,TBS-T洗5×5 min,加入二抗溫育1 h,TBS-T洗5×5 min,最后進行顯色。
2 結果
2.1 朱茯苓的活性成分及靶點預測
通過TCMSP平臺、TCMID數據庫、BATMAN-TCM數據庫、STITCH數據庫以及文獻查閱,收集朱茯苓的活性成分并預測其潛在靶點,篩除重復化合物及缺少靶點預測的化合物后,使用Pubchem數據庫驗證活性成分的分子結構并獲取PubChem CID等信息。結果共篩選朱茯苓活性成分33種,其中茯苓32種、朱砂1種,經過Uniprot篩選和校正的潛在靶點有267個。表1為朱茯苓的活性成分信息。

表1 朱茯苓的活性成分信息
2.2 化合物-靶點網絡
在Cytoscape中構建朱茯苓的化合物-靶點相互作用網絡,使用Network Analyzer進行拓撲分析。化合物-靶點網絡共有300個節點(包括 33個化合物和267個靶點),453條邊。網絡中一個節點的度(degree)表示網絡中和節點相連接的路線條數,活性成分度值越高,作用的潛在靶點越多,活性成分的度值越高說明該成分越可能是核心活性成分。該網絡中每個活性成分平均有13.7個靶點,度值中位數為9。拓撲分析結果顯示,15個活性成分的作用靶點≥10個,其中麥角胺(8223)、齒孔醇(9803310)、腺嘌呤(190)、去氫齒孔酸(15250826)等四個活性成分的作用靶點≥30個,上述15個高度值活性成分可作為朱茯苓的核心活性成分。圖1為朱茯苓的化合物-靶點相互作用網絡,橙色節點為靶點,藍色節點為活性成分,其中深藍色節點為核心活性成分。表2為degree≥10的核心活性成分拓撲參數表。

表2 核心活性成分拓撲參數表
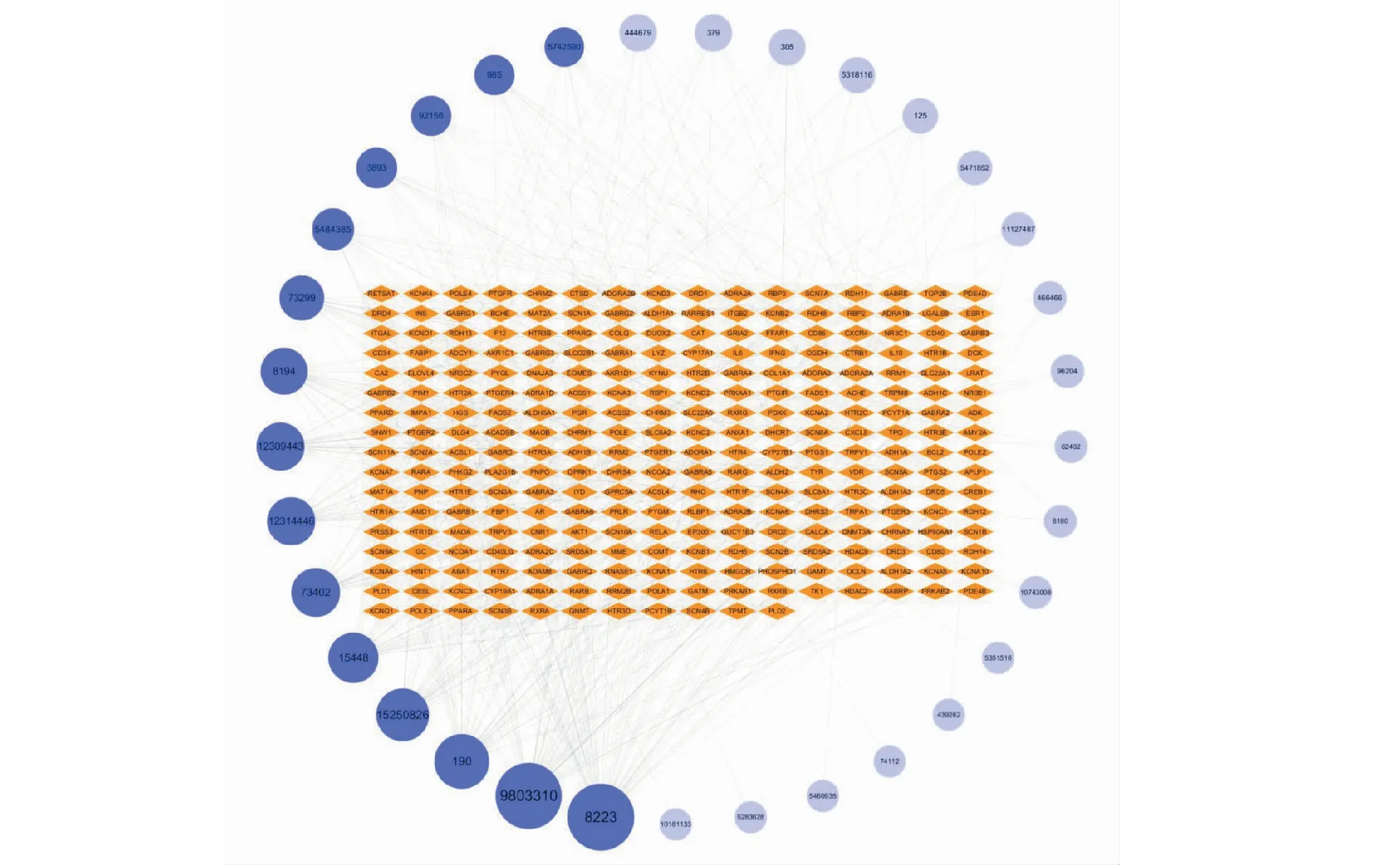
圖1 朱茯苓治療失眠的化合物-靶點網絡圖Fig.1 The compound-target network of Zhufuling in the treatment of insomnia
2.3 交集靶點間的相互作用網絡
從OMIM數據庫、TTD數據庫、CTD數據庫和GeneCards數據庫共篩選到258個失眠相關靶點,朱茯苓的潛在靶點與失眠相關靶點共存在36個交集靶點,將36個交集靶點上傳String數據庫,獲得高置信度的靶點間相互作用信息,在Cytoscape中構建交集靶點間的相互作用網絡。使用Network Analyzer進行拓撲分析,結果為介度中心度(betweenness centrality,BC)中位數為0.026 338 32,緊密中心度(closeness centrality,CC)中位數為0.45,度(degree)中位數為5,表3為核心靶點的拓撲參數表,圖2為朱茯苓治療失眠的預測靶點間相互作用網絡圖,節點直徑與度值大小成正比,深色節點為核心靶點。結果表明共有13個靶點的拓撲參數滿足上述中位數卡值,可作為朱茯苓治療失眠的核心靶點。
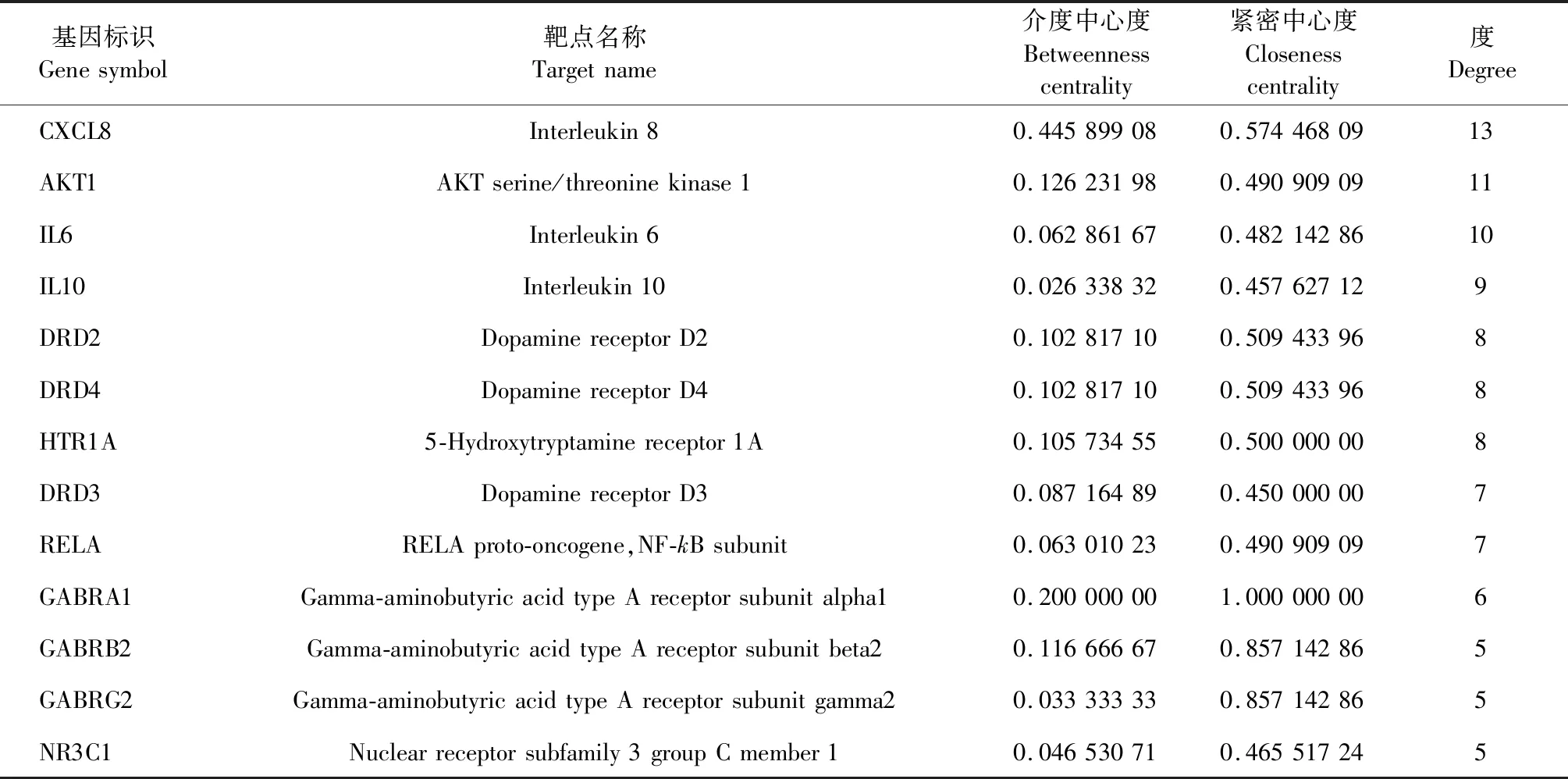
表3 朱茯苓治療失眠的核心靶點拓撲參數表
圖2 朱茯苓治療失眠的靶點蛋白高置信度交互作用網絡圖Fig.2 The high confidence interaction network of target protein of Zhufuling in the treatment of insomnia
2.4 器官定位結果
基于BioGps數據庫對朱茯苓治療失眠的潛在靶點進行器官定位分析,結果見圖3,圖3為朱茯苓治療失眠潛在靶點的器官定位圖,其中深紅色靶點為核心靶點。結果表明36個交集靶點中11個靶點作用于腦,6個靶點作用于心,3個靶點作用于肝,2個靶點作用于肺,14個靶點作用于淋巴、小腸等其他器官。說明朱茯苓主要通過對腦、心及淋巴等器官的共同作用實現對失眠的治療效果。
2.5 富集分析結果
圖4為GO功能富集分析條形圖,GO功能富集分析共富集到P<0.05的GO條目189個,包括154個生物過程(biological process,BP)條目、16個細胞組分(cell components)條目、19個分子功能(molecular function)條目。其中GABA信號通路(gamma-aminobutyric acid signaling pathway)、5-羥色胺(5-HT)信號通路(serotonin receptor signaling pathway)、多巴胺(DA)突觸傳遞(synaptic transmission,dopaminergic)、GABA-A型受體活動(GABA-A receptor activity)等條目P值小且與失眠密切相關。圖5為KEGG通路富集分析氣泡圖,KEGG通路富集分析共富集到24條與失眠相關的通路,其中刺激神經組織的互動(neuroactive ligand-receptor interaction)、DA能神經突觸(dopaminergic synapse)、5-HT神經突觸(serotonergic synapse)、逆行神經信號(retrograde endocannabinoid signaling)、cAMP信號通路(cAMP signaling pathway)、GABA受體神經突觸(GABAergic synapse)等條目P值最小。
2.6 化合物-靶點-通路網絡
在Cytoscape中構建化合物-靶點-通路網絡,圖6為朱茯苓治療失眠的化合物-靶點-通路網絡圖,其中深綠色節點為核心活性成分,深藍色節點為核心靶點。網絡共有79個節點和188條邊,包括24種活性成分,33個靶點和24條KEGG通路。可見,朱茯苓通過多種成分的多個靶點作用于多條失眠相關的通路,實現對失眠的治療作用。
圖3 朱茯苓治療失眠潛在靶點的器官定位圖Fig.3 The organ location map of potential target of Zhufuling in the treatment of insomnia
2.7 分子對接結果
選取兩個核心靶點GABRA1和GABRG2與相應核心活性成分進行分子對接。從PDB數據庫篩選的GABRA1受體蛋白PDB-ID為6HUK,Ligand-ID為HOZ;GABRG2受體蛋白PDB-ID為6HUJ,Ligand-ID為NAG。使用分子對接模擬軟件Autodock_vina對GABRA1、GABRG2兩個靶點與10個核心活性成分及陽性對照藥物艾司唑侖進行分子對接驗證,計算活性成分、艾司唑侖與受體蛋白間的最低結合能。
表4為分子對接最低結合能計算結果,圖7為茯苓酸與兩種受體蛋白的分子對接可視化結果。表4結果表明所有活性成分與受體蛋白的最低結合能均遠小于-5.0 kJ/mol,結合圖7的分子對接可視化結果,可以說明,GABRA1、GABRG2兩個靶點能夠與活性成分自發結合并借助氫鍵等分子間作用力形成較為穩定的構象。
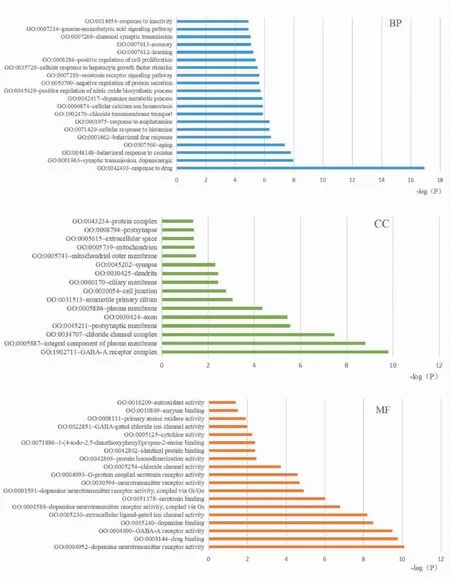
圖4 GO生物功能富集條形圖Fig.4 The bar chart of GO biological function enrichment
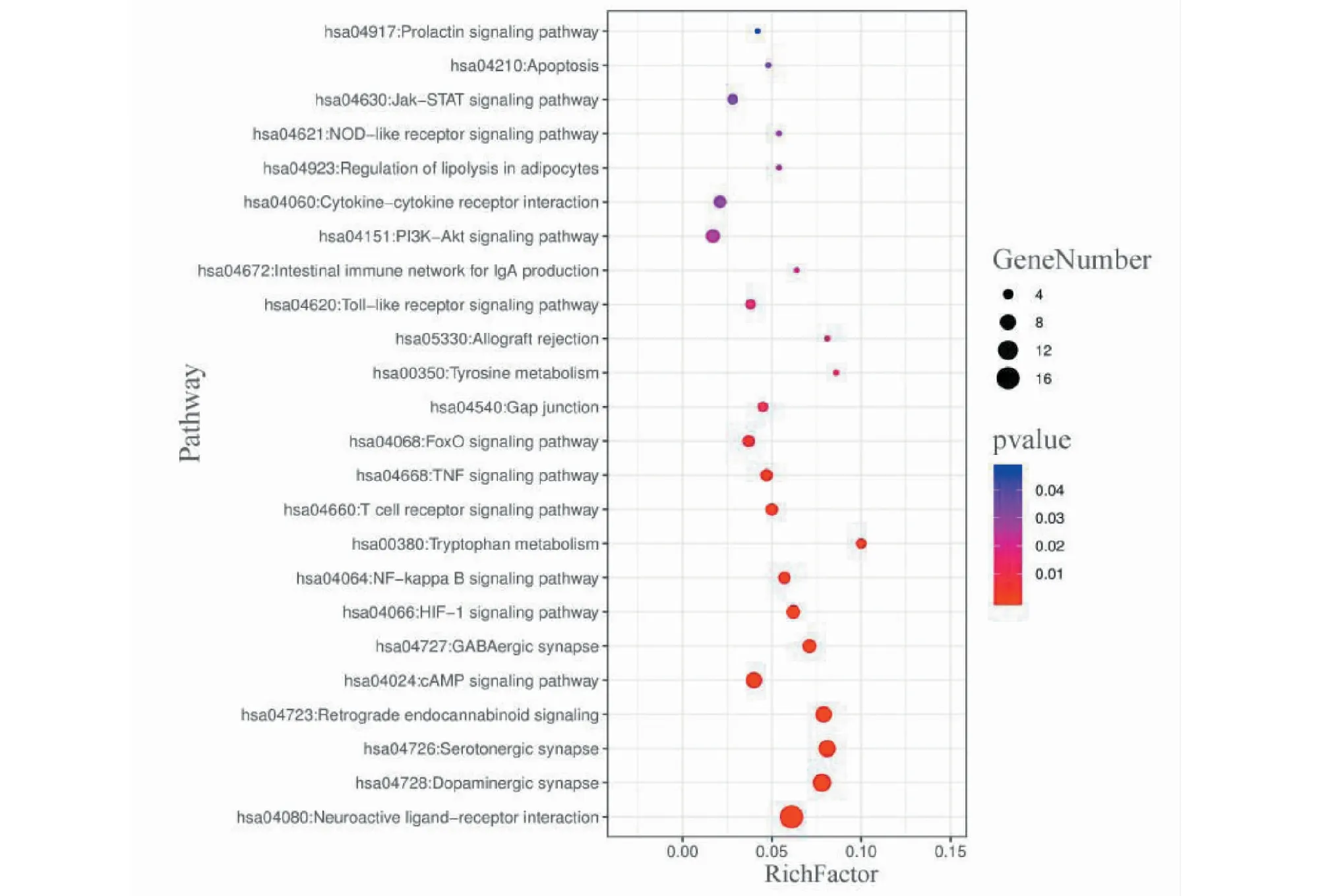
圖5 KEGG通路富集分析氣泡圖Fig.5 The bubble chart of KEGG pathway enrichment analysis
圖6 朱茯苓治療失眠的化合物-靶點-通路網絡Fig.6 The compound-target-pathway network of Zhufuling in the treatment of insomnia
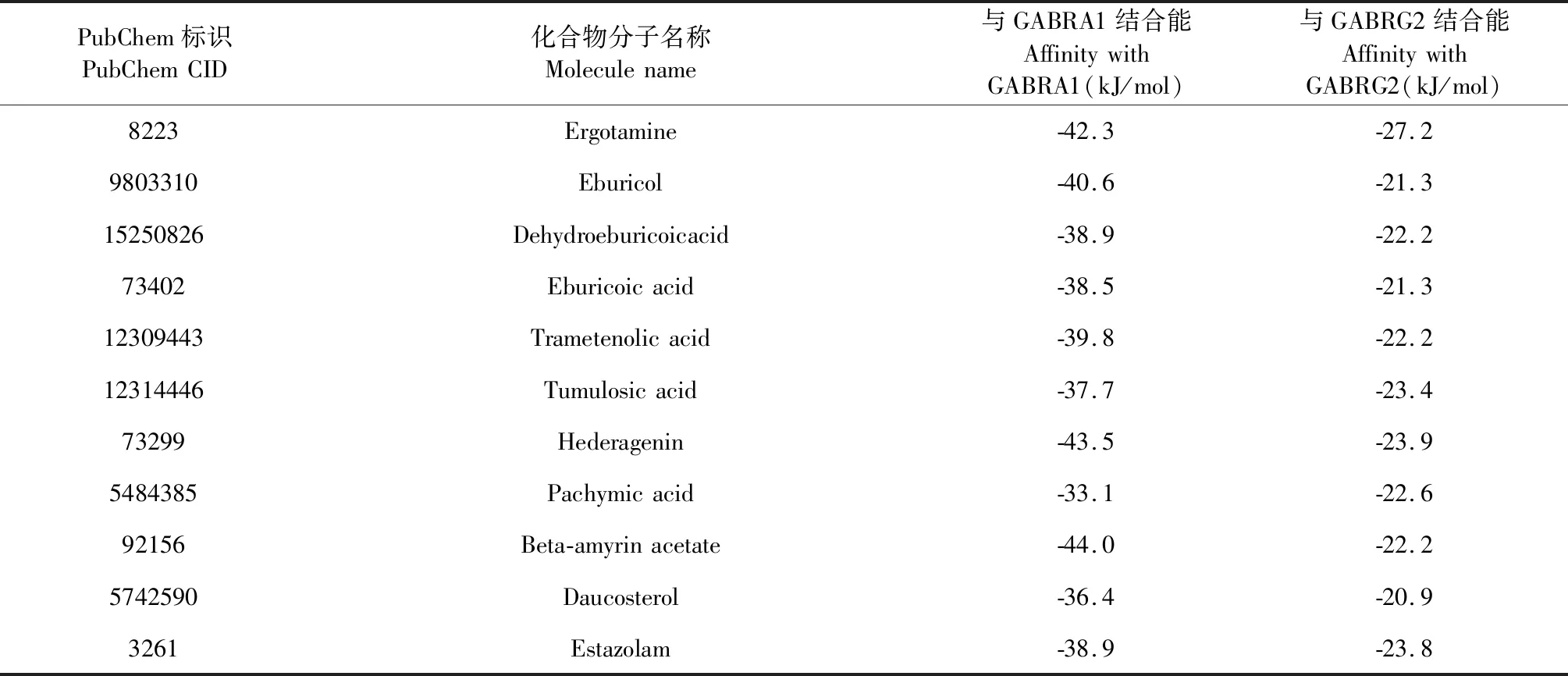
表4 活性成分與受體蛋白的最低結合能
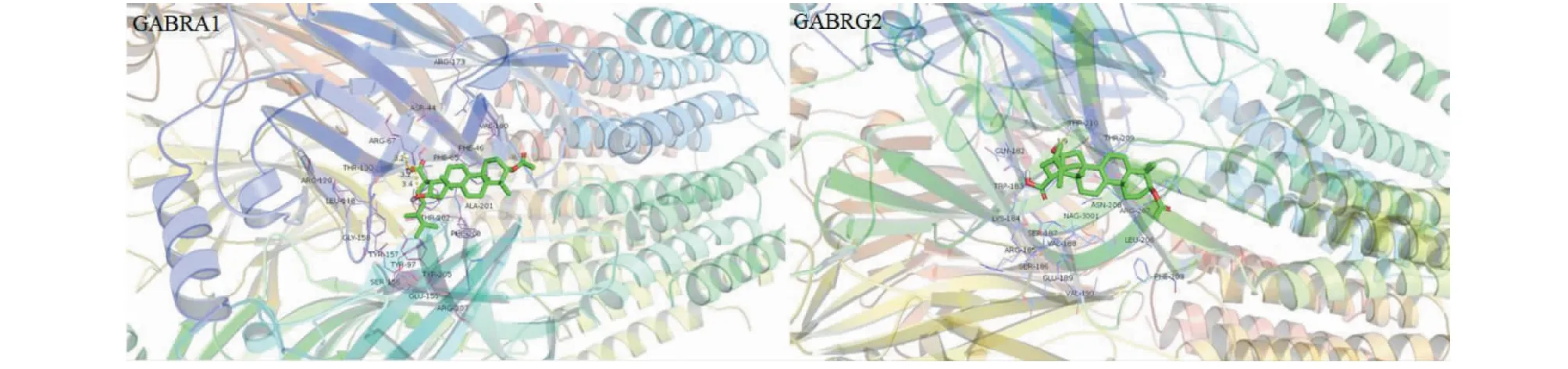
圖7 茯苓酸(5484385)與兩種受體蛋白的分子對接可視化結果Fig.7 The visualization results of molecular docking between pachymic acid (5484385) and two receptor proteins
2.8 朱茯苓對小鼠腦組織 GABRA1和GABRG2蛋白表達的影響
Western blot結果見圖8和圖9。與生理鹽水組比較,朱茯苓中、高劑量組小鼠腦組織中GABRA1和GABRG2蛋白表達明顯增加(P<0.01)可以說明朱茯苓在一定劑量時可以促進GABRA1和GABRG2蛋白的表達。

圖8 各組小鼠腦組織中GABRA1和GABRG2蛋白表達電泳Fig.8 The expression electrophoresis of GABRA1 and GABRG2 in brain tissue of mice in each group注:1~5分別為生理鹽水、艾司唑侖、朱茯苓水煎液低、中、高劑量組。Note:1-5 are saline,estazolam,Zhufuling water decoction low,medium and high dose groups,respectively.
3 討論
朱茯苓具有鎮靜安神的功效,是治療失眠不寐的常用中藥,臨床上應用廣泛且療效顯著。本研究基于多成分、多靶點作用的研究思路,應用網絡藥理學技術,分析朱茯苓治療失眠的靶點,闡述朱茯苓治療失眠的機制,為朱茯苓的實驗研究及臨床應用提供科學依據。
茯苓主要含三萜類和多糖類兩種化合物,此外還含有其他成分如甾體類、氨基酸、揮發油、膽堿、腺嘌呤及鉀鹽等微量元素[10]。在化合物-靶點網絡中高度值、含有多個作用靶點的核心活性成分多為三萜類化合物及其衍生物,如茯苓酸(5484385)、土莫酸(12314446)、齒孔酸(73402)、去氫齒孔酸(15250826)等。三萜類化合物具有廣泛的藥理活性,如利尿、抗氧化、抗腫瘤、抗炎、鎮靜等[11]。有研究表明,茯苓總三萜能對抗電休克及戊四唑驚厥發作,其機制與降低海馬區門冬氨酸(Asp)和谷氨酸(Glu)含量有關,具有鎮靜興奮性神經元和抗驚厥等作用[12]。Gao等[13]研究發現茯苓總三萜具有顯著的鎮靜作用,并能調節大腦中GABA和Glu的含量。朱砂是一種礦物藥,歸心經,中醫以其為安神要藥,臨床上主要用于失眠多夢,心悸易驚,小兒驚風等,具有解毒安神、清心鎮驚的功效,效果較好。Li等[14]對朱砂進行的研究結果顯示,朱砂的抗心律失常作用可能是其鎮心安神功效的主要基礎之一。朱砂含有HgS、MgS、Bi、Fe、Ba、Mn、Sb、As、Hg2+、HgCl2等[15],HgS 不溶于水,在機體內很難吸收,但它是朱砂的主要活性成分,可在人體內酸效應及絡合效應的作用下發生解離,并與體內的氨基酸等生物分子發生絡合反應后生成具有強烈生理活性及毒性較小的絡合物從而發揮藥效[16]。朱砂所含的可溶性汞鹽溶于水,游離汞和微量金屬元素不溶于水,朱砂的主要毒性成分是可溶性汞鹽[17],由于朱砂有毒,因此臨床上使用朱砂時一般需將其采用水飛法炮制后再使用,水飛可降低朱砂中的可溶性汞鹽含量,從而達到減毒增效的作用。朱茯苓,其實就是朱砂均勻拌于茯苓的表面而制得的,因此朱茯苓含有朱砂和茯苓兩種中藥,其中朱砂用量較少,因此筆者猜測朱茯苓發揮鎮靜安神作用的成分主要來源于茯苓,而朱砂可能是通過與茯苓相協同,達到增強寧心安神的效果。在進行網絡藥理學的研究時,朱茯苓同時具有朱砂和茯苓兩種中藥的化學成分,然而TCMID和BATMAN-TCM等數據庫中所對應的朱砂的成分只提供了HgS的信息,因此在活性成分的選擇上,選取了茯苓的比較常用的活性成分和朱砂中的主要成分HgS。在活性成分篩選時考慮活性成分的OB值和DL值,并結合文獻報道,納入某些OB和DL值很低但文獻報道其活性較好的活性成分。

圖9 朱茯苓水煎液不同劑量對小鼠腦組織GABRA1和GABRG2 蛋白表達的影響(n=3)Fig.9 Effect of Zhufuling decoction on protein expression of GABRA1 and GABRG2 in brain tissue of mice (n = 3)注:與生理鹽水組比較,**P<0.01。Note:Compared with the normal saline group,**P<0.01.
基于BioGPS數據庫進行的交集靶點器官定位分析結果顯示,朱茯苓主要通過作用于腦、心、肺、肝、淋巴等器官實現對失眠的干預效果。中醫認為腦為“元神之府”,主生命活動、精神意識及感覺運動,臟象學說將腦的生理病理統歸于心而分屬于五臟中。心為“君主之官”,主藏神,與腦協同作用調控人的精神、意識、思維等;主血脈,將血上供于腦,血足則腦髓充盈。心腦相通,則神志活動正常,睡眠良好。同時朱茯苓潛在靶點的多器官分布體現了中醫理論的整體觀,即各臟器間互相影響、互相聯系、協同作用,實現對整個機體的調節[18]。
利用Autodock_Vina對GABRA1和GABRG2兩個靶點與10個核心活性成分進行分子對接驗證,結果顯示上述兩個靶點的受體蛋白均能與核心活性成分較穩定的自發結合,而且大部分活性成分與靶點蛋白的最低結合能高于陽性對照的最低結合能。由此可以推測,朱茯苓可能通過茯苓酸等活性成分作用于GABA受體,從而達到治療失眠的效果。
在Western blot實驗驗證部分結果顯示,相對于空白組,艾司唑侖組、朱茯苓中、高劑量組小鼠腦組織中GABRA1和GABRG2蛋白表達明顯增加(P<0.01),說明朱茯苓能夠提高腦內GABRA1和GABRG2兩種受體蛋白的表達,證實了朱茯苓是通過對GABRA1、GABRG2兩個核心靶點的基因及蛋白的直接作用,從而發揮其藥理作用的。同時,Shah等[19]的研究發現,茯苓酸可通過介導GABA能系統增強戊巴比妥的催眠作用,茯苓酸可以改變GABA-A受體各亞基的水平從而達到鎮靜催眠的效果,與Western blot實驗結果共同印證了分子對接結果的合理性。
GO功能和KEGG通路富集分析結果中,GABA信號通路、5-HT信號通路、5-HT神經突觸、GABA受體神經突觸、DA突觸傳遞等條目P值較小且富集基因較多。GABA是一種抑制性神經遞質,具有催眠、鎮靜和抗焦慮等功能。GABA的調控通過GABA受體發揮作用,α1與β2和γ2組成的GABA-A受體亞型在腦內數量最多,約占全部GABA-A受體的43%[20]。Jiang等[21]發現內因性失眠癥患者中樞重要的抑制性神經遞質GABA顯著降低。Winkelman等[22]從質子磁共振譜得出,原發性失眠患者GABA水平較對照組低30%。大多數鎮靜催眠藥物共有的主要藥理作用機制是通過神經遞質GABA或通過刺激GABA-A受體、抑制5-HT的1A受體發揮鎮靜作用,GABRA等基因所參與的神經活性配體-受體相互作用通路與神經遞質的傳遞在失眠的治療過程中發揮著重要的作用[23]。5-HT和DA是大腦內單胺類神經遞質,5-HT的各受體亞型具有調節睡眠、覺醒周期的作用,激動突觸前5-HT1A自身受體,可延長慢波睡眠,減少覺醒;激動突觸后5-HT1A受體,可抑制睡眠并促進覺醒[24]。DA起著維持覺醒和行為興奮的作用。當各種原因使其維持覺醒和行為興奮的作用受到抑制時,亦可影響睡眠、覺醒周期。相關研究證明[25],失眠患者的5-HT、DA水平與健康人群存在明顯差異,而通過藥物改善患者的5-HT、DA水平,可以有效地改善患者的失眠癥狀。由此可見,朱茯苓對GABA、5-HT和DA等神經遞質的調節可能是朱茯苓治療失眠的重要機制。
綜上所述,本研究應用網絡藥理學方法對朱茯苓治療失眠的靶點進行了分析,對36個交集靶點進行了器官定位分析,對GABRA1和GABRG2兩個靶點進行了分子對接模擬,驗證了GABA能系統機制的重要作用及核心活性成分篩選的合理性,為實驗驗證提供依據。化合物-靶點-通路網絡體現了朱茯苓多成分、多靶點、多途徑的作用特點。富集分析結果提示GABA信號通路、5-HT信號通路、DA突觸傳遞等通路和生物過程的重要作用。本研究為朱茯苓治療失眠機制的進一步研究提供了新思路和新方法,為朱茯苓的臨床應用提供了科學依據。

