過氧化氫誘導介孔CeO2的合成及對酸性橙7有機染料的吸附研究
楊承偉,何 倩,葉大偉,錢珍妮,翁郭鎣,金芷如,徐要輝,b*
(樂山師范學院 a.電子與材料工程學院;b.功能材料實驗室,四川 樂山 614000)
0 引言
目前,水體污染是世界十大環境問題之一,水作為生命之源,它的污染嚴重威脅著生物體的健康和生命。由造紙、紡織和皮革等行業排放的污水中含有大量的有機染料,是目前重要的污染源之一,其中,偶氮染料廢水的排放量占所有染料廢水總排放量的70%左右,這些染料廢水一般具有毒性,具有致癌的風險,且很難被生物降解[1]。近年來,國內外研究者一直致力于偶氮染料的處理,發展了不同的凈化方法,例如膜分離法[2]、催化降解法[3]、生物降解法[4]和超聲波氣振技術[5]等。其中,吸附法由于具有工序簡單,成本低和效率高等特點,被廣泛應用于有機染料廢水的處理,而具有孔結構和高比表面積的吸附劑更是備受青睞[6]。
二氧化鈰(CeO2)作為一種重要的稀土氧化物,在催化劑、固體氧化物燃料電池、氧氣傳感器以及污水治理等方面具有廣泛的應用[7-10]。與塊狀CeO2相比,具有介孔結構的CeO2擁有豐富、有序的孔道結構,因此具有更高的比表面積,在實際應用中可以大大優化和改善其使用性能。目前,制備介孔CeO2的方法主要是模板法,即采用多孔二氧化硅(SiO2)等作為硬模板或者采用表面活性劑(例如CTAB、P123等)作為軟模板,首先合成模板劑與鈰化合物的復合物前驅體,之后通過物理或化學方法去除模板劑,最終再經熱處理工藝得到具有介孔結構的CeO2[11-14]。模板法雖然可以制備性能優異的介孔CeO2,但通常會采用有機危險試劑(如丙酮)、酸或堿試劑、高溫焙燒等去除模板劑,繼而增加了介孔CeO2的制備成本,同時容易造成二次環境污染。因此,發展一種低成本、環境友好型工藝制備介孔CeO2是當前研究的重要內容。
因此,本論文提供了一種在不添加模板劑的條件下制備介孔CeO2粉末的思路,運用溫和的濕法化學法,以Ce(NO3)3·6H2O、(NH4)2CO3、H2O2和H2O為原料,在室溫下合成了具有高比表面積的介孔CeO2粉末,避免了模板劑的使用以及高溫焙燒等工序,大大縮短了了實驗流程、降低了實驗成本、減少了能耗。同時,考察了所得介孔CeO2產品對酸性橙7偶氮染料的吸附效果。
1 實驗
1.1 實驗試劑
六水合硝酸鈰(Ce(NO3)3·6H2O,99.95%)和碳酸銨((NH4)CO3,AR)分別購買于上海阿拉丁生化科技股份有限公司和上海麥克林生化科技公司,過氧化氫(H2O2,30 wt.%)和無水乙醇(≥99.7%)均購買于成都市科隆化學品有限公司,酸性橙7(AO7,>97.0%)購買于梯希愛上海化成工業發展有限公司。此外,實驗過程中均采用蒸餾水作為溶劑,同時蒸餾水還用于試劑的溶解以及樣品的洗滌等。
1.2 樣品合成
以Ce(NO3)3·6H2O作為鈰源,以(NH4)2CO3作為沉淀劑,以蒸餾水作為溶劑,采用化學沉淀法首先合成鈰的前驅體,之后添加不同濃度的H2O2作為氧化劑,用于實現鈰前驅體向CeO2的物相轉變。具體操作如下:室溫下,將10 mL (NH4)2CO3水溶液(0.6 mol/L)滴加到正在攪拌的20 mL Ce(NO3)3·6H2O水溶液(0.2 mol/L)中,溶液中立即產生白色沉淀。用濃度為30 wt.%的H2O2配置成體積為12 mL、濃度為5~30 wt.%的H2O2水溶液。將不同濃度的H2O2水溶液滴入到上述正在攪拌的白色懸浮液沉淀中,白色沉淀立即轉為橘黃色,繼續攪拌反應5 min,之后靜置6 h。最后,用蒸餾水和無水乙醇洗滌數遍,在80 ℃下干燥24 h后得到淡黃色的CeO2粉末。
1.3 表征
采用X射線衍射儀(XRD,DX-2700)對所得樣品進行物相分析,射線源為Cu靶的K射線,管電壓為30 kV,管電流為25 mA;采用掃描電子顯微鏡(SEM,JSM-7500)觀察所得樣品的形貌和尺寸;采用比表面積與孔隙度分析儀(ASAP 2460)對CeO2的比表面積、孔徑和孔容進行分析。
1.4 吸附性能測試
以AO7染料為吸附對象考察所得介孔CeO2樣品的吸附性能。具體操作如下:室溫下,將0.2 g CeO2粉末加入到100 mL 140 mg/L的AO7水溶液中,并進行震蕩(速度為200 rpm)。分別在10、30、60和120 min時取樣,并立刻離心并取上清液。使用U-3900型紫外分光光度計測量上清液在吸收波長為484 nm處的吸光度A,并通過公式(1)計算CeO2在t時刻對AO7染料的吸附率(%)。注:吸附實驗的所有操作均在避光的條件下進行。
(1)
其中,A0為初始AO7水溶液的吸光度,At為吸附反應t時刻時AO7水溶液的吸光度(t= 0、10、30、60和120 min)。
2 結果及討論
2.1 物相分析
采用XRD技術表征所得樣品的物相結構。圖1是在室溫條件下將(NH4)2CO3水溶液添加到Ce(NO3)3·6H2O水溶液后所得鈰前驅體的XRD圖譜。從圖1中可以看出,其物相結構主要為Ce2(CO3)3·8H2O(JCPDS No. 38-0377)。此外,從XRD圖譜中還可以看出,Ce2(CO3)3·8H2O物相的特征峰強度高,且峰形尖銳,根據布拉格方程可知,只有滿足衍射條件的晶面才能參加X射線的衍射,參加衍射的晶粒數目越多其特征衍射峰也就越強,所以前驅體樣品中的Ce2(CO3)3·8H2O的結晶度是比較高的。
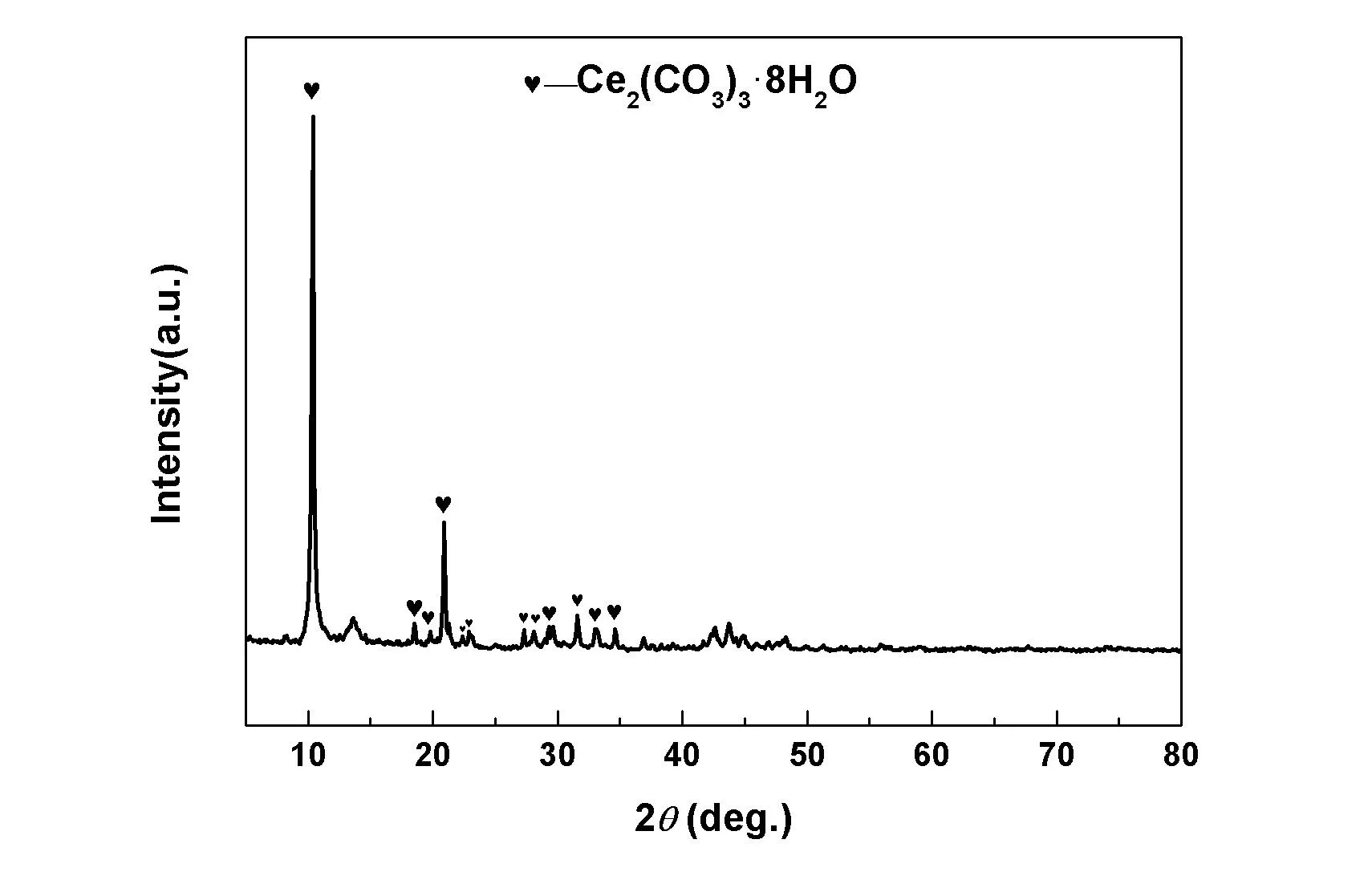
圖1 室溫下(NH4)2CO3添加到Ce(NO3)3·6H2O后所得鈰前驅體的XRD圖譜
圖2是向Ce2(CO3)3·8H2O的懸浮液中添加不同濃度的H2O2后所得一系列樣品的XRD圖譜。從圖2中可以看出,所有樣品的XRD圖譜均在2θ約為28、47和56位置處出現了三個明顯的衍射峰,對應的物相為立方螢石結構的CeO2(JCPDS No. 34-0394),相應的晶面分別為(111)、(220)和(311)。此外,在圖2的XRD圖譜中并沒有出現其它物相的衍射峰,如Ce2(CO3)3·8H2O,表明Ce2(CO3)3·8H2O前驅體在H2O2氧化劑的作用下已經完全轉變為了CeO2,所得樣品的純度較高。從圖2中可以明顯的看出,隨著H2O2溶液濃度的增加,所得CeO2樣品的特征衍射峰出現了寬化現象,XRD衍射峰的寬化現象是由于樣品的晶粒尺寸變小、晶格畸變增大而導致的。所以,H2O2溶液的濃度在此實驗中對于CeO2樣品的晶粒尺寸具有一定的影響。
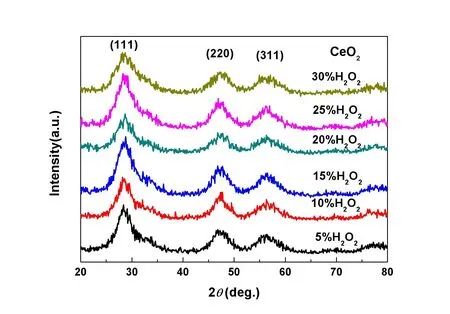
圖2 室溫下向Ce2(CO3)3·8H2O的懸浮液中引入不同濃度H2O2溶液后所得樣品的XRD圖譜Fig. 2 XRD Patterns of CeO2 Samples Obtained Following the Addition of H2O2 with Different Concentrations to Ce2(CO3)3·8H2O Suspension at Room Temperature
2.2 吸附性能分析
圖3是向Ce2(CO3)3·8H2O的懸浮液中引入不同濃度H2O2溶液(5~30%)后所得CeO2樣品對AO7染料隨時間變化的吸附率。從圖3中可以看出,除了H2O2濃度為5%時所得CeO2樣品外,其他CeO2樣品在吸附反應開始的10 min內對AO7染料的吸附較快,隨后繼續延長時間,對AO7的吸附逐漸變慢,并且在60 min時逐漸趨于平衡,表明吸附達到飽和,其吸附率均接近100 %。此外,CeO2樣品對AO7的吸附率從H2O2濃度為5%到10%有很明顯的提升,并且在H2O2濃度為15%時所得CeO2樣品對AO7的吸附率達到最大,隨后繼續增加H2O2的濃度,所得CeO2樣品對AO7的最終吸附率相差不大,但吸附相對較為緩慢,這可能是因為H2O2的濃度在15%時對CeO2的顆粒度和孔道尺寸方面的調控達到了最優。

注:CeO2吸附劑的濃度:1.0 g/L;AO7的初始濃度:140 mg/L;溶液的體積:100 mL;攪拌速度:200 rpm;反應溫度:室溫;光照條件:避光。
2.3 形貌分析
采用SEM技術觀察CeO2樣品的微觀形貌和尺寸。圖4是使用H2O2溶液濃度為15%時所制備CeO2粉末的SEM圖片。從圖4中可以看出,CeO2樣品的形貌是由許多細小的類球形顆粒組成的團聚體,顆粒尺寸大小均勻,且處于納米級別。

圖4 H2O2溶液濃度為15%時所得CeO2粉末的SEM圖片
2.4 孔結構及比表面積分析
采用N2吸附-脫附實驗表征CeO2樣品的孔結構以及比表面積。圖5是向Ce2(CO3)3·8H2O懸浮液中添加15% H2O2后所得CeO2樣品的N2吸附-脫附曲線。從圖5中可以看出,CeO2樣品的N2吸附-脫附曲線在相對壓力范圍為P/P0= 0.7~1.0區間出現了滯后回線,屬于典型的II型等溫線,表明所得CeO2樣品為介孔材料[15]。采用Brunauer-Emmett-Teller方法計算CeO2樣品的比表面積,其值高達130.0 m2/g。此外,采用Barret-Joyner-Halenda方法計算CeO2樣品的孔徑和孔容,其值分別為7.70 nm和0.2598 cm3/g。
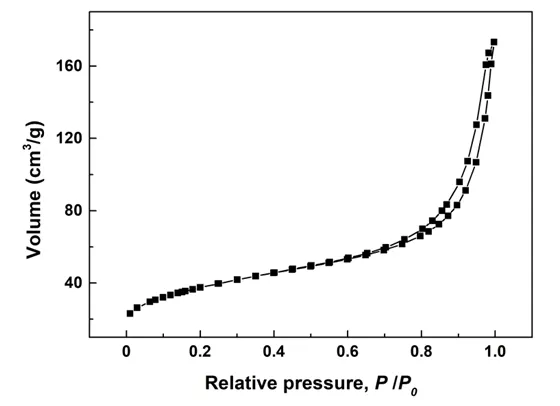
圖5 H2O2溶液濃度為15%時所得CeO2粉末的N2吸附-脫附曲線
表1給出了最近幾年采用模板法合成介孔CeO2的相關報道,包括模板劑的種類、模板劑的去除工藝和比表面積的大小。從表1中可以看出,PEO、CTAB和Pluronic-P-123等表面活性劑是常用的軟模版劑,需要采用熱處理的方式(即焙燒工藝)去除軟模版劑,焙燒溫度范圍為400~600C,焙燒時間為2~4 h。而具有多孔結構的二氧化硅(SiO2)是常用的硬模板劑,需要采用NaOH溶液溶解和去除模板劑,同時也需要采用焙燒的方式實現前驅體向CeO2的物相轉變或者提高CeO2樣品的結晶度焙燒溫度范圍為400~600C,焙燒時間為4~6 h。在本論文的工作中,所得介孔CeO2的比表面積為130.0 m2/g,通過對比表1中介孔CeO2的比表面積可以發現,本論文所提供的方法制備得到的介孔CeO2的比表面積處于中上水平。但從制備工藝和成本上分析,本論文中制備介孔CeO2的方法更具優勢:首先,不添加任何軟/硬模板劑,從而避免了模板劑的去除工藝;其次,未使用焙燒工藝,大大減少了能耗;最后,操作簡單、條件溫和、成本低。因此,我們在本論文中提供的制備介孔CeO2的方法具有很大的發展空間,有望實現批量生產。

表1 采用模板法合成介孔CeO2的最新報道
3 結論
在不添加模板劑的前提下,室溫下采用溫和的濕法化學法合成了具有介孔結構的CeO2粉末。實驗流程主要分為兩個步驟:首先,以Ce(NO3)3·6H2O為鈰源,(NH4)2CO3為沉淀劑,水為溶劑,運用化學沉淀法合成Ce2(CO3)3·8H2O前驅體;之后引入H2O2作為氧化劑,用以實現Ce2(CO3)3·8H2O前驅體向CeO2的物相轉變。所得介孔CeO2對AO7偶氮染料展現出了優良的吸附性能,當H2O2的濃度為10 wt.%以上時所合成的CeO2樣品,在吸附反應為60 min時可將初始濃度為140 mg/L的AO7溶液幾乎完全吸附。N2吸附-脫附實驗表明,H2O2的濃度為15 wt.%時所得到的CeO2樣品具有介孔結構,其比表面積高達130.0 m2/g,孔徑為7.70 nm,孔容為0.2598 cm3/g。最重要的是,本論文提供的制備介孔CeO2的思路可以拓展至制備其他介孔金屬氧化物材料,為介孔氧化物材料的制備提供了一種新思路。

