離子交換法脫除磷酸中錳離子的動態吸附研究
莊海波,楊 林,鄧 強,葉潤州,吳趙敏
(四川大學化學工程學院,四川成都610065)
磷酸是重要的化工原料,其廣泛應用于肥料、食品、制藥、農藥等領域[1]。磷酸的生產工藝主要有熱法磷酸和濕法磷酸。熱法磷酸工藝雖可制得高純度的磷酸,但其對磷礦的品位要求較高,且同時存在著電能耗量大、生產成本高和環境污染嚴重等缺點[2]。在磷礦資源逐漸貧化的背景下,濕法磷酸工藝逐漸成為工業磷酸生產的主流工藝,因為其不僅可以有效利用中低品位磷礦,而且有著能耗低、工藝簡單、生產成本低、環境污染小等優點[3]。然而,中國的中低品位磷礦資源以膠磷礦為主[4],膠磷礦中夾雜著許多雜質伴生礦物,浮選富集時并不能將其與磷灰石完全分離,在酸解槽中雜質礦物也會參與酸解反應,使得鐵鋁鎂錳[5-8]等金屬離子混入到濕法磷酸產品中,導致磷酸產品的濃度和品質降低。因此,在濕法磷酸用于下游磷化工產品的生產前,必須對其中的雜質離子進行凈化處理。
近年來,濕法磷酸的凈化方法主要有化學沉淀法[9]、溶劑萃取法[10]、濃縮結晶法[11]、乳化液膜法[12]、離子交換法[13-15]等,但這些方法都各自存在缺陷,例如化學沉淀法凈化程度較低,溶劑萃取法處理成本較高,濃縮結晶法生產速度慢,乳化液膜法液膜穩定性弱,離子交換法有待充分研究。離子交換法目前雖存在脫除對象局限于金屬陽離子和樹脂用量規模大等缺點,雖然其具有操作簡單便捷、反應速度快、環保、耗能低和磷酸產品純度高等眾多優點,但其在濕法磷酸凈化領域的應用和凈化效果還有待發展和提高。國內外已有一些學者采用離子交換樹脂對磷酸中鐵、鋁、鎂等金屬離子展開脫除凈化研究,而利用離子交換樹脂對磷酸中錳離子的脫除研究還未見報道。因此,本文采用離子交換技術脫除磷酸中的錳離子,系統地研究了進液流量、磷酸溶液初始錳濃度、體系溫度等對錳離子吸附效果的影響,以期為離子交換技術在濕法磷酸凈化領域的研究和應用提供理論依據和實踐指導。
1 實驗部分
1.1 實驗原料和儀器
試劑:磷酸(H3PO4)、硫酸(H2SO4)、硝酸(HNO3)、一水硫酸錳(MnSO4·H2O),以上試劑均為分析純。本文使用的含錳磷酸溶液使用磷酸、一水硫酸錳和去離子水配制。陽離子交換樹脂Sinco-430,其基本性質如表1 所示。
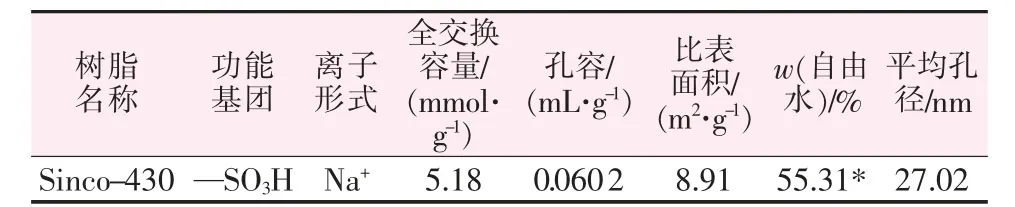
表1 陽離子交換樹脂Sinco-430 的基本性質
儀器:DJ-2002 型電子天平;SHB-III 型循環水真空泵;UPH-I-100L 型超純水儀;BT100-1F 型蠕動泵;Optima 7000DV 型電感耦合等離子體發射光譜儀;DHG-9070A 型電熱恒溫鼓風干燥箱;DF-101S 型集熱式恒溫磁力攪拌器。
1.2 實驗方法
以陽離子交換樹脂Sinco-430 為填料,將其裝填于內徑為20 mm 和高度為300 mm 的離子交換柱(有機玻璃材質)中。在實驗前使用去離子水充分浸濕床體內離子交換樹脂,而后用蠕動泵輸送磷酸溶液自下而上通過離子交換柱,測定不同時刻流出液中的錳離子濃度,動態吸附實驗裝置如圖1 所示。
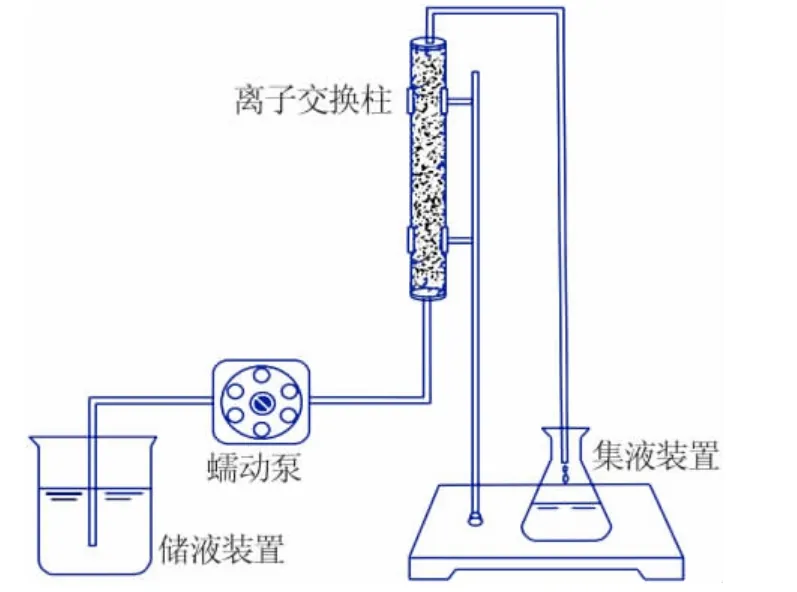
圖1 動態吸附實驗裝置示意圖
進液流量對吸附效果的影響: 溫度T 為20 ℃,磷酸溶液的初始錳質量濃度C0為10.22 mg/mL,磷酸溶液P2O5質量分數為20%,進液流量q 分別設定為2.5、4.0、5.0 mL/min,實驗開始后特定時間移取流出液并測定錳質量濃度Ct,直至流出液的錳濃度與原料液相同時為止,實驗結束后以Ct/C0對t 作圖,制作出不同進液流量下的動態吸附曲線。
初始錳濃度對吸附效果的影響:溫度T 為20 ℃,進液流量q 為4.0 mL/min,磷酸溶液的P2O5質量分數為20%,溶液初始錳質量濃度C0分別設定為7.60、10.22、12.78 mg/mL,實驗開始后特定時間移取流出液并測定錳質量濃度Ct,直至流出液的錳濃度與原料液相同時為止,實驗結束后以Ct/C0對t 作圖,制作出不同初始錳濃度下的動態吸附曲線。
溫度對吸附效果的影響:進液流量q 為4.0 mL/min,磷酸溶液的P2O5質量分數為20%,溶液的初始錳質量濃度C0為10.22 mg/mL,溫度T 分別設定為20、35、50 ℃,實驗開始后特定時間移取流出液并測定錳質量濃度Ct,直至流出液的錳濃度與原料液相同時為止,實驗結束后以Ct/C0對t 作圖,制作出不同溫度下的動態吸附曲線。
1.3 分析方法
本論文磷酸溶液中的錳濃度均采用電感耦合等離子體發射光譜儀(ICP-OES)測定。實驗中溶液的錳濃度測定步驟如下:1)精確量取10 μL 溶液樣品于20 mL 樣品瓶中,加入15 mL 質量分數為2%的硝酸溶液,搖勻;2)上機進行ICP-OES 檢測,得到測試結果為X。若含錳磷酸溶液的密度為ρ(g/mL),則原溶液中錳質量濃度C(mg/L)和錳質量分數w(%)分別為:


1.4 動態吸附曲線參數計算
圖2 中動態吸附曲線將矩形區域一分為二,左邊空白區域表示樹脂對磷酸中錳離子的吸附容量,右邊為動態吸附曲線與橫軸Ct/C0=0 之間的陰影區域。曲線下的陰影區域面積Aa、實驗吸附容量Qe,exp以及吸附率Y 可分別用式(3)、(4)和(5)計算:
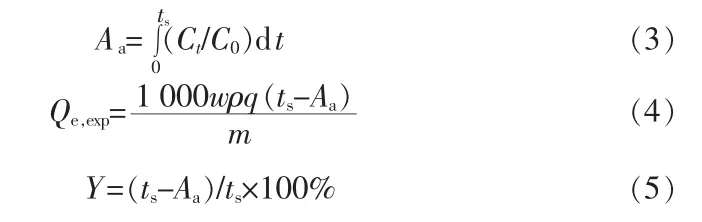
式中:w 是原料液的錳質量分數,%;ρ為原料液的密度,g/cm3;q為原料液的進液流量,mL/min;ts為樹脂吸附飽和的時間,min;m為填充樹脂的質量,g;Qe,exp為動態吸附實驗的實際吸附量,mg/g;Y為樹脂對錳的吸附率,%。
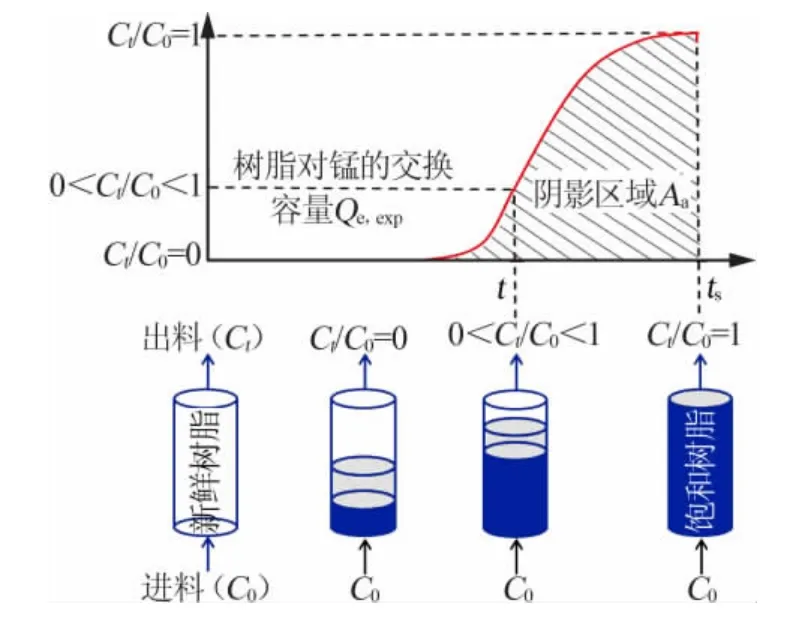
圖2 動態吸附曲線與過程示意圖
1.5 動態吸附模型
本文采用Thomas 模型、Yoon-Nelson 模型和Yan 模型[16-18]模擬樹脂對磷酸中錳離子吸附過程,3 種動態吸附模型的方程式見(6)、(7)、(8),式(9)為Yan 模型理論飽和吸附量計算式。
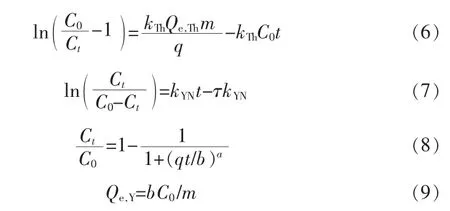
式中:Ct為流出液的錳離子質量濃度,mg/mL;C0為原料液的錳離子質量濃度,mg/mL;kTh為Thomas 模型速率常數,mL/(min·mg);m 為交換柱裝填樹脂質量,g;q為原料液進液流量,mL/min;Qe,Th為平衡時樹脂飽和吸附容量,mg/g;t為動態脫附時間,min;kYN為Yoon-Nelson 模 型 吸 附 反 應 速 率 常 數,1/min;τ為50%吸附劑穿透所需時間,min;a 和b(mL)為Yan模型參數;Qe,Y為Yan 模型理論計算的飽和吸附量,mg/g。
2 結果與討論
2.1 工藝條件對錳離子吸附效果的影響2.1.1 進液流量對錳離子吸附效果的影響
不同進液流量下的實驗特征參數列于表2,相應的動態吸附曲線如圖3 所示。隨著磷酸溶液進液流量的增加,離子交換樹脂床層被完全飽和的時間逐漸縮短。當進液流量為2.5、4.0、5.0 mL/min 時,離子交換柱床層的飽和時間分別為80、64、52 min,這是因為當溶液初始錳濃度相同時,增大進液流量時單位時間內流過樹脂床層的錳離子質量也隨之增大,使得樹脂達到飽和的時間縮短。此外,本文發現原料液進液流量增大時,圖3 中動態吸附曲線的斜率增大,這是因為在較高的進液流量下,樹脂表面的液膜變薄,導致液膜擴散阻力減小,所以吸附速率有所增大。

表2 不同進液流量下樹脂對錳離子吸附效果的特征參數
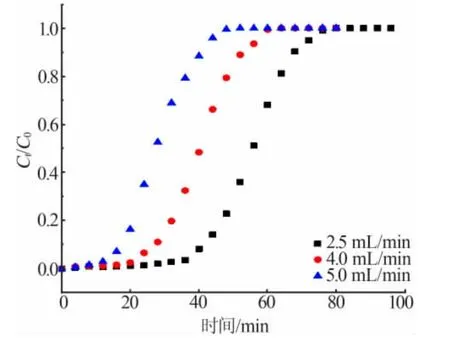
圖3 不同進液流量下樹脂對磷酸中錳離子的動態吸附曲線
進液流量分別為2.5、4.0、5.0 mL/min 時,實驗平衡吸附量分別為56.50、65.69、67.94 mg/g。樹脂總吸附量先增大后減小,這是因為進液流量的增大,一方面減小了液膜擴散阻力,造成吸附速率增大,導致總吸附量增大; 另一方面,樹脂與溶液的接觸時間縮短,導致吸附劑與磷酸溶液之間未能有效接觸,繼而樹脂的吸附效果減弱,導致樹脂總吸附量減小。此外,當進液流量從2.5 mL/min 增大到5.0 mL/min時,樹脂的總吸附效率從68.57%降低到54.02%,這是因為隨著原料液進液流量的增大,含錳磷酸溶液的滯留時間減少,錳離子與吸附劑的接觸時間較短,樹脂不能及時吸附流過離子交換柱的錳離子,所以體系的平衡吸附效率Y 逐漸降低。因此,在較低的進液流量下,離子交換柱對錳離子的吸附效率更高,綜合考慮吸附效率與吸附速率,4.0 mL/min 為適宜的進液流量。
2.1.2 溶液初始錳濃度對錳離子吸附效果的影響
不同初始錳濃度下的實驗特征參數列于表3,相應的動態吸附曲線如圖4 所示。隨著磷酸溶液初始錳濃度的增加,圖4 中的動態吸附曲線逐漸左移,離子交換樹脂床層被完全飽和的時間逐漸縮短。當溶液錳離子質量濃度為7.60、10.22、12.78 mg/mL時,交換柱樹脂的飽和時間分別為80、64、60 min,這是因為隨著溶液初始錳濃度的增大,單位時間內流入離子交換柱內的錳離子質量增大,同時交換柱內錳離子濃度梯度也增大,這使得錳離子傳質系數增大,因此樹脂對錳的吸附速率增大。
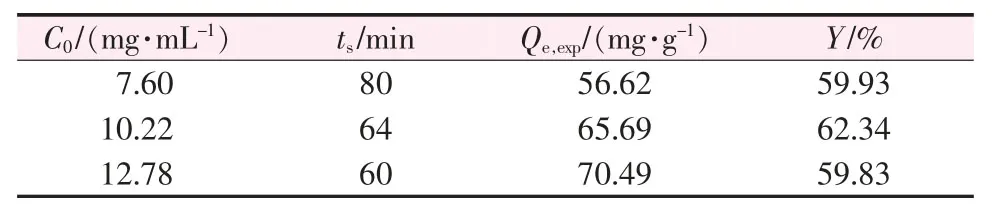
表3 不同初始錳濃度下樹脂對錳離子吸附效果的特征參數
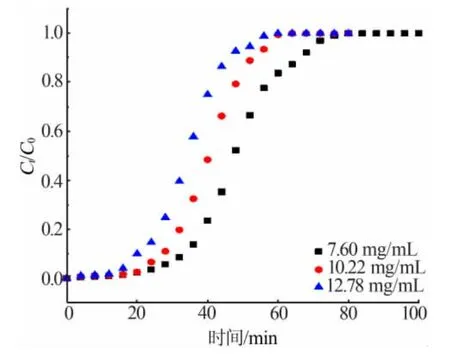
圖4 不同初始錳濃度下樹脂對磷酸中錳離子的動態吸附曲線
隨著原料液初始錳濃度的增大,錳離子進入樹脂內部孔道的傳質推動力也增大,故而溶液初始錳質量濃度從7.60 mg/mL 增加到12.78 mg/mL 時,樹脂的總吸附量從56.62 mg/g 增加到70.49 mg/g。溶液中錳離子濃度梯度的增大加快了樹脂對錳離子的吸附速率,故而樹脂的飽和時間ts隨溶液初始錳濃度增大而逐漸縮短。另外,本文發現隨著溶液初始錳濃度的增大,樹脂的總吸附效率先增大后減小,這是因為溶液初始錳濃度較低時達到的平衡狀態下,樹脂內部尚且還存在著可用的交換位點,而隨著溶液初始錳濃度的增大,樹脂內剩余的可用交換位點被逐漸占據,溶液中過量的錳離子無法被樹脂吸附固定,因而樹脂的吸附效率先增大后降低。
2.1.3 溫度對錳離子脫除效果的影響
不同溫度下的實驗特征參數列于表4,相應的動態吸附曲線見圖5。從表4 可以發現:隨著體系溫度的升高,樹脂達到飽和狀態的時間逐漸縮短。溫度為20、35、50 ℃時,樹脂達到飽和狀態的時間分別為64、62、60 min,這是因為隨著體系溫度的升高,一方面溶液的黏度也隨之減小,這增大了錳離子向樹脂內部孔道的擴散速率;另一方面吸附為吸熱反應,升高溫度使平衡向錳離子被吸附的方向移動,這也增大了體系的吸附速率,因此樹脂達到飽和的時間縮短。此外,由于吸附反應速率的提高,在相同的初始錳濃度和進液流量條件下,樹脂吸附率也自然隨著溫度提高而增大,分別為62.34%、63.55%、63.70%。此外,隨著體系溫度的升高,樹脂的平衡吸附量逐漸減小,可能是因為溫度的升高縮短了樹脂達到吸附平衡的時間,減少了進入交換柱內的錳離子質量,盡管溫度的升高增大了吸附效率。綜合考慮樹脂的吸附率和平衡吸附量,35 ℃為適宜的溫度條件。

表4 不同溫度下樹脂對錳離子吸附效果的特征參數
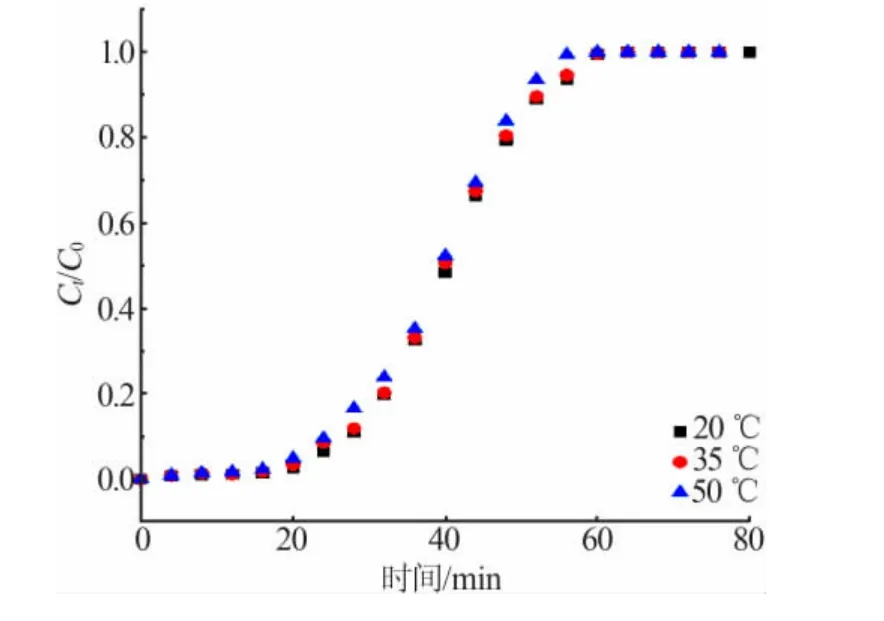
圖5 不同溫度下樹脂吸附錳離子的動態吸附曲線
2.2 動態吸附模型的擬合計算
2.2.1 Thomas 模型的擬合計算
由表5(Thomas 模型參數)可以發現:隨著原料液進液流量的增大和溫度的升高,反映吸附速度快慢的Thomas 模型速率常數kTh逐步增大,這是因為流量增大導致液膜擴散阻力減小,同時單位時間內流經交換柱的錳離子量也增大,因而樹脂對錳離子的吸附速率增大。體系溫度升高一方面降低了磷酸溶液的黏度,減小了錳離子向樹脂內部孔道擴散的阻力,另一方面使得吸附反應平衡向錳離子被吸附的方向移動,所以速率常數kTh隨溫度升高而增大。然而,隨著原料液濃度的增大,速率常數kTh逐漸減小,這意味著在低濃度下較慢的擴散轉移能增強樹脂的吸附能力。由Thomas 模型計算得到的樹脂平衡吸附量Qe,Th與實驗平衡吸附量Qe,exp相近,偏差介于4.92%~13.31%。另外,Thomas 模型的線性相關系數R2介于0.951 8~0.992 7,表明Thomas 模型與不同實驗條件下的吸附實驗數據均較為契合,亦即ln(C0/Ct-1)與t 之間有著顯著的線性相關性。
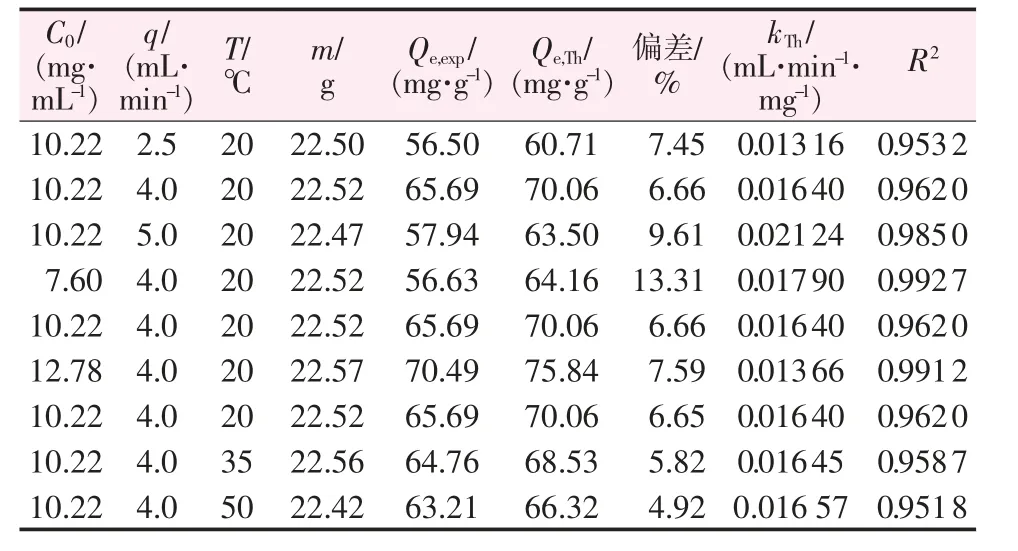
表5 不同實驗條件下樹脂對磷酸中錳離子動態吸附的Thomas 模型參數
2.2.2 Yoon-Nelson 模型擬合計算
表6 列出了Yoon-Nelson 模型的相關參數,由表6 可知,隨著進液流量、溶液初始錳濃度和體系溫度的增大,吸附反應速率常數kYN均隨之增大,增大的原因參見Thomas 模型反應速率常數。由Yoon-Nelson 模型參數計算得到的τcal與實驗實際值τexp均列于表6,其偏差值介于5.66%~12.73%。此外,Yoon-Nelson 模型的線性相關系數R2介于0.927~0.993,表明ln[Ct/(C0-Ct)]與t 之間存在較為顯著的線性相關性。
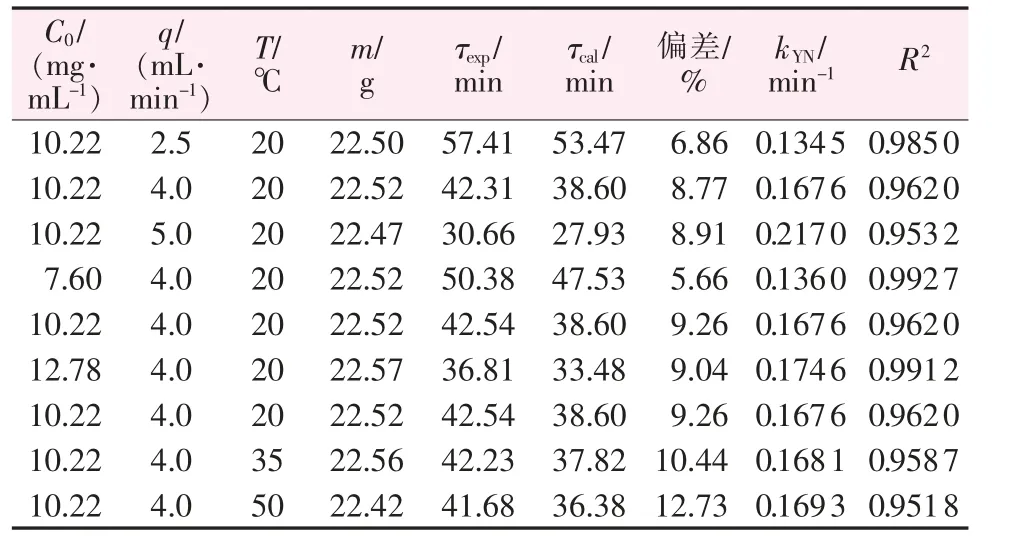
表6 不同條件下樹脂對磷酸中錳離子動態吸附的Yoon-Nelson 模型參數
2.2.3 Yan 模型擬合計算
Yan 模型的相關參數均列于表7。從表7 可知:Yan 模型計算而得的樹脂平衡吸附容量Qe,Y與實際實驗值Qe,exp比較契合,最大偏差值不超過12.76%,表明Yan 模型對本實驗體系具有較好的預測和指導能力。此外,Yan 模型的線性相關系數R2介于0.993 4~0.998 6,均要高于Thomas 模型和Yoon-Nelson 模型,表明Yan 模型與吸附實驗數據之間相關性顯著,可用于描述和預測本實驗體系下樹脂對錳離子的動態吸附行為。
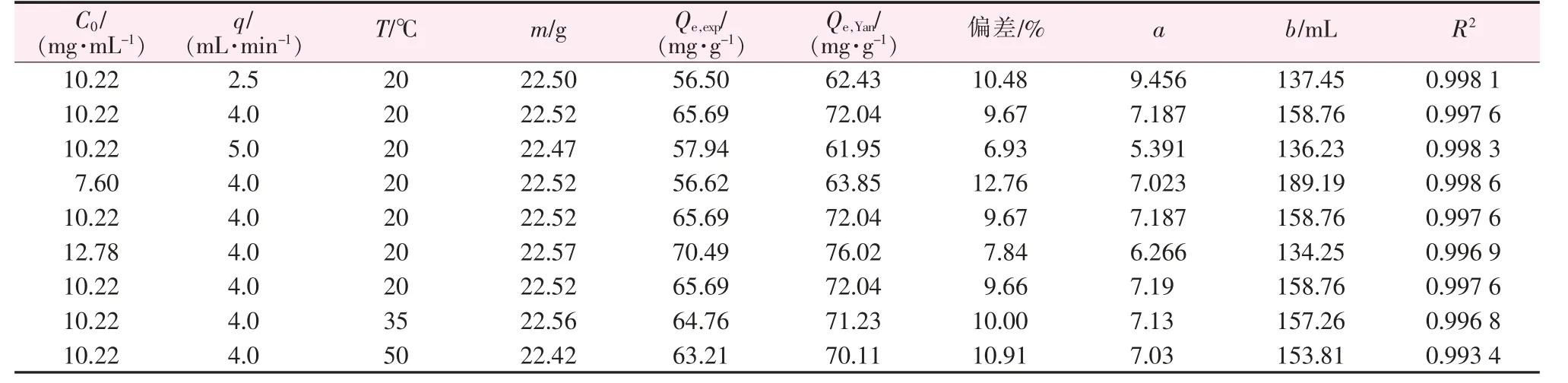
表7 不同條件下樹脂對磷酸中錳離子動態吸附的Yan 模型參數
綜合考慮上述3 種動態吸附模型,Yan 模型的計算參數值Qe,Y與實際實驗值Qe,exp非常接近,而且Yan 模型的線性相關系數均大于0.993 4,遠高于Thomas 和Yoon-Nelson 模型,因此Yan 模型最適合于描述本吸附實驗的數據。
3 結論
本文采用動態吸附的實驗方法,研究了進液流量、溶液初始錳濃度、溫度等因素對磷酸溶液中錳離子吸附效果的影響,并且采用了3 種不同的動態吸附模型對實驗數據進行了擬合研究,得到了如下結論:1)增大進液流量、提高溶液初始錳濃度及升高溫度均有利于縮短樹脂飽和時間,但進液流量的增大會降低樹脂的吸附率,而溫度的升高則會降低樹脂的飽和吸附量。2)在進液流量為4.0 mL/min、溶液初始錳質量濃度為10.22 mg/mL、體系溫度為35 ℃條件下,樹脂對錳離子的飽和吸附量為64.76 mg/g,吸附效率為63.55%。3)采用Thomas、Yoon-Nelson 和Yan 3 種吸附模型對動態吸附過程數據進行擬合,發現Yan 模型的擬合效果優于Thomas 和Yoon-Nelson 模型,其擬合相關系數R2均在0.993 以上,而且由其計算得出的平衡吸附量與實驗測定值的相對偏差僅為6.93%~10.91%。

