新生兒耐碳青霉烯類腸桿菌感染影響因素
許 渝,黃硯屏,羅萬軍
(華中科技大學同濟醫(yī)學院附屬武漢兒童醫(yī)院/武漢市婦幼保健院 1. 醫(yī)院感染管理辦公室; 2. 新生兒內科,湖北 武漢 430016)
近年來,耐碳青霉烯類腸桿菌科細菌(carbape-nem-resistant Enterobacteriaceae, CRE)感染有增多趨勢,CRE對臨床上應用的絕大多數(shù)抗菌藥物耐藥,治療困難,易在醫(yī)院內造成傳播,甚至引起醫(yī)院感染暴發(fā)。新生兒抵抗力低下、生理功能不完善,很多抗菌藥物不適宜使用,CRE感染的治療較大齡兒童及成人面臨更大的挑戰(zhàn)。現(xiàn)分析武漢兒童醫(yī)院2016—2018年新生兒病區(qū)CRE感染特征及危險因素,為新生兒CRE感染防控和抗菌藥物合理使用提供依據。
1 對象與方法
1.1 研究對象 收集武漢兒童醫(yī)院2016年1月1日—2018年12月31日新生兒病區(qū)確診為CRE感染的68例新生兒(CRE組),隨機選取同期同病房碳青霉烯類敏感腸桿科細菌(carbapenem-sensitive Enterobacteriaceae, CSE)感染的50例新生兒(CSE組)進行回顧性病例對照研究。
1.2 細菌鑒定及儀器 所有菌株均采用德國布魯克RapifleX MALDI typer飛行質譜儀進行細菌鑒定,法國生物梅里埃細菌鑒定及藥敏系統(tǒng)進行細菌鑒定及藥敏測試。判定標準及結果解釋參照美國臨床實驗室標準化協(xié)會(CLSI)2016年版規(guī)則。
1.3 CRE感染病例的診斷 院感科工作人員和臨床醫(yī)生根據病原學檢驗結果,結合新生兒臨床表現(xiàn),參考2011年《醫(yī)療機構耐藥菌MDR、XDR、PDR的國際標準化定義專家建議(草案)》進行CRE感染病例的判斷。參照2001年衛(wèi)生部批準頒發(fā)的《醫(yī)院感染診斷標準(試行)》[1],由院感科工作人員和臨床醫(yī)生共同判定是醫(yī)院感染還是社區(qū)感染。

2 結果
2.1 CRE感染菌種及感染部位 新生兒病區(qū)2016—2018年確診新生兒CRE感染68例,其中肺炎克雷伯菌感染60例(88.24%),大腸埃希菌感染7例(10.29%),產酸肺炎克雷伯菌感染1例(1.47%)。CSE感染50例,其中肺炎克雷伯菌感染29例(58.0%),大腸埃希菌感染21例(42.0%)。CRE組醫(yī)院感染38例(55.88%),CSE組醫(yī)院感染6例(12.00%),兩組比較,差異有統(tǒng)計學意義(P<0.05)。兩組新生兒均以下呼吸道感染為主,感染部位構成比較,差異無統(tǒng)計學意義(χ2=2.178,P=0.795),見表1。

表1 新生兒CRE和CSE感染部位比較
2.2 CRE感染單因素分析 單因素分析結果顯示,出生胎齡、出生體重、新生兒呼吸窘迫綜合征、氣管插管、機械通氣日數(shù)、PICC置管史、抗菌藥物使用時間、抗菌藥物使用種類≥3種、碳青霉烯類藥物使用史、糖皮質激素藥物使用史、住院時間各組比較,差異有統(tǒng)計學意義(均P<0.05),見表2、3。

表2 新生兒CRE感染單因素分析(計數(shù)資料)
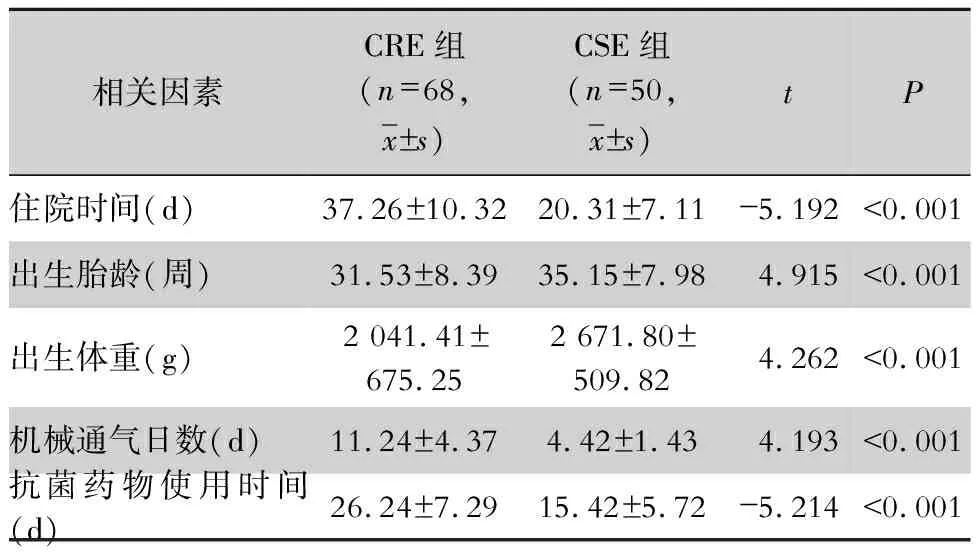
表3 新生兒CRE感染單因素分析(計量資料)
2.3 CRE感染多因素logistic回歸分析 將單因素分析中有統(tǒng)計學意義的變量納入多因素logistic回歸分析,結果顯示,低出生體重、機械通氣日數(shù)、碳青霉烯類藥物使用史是CRE感染的獨立相關因素(均P<0.05)。出生體重OR值<1,說明隨著出生體重增加,CRE感染風險下降。機械通氣日數(shù)、碳青霉烯類藥物使用史OR值>1,說明隨著機械通氣日數(shù)增加,或使用碳青霉烯類藥物,CRE感染風險增加。見表4、5。

表4 新生兒CRE感染相關變量賦值表

表5 新生兒CRE感染多因素logistic回歸分析
3 討論
近年來,隨著碳青霉烯類抗生素在臨床上廣泛使用,腸桿菌科細菌對碳青霉烯類耐藥率呈逐年上升趨勢[2-3]。CHINET中國細菌耐藥性監(jiān)測顯示,2017年肺炎克雷伯菌對碳青霉烯類藥物的耐藥率較2005年上升幅度高達8倍[3]。CRE的耐藥基因可在菌種間快速傳播,造成醫(yī)院感染的暴發(fā)與流行[4]。一項對住院患兒30 d死亡率風險分析的多中心研究發(fā)現(xiàn),CRE患兒的死亡率是碳青霉烯敏感腸桿菌感染患兒的6倍[5]。CRE感染率的不斷攀升,給兒童醫(yī)院感染控制提出了嚴峻的考驗。
新生兒抵抗力低下、生理功能不完善,抗菌藥物選擇范圍窄,碳青霉烯類抗生素使用率高,為CRE感染的高危人群,據郭燕等[6]報道,新生兒期CRE的檢出率最高。兒童CRE菌株主要為克雷伯菌屬,其次為大腸埃希菌等[6]。本研究顯示,CRE感染菌株中肺炎克雷伯菌占88.24%,大腸埃希菌占10.29%,與上述報道相符。新生兒CRE醫(yī)院感染發(fā)生率高于CSE,CRE主要為醫(yī)院感染,而CSE主要為社區(qū)感染。CRE可以通過克隆方式在種屬細菌間進行耐藥基因的快速傳播,并可通過共用醫(yī)療設備、手等進行接觸傳播[7],因此,CRE易發(fā)生醫(yī)院感染。
本研究顯示,小胎齡、低出生體重為新生兒感染CRE的危險因素,其中低出生體重為獨立的危險因素。小胎齡、低出生體重較足月、正常出生體重新生兒發(fā)育不成熟,免疫力低,容易合并新生兒呼吸窘迫綜合征等各種并發(fā)癥,常需進行各種侵入性操作,易長期暴露于各種抗菌藥物,均有可能誘發(fā)CRE感染。產碳青霉烯酶是腸桿菌科細菌對碳青霉烯類抗生素耐藥的主要機制之一,NDM-1酶是一種常見的碳青霉烯酶,該菌株具有克隆多樣性。研究[8]表明,低出生體重的新生兒攜帶NDM-1 CRE引起的敗血癥發(fā)生率顯著較高。
抗菌藥物使用時間、抗菌藥物使用種類≥3種、使用碳青霉烯類藥物為新生兒感染CRE的危險因素,其中使用碳青霉烯類抗生素為獨立的危險因素,與相關報道[9-10]一致。Pannaraj等[11]報道,抗菌藥物長期使用與兒童CRE感染相關性最大。長期廣譜抗菌藥物的使用常導致菌群失調,改變機體正常菌群,增加CRE等耐藥菌定植機會。CRE定植患者有10%~30%概率發(fā)生感染,同時CRE定植者也是潛在播散者[12]。另有研究[13]顯示,抗菌藥物使用種類較多是發(fā)生多重耐藥菌定植的主要危險因素之一。據報道,除了碳青霉烯類藥物,第三代頭孢菌素或氨基糖苷類治療亦可能會促進CRE定植或感染[14-15]。
氣管插管、PICC置管術、留置胃管等侵入性操作為新生兒感染CRE的危險因素,其中機械通氣時間為獨立的危險因素。侵入性操作破壞了新生兒的生理學防御屏障,有利于病原微生物的入侵,增加了CRE醫(yī)院感染的風險。本研究結果顯示,新生兒CRE感染以下呼吸道感染為主,常需機械通氣治療,而呼吸機管道易污染,導致CRE定植。呼吸機回氣口等醫(yī)療器材表面CRE檢出率達10%,醫(yī)療器材是CRE交叉?zhèn)鞑サ闹匾橘|[16]。
新生兒CRE易發(fā)生醫(yī)院感染,對臨床常用抗菌藥物高度耐藥,治療難度大。應針對危險因素,盡量減少侵入性操作,合理應用抗菌藥物,對高危新生兒進行定植篩查,積極采取綜合性的感染防控策略,以有效預防和控制新生兒CRE感染和傳播。

