高暴露(001)面BiOBr/Ti3C2復合光催化劑的制備及其可見光催化性能
李志鋒,譚 杰,楊曉飛,藺祖弘,郇正來,張婷婷,2
(1. 北京化工大學 化學工程學院,北京 100029; 2. 北京市環境污染控制與資源化工程研究中心,北京 100029)
TiO2具有物理和化學性質穩定、光催化活性高、無毒及成本低等優點,得到了廣泛研究[1-2]。但是,TiO2禁帶寬度為3.2 eV,屬于寬帶隙半導體,只能吸收占太陽光譜5%的紫外光,極大地限制了其實際應用[3]。因此,開發具有優異可見光催化活性的光催化劑逐漸成為研究熱點。
近年來,BiOBr可見光催化劑逐漸引起關注,它具有正方氟氯鉛礦結構,屬于四方晶系[4]。鉍氧層([Bi2O2]2+)和鹵素層(X-)的交替排列,具有開放式的晶體結構和間接躍遷的帶隙結構,這種獨特的結構性質使光生電子-空穴對可以得到有效分離,從而提高BiOBr的光催化活性[5-6]。BiOBr具有合適的帶隙寬度和可見光響應能力[7],但是對可見光利用率有限,光生載流子的分離效率還有待提高[8]。為此,研究者分別從形貌調控、晶面調控、引入助催化劑和構建異質結體系等方面進行了大量的改性研究[8-11],以提高BiOBr的可見光催化活性。
Ti3C2是一種新型二維過渡金屬碳化物,具有良好的導電性、優異的化學結構穩定性和親水性,得到了催化領域研究者的廣泛關注,被大量應用于與其他半導體光催化劑復合構建異質結來提高催化活性。密度泛函理論計算表明Ti3C2具有突出的金屬導電性[12],在與其他半導體界面的連接處易形成肖特基勢壘,內建電場的產生有效地改善了光催化劑光生電子-空穴對的分離,從而提高其催化活性[13]。Peng等[14]以Ti3C2作為鈦源,通過水熱法原位生長具有高暴露(001)面的TiO2,界面肖特基結的形成改善了TiO2對甲基橙染料的降解效果。Cai等[15]通過靜電自組裝方法合成了Ag3PO4/Ti3C2肖特基結光催化劑,與Ag3PO4/RGO和Ag3PO4光催化劑相比,Ag3PO4/Ti3C2光催化劑降解2,4-二硝基苯酚的表觀速率分別提高了1.5和9倍。近期,也有少量研究表明,通過BiOBr和Ti3C2復合催化劑的構建,可以提升BiOBr對有機污染物的光催化降解速率及產氫效率[16-18]。由此可見,Ti3C2作為助催化劑具有較好的應用前景,但還未見高暴露(001)面BiOBr與Ti3C2復合催化劑的改性研究報道。
本研究通過簡易水解法合成具有高暴露(001)面的BiOBr/Ti3C2復合光催化劑,通過引入不同量Ti3C2確定最佳復合比例,采用多種表征手段對催化劑結構和光學特性進行分析,最后通過對羅丹明B染料廢水的降解和循環實驗來評價催化劑的性能和穩定性。
1 實驗方法
1.1 原料與試劑
五水硝酸鉍、溴化鉀、羅丹明B、氫氟酸、對苯醌、草酸銨均購自阿拉丁生化科技股份有限公司,異丙醇購自麥克林生化科技股份有限公司,Ti3AlC2購自吉林11科技有限公司。藥品均為分析純,使用過程中不需要進一步提純。實驗用水為去離子水。
1.2 材料制備
1.2.1 Ti3C2的制備
通過HF刻蝕Ti3AlC2制備層狀Ti3C2納米片:將1.0 g Ti3AlC2粉末置于氫氟酸(30 mL,49wt%)溶液中,二者混合后在35 ℃下連續攪拌24 h,然后用去離子水反復洗滌混合溶液至中性,并離心收集層狀Ti3C2粉末,最后在60 ℃下真空干燥12 h備用。
1.2.2 高暴露和非高暴露(001)面BiOBr的制備
首先將1.0 mmol KBr溶解于15 mL去離子水中,得到A溶液,然后將1.0 mmol Bi(NO3)3·5H2O分散于15 mL無水乙醇中,超聲分散得到B懸浮液。A溶液加熱至90 ℃時,將上述B溶液滴入A溶液中,攪拌均勻后在90 ℃反應3 h。反應結束后冷卻至室溫,過濾收集BiOBr,然后在70 ℃下真空干燥10 h,制得高暴露(001)面BiOBr,記為BiOBr。
將15 mL無水乙醇換為15 mL去離子水,按同樣步驟制得非高暴露(001)面BiOBr,記為FBiOBr。
1.2.3 高暴露和非高暴露(001)面BiOBr/Ti3C2的制備
首先將一定量層狀Ti3C2分散于上述A溶液中,加熱至90 ℃時,將B溶液滴入A溶液,在90 ℃下反應3 h。反應結束后冷卻至室溫,過濾收集BiOBr/Ti3C2復合物,然后在70 ℃下真空干燥10 h。制得的高暴露(001)面BiOBr/Ti3C2復合光催化劑,按層狀Ti3C2添加量的不同(10.0wt%、20.0wt%、30.0wt%)分別記為BT-10、BT-20、BT-30。
按照上述步驟制備非高暴露(001)面BiOBr/Ti3C2復合光催化劑,層狀Ti3C2添加量為20.0wt%的記為FBT-20。
1.3 材料表征
采用X射線衍射儀(D8 Advance,德國Bruker-AXS公司)對粉末材料的晶體物相進行表征,靶源為Cu Kα射線,波長λ為0.15406 nm,測試電壓為40.0 kV、電流為40.0 mA,掃描范圍為5°~90°。通過X射線光電子能譜儀(ESCALAB 250XI,美國賽默飛公司)測定樣品的化學組成,以C1s位于284.8 eV處的表面污染碳作為結合能的校正基準。采用掃描電子顯微鏡(Gemini SEM 300/VP,德國卡爾蔡司公司)、透射電子顯微鏡(JEM-2010,日本電子)和能譜儀(EDS)表征樣品的微觀形貌和元素組成。利用紫外-可見漫反射光譜儀(UV-3600,日本島津公司)獲取樣品光學性質,以BaSO4作為參比。利用熒光光度計(F-7000,日本日立公司)測試樣品的發光性能,激發波長為350 nm。
1.4 光催化性能實驗
通過在可見光照射條件下降解羅丹明B(RhB)溶液來測定光催化劑的光催化活性。將50.0 mg的樣品分散于100 mL 20 mg/L的RhB溶液中,在避光條件下攪拌60 min以達到吸附-解吸平衡。可見光源為500 W的氙燈,并用濾光片濾去波長小于420 nm的光。在光照條件下,每間隔15 min取5 mL上清液,在RhB的最大吸收波長554 nm處測定吸光度,然后通過朗伯-比爾公式計算RhB的降解率:
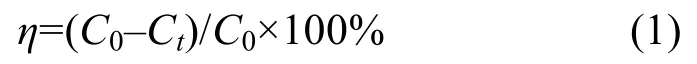
其中:η為降解率;C0為暗吸附平衡后RhB溶液的吸光度;Ct為某時刻光照反應后RhB溶液的吸光度。
2 結果與討論
2.1 表征結果
2.1.1 XRD分析
通過XRD分析樣品的晶體結構,從圖1中可見,MAX相Ti3AlC2在2θ=39.05°處出現的較強衍射峰[19],對應Ti3AlC2的(104)晶面,經過HF刻蝕之后,(104)晶面衍射峰完全消失,位于2θ=9.32°處的(002)晶面衍射峰和2θ=19.07°的(004)晶面衍射峰加寬并向低角度移動,表明刻蝕后的Ti3AlC2成功去除了夾層Al,并且完成了向層狀Ti3C2的轉變[20]。由圖1(a)可知,BiOBr和FBiOBr具有窄而尖的衍射峰,表明樣品的結晶性較好,且所有衍射峰與四方相BiOBr的衍射峰(JCPDS 09-0393)一致。另外,BiOBr樣品的(001)晶面衍射峰強度明顯強于FBiOBr,表明其具有高暴露的(001)晶面[21]。與其它晶面相比,(001)晶面具有較高的表面能及較強的終端氧原子密度,能呈現出更好的電荷轉移能力和催化活性[22]。BT-x和FBT-20復合催化劑都顯示出BiOBr 的特征峰,但未出現Ti3C2的特征峰,這是因為與BiOBr相比,Ti3C2結晶性較差,特征峰衍射強度較低。
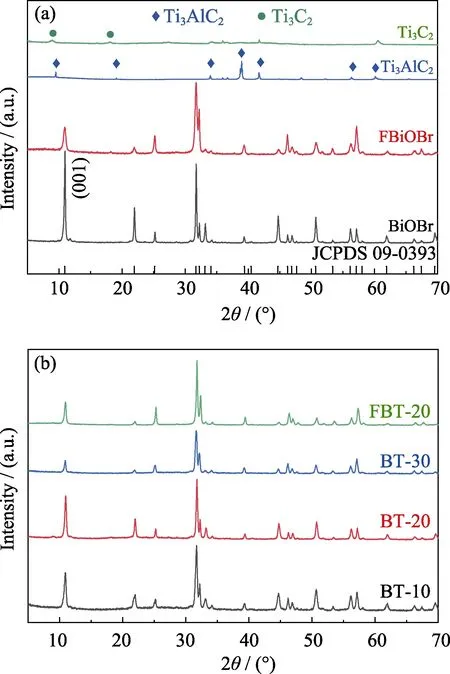
圖1 Ti3C2,Ti3AlC2,FBiOBr,BiOBr(a)和FBT-20,BT-x(b)樣品的XRD圖譜Fig. 1 XRD patterns of samples Ti3C2,Ti3AlC2,FBiOBr,BiOBr (a) and samples FBT-20,BT-x (b)
2.1.2 SEM和EDS分析
采用SEM觀察BiOBr、Ti3C2和BT-20樣品的形貌。從圖2(a,b)中可以看出,BiOBr樣品呈二維薄片狀,堆疊生長,尺寸約為0.3~2.0 μm; Ti3C2則呈典型的手風琴結構。圖2(c,d)直觀地呈現了BiOBr與Ti3C2的復合情況,可以看到BiOBr堆疊生長于Ti3C2表面兩側,與Ti3C2表面緊密結合。Ti3C2為良好的導電體[12],可以為電子傳遞提供良好的通道,有利于BiOBr的光生載流子的轉移,促進光生電子-空穴對的分離[15]。由圖2(e)所示,通過EDS對BT-20樣品進行元素掃描,發現C、O、Ti、Br和Bi 元素均勻分布,進一步表明實驗成功制備了BiOBr/Ti3C2復合光催化劑。
2.1.3 TEM/HRTEM分析
采用TEM/HRTEM進一步研究BiOBr的微觀結構。圖3(a)為BiOBr的TEM照片,可以看出BiOBr的厚度較薄,呈現薄片狀。由圖3(b)的HRTEM照片可以清晰地看到,兩組晶面間距為0.277 nm的晶格條紋相互垂直,分別對應BiOBr的(110)和面。由圖3(c)的選區電子衍射(SAED)可知,(110)和(200)面成45°夾角,該角度值與BiOBr的晶面角理論值相符。因此BiOBr片層表面垂直方向為[001]晶軸方向,納米片的上下表面為(001)晶面,側面為(110)和晶面(圖3(d))[23]。晶體在生長過程中總是趨于降低晶體的總表面能,因此納米片會盡量地隱藏高表面能的晶面來獲得總表面能較低的晶體結構[24]。對于具有高暴露(001)晶面的BiOBr納米片樣品來說,(001)高能晶面傾向于堆疊來減少它的暴露,這與SEM的分析結果一致。
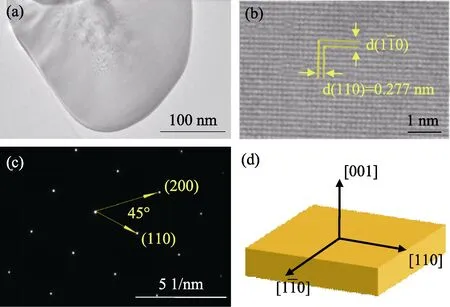
圖3 BiOBr樣品的TEM照片(a),HRTEM照片(b),SAED圖案(c)以及晶體生長方向機理圖(d)Fig. 3 TEM/HRTEM images (a-b),SAED pattern (c) and schematic illustrations of crystal orientation (d) of BiOBr sample
2.1.4 XPS分析
圖4為BiOBr和BT-20樣品的XPS圖譜,由BT-20的XPS全譜圖可以清晰地觀察到存在Br、O、Bi和Ti元素,這與EDS結果一致。與BiOBr相比,BT-20的Br2d、Bi4f、O1s的出峰位置所對應的結合能有所增大,這可能是由于引入高導電性Ti3C2導致BiOBr周圍的電荷密度降低,從而增強了復合催化劑表面的結合能[13]。當Ti3C2與BiOBr接觸后,光生電子的轉移路徑從BiOBr導帶處轉移至Ti3C2表面,促進界面肖特基結能壘的形成,進一步在BiOBr與Ti3C2的界面間形成內建電場,定向轉移光生電子,有效地抑制光生載流子的復合,從而提高了光催化劑的光催化活性[25]。
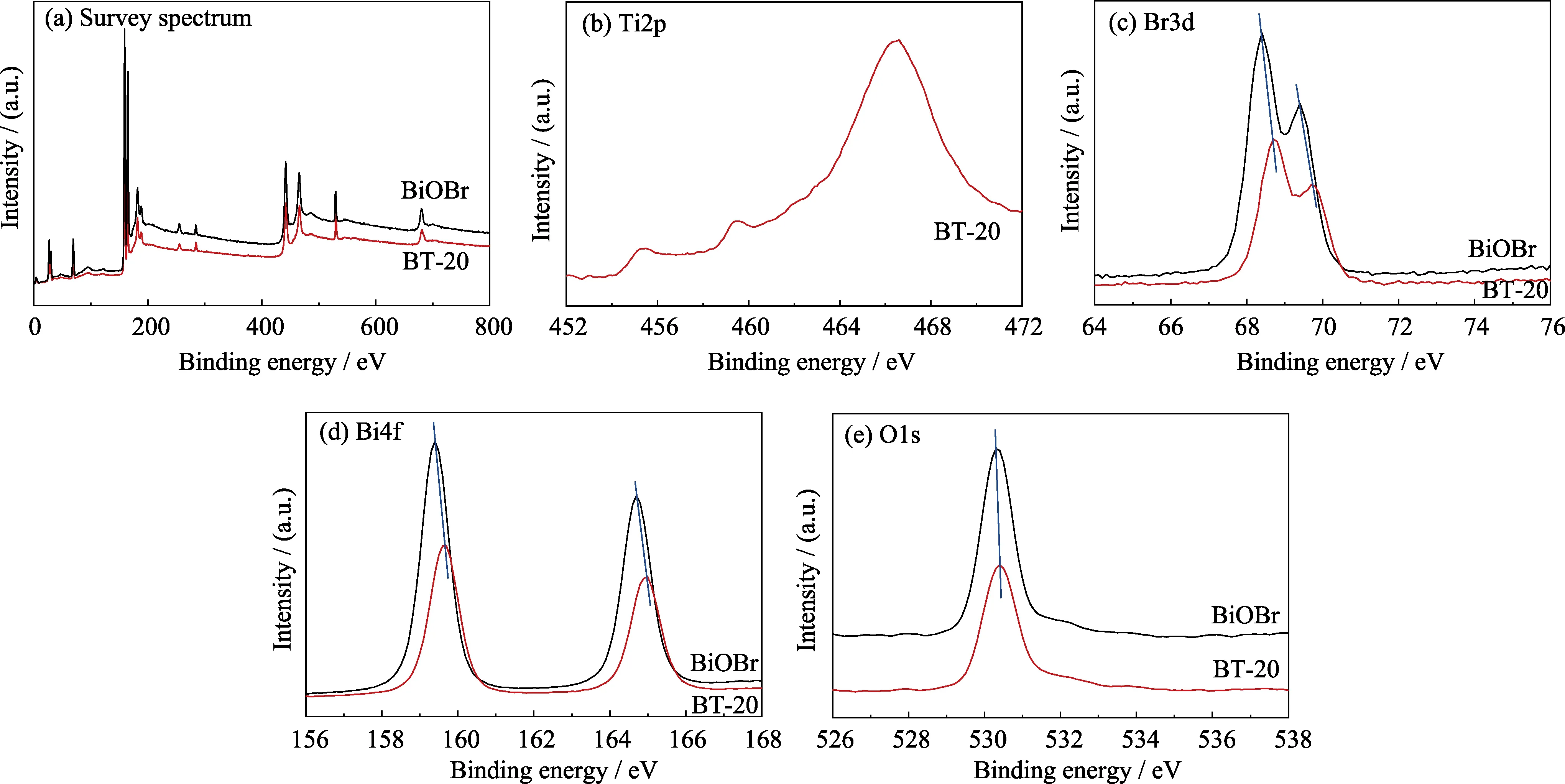
圖4 BiOBr和BT-20樣品的XPS譜圖Fig. 4 XPS spectra of samples BiOBr and BT-20(a) Survey spectra; (b) Ti2p; (c) Br3d; (d) Bi4f; (f) O1s
2.1.5 光學性質分析
通過紫外可見漫反射圖譜研究催化劑的光學性質。由圖5(a)可知,樣品具有吸收紫外和可見光的能力,BiOBr的吸收邊位于430 nm處,引入層狀Ti3C2后,BiOBr/Ti3C2復合光催化劑的吸收邊紅移至460 nm,且在可見光區具有更強的吸收,這表明引入層狀Ti3C2拓寬了BiOBr的可見光響應區域。禁帶寬度Eg可由下式進行計算[26]:
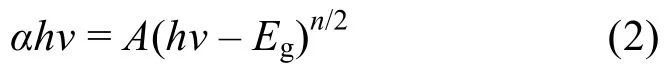
其中,n值由半導體催化劑的帶間躍遷類型決定,直接躍遷型n為1,間接躍遷型n為4。由于BiOBr的躍遷屬于間接躍遷型,即n為4[27]。由圖5(b)可知,BiOBr和BT-20的禁帶寬度分別為2.75和2.40 eV,BT-20禁帶寬度小于BiOBr,表明BiOBr/Ti3C2復合光催化劑具有更好的可見光響應能力。
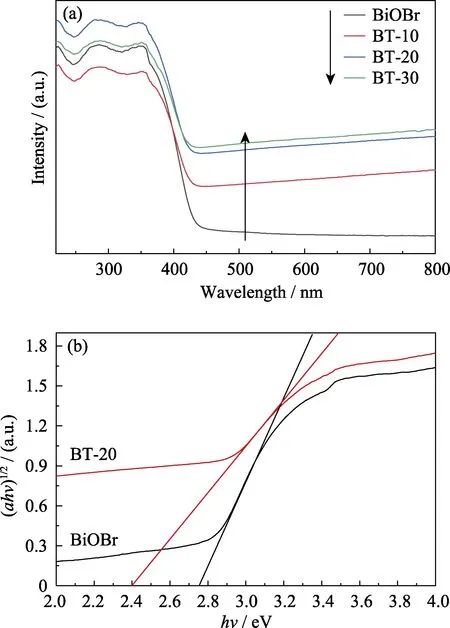
圖5 BiOBr和BT-x樣品的紫外可見漫反射光譜(a)及(αhv)1/2-hv曲線(b)Fig. 5 UV-Vis diffuse reflectance spectra (a) and (αhv)1/2-hv curves (b) of samples BiOBr and BT-x
通過光致發光光譜研究光催化劑光生電子-空穴對的轉移和重組行為。由圖6可知,與BiOBr相比,BiOBr/Ti3C2復合光催化劑的熒光強度明顯降低,其中,BT-20的熒光強度最低,這表明引入適量具有高導電性的Ti3C2能轉移光生電子,促進光生電子-空穴對的分離。
2.2 可見光催化降解性能
通過在可見光(λ>420 nm)照射下降解RhB溶液來評價BiOBr/Ti3C2復合光催化劑的光催化活性。如圖7(a)所示,在無催化劑的對照實驗中,RhB幾乎沒有發生降解。BT-20復合材料的光催化降解性能最高,光照60 min后其對RhB的降解率可達97.1%,比BiOBr、FBiOBr、FBT-20分別提高了34.7%、48.8%、16.81%。隨著Ti3C2引入量的增加,BT系列樣品中BiOBr的捕光能力有所下降,由此可見,引入適量Ti3C2可使BiOBr/Ti3C2達到最佳的電荷分離效率和捕光能力[16]。
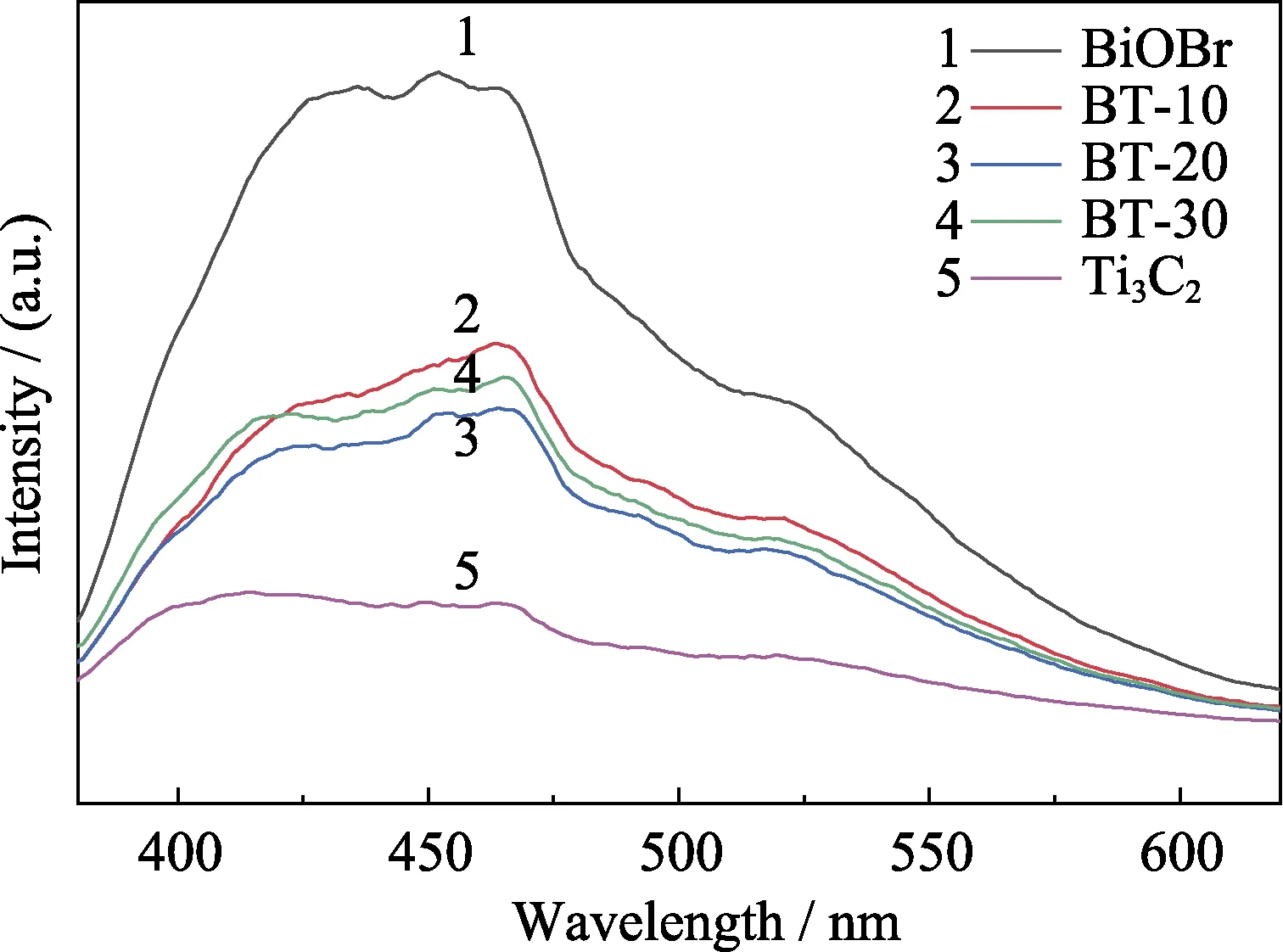
圖6 BiOBr和BT-x樣品的PL圖譜Fig. 6 PL spectra of samples BiOBr and BT-x
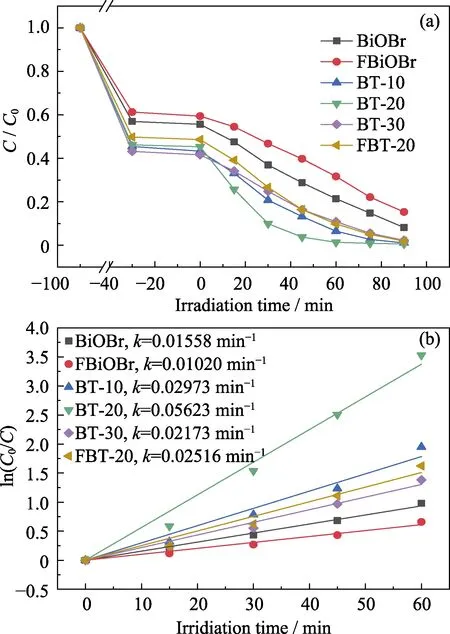
圖7 BiOBr和BT-x樣品的可見光催化降解RhB(a)及偽一級動力學曲線(b)Fig. 7 Photocatalytic degradation activity of samples BiOBr and BT-x for RhB (a) and pseudo first-order kinetic curves (b)under visible light irradiation
為了定量研究樣品的光催化活性,采用偽一級動力學方程ln(C/C0)=kt對樣品光催化降解RhB的反應進行擬合,其中k為降解速率常數(min-1)[28]。圖7(b)中BiOBr、FBiOBr、BT-10、BT-20、BT-30、FBT-20六條擬合曲線相關系數分別為0.9952、0.9901、0.9862、0.9934、0.9905、0.9858,符合偽一級動力學模型[29]. 如圖7(b)所示,BiOBr的降解速率常數為0.01558 min-1,是FBiOBr的1.5倍,表明BiOBr光催化活性優于FBiOBr,這是由于高暴露(001)面可以呈現出更好的光生電子-空穴對的遷移能力[22]。BT-10、BT-20、BT-30、FBT-20復合材料光催化降解速率常數分別為0.02973、0.05623、0.02173、0.02516 min-1,均高于BiOBr,其中BT-20的降解速率常數分別是BiOBr和FBT-20的3.6和2.2倍。結果表明,引入Ti3C2使得BiOBr與Ti3C2界面形成肖特基結勢壘,促進BiOBr/Ti3C2復合材料光生電子-空穴對的分離,從而大大提高了其可見光催化性能。
2.3 穩定性測試
光催化劑的穩定性也是評價其性能的一項重要指標。為考察復合光催化劑的穩定性,對催化劑進行了再循環實驗。循環實驗與降解實驗步驟一致,光降解90 min后,通過離心回收催化劑,進行下一次實驗。如圖8所示,經過5次循環后,催化劑對RhB降解率仍高達91.0%,表明BT-20復合光催化劑具有良好的穩定性。
2.4 機理分析
為了探究BiOBr/Ti3C2復合材料的光催化機理,通過自由基和空穴捕獲實驗確定其在可見光下降解RhB過程中的主要活性物種[30]。選用一水合草酸銨(AO)作為空穴(h+)捕獲劑[31],苯醌(BQ)作為超氧自由基(·O2-)捕獲劑[32],異丙醇(IPA)作為羥基自由基(·OH)捕獲劑[33],捕獲劑添加量均為5 mmol/L。三種捕獲劑對催化劑降解性能的影響如圖9所示。當加入IPA后,BT-20復合光催化劑的光催化活性幾乎沒有受到影響; 加入BQ后,BT-20的降解性能受到顯著影響,反應90 min后RhB降解率減少了68.0%; 加入AO后,RhB的降解率減少26.0%。由此可見,在BT-20復合材料光催化降解RhB的過程中,·O2-為其主要活性物種,h+為次要活性物種,·OH作用最小。
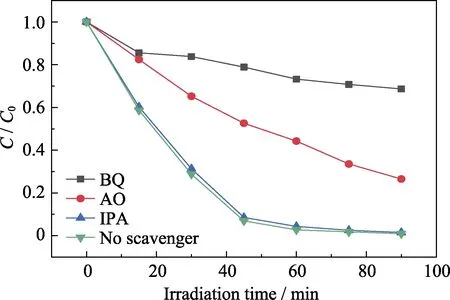
圖9 可見光照射下BT-20光催化降解RhB的活性物種捕獲結果Fig. 9 Eあect of scavengers on the degradation of RhB with BT-20 under visible light irradiation
通過經驗公式計算BiOBr的價帶電勢(EVB)和導帶電勢(ECB)[34]:
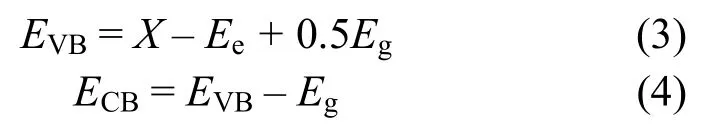
其中,X為絕對電負性,BiOBr的絕對電負性為6.18 eV[35];Ee為自由電子在標準氫電極的勢能,約為4.50 eV;Eg為半導體催化劑的禁帶寬度,BiOBr的Eg為2.75 eV。由計算可得,BiOBr的EVB和ECB分別為3.06和0.31 eV。
BiOBr屬于n型半導體,BiOBr的費米能級靠近導帶,當兩者形成緊密的界面接觸并在可見光的照射下,Ti3C2和BiOBr之間的費米能級差驅使BiOBr導帶處的電子遷移至Ti3C2處,直至兩者費米能級達到平衡,并伴隨著導帶和價帶能級向上彎曲,在界面處形成界面肖特基結能壘[36-37]。
基于以上分析,BiOBr/Ti3C2肖特基結光催化劑的光催化機理可由圖10所示。在可見光照射下,BiOBr激發產生光生電子-空穴對,形成內建電場促使BiOBr導帶處的光生電子單向跨越肖特基結能壘流入Ti3C2捕獲場,從而有效地分離載流子,遷移至Ti3C2處的光生電子將O2還原為·O2-,·O2-繼而氧化RhB,同時BiOBr價帶處具有強氧化性的空穴直接氧化降解RhB。
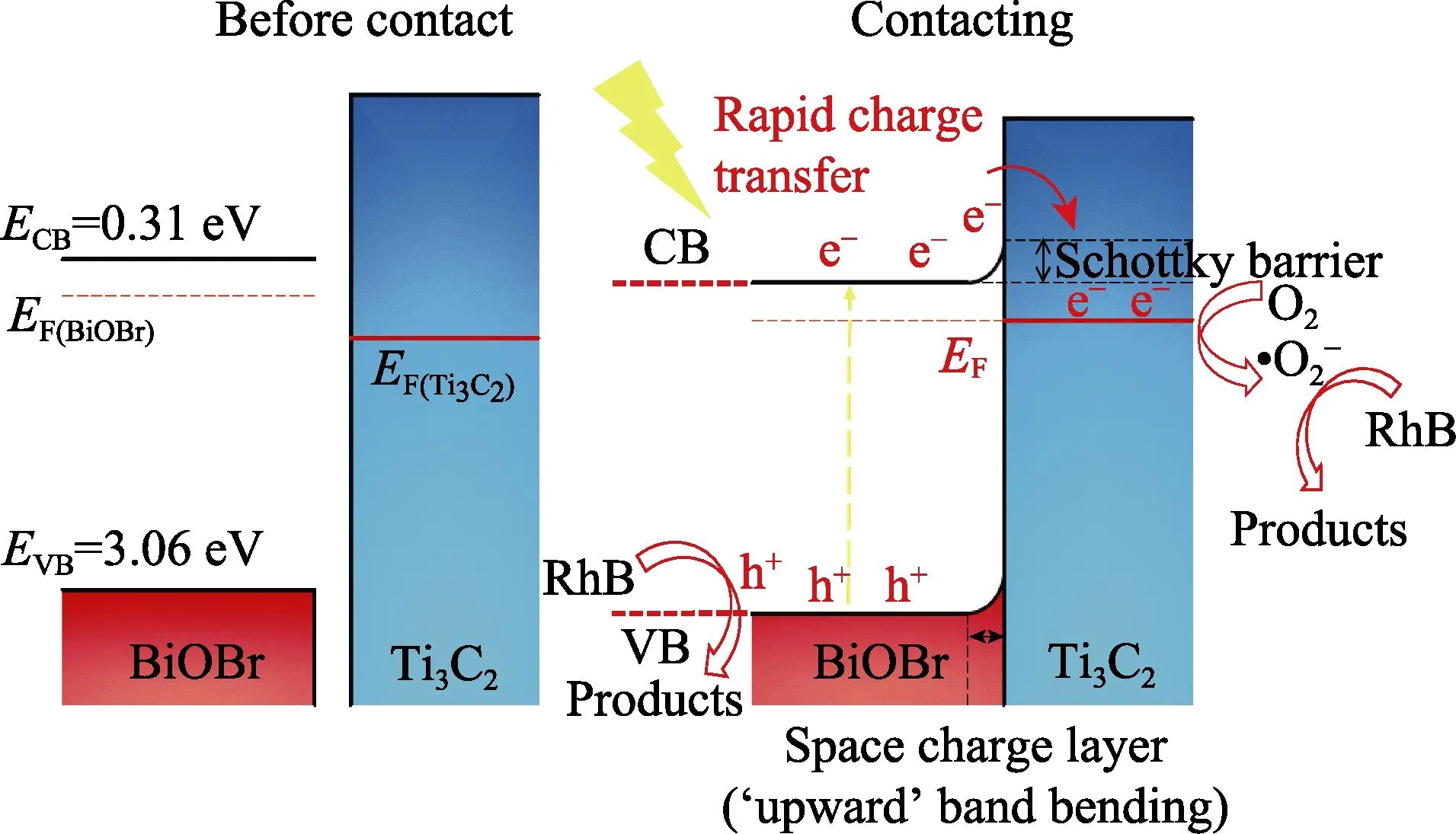
圖10 BiOBr/Ti3C2體系可見光催化降解RhB的機理Fig.10 Photocatalytic mechanism of the BiOBr/Ti3C2 composite on RhB
3 結論
通過水解法對具有高暴露(001)面的BiOBr與Ti3C2進行復合,制備出一系列高暴露(001)面BiOBr/Ti3C2復合光催化劑。與BiOBr相比,BT-20復合光催化劑降解RhB的效果最優,降解速率常數為BiOBr的3.6倍,并具有良好的循環穩定性。機理分析表明BiOBr與Ti3C2界面形成肖特基結能壘,促進光生電子快速向Ti3C2轉移,抑制了光生電子-空穴對的復合,從而提高了BiOBr的光催化活性。本研究合成的高暴露(001)面BiOBr/Ti3C2光催化劑,為構建新型高效的肖特基結光催化劑體系提供了一種可行的途徑。

