高血壓合并阻塞性睡眠呼吸暫停低通氣綜合征患者血壓變異性與左室肥厚的關系
黃素華,謝莉萍
(龍巖市第一醫院,福建 龍巖 364000)
高血壓作為心血管疾病危險因素,不僅通過平均血壓,還通過血壓變異性(BPV)和血壓晨峰增加高血壓靶器官損害和心腦血管事件[1-2]。阻塞型睡眠呼吸暫停低通氣綜合征(OSAHS)亦是心腦血管疾病的危險因素,與高血壓可共存同一患者從而加重靶器官損害。本研究通過對患者行心臟彩超、動態血壓檢查,探討高血壓合并OSAHS患者血壓變異性與左室肥厚關系。
1 資料與方法
1.1一般資料:入選2018年9月~2019年7月我院住院高血壓患者173例。排除標準:繼發性高血壓、糖尿病、肝腎功能不全、慢性阻塞性肺疾病、急性冠脈綜合征、腦卒中。OSAS診斷標準參照(OSAS診療指南》 并經多導睡眠監測明確診斷[3]。根據呼吸暫停低通氣指數(AHI) ,患者分為高血壓合并輕度OSAHS組(AHI 5~14)64例、高血壓合并中度OSAHS組(AHI 15~30)60例和高血壓合并重度OSAHS組(AHI>30)49例。
1.2動態血壓測量:所有患者進行24 h動態血壓監測,設定日間(6∶00~22∶00)每30 min測血壓1次,夜間為(22∶00~6∶00)每60 min測血壓1次,自動記錄24 h、日間、夜間平均血壓及標準差。
1.3彩超檢查:通過超聲心動圖測量室間隔厚度、左室舒張末期內徑、左室舒張末期后壁厚度,計算左心室質量(LVM),左心室質量指數(LVMI)=LVM/體表面積,LVH 診斷標準:LVMI>125 g/m2(男性)、>110 g/m2(女性)。
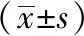
2 結果
2.1組間一般資料比較:與高血壓伴輕度OSAHS組比較,高血壓伴重度OSAHS組有更高的體質量指數,差異有統計學意義(P<0.05)。其余年齡、性別、血糖、三酰甘油、總膽固醇、高密度脂蛋白、肌酐組間比較,差異無統計學意義(P<0.05),見表1。

表1 三組一般資料比較
2.2組間平均血壓比較:三組患者24 h SBP、dSBP、nSBP隨 AHI的增加而明顯升高,差異均有統計學意義(P<0.05)兩組間舒張壓比較,差異無統計學意義(P>0.05)。見表2。
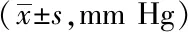
表2 三組平均血壓比較
2.3三組間BPV比較:三組患者 24hSBPSD、dSBP SD、 nSBP SD、 隨 AHI的增加而明顯升高 ,夜間血壓下降隨AHI的增加而下降,差異有統計學意義(P<0.05),見表3。
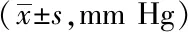
表3 三組血壓變異性比較
2.4組間左室肥厚指標比較:與高血壓伴輕度OSAHS組比較,高血壓伴中度OSAHS組、高血壓伴重度OSAHS組有更高的LVMI、LVH檢出率,差異有統計學意義(P<0.05)。與高血壓伴中度OSAHS組比較,高血壓伴重度OSAHS組有更高的LVMI、LVH檢出率,差異有統計學意義(P<0.05)。(P<0.05),見表4。

表4 三組左室肥厚比較
3 討論
OSASH不僅可影響高血壓患者血壓均值,還影響其血壓節律。本研究發現,24 h SBP、dSBP、nSBP、隨 AHI的增加而明顯升高,夜間血壓下降程度隨AHI的增加而下降,差異均有統計學意義,和既往研究結果[4]一致。 高血壓合并OSASH,夜間反復低氧、高碳酸血癥,交感神經活性反射性增加,夜間血壓升高,出現夜間血壓下降不足,出現反勺型、非勺型血壓節律。
多個研究表明[4-5],相對于單純高血壓患者,高血壓伴有OSASH患者血壓變異性升高 ,變異性程度隨著睡眠呼吸暫停嚴重程度而增加,與AHI存在相關。本研究發現,24hSBPSD、dSBP SD、 nSBPSD、隨 AHI的增加而明顯升高。OSASH睡眠時低氧血癥和高碳酸血癥,通過刺激交感神經,外周化學感受器,激活腎素-血管緊張素-醛固酮系統等途徑,損傷內皮功能,一氧化氮和內皮素等血管舒張因子釋放失衡,導致血壓變異性升高[6-8]。低氧血癥促使炎性因子釋放增多,加速血管重塑,促進了高血壓的發生和發展[9]。
本研究發現,高血壓合并呼吸暫停患者LVMI、LVH檢出率隨著呼吸暫停嚴重程度的升高,LVMI、LVH檢出率亦隨之加重。既往研究 認為高血壓合并左室肥厚組有更高的睡眠呼吸低通氣指數,睡眠呼吸低通氣指數是LVH的獨立危險因素。夜間呼吸暫停、間歇性低氧狀態,導致交感-迷走神經紊亂,炎癥介質異常釋放、損傷內皮細胞,血壓、血壓變異性升高、異常血壓節律等多種途徑導致LVH。
高血壓合并OSASH患者,隨著睡眠呼吸暫停嚴重程度的增加,血壓均值、血壓變異性增加,左室肥厚隨之增加。合并OSASH的高血壓患者,除了關注血壓均值還需注意血壓變異性,常規降壓治療同時,采用CPAP治療睡眠呼吸暫停,有利于延緩心臟損害。

