經頸靜脈肝內門體分流術治療土三七所致肝竇阻塞綜合征1例
胡乾坤 蔣旭華 王倩倩 陳良 黃玉仙
患者,男,63歲,退休職工。因“腹脹、納差、腹圍增大1月余”于2019年6月25日至上海市公共衛生臨床中心就診。患者發病前1月曾間斷服用自制“三七藥酒”治療腰腿痛,后逐漸出現腹脹、納差、腹圍增大,伴雙下肢水腫,無發熱、畏寒、寒戰,無惡心、嘔吐,無嘔血、黑便等不適。患者入院前10 d至當地醫院就診,查血常規:PLT 93×109/L;肝功能:ALT 218 U/L,AST 154 U/L,Alb 30 g/L,TBil 32.1 μmol/L,DBil 17.9 μmol/L;凝血功能:PT 17.5 s,INR 1.53;腹部超聲示腹腔大量積液。當地醫院予腹腔穿刺抽液,腹水常規、生化檢查未見異常,腹水細菌培養:陰性。予保肝、利尿、輸注白蛋白等治療7 d,患者腹脹、納差癥狀無改善。復查PLT 86×109/L,ALT 118 U/L,AST 124 U/L,Alb 32 g/L。患者為求進一步診療轉入我院。患者無吸煙、飲酒史,否認病毒性肝炎病史。
入院查體:體溫36.8℃,脈搏77次/分,呼吸20次/分,血壓130/76 mmHg;神志清,精神可;皮膚、鞏膜輕度黃染,肝掌(-),蜘蛛痣(-),肝頸靜脈回流征(-);心肺聽診無異常;腹膨隆,無腹壁靜脈曲張,腹軟,無壓痛、反跳痛,肝脾肋緣下未觸及,移動性濁音(+)。輔助檢查:血常規:WBC 4.44×109/L,Hb 154 g/L,PLT 73×109/L;炎癥指標:ESR 20 mm/h,CRP 7.86 mg/L,PCT 0.19 ng/mL;肝功能:ALT 148 U/L,AST 127 U/L,ALP 85 U/L,γ-GT 126 U/L,TBil 45.4 μmol/L,DBil 25.9 μmol/L,Alb 33 g/L,Glo 26 g/L,白球比例1.27;腎功能:Cr 84.1 μmol/L,eGFR 84.7 mL/(min×1.73 m2);凝血功能:PT 21.3 s,INR 1.86。HAV、HBV、HCV、HDV、HEV、梅毒、HIV、CMV、EBV血清免疫學檢查均陰性,抗核抗體譜(-)。腹水常規:淡黃色,微渾,白細胞手工計數 155×106/L ,紅細胞手工計數 2000×106/L,單個核細胞百分比 85.0% ,李凡他試驗(+);腹水生化:總蛋白22 g/L,白蛋白14 g/L, 腺苷脫氨酶8.9 U/L,血清-腹水白蛋白梯度>11 g/L;腹水細菌、分枝桿菌、真菌涂片及培養均陰性。腹部超聲:肝臟形態基本正常,肝脂肪輕度浸潤;門靜脈擴張、流速減低;腹腔大量積液。腹部CT:肝臟體積尚可,表面光滑,各葉比例勻稱,肝裂增寬。肝實質密度均勻;增強掃描動脈期肝左、右葉血管纖細,血管分支顯示不佳,肝實質未見明顯強化;門靜脈期肝左、右葉主干顯示清晰,遠端變細、顯示不清,肝實質呈“地圖狀”不均勻強化(圖1A)。進一步行經頸靜脈肝穿刺活檢,病理提示肝小葉部分肝細胞疏松化,肝竇擴張、充血,可見灶片融合性肝細胞壞死伴液化,匯管區炎性細胞浸潤(淋巴細胞為主),輕度纖維組織增生,不除外小靜脈或小膽管阻塞性肝損傷(圖2)。綜合考慮患者診斷為肝竇阻塞綜合征。予還原型谷胱甘肽、丁二磺酸腺苷蛋氨酸保肝退黃,螺內酯、呋塞米利尿,特利加壓素降低門靜脈壓力,前列地爾改善微循環,低分子肝素鈣抗凝,哌拉西林鈉他唑巴坦抗感染,補充人血白蛋白等治療。患者腹脹、納差等癥狀無改善,腹水難以糾正,同時PLT降低至52×109/L,TBil上升至73.7 μmol/L,Cr上升至119.4 μmol/L,eGFR降低至56.5 mL/(min×1.73 m2)。經院內多學科會診后,于2019年7月14日行經頸靜脈肝內門體分流術(transjugular intrahepa-tic portosystemic shunt,TIPS)治療。患者門靜脈壓力由術前23 mmHg下降至術后14 mmHg,腹水明顯消退。術后口服利伐沙班抗凝,期間復查血常規、肝腎功能等均明顯改善,予辦理出院。1月后隨訪,查PLT 82×109/L,ALT 44 U/L,TBil 25.4 μmol/L,Cr 58.6 μmol/L,eGFR 128.6 mL/(min×1.73 m2),PT 18.4 s,INR 1.72;腹部CT所見肝實質密度較均勻,動脈期肝實質強化程度較低,門靜脈期肝右葉強化略低于肝左葉,門靜脈-下腔靜脈支架置入(圖1B)。3月后隨訪,患者一般情況可,腹部B超示門靜脈至下腔靜脈支架內血流通暢。
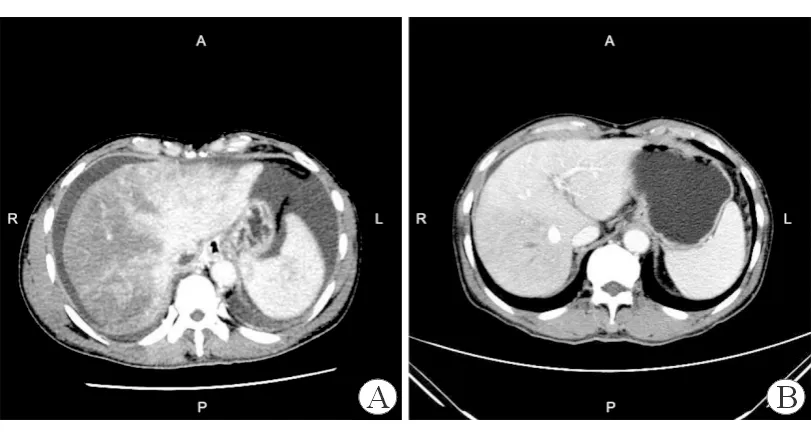
A:入院時腹部CT檢查示門靜脈期肝實質呈“地圖狀”不均勻強化;B: TIPS治療1月后復查腹部CT示肝實質密度較均勻,門靜脈期肝右葉強化略低于肝左葉,門靜脈-下腔靜脈支架置入
討論肝竇阻塞綜合征(hepatic sinusoidal obstruction syndrome,HSOS),也稱肝小靜脈閉塞病(hepatic veno-occlusive disease, HVOD),是由各種原因導致的肝血竇、肝小

A:HE染色(40);B:Masson染色(40)。肝小葉部分肝細胞疏松化,肝竇擴張、充血,可見灶片融合性肝細胞壞死伴液化,匯管區炎性細胞浸潤(淋巴細胞為主)
靜脈和小葉間靜脈內皮細胞水腫、壞死、脫落進而形成微血栓,引起肝內淤血、肝損傷和門靜脈高壓的一種肝臟血管性疾病[1]。國外報道的HSOS病因多與造血干細胞移植(hematopoietic stem cell transplantation,HSCT)前應用大劑量細胞毒性藥物有關[2-3],而在國內誤服含有吡咯生物堿(pyrrolidine alkaloid, PA)的中草藥如土三七、野百合、千里光等是導致該病的主要原因[4-5]。本例患者發病前1月有“三七藥酒”服用史,持續性腹脹、肝區疼痛和腹水,血清TBil升高,腹部CT示門靜脈期肝實質呈“地圖狀”不均勻強化,同時肝組織病理活檢提示肝竇擴張、充血,可見灶片融合性肝細胞壞死伴液化。參照《吡咯生物堿相關肝竇阻塞綜合征診斷和治療專家共識意見(2017年,南京)》[1],符合PA相關HSOS診斷。
目前,尚無治療PA相關HSOS的特效方法。國內研究表明PA相關HSOS在保肝、利尿、改善微循環等對癥處理的基礎上聯合抗凝藥物可以提高治愈率或好轉率[5-7]。然而,本例患者在轉入我院后聯合低分子肝素抗凝治療,門脈高壓性腹水仍難以糾正,同時肝腎功能進行性惡化。分析原因如下:①患者誤服土三七的時間較長,PA在肝內轉換為有細胞毒性的代謝產物,造成了肝竇內皮細胞和肝細胞的持續性損傷。②患者在當地醫院就診時,未及時進行抗凝治療。
TIPS能否用于治療HSOS尚存在爭議[8]。國內一項研究報道23例PA相關HSOS患者,在對癥處理或聯合抗凝治療無效后行TIPS治療,術后1周22例出現腹水明顯消退,僅1例死于TIPS并發癥,隨訪期22例均存活[9]。國外研究則認為,TIPS雖然能夠降低HSCT相關HSOS患者門靜脈壓力、減少腹水生成,但不能提高HSCT相關HSOS患者的遠期存活率[10]。造成上述研究結果不一致的原因可能是國內HSOS通常由誤服含PA的中草藥所致,患者多無致病性基礎疾病;而國外HSOS多發生在骨髓移植、放射性肝病、實體腫瘤化療或肝移植術后,患者基礎情況差。本例患者在對癥處理聯合規范抗凝治療過程中,血清ALT、TBil持續異常、PLT和eGFR呈進行性下降趨勢且腹腔積液難以糾正。經TIPS治療后,患者持續門靜脈高壓和頑固性腹水得到有效控制,提示TIPS治療對PA相關HSOS有治療價值。

