過氧化鈉與水反應機理的探究實驗
陳頭平
摘? 要:過氧化鈉與水反應后的溶液中滴入酚酞溶液,振蕩后出現紅色褪色的現象。為探究該反應的褪色的原因而進行實驗設計、實驗驗證,進而探究出過氧化鈉與水反應的機理。
關鍵詞:過氧化鈉;酚酞溶液;褪色;反應機理;過氧化氫
問題提出:在學習“鈉的重要化合物”(人教版)時,P55實驗3-5:把水滴入盛有少量過氧化鈉固體的試管中,立即把帶火星的木條放在試管口,檢驗生成的氣體。用手輕輕摸一摸試管外壁,有什么感覺?然后向反應后的溶液中滴入酚酞溶液,有什么現象發生?
實驗中向反應后的溶液中滴入酚酞溶液,觀察到的溶液先變紅振蕩后又出現褪色的現象。酚酞溶液變紅后為何會褪色呢?
猜想:1.實驗中Na2O2過量,Na2O2的強氧化性將紅色漂白;2.過氧化鈉與水反應生成氫氧化鈉和氧氣,可能氫氧化鈉的濃度對酚酞變色的影響,也可能產生的氧氣使酚酞變色;3.過氧化鈉與水反應不是一步完成的,中間產物有漂白性。
理論探討:
查閱《化學》必修一教師教學用書(人教版):Na2O2易潮解,與水或稀酸作用時生成過氧化氫并放熱,過氧化氫不穩定,立即分解放出氧氣:先與水發生復分解反應,生成過氧化氫:Na2O2+2H2O===2NaOH+H2O2,過氧化氫不穩定分解2H2O2===2H2O+O2↑。查閱高等無機化學教程,也有類似的解釋。
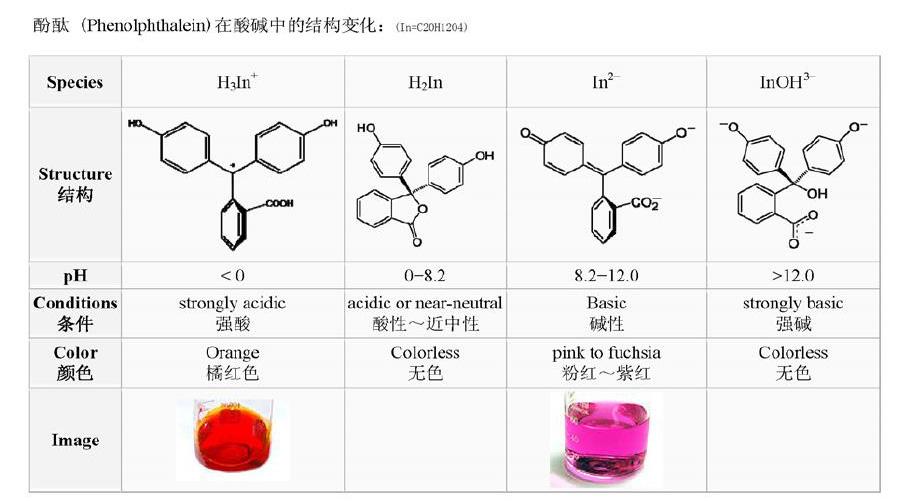
酚酞溶液在不同酸堿環境下的結構:
實驗一:
實驗目的:酚酞溶液在不同酸堿環境下變色實驗對照。
實驗藥品:5mol/L H2SO4的溶液、0.05 mol/L H2SO4的溶液、0.001 mol/LNaOH的溶液、1 mol/LNaOH的溶液、酚酞溶液。
實驗儀器:pH試紙(或pH計)、比色卡、玻璃棒。
實驗步驟:1.分別測出四種溶液的pH。
2.分別取少量四種溶液滴入酚酞溶液觀察現象。
實驗現象:5mol/L H2SO4的溶液呈橘紅色,0.05 mol/L H2SO4的溶液呈無色,0.001 mol/LNaOH的溶液呈紫紅色,1 mol/LNaOH的溶液呈無色。
實驗結論:溶液的堿性過強(pH>12)滴入酚酞溶液也呈現無色現象。
實驗二:
實驗目的:探究O2是否能使顯紅色的酚酞溶液褪色。
實驗藥品:H2O2、酚酞溶液、MnO2。
實驗儀器:試管、試管架、帶有導氣管的單孔膠塞、膠頭滴管。
實驗步驟:1.將少量NaOH固體投入蒸餾水中,制成低濃度的NaOH溶液,再將酚酞試劑滴入NaOH溶液中使其變紅。
2.向一只試管中加入H2O2,再向其中加入MnO2,并將制得的氧氣通入紅色NaOH溶液中,并觀察現象。
實驗現象:滴有酚酞顯紅色的NaOH溶液無褪色現象。
實驗結論:O2不能使滴有酚酞顯紅色的NaOH溶液褪色。
實驗三:
實驗目的:探究H2O2是否能是紅色酚酞褪色。
實驗藥品:H2O2(濃、稀)、酚酞溶液、NaOH固體。
實驗器材:試管、膠頭滴管、藥匙。
實驗步驟:
1.將少量NaOH固體投入蒸餾水中,制成低濃度的NaOH溶液,再將酚酞試劑滴入NaOH溶液中使其變紅。
2.將紅色NaOH溶液分別倒入兩只試管中。
3.分別向兩只試管中加入濃、稀H2O2,并觀察現象。
實驗現象:加入稀H2O2的試管中無明顯現象,而加入濃H2O2的試管,不久紅色褪去。
實驗結論:濃度高的H2O2能使滴有酚酞顯紅色的NaOH溶液褪色。
實驗四:
實驗目的:探究Na2O2的用量對實驗的影響。
實驗藥品:Na2O2粉末、水、酚酞溶液。
實驗儀器:試管、藥匙。
實驗步驟:
1.取3支試管均裝10ml水。
2.分別向3支試管中加①1/3藥匙的Na2O2、②1/2藥匙的Na2O2、③1藥匙的Na2O2。
3.用帶火星的木條放在試管口。
4.向反應后的溶液中滴入酚酞溶液并振蕩。
實驗現象:①號試管帶火星的木條變明亮,酚酞溶液紅色褪色時較長。③號試管帶火星的木條復燃,酚酞溶液的紅色迅速褪去。
實驗結論:Na2O2的用量越多,酚酞溶液紅色褪去得越快。
實驗五:
實驗目的:證明H2O2的存在與作用。
實驗藥品:Na2O2粉末、MnO2、冰水。
實驗儀器:藥匙、試管、燒杯。
實驗步驟:
1.用藥匙將Na2O2加入試管中,再加入少量冰水,并將試管置于裝有冰的燒杯中反應。
2.用帶火星的木條放在試管口檢驗(現象不明顯)。
3.取上層清液分別裝于兩支試管中,向其中一支加入MnO2,用帶火星的木條放在試管口檢驗,待完全反應后,再次取上層清液于另一試管中并向其中滴入酚酞溶液并振蕩。
4.向另一試管中直接滴入酚酞溶液。
實驗現象:當向溶液中加入MnO2后,有氣泡產生,待反應完全后,取上層清液于另一試管中,向試管中的液體內加入水稀釋后,再加入酚酞試劑,可看到溶液變為紅色。
實驗結論:因為加入MnO2后,有大量氣體生成,則證明溶液中存在過氧化氫,當H2O2完全分解后,將所得溶液稀釋后加入酚酞,溶液變為紅色振蕩后不褪色,即可說明溶液紅色褪色的確是溶液中過氧化氫的作用。
探究結論:
過氧化鈉與水反應后的溶液,加入酚酞后,溶液先變紅后褪色,其中溶液褪色是因為反應過程中產生了過氧化氫,主要是過氧化氫的作用使溶液褪色。當然,由于反應后,溶液中氫氧化鈉的濃度較大,所以它也應該起到了一定作用。因此我們認為酚酞褪色是由于過氧化氫的強氧化性和氫氧化鈉溶液的pH過高超出酚酞變色范圍共同作用所致。通過實驗探究證明,“過氧化鈉與水反應的機理”與所查閱資料所相吻合。
★ 基金項目:本文系湖南省教育科學“十二五”規劃2015 年度湖南省教育科學研究基地專項課題“‘魅力課堂學習共同體建構的實踐與研究”(課題批準號:XJK015BJD031)的階段性成果

