4種人工快速滲濾系統填料對氮磷的吸附和解吸特性研究
晏雯雯,張國珍,2,張超,武福平,師旭軍,王萬紅
(1.蘭州交通大學 環境與市政工程學院,甘肅 蘭州 730070;2.寒旱地區水資源綜合利用教育部工程研究中心,甘肅 蘭州 730070)
西北干旱地區農灌水資源匱乏,農田施肥導致面源污染加劇[1-3]。然而,該地區污水處理都以達標排放為目標,雖然減少了污水處理成本,卻浪費了污水中的氮磷。
人工快速滲濾系統具有占地面積較小、運行成本低和不排泥等優點[4-6]。通過選用適宜的填料,既可以使其出水達到農灌水質標準,又可以充分保留污水中的氮磷。但不同研究者在填料篩選實驗中,所用的填料種類和實驗步驟各不相同,且少有進行氮磷吸附和解吸的完整實驗,故其可比性不強[7-12]。本文在前人研究的基礎上,初步篩選了4種填料,通過吸附和解吸實驗,研究了其對氮磷的吸附和解吸特性,以期篩選出適宜的填料。
1 實驗部分
1.1 材料與儀器
黏土陶粒、頁巖陶粒、細砂(2~3 mm)、粗砂(3~5 mm)均購買于網上,工業品,為避免供試填料表面殘留的含氮物質及含磷物質影響其對氮、磷的吸附解吸實驗結果,所有填料均用無氨水沖洗,并在105 ℃下干燥2 h后備用;NH4Cl、KH2PO4、無水乙醇、CaCl2均為分析純。
FA2004電子天平;5B-1B COD快速測定儀;THZ-82A汽浴恒溫振蕩器;202-00電熱恒溫干燥箱;DGL-50B立式蒸汽滅菌器;HH-S6電熱恒溫水浴鍋;UV-2800A紫外可見分光光度計;TGL-15B高速離心機。
1.2 動力學吸附
稱取填料5 g于250 mL的具塞錐形瓶中,分別加入20 mg/L的NH4Cl(KH2PO4)溶液100 mL,置于氣浴恒溫振蕩器中,在25 ℃、150 r/min條件下分別振蕩0.5,1,2,4,8,24,48 h,離心(3 000 r/min)10 min 后,測定上清液中的氨氮(磷)含量。
1.3 等溫吸附
稱取填料5 g于250 mL的具塞錐形瓶中,分別加入濃度為5,10,20,50,80,100 mg/L的NH4Cl(KH2PO4)溶液100 mL,置于氣浴恒溫振蕩器中,在25 ℃、150 r/min條件下振蕩24 h,離心(3 000 r/min)10 min 后,測定上清液中的氨氮(磷)含量。
1.4 等溫解吸
經等溫吸附后的填料,用無水乙醇洗滌,離心后倒去上清液。加入 0.02 mol/L 的 CaCl2溶液20 mL,在25 ℃、150 r/min條件下振蕩 24 h,離心(3 000 r/min)10 min后,測定上清液中的氨氮(磷)含量。
1.5 擬合方法
對于恒溫條件下固體表面發生的吸附現象,常用Langmuir方程和Freundlich 方程來表示其表面的吸附量和介質中溶質平衡濃度之間的關系[13-14],表達式如下:
q=qmKC/(1+KC)
(1)
q=kC1/n
(2)
式中q——填料對氨氮(磷)的吸附量,mg/g;
qm——填料對氨氮(磷)的飽和吸附量,mg/g;
C——吸附平衡時氨氮(磷)的濃度,mg/L;
K、k和n——均為常數。
2 結果與討論
2.1 填料對氨氮的動力學吸附特性
4種填料對氨氮的動力學吸附曲線見圖1。

圖1 填料對氨氮的動力學吸附曲線Fig.1 Kinetic adsorption curve of ammonia nitrogen by packing
由圖1可知,在0~2 h內,4種填料對氨氮的吸附量都快速增加,且吸附量由大到小依次為:細砂>粗砂>頁巖陶粒>黏土陶粒,這說明這4種填料都能在短時間內實現對氨氮的快速吸附。在2~4 h內,細砂和粗砂對氨氮的吸附速率開始降低,頁巖陶粒對氨氮的吸附量繼續快速增加,而黏土陶粒對氨氮的吸附量開始減少,這可能是振蕩使黏土陶粒前期累積吸附的氨氮釋放出來,且解吸量大于吸附量所致[15]。在4~48 h內,細砂對氨氮的吸附量先保持不變、再減小,最后增加;而粗砂對氨氮的吸附量先減小、再增加、最后減小;但總的來說,在這段時間內,細砂和粗砂對氨氮吸附量的變化很小;這說明細砂和粗砂可以在較短的時間內達到對氨氮的吸附平衡,且長時間的吸附不僅不利于它們增加對氨氮的吸附量,反而可能會降低它們對氨氮的吸附量;而頁巖陶粒對氨氮的吸附量經歷了先緩慢增加,再快速增加,最后緩慢降低;在24 h時,頁巖陶粒對氨氮的吸附量超過了粗砂,且與細砂相接近,這說明在吸附前期,頁巖陶粒對氨氮的吸附量小于細砂和粗砂,但在吸附后期有趕超它們的趨勢;而黏土陶粒對氨氮的吸附量又開始緩慢增加,但增加的吸附量較少。在0~48 h內,細砂對氨氮的吸附量始終大于粗砂,這主要是因為較小粒徑的填料具有較大的比表面積,故其對氨氮的吸附效果較好[9];而頁巖陶粒對氨氮的吸附量始終是最小的,且小于0.06 mg/g。
2.2 填料對氨氮的等溫吸附特性
4種填料對氨氮的等溫吸附曲線見圖2。

圖2 填料對氨氮的等溫吸附曲線Fig.2 Isothermal adsorption curve of ammonia nitrogen by fillers
由圖2可知,隨著氨氮濃度的提高,4種填料對氨氮的吸附量都逐漸增加,但增加的趨勢有所不同。黏土陶粒對氨氮的吸附量一直都是緩慢增加,在氨氮濃度為100 mg/L時,其對氨氮的吸附量也沒有超過0.12 mg/g。在氨氮濃度為0~10 mg/L時,細砂和粗砂對氨氮的吸附量差別不大,但當氨氮濃度超過10 mg/L時,與粗砂相比,細砂對氨氮吸附的優勢逐漸顯現,這說明在處理低濃度氨氮污水時,細砂和粗砂的效果相差不大,而在處理較高濃度氨氮污水時,細砂對氨氮的去除率較高。在氨氮濃度為0~80 mg/L時,頁巖陶粒對氨氮的吸附量始終快速增加,當氨氮濃度超過80 mg/L時,其對氨氮的吸附量開始緩慢增加。在氨氮濃度為0~100 mg/L時,對氨氮的吸附量由大到小依次為:頁巖陶粒>細砂>粗砂>黏土陶粒,這說明無論是何種濃度的氨氮污水,頁巖陶粒對氨氮的去除率都是最高的,而黏土陶粒對氨氮的去除率最低,這與盧少勇的研究結果一致[8]。
4種填料對氨氮的Langmuir和Freundlich擬合等溫吸附方程及相關系數見表1。

表1 填料對氨氮的Langmuir和Freundlich擬合等溫吸附方程及相關系數Table 1 Isothermal adsorption equation and relevant coefficient of ammonia nitrogen fitted by Langmuir and Freundlich fillers
由表1可知,用Langmuir等溫吸附方程擬合時,細砂的擬合效果最好,黏土陶粒的擬合效果最差,4種填料對氨氮的飽和吸附量由大到小依次為:頁巖陶粒>細砂>粗砂>黏土陶粒;而用Freundlich等溫吸附方程擬合時,黏土陶粒的擬合效果最好,粗砂的擬合效果最差;k值越大,填料對氨氮吸附能力越強[8,16-17],4種填料的k值由大到小依次為:頁巖陶粒>細砂>粗砂>黏土陶粒。
2.3 填料對氨氮的等溫解吸特性
當處理后的出水用于農灌時,對于所選的填料,不僅要對氨氮的吸附量較少,而且要對氨氮的解吸率較高,這樣才能最大限度地保留污水中的氮。4種填料對氨氮的解吸率見表2。

表2 填料對氨氮的解吸率Table 2 Ammonia nitrogen desorption rate by fillers
由表2可知,4種填料對氨氮的解吸率由大到小依次為:黏土陶粒>細砂>粗砂>頁巖陶粒。黏土陶粒、細砂和粗砂對氨氮的解吸率都>50%,說明它們主要通過物理吸附作用去除水中的氨氮,而頁巖陶粒對氨氮的解吸率<30%,說明其主要通過離子交換作用去除水中的氨氮[8]。細砂的解吸率高于粗砂,這主要是因為較小粒徑的填料具有較大的比表面積,填料之間碰撞的接觸面較大,故其解吸率較高[9]。
2.4 填料對磷的動力學吸附特性
4種填料對磷的動力學吸附曲線見圖3。

圖3 填料對磷的動力學吸附曲線Fig.3 Kinetic adsorption curve of phosphorus by fillers
由圖3可知,在0~4 h內,頁巖陶粒對磷的吸附量快速增加。在4~48 h內,頁巖陶粒對磷的吸附量先減小、后增大、再減小,但總的來說,在這段時間內,頁巖陶粒對磷吸附量的變化很小。這說明頁巖陶粒可以在較短的時間內達到對磷的吸附平衡,且長時間的吸附不僅不利于其增加對磷的吸附量,反而可能會降低其對氨氮的吸附量。在0~48 h內,黏土陶粒、細砂和粗砂對磷的吸附量總體趨勢是緩慢增加的,某些時段它們對磷的吸附量也出現了緩慢減少,但總體來看,它們對磷的吸附量很少,且隨時間變化很小,黏土陶粒對磷的最大吸附量<0.01 mg/g,細砂和粗砂對磷的最大吸附量<0.015 mg/g。在0~48 h內,4種填料對磷的吸附量由大到小依次為:頁巖陶粒>細砂>粗砂>黏土陶粒,但細砂和粗砂對磷的吸附量相差很小,且與黏土陶粒差別不大。
2.5 填料對磷的等溫吸附特性
4種填料對磷的等溫吸附曲線見圖4。
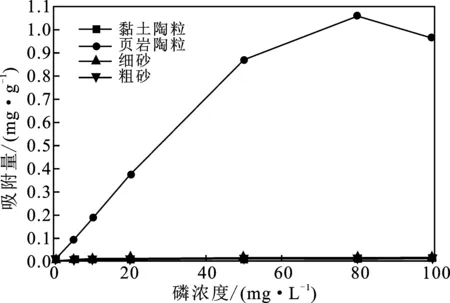
圖4 填料對磷的等溫吸附曲線Fig.4 Isothermal adsorption curve of phosphorus by fillers
由圖4可知,隨著磷濃度的提高,4種填料對磷的吸附量幾乎都逐漸增加,但他們增加的趨勢有所不同。在磷濃度為0~50 mg/L時,頁巖陶粒對磷的吸附量始終快速增加,在磷濃度為50~80 mg/L時,其對磷吸附的增量有所放緩,當磷濃度超過80 mg/L 時,其對磷的吸附量反而減少。隨著磷濃度的提高,黏土陶粒、細砂和粗砂對磷的吸附量都緩慢增加,但它們對磷的吸附量很少,且變化很小。在磷濃度為0~100 mg/L時,對磷的吸附量由大到小依次為:頁巖陶粒>細砂>粗砂>黏土陶粒,這說明無論是何種濃度的含磷污水,頁巖陶粒對磷的去除率都是最高的,而黏土陶粒對磷的去除率最低,但細砂和粗砂對磷的吸附量相差很小,且與黏土陶粒差別不大。
4種填料對磷的Langmuir和Freundlich擬合等溫吸附方程及相關系數見表3。

表3 填料對磷的Langmuir和Freundlich擬合等溫吸附方程及相關系數Table 3 Isothermal adsorption equation and relevant coefficient fitted by Langmuir and Freundlich for phosphorus by fillers
由表3可知,用Langmuir等溫吸附方程擬合時,頁巖陶粒的擬合效果最好,黏土陶粒的擬合效果最差,4種填料對磷的飽和吸附量由大到小依次為:頁巖陶粒>細砂>粗砂>黏土陶粒;而用Freundlich等溫吸附方程擬合時,黏土陶粒的擬合效果最好,粗砂的擬合效果最差;k值越大,填料對磷吸附能力越強[9,16-17],4種填料的k值由大到小依次為:頁巖陶粒>細砂>粗砂>黏土陶粒。
2.6 填料對磷的等溫解吸特性
當處理后的出水用于農灌時,對于所選的填料,不僅要對磷的吸附量較少,而且要對磷的解吸率較高,這樣才能最大限度地保留污水中的磷。4種填料對磷的解吸率見表4。

表4 填料對磷的解吸率Table 4 Phosphorus desorption by fillers
由表4可知,4種填料對磷的解吸率由大到小依次為:黏土陶粒>細砂>粗砂>頁巖陶粒。4種填料對磷的解吸率都不高。細砂的解吸率高于粗砂,這主要是因為較小粒徑的填料具有較大的比表面積,填料之間碰撞的接觸面較大,故其解吸率較高[9]。
3 結論
(1)4種填料對氨氮和磷的飽和吸附量由大到小依次為:頁巖陶粒>細砂>粗砂>黏土陶粒,對氨氮和磷的解吸率由大到小依次為:黏土陶粒>細砂>粗砂>頁巖陶粒。
(2)對于人工快速滲濾系統而言,當其處理后的出水用于農灌時,為了提高其水力負荷、減少其堵塞的可能性,應該選擇黏土陶粒和粗砂作為其填料。

