光交聯絲素蛋白水凝膠的制備及生物醫學應用
李祥明,王增凱,董明東,劉 磊
(江蘇大學材料科學與工程學院新材料研究院,江蘇 鎮江 212013)
1 前 言
水凝膠是通過物理或/和化學交聯的三維網絡結構,是一類高度模擬軟組織特性的材料,能夠吸收高達自身重量70%的水分。此外,水凝膠具有細胞外基質(ECM)的特性,能夠為細胞的活動和組織的形成提供穩定的微環境,在藥物釋放與組織工程等方面具有廣泛的應用[1]。目前用于制備水凝膠的聚合物有很多,包括合成聚合物和天然聚合物,其中天然聚合物因具有生物相容性好、免疫反應低和可生物降解等優點[2-4],被廣泛應用于組織工程和藥物遞送等領域。
蠶絲是蠶在結繭時吐出來的天然蛋白質纖維(圖1a)[5],主要由約70%的絲素蛋白和30%的絲膠蛋白組成,在紡織業中的使用已經有幾千年的歷史,作為手術縫線也已有很長的時間[6]。作為一種天然聚合物,絲素蛋白具有眾多優點,如來源豐富、生物相容性好、力學性能優異、可生物降解以及可化學改性等[7]。近年來,研究者對不同形式的絲素蛋白基材料在生物醫學方面的應用開展了廣泛的研究,包括凝膠[8]、膜[9]、纖維[10]、管[11]、海綿[12]和微球[13]等(圖1b)[14]。其中,水凝膠是絲素蛋白基材料的重要形式之一。絲素蛋白獨特的分子結構,使得能夠通過多種方法將其制備為水凝膠,這些水凝膠具有眾多可調控的性能,并已在生物醫學領域取得了廣泛應用。其中,光交聯絲素蛋白水凝膠由于制備條件溫和、副產物少、反應過程容易控制,引起了研究者的關注。本文對光交聯絲素蛋白水凝膠的制備方法與應用進行了綜述。首先介紹絲素蛋白的制備、結構和性質,然后闡述光交聯絲素蛋白水凝膠的制備方法及其在生物醫學領域中的應用,充分展示光交聯絲素蛋白水凝膠的特點與優勢,并討論了未來的發展方向。

圖1 家養桑蠶及其結出來的繭(a)[5];用蠶繭中絲素蛋白加工成的凝膠、纖維、膜、微球、管和海綿等眾多形式的材料(b)[14]Fig.1 Bombyx mori silkworm and cocoon(a)[5]; Various materials such as gels, fibers, films, microspheres, tubes and sponges processed by silk fibroin extracted from silkworm cocoons(b)[14]
2 絲素蛋白分子的結構和特性
目前在生物醫學領域研究最為廣泛的是家養的桑蠶絲,桑蠶絲由芯部的絲素蛋白(silk fibroin, SF)纖維和包覆在絲素蛋白纖維表面的絲膠蛋白組成(圖2a)[5]。桑蠶絲在使用前往往先將SF纖維外層包裹的絲膠蛋白去除(稱作脫膠)(圖2a)[5],脫膠普遍采用的方法是將蠶繭浸泡在一定濃度的碳酸鈉沸水中煮特定的時間,脫膠時間是影響SF分子質量的關鍵因素[14],因此必須嚴格控制。為了得到再生SF水溶液,需要對脫膠后的SF纖維進行進一步溶解(圖2a)[5]。常用的方法是將脫膠后的SF纖維溶解在9.3 mol/L的溴化鋰(LiBr)水溶液和摩爾比為1∶2∶8的氯化鈣-乙醇-水三元體系中進行處理,并進一步在去離子水中透析3 d左右,然后離心或過濾以去除雜質,便可得到再生SF水溶液[14, 15]。
SF是構建SF基材料的基元。它主要由重鏈和輕鏈構成,其中輕鏈的相對分子質量僅為26 kDa,而重鏈的相對分子質量則高達390 kDa,它們通過二硫鍵連接在一起,另外還有一種含量較少的糖蛋白(P25)以疏水作用的方式與重鏈和輕鏈相結合[5],三者復合形成膠束單元,在蠶的紡絲腺體內流動,最終在多種因素的協同作用下形成SF纖維[16-18]。在SF分子的組成上,輕鏈由非重復性且親水性較高的氨基酸序列組成,而重鏈則含有較多重復性的疏水氨基酸序列,包括甘氨酸-丙氨酸-甘氨酸-丙氨酸-甘氨酸-絲氨酸(GAGAGS)和甘氨酸-丙氨酸/絲氨酸/酪氨酸(G-A/S/T)二肽序列,這些疏水性較強的序列形成12個結晶區域并與親水性的非結晶區序列交替分布形成一整條重鏈[5, 19](圖2b)。其中,甘氨酸含量較高的重復序列可以在眾多因素(如溫度、甲/乙醇、剪切力、金屬離子和pH等)的誘導下形成疏水性較強的反平行β-折疊納米結晶區域[20, 21],利用SF的這一特性,外部誘導可以使SF分子構象由無定形結構向β-折疊結構轉變,從而形成交聯網絡,這是制備SF基水凝膠常用方法的基本原理。
SF纖維有著優異的力學性能,這一方面得益于結晶區內β-折疊結構在納米空間上存在的限制;另一方面,SF纖維具有明顯的層級結構,這種基于β-折疊自組裝形成的層級結構(圖2c)對增強SF纖維的力學性能同樣起到至關重要的作用[22, 23]。β-折疊在SF基材料力學性能上也扮演了重要的角色,β-折疊含量不同,材料的力學性能也有所不同。為此,很多研究者嘗試通過不同方式處理SF基材料,以調控材料內部β-折疊的含量。例如,室溫退火能夠誘導30%的β-折疊形成,而高壓蒸汽處理能得到含量大約為60%的β-折疊[24]。此外,采用SF制備的材料具有可降解的特性[25]。研究表明,這種降解性能受材料內β-折疊含量的影響,因此可以通過控制β-折疊的含量來調控材料的降解性能[26, 27]。值得注意的是,富含β-折疊的SF基材料并不像阿爾茲海默癥中通過β-折疊組裝的淀粉樣多肽聚集體有著致病性[28]。研究結果表明,SF基材料具有很好的生物相容性,早在1993年就被美國食品和藥物管理局(FDA)批準作為生物材料使用[29-31]。
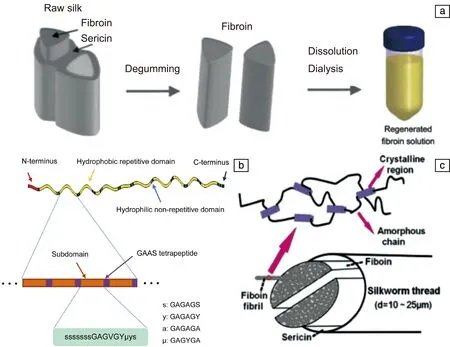
圖2 蠶絲纖維的宏觀結構和再生絲素蛋白水溶液的制備過程(a)[5];絲素蛋白重鏈的分子結構(b)[5];蠶絲纖維的層級結構(c)[22]Fig.2 Macrostructure of silk fiber and preparation process of regenerated silk fibroin aqueous solution (a)[5]; Molecular structure of the heavy chain of silk fibroin (b)[5]; The hierarchical structure of silk fibers (c)[22]
3 絲素蛋白基水凝膠的制備方法
由于具有良好的生物相容性,SF在生物材料中得到了廣泛使用,尤其是SF基水凝膠更受青睞。根據聚合物組成的不同,SF基水凝膠可以分為純SF水凝膠和共聚SF水凝膠。純SF水凝膠指參與水凝膠形成的聚合物組分只有SF,而共聚SF水凝膠指除了SF以外還有其他聚合物組分。參與SF共聚的聚合物通常包括聚乙二醇(PEG)[32]和聚乙烯醇(PVA)[33]等合成聚合物,以及蛋白質[34]和多糖[35]等天然聚合物。對于一些特殊的應用環境,單一組分制備的水凝膠表現出來的性能往往無法滿足實際應用的需求,因此通過與其它材料復合來調控它們的性能成為有效的解決方案。SF與其他聚合物組分通過共混制備的復合水凝膠,能夠實現SF與其他聚合物性能之間的互補,從而得到性能增強的材料。
根據交聯機制,可以將SF基水凝膠分為物理交聯水凝膠和化學交聯水凝膠。物理交聯SF基水凝膠是指參與水凝膠形成的聚合物鏈通過非共價鍵相互作用形成交聯網絡,如氫鍵、靜電作用和疏水相互作用等[36]。SF分子結構中交替排列的重復序列具有較強的疏水性,在外界因素作用下易發生疏水區域的自組裝,形成β-折疊結構的物理交聯網絡。常用的物理交聯手段包括升高溫度[37]、旋流處理[38]和超聲處理[39]等。物理交聯時間普遍較長,且由于分子之間形成β-折疊限制了聚合物鏈的移動,得到的水凝膠雖然強度較高但是通常較脆。化學交聯SF基水凝膠是指參與水凝膠形成的聚合物鏈之間形成了共價鍵交聯[40],這種方法通常包括交聯劑交聯、酶交聯和光交聯。其中,交聯劑交聯是一種簡便的化學交聯方法,戊二醛和京尼平是常用的水凝膠交聯劑,它們能夠與蛋白質分子鏈上的側基反應生成共價鍵。SF分子鏈側基上含有較多活性官能團,如羥基、羧基和氨基等,可以為這些交聯劑化學交聯提供活性位點[41, 42]。但是需要注意的是,戊二醛等交聯劑可能存在毒性,當這些交聯劑制備的水凝膠用作醫用材料時,如果它們從水凝膠內釋放到周圍組織中,可能對機體產生毒性[4]。對于化學交聯的SF基水凝膠,研究者又發展出了酶交聯和光交聯SF基水凝膠。酶交聯是一種更綠色安全的方法,其凝膠化能夠在體溫、中性pH和水溶液環境下進行。這種溫和的方法有利于細胞和一些不穩定活性分子的包埋,而且可以實現前驅液可注射的原位凝膠化。酶交聯法雖然具有眾多優點,但是也有很多不足,如凝膠時間較長、酶容易失活,從而導致交聯形成凝膠的效率下降等。與酶交聯相比,光交聯不僅具有制備條件溫和、副產物少、生物相容性好的優點,還克服了酶交聯耗時長的缺點,同時這種高效率的交聯方式還具有較高的可控性。
4 光交聯絲素蛋白基水凝膠
4.1 光交聯體系及其優勢
光交聯SF基水凝膠的制備機理主要源于自由基引發鏈聚合反應。光引發劑在吸收光源的能量后形成自由基,攻擊預聚物上面的活性基團,受攻擊的活性基團之間發生化學反應從而形成聚合物鏈之間的交聯。光引發交聯制備水凝膠通常包括3個要素:光源、光引發劑和帶有活性基團的預聚物。光源通常包括紫外光(200~400 nm)和可見光(400~800 nm),其中紫外光使用較為廣泛,但其可能對DNA造成破壞并導致細胞死亡[43],因此,人們漸漸避免使用紫外光,改用可見光引發交聯,減少可能造成的損害。
在選擇光引發劑時,需要考慮光引發劑產生的自由基的潛在細胞毒性,特別是應用于生物醫藥方面時需要尤為注意[44]。自由基聚合光引發劑因其優異的生物相容性得到了廣泛的應用,其中Irgacure 2959具有適度的水溶性、低的細胞毒性和相對較小的免疫原性等優點,因此被普遍使用在紫外光引發聚合中。此外,一些引發效率高、生物相容性好和水溶性更好的光引發劑,如苯基-2,4,6-三甲基苯甲酰基膦酸鋰(LAP)和偶氮引發劑VA-068也逐漸進入人們的視野并得到應用[45]。與此同時,為了避免使用紫外光聚合造成的潛在危害,可見光下構建的交聯系統引起了人們的注意。與紫外光相比,可見光具有更高的安全性,同時在可見光下使用的光引發劑如曙紅Y和樟腦醌等具有相對更低的細胞毒性和更高的水溶性[45, 46]。因此,在可見光下構建的交聯系統用于醫用材料中更凸顯優勢。然而,在比紫外光能量低的可見光下交聯,固化速率可能會變慢[47]。
帶有活性基團的預聚物是制備光交聯水凝膠的另一個必備要素。預聚物的活性基團是指在光交聯過程中,經光引發劑作用后能夠發生化學反應并使聚合物發生交聯的官能團。這些官能團可以是聚合物分子自身攜帶的,也可以是額外修飾的,主要起交聯作用。預聚物的選擇決定了最終水凝膠的很多關鍵性能,如降解性能和力學性能等。例如,同樣采用紫外光交聯的體系,以合成聚合物聚乙二醇二丙烯酸酯(PEGDA)制備的水凝膠和天然蛋白質甲基丙烯酸甲酯化明膠(GelMA)制備的水凝膠在降解性能和力學性能方面都存在明顯差異。
與其他的交聯方式相比,光驅動聚合物交聯形成水凝膠的方法具有眾多優點。首先,通過光源的開關,能夠很容易地實現聚合反應的開始和終止;其次,可以通過精確調節光劑量來實現材料功能的可調性;此外,能夠實現對曝光時間和空間的精確控制,從而達到對材料整體或局部生物學性能的調控;最后,光驅動聚合能夠在體內以一種非入侵的方式進行,具有良好的生物醫學應用前景[47]。
4.2 光交聯絲素蛋白基水凝膠的制備方法
基于以上優點,近年來研究人員做了大量的工作,試圖將光交聯方法與SF的特性結合,制備出性能出眾的水凝膠。按照光交聯體系中所使用的光源,可以將光交聯SF基水凝膠分為紫外光交聯SF基水凝膠和可見光交聯SF基水凝膠。
4.2.1 紫外光交聯絲素蛋白基水凝膠
紫外光驅動制備水凝膠在很多聚合物中都有研究,如PEGDA、GelMA和透明質酸(MeHA)等[48-50]。這些紫外光交聯系統的共同特點是利用光引發劑形成的自由基攻擊聚合物分子上的乙烯基團,隨后乙烯基團間進一步反應,促使聚合物分子間形成化學鍵,最終形成水凝膠[51]。乙烯基團間反應形成的共價鍵在交聯的過程中起到了重要的作用,明膠和透明質酸等天然聚合物中修飾的乙烯基,也是起到同樣的交聯作用。
對于SF來說,盡管在早期就有研究將乙烯基團接枝到脫膠SF纖維表面[52, 53],但是在SF分子鏈上進行修飾的研究并不多,而且相關水凝膠的研究也鮮有報道。因此,制備紫外光交聯SF基水凝膠經常采用的策略是將沒有紫外光交聯能力的SF與具有紫外光交聯能力的其他聚合物進行共混,制備半互穿網絡(semi-IPN)水凝膠和互穿網絡(IPN)水凝膠。半互穿網絡水凝膠是指當有兩種或兩種以上的聚合物共混制備水凝膠時,若只有其中一種聚合物發生交聯形成聚合物網絡,而其他聚合物只是簡單地分布在這些網絡之間,則會形成半互穿網絡水凝膠。若每種聚合物交聯得到單獨的網絡并交織在一起,則會形成互穿網絡水凝膠[33]。在半互穿網絡水凝膠的研究中,Kunda等制備出了光交聯的聚乙烯醇(PVA)/SF半互穿網絡水凝膠,經甲基丙烯酸異氰基乙酯修飾后PVA具有光交聯的能力,將其與SF共混并經紫外光引發聚合,便會形成半互穿網絡水凝膠。其中能夠在紫外光下交聯的PVA形成自己單獨的網絡,SF不具備交聯能力,便會分布在PVA形成的網絡之間[33]。在互穿網絡水凝膠的研究中,Xiao等將GelMA與SF共混制備出了GelMA和SF分別獨立交聯的雙網絡水凝膠。GelMA是明膠經甲基丙烯酸酐修飾后的產物,具有紫外光交聯能力,GelMA在紫外光和光引發劑Irgacure 2959存在的條件下發生交聯,形成化學交聯的明膠網絡,隨后將其暴露于甲醇溶液中,誘導SF形成β-折疊結構的物理交聯網絡,兩個網絡交織在一起形成互穿網絡水凝膠(圖3)。與GelMA/SF形成的半互穿網絡水凝膠相比,這種互穿網絡水凝膠在機械強度和降解性能方面都有大幅度的改善[34]。但是用于包載細胞等活性物質時,往往要避免使用有機溶劑。因此,研究者在此基礎上進一步改進方法,采用超聲而非甲醇處理的方法誘導SF形成β-折疊網絡,從而避免有機溶劑對細胞等活性物質的損傷。此外,采用改進方法制得的GelMA/SF互穿網絡水凝膠顯示出高溶脹率、優異的力學性能以及對膠原酶酶促降解的抵抗能力[54]。互穿網絡水凝膠具有單一聚合物網絡無法呈現的性能,可以通過調控聚合物的比例實現對材料性能的調控,這被稱為協同增益現象,在其它研究中也有類似報道[55, 56]。因此,利用紫外光引發交聯制備的SF互穿網絡水凝膠,不僅能夠實現光驅動體系下SF參與水凝膠的制備,而且能夠實現SF和其他聚合物之間性能的互補,達到意想不到的增益效果,這一思路在SF水凝膠開發中具有巨大的潛力。
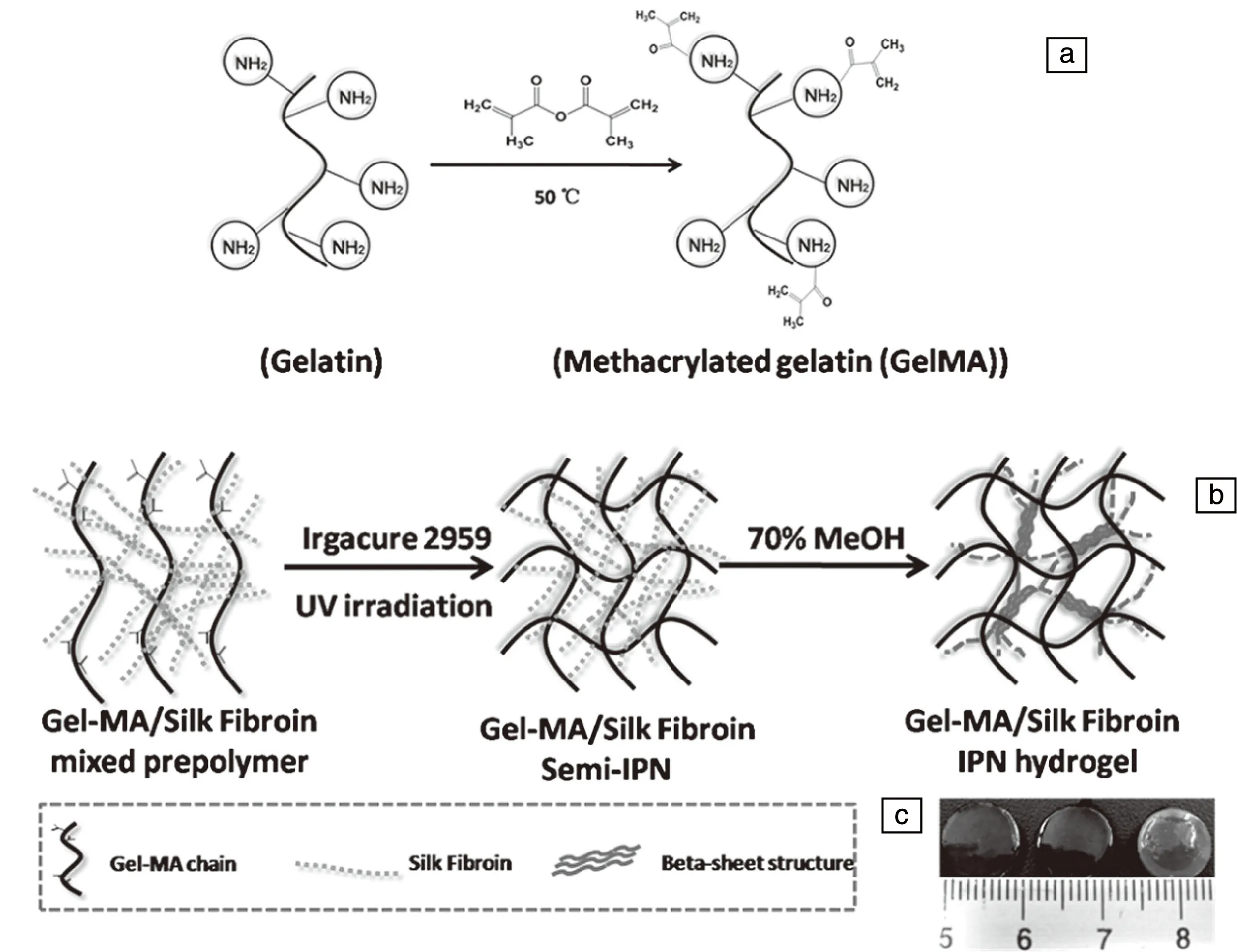
圖3 改性明膠(a)和GelMA/SF互穿網絡水凝膠(b)制備示意圖;GelMA水凝膠、GelMA/SF-1半互穿網絡水凝膠和GelMA/SF-1互穿網絡水凝膠(從左往右)的光學照片(c)[34]Fig.3 Schematic diagram of preparation of gelatin methacrylate (a) and GelMA/SF IPN hydrogel (b); Representative optical images of GelMA, GelMA/SF-1 semi-IPN and GelMA/SF-1 IPN hydrogel (from left to right)(c)[34]
最近,在SF分子鏈上修飾乙烯基團進行光交聯水凝膠制備的研究取得進展。Kim等在SF溶解的過程中,將甲基丙烯縮水甘油酯(GMA)單體加入到溶解1 h的SF/LiBr混合液中,然后在60 ℃下攪拌3 h后進行透析和凍干,即可得到乙烯基團修飾的SF分子(圖4a和4b)[57]。整個修飾過程在水溶液中完成,不使用有機溶劑,綠色環保。為了增加SF修飾時的穩定性和修飾后的水溶性,他們首先降解SF,然后將降解的SF溶解于氯化鋰/二甲基亞砜中,隨后加入甲基丙烯酸異氰基乙酯并在氮氣保護下實現了乙烯基團在SF分子上的修飾。修飾后的SF在磷酸緩沖鹽溶液(PBS緩沖液)中顯示出很好的溶解性,制備得到的水凝膠展現出很好的彈性和觸變性[58]。此外,他們利用3D打印技術將修飾后的SF水溶液作為打印墨水,實現了各種器官的高分辨率打印。利用光引發交聯提高水凝膠的穩定性,打印出來的三維結構水凝膠具有較高的分辨率(圖4c)和優異的回彈性(圖4d)[57]。除SF分子修飾外,有研究報道在SF納米/微米顆粒上修飾乙烯基團。將這些修飾后的顆粒與修飾了乙烯基團的殼聚糖共混,在紫外光下進行共聚,實現光交聯SF水凝膠的制備[59],成功在SF分子上修飾乙烯基團,使得單獨的SF在紫外光下能夠交聯形成水凝膠網絡,這將豐富光交聯SF水凝膠的制備方法和拓寬SF水凝膠的應用范圍。
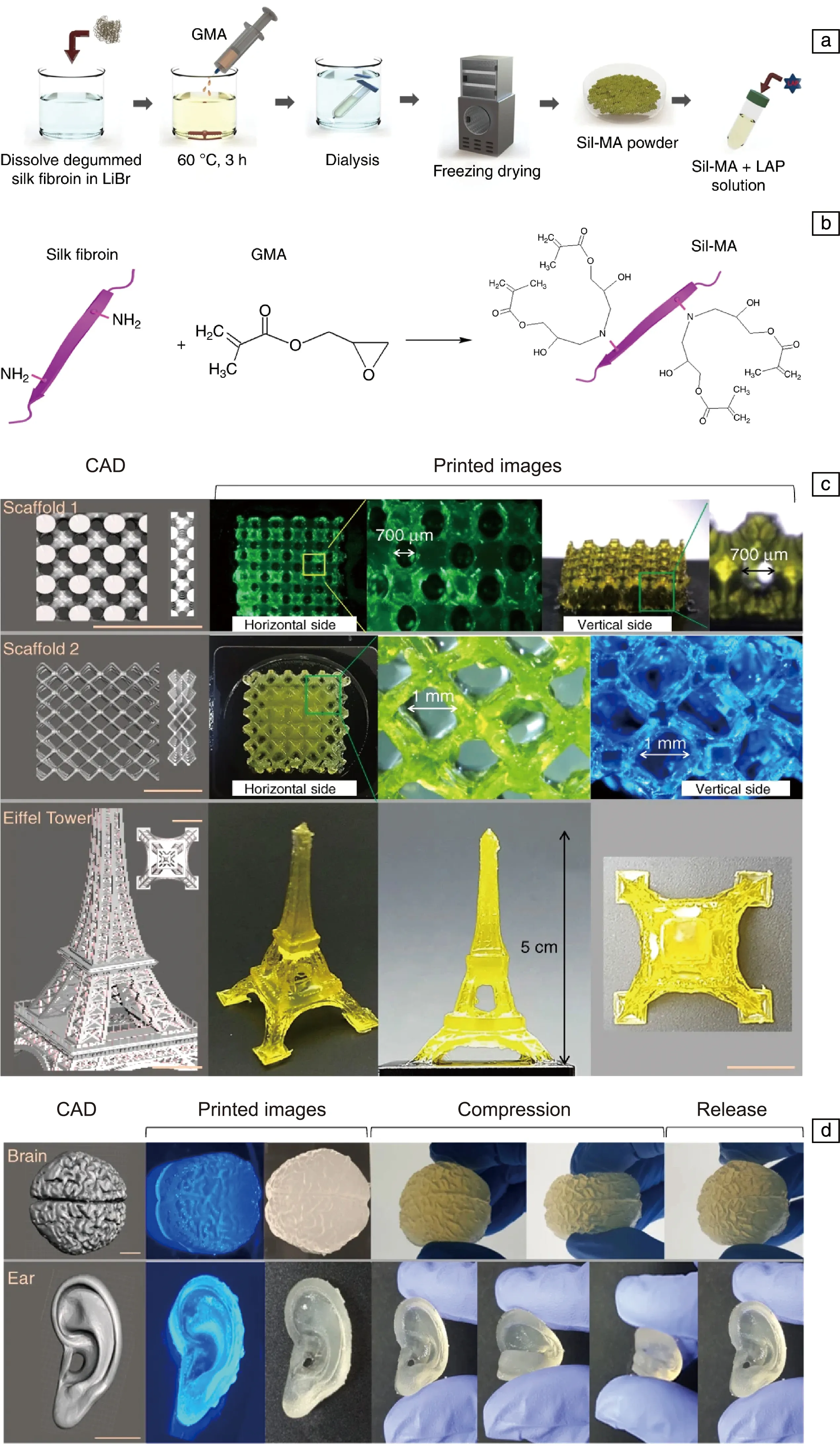
圖4 GMA改性SF的制備(a);GMA改性SF分子的示意圖(b);3D打印的三維結構SF水凝膠具有較高的分辨率(c)和優異的回彈性(d)[57]Fig.4 Preparation of GMA modified SF (a); Schematic diagram of modification of SF molecule with GMA (b); 3D printed three-dimensional structure SF hydrogels with high resolution (c) and excellent resilience (d)[57]
除了以上方法外,利用核黃素在紫外光下交聯SF也被研究者報道。核黃素是一種天然的光引發劑,其光交聯是非特異性的,在很多材料如PEG、膠原蛋白和藻酸鹽的交聯中均有應用。Kuang等將核黃素和辣根過氧化物酶(HRP)添加到SF水溶液中,并向反應體系中持續通入氧氣,在紫外光照下,核黃素被激發產生活性氧自由基,這些活性氧自由基能夠與SF分子上的氨基和苯酚基等作用,最終引發SF交聯形成水凝膠。這種水凝膠具有很好的彈性和透明度,在細胞培養中展現出優異的細胞相容性。雖然該方法避免了SF上的修飾,制備的水凝膠也具有一定的優異特性,但是這種方法形成水凝膠的時間相對較長(大約30 min),仍有很大的改進空間[60]。
4.2.2 可見光交聯絲素蛋白基水凝膠
與紫外光驅動的光交聯SF基水凝膠相比,可見光交聯SF水凝膠的報道相對較少。Whittaker等提出了在可見光(452 nm)下釕介導SF交聯形成水凝膠的方法,在該體系下,釕作為催化劑,過硫酸銨充當電子受體,在可見光下形成的中間體使得SF分子上的酪氨酸被氧化并發生相互間的反應,形成二酪氨酸交聯(圖5)。研究結果表明,利用該方法制備出的水凝膠在完全吸水的情況下表現出約78 MPa的儲能模量,對小鼠的軟骨前細胞培養表現出良好的生物相容性和細胞增殖效果。此外,這種方法實現SF凝膠化的轉變僅僅需要2 min,克服了京尼平和酶交聯耗時長的缺點[61]。為了調控并改善水凝膠的力學性能,Whittaker和Balu等又進一步利用此原理制備出釕介導的可見光交聯SF/彈性蛋白共聚水凝膠、SF/聚(N-乙烯基己內酰胺)雙網絡水凝膠和SF/石墨烯復合水凝膠[62-64]。這些水凝膠都表現出與干細胞之間具有良好的相容性,以及在兆帕范圍內儲能模量的可調控性。然而,該方法使用的催化劑釕和電子受體過硫酸銨具有潛在的毒性[65, 66]。為此,Applegate等提出用核黃素作為光引發劑、在可見光下驅動SF交聯的策略。前面曾提到核黃素作為紫外光引發劑交聯SF,事實上,核黃素也可以作為引發劑在可見光下交聯SF。在可見光下,核黃素吸收光能后奪取SF分子上酪氨酸的電子并形成酪氨酸自由基,酪氨酸自由基之間發生反應最終生成二酪氨酸鍵。此方法在一定程度上和釕介導的SF光交聯有相似的地方,但是避免了其潛在的毒性。該方法形成的SF水凝膠同樣表現出良好的彈性以及光學透明性,這可能是二酪氨酸鍵交聯形成SF水凝膠的共同特點[66]。
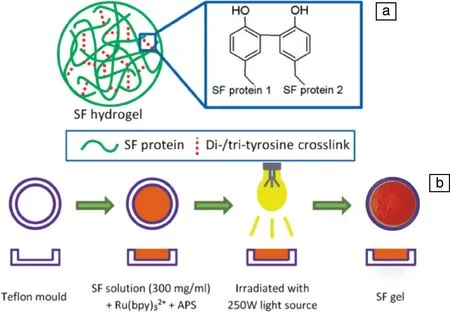
圖5 釕介導絲素蛋白分子酪氨酸交聯示意圖(a);釕介導絲素蛋白交聯制備水凝膠的過程(b)[61]Fig.5 Schematic diagram for ruthenium-mediated tyrosine cross-linking of SF (a); The procedure of constructing the ruthenium-mediated SF cross-linking hydrogel (b)[61]
5 光交聯絲素蛋白基水凝膠的應用
5.1 藥物釋放
人體的一些組織如骨和軟骨等天生缺乏血管,當這些部位發生病變或者受到外界損傷時,全身性給藥比較困難。在這類情況下,局部給藥效率較高,成為替代全身性給藥的治療方法。水凝膠作為局部給藥的藥物載體材料,不僅具有獨特的結構和性質,還可以負載藥物分子進行緩釋,因而受到廣泛關注。近年來,研究者對局部給藥治療中作為藥物載體的光交聯SF基水凝膠進行了初步探索。
Kundu等評估了模型藥物熒光標記的右旋糖酐在SF/PVA光交聯半互穿網絡水凝膠中的釋放性能。結果表明,右旋糖酐的釋放特性依賴水凝膠中SF的含量和右旋糖酐的相對分子質量。通過控制SF的含量或者右旋糖酐的相對分子質量能夠實現對藥物釋放的調控,這種可控的水凝膠體系具有作為緩釋藥物遞送載體的潛力[33]。視黃酸是維生素A的代謝產物,在眼睛發育和信號傳導過程中起著至關重要的作用,Bhattacharjee等將其偶聯到核黃素光交聯的SF水凝膠上,用于角膜基質細胞的培養。研究結果表明,這種水凝膠能更好地支持細胞粘附、增殖,促使細胞外基質的形成和角膜細胞相關基因的表達[67]。考慮到SF基水凝膠的生物相容性優勢,它更適合遞送激素類和多肽類等具有高生物活性的藥物,還可以通過控制光交聯程度實現藥物的可控釋放,如長效釋放和短期釋放等。
5.2 組織工程
光交聯SF水凝膠具有固化效率高、水凝膠性能可控性高和易原位成膠等優點,在組織工程中具有巨大的應用潛力。近年來,光交聯SF水凝膠在組織工程特別是在軟骨組織工程的應用中取得了突破性進展。在軟骨組織工程中,來自膝關節、氣管等組織的軟骨細胞可在人工基質上生長,經皮下植入并在體內成熟后,表現出類天然軟骨組織的形態學和生物學功能。基于此,Hong等將甲基丙烯酸縮水甘油酯修飾的SF通過3D打印的方式制成水凝膠,并用于軟骨細胞的體外分化能力研究和小鼠氣管體內移植的可行性研究。經過長達4周的體外細胞培養,這種水凝膠依然能夠維持軟骨細胞的活性,并支持細胞的增殖和分化。兔模型上氣管的體內移植實驗表明,移植的SF水凝膠周圍有新的軟骨樣組織和上皮細胞形成。該研究表明,利用3D打印制備的SF水凝膠可應用于軟骨再生等相關的組織工程領域[68]。此外,外傷或疾病等對角膜造成的損傷會影響視力甚至可能導致失明,角膜移植在治療角膜疾病或角膜損傷上表現出良好的治療效果,但是可用于角膜治療的供體往往比較有限,目前角膜組織工程為這一問題提供了解決方案。光交聯SF水凝膠在角膜組織工程上也有應用。核黃素可見光交聯的SF水凝膠具有透明度高、與角膜接觸緊密和彈性好等優點,有望在醫用領域作為人工角膜使用[66]。另一方面,負載視黃素的紫外光交聯SF水凝膠用于體外促進人角膜干細胞的生長和分化研究。實驗結果表明,這種復合SF支架對人角膜細胞的形成具有促進作用[67]。
5.3 其他應用
以肽和蛋白質構建的具有精確空間圖案以及微納米結構的生物材料有著重要的應用。光刻技術為加工這些復雜圖案和結構提供了一種快速、直接和高保真的選擇。利用光刻技術將乙烯基改性SF溶解在六氟異丙醇或甲酸中,將其作為光致抗蝕劑,在紫外光下構造精密復雜圖案已經得到實現[69, 70]。此外,在可見光下以核黃素作為光引發劑,水作為溶劑,利用SF作為光致抗蝕劑,光刻得到的圖案能達到40~50 μm的分辨率[67, 71]。通過這些手段得到的具有微結構的材料可作為生物友好的納米結構支架和柔性微設備來研究基底和細胞的相互作用,同時也可應用于生物電子學、光子學和治療學等領域的研究[72]。
6 結 語
近年來,由于光響應的眾多優點,光驅動聚合物形成凝膠的研究成為熱點。利用紫外光和可見光驅動形成SF基水凝膠的研究取得了階段性進展。這些水凝膠可用于藥物釋放和組織工程等相關生物醫用領域,盡管取得了一些階段性成果,但目前仍有很多問題需要解決,仍有很多工作需要進一步探索。首先,雖然目前已經開發出了多種光交聯制備SF水凝膠的方法,但部分光交聯體系下,SF形成水凝膠的機理還有待進一步的理解;其次,制備的水凝膠作為載藥或組織工程支架在體內使用時,藥物遞送性能、力學性能和降解性能等還需深入研究;最后,利用光交聯的優勢,將SF與其他功能性、生物學信號豐富的聚合物或無機物相結合,制備出能滿足實際需求的復合材料,還有待進一步發展和探索。這些研究和探索將為構建SF基生物醫用材料提供良好的理論和實驗指導,最終使這些材料在臨床中得到應用。

