不同呼吸支持模式對早產兒視網膜病發生及血清IGF-1與VEGF水平的影響觀察
余 瑜,馬曉利,鐘桂朝,田汝銀
(廣東省深圳市人民醫院兒科,廣東 深圳 518000)
早產兒視網膜病(ROP)是新生兒由于視網膜神經血管發育異常,脆性大,易滲出和出血,形成視網膜瘢痕,這些瘢痕受到牽拉會脫離視網膜,引起視力受損[1],而且具有潛在性地致盲危險。足月兒視網膜血管和視網膜發育完全,不發生ROP[2]。低體重、極低體重出生早產兒視網膜血管和視網膜發育不完善,是ROP的高發人群。近年來,早產兒ROP的發生受到臨床的高度關注[3],2012年衛生部組織,對各地ROP進行專項檢查,反映了國家對ROP的重視程度。一些危險因素的研究表明,ROP的發生與早產、高氧、感染、低出生體質量有關[4-7]。其中出生后氧療被認為是ROP的獨立危險因素[8]。為此,本研究采用前瞻性隊列研究,對經鼻持續性氣道正壓通氣(nasal continuous positive airway pressure,NCPAP)、加溫濕化高流量經鼻導管通氣(heated humidified high flow nasal cannula,HHHFNC)、常頻機械通氣(conventional mechanical ventilation,CMV)三種呼吸支持方式患兒ROP發生及嚴重程度,并比較各組患兒呼吸支持開始時和撤機前血清低血漿胰島素樣生長因子-1(IGF-1)與血管內皮生長因子(VEGF)含量,為臨床呼吸支持方式的選擇提供參考,現報告如下。
1 資料與方法
1.1一般資料:選擇我院2017年4月~2018年6月327例胎齡<34周需行呼吸支持的早產兒作為研究對象,納入標準:出生體質量<2 000 g或胎齡<34周,出生后需行呼吸支持治療,吸氧時間2周及以上早產兒;排除標準:唇、腭裂,先天性呼吸道畸形等先天畸形疾病患兒,先天性心臟病、腦、肺發育不良等遺傳代謝疾病患兒,未堅持到末次ROP篩查患兒。根據呼吸支持模式分為三組,142例經鼻持續性氣道正壓通氣(NCPAP)患兒為NCPAP組,102例加溫濕化高流量經鼻導管通氣(HHHFNC)患兒為HHHFNC組,83例常頻機械通氣(CMV)患兒為CMV組;各組患兒性別、產前使用糖皮質激素構成、胎齡、出生時體重、5 min Apgar評分差異均無統計學意義(P>0.05)。詳見表1。
表1 各組患兒基線資料比較

組別例數性別(例)男女平均胎齡(x±s,周)出生體重(x±s,g)5 min Apgar評分(x±s,分)產前使用糖皮質激素(例)NCPAP組142776529.57±1.861 227.65±205.899.33±0.8782HHHFNC組102554729.36±1.741 208.53±194.719.26±0.9456CMV組83453828.79±1.131 193.42±172.909.04±1.0144
注:三組間各項比較,P>0.05
1.2呼吸支持方法:HHHFNC組患兒采用的CE0120型Flexicare Medical Ltd濕化器(Fisher&Paykel 公司),鼻導管外徑為0.2cm,初始參數:吸入氧流量(Flow)5~6 L/min,濃度(FiO2)30%~50%,加溫濕化吸入氣體溫度37℃;空氧混合儀視患兒血氣分析與病情調整給氧流量范圍在2~6 L/min。注意鼻腔與鼻導管間留一定間隙,不形成密閉空間。NCPAP組采用infant flow system CPAP 呼吸機(Stephen 公司),初始參數:Flow 5~6 L/min,FiO230%~50%,呼氣末正壓(PEEP)5~6 cm H2O(1 cm H2O=0.098 kPa),固定鼻塞與帽子,使其形成密閉空間,視患兒血氣分析與病情調整氣道壓力與給氧濃度。CMV組采用SLE5000 Infant Ventilator 呼吸機,初始參數:RR 30~40 次/min,FiO240%~50%, PIP 18~22 cm H2O,PEEP 4~6 cm H2O,模式為同步間歇指令通氣、輔助/控制通氣,視患兒血氣分析與病情調整呼吸機參數。患兒呼吸困難、胸片肺部情況改善,無呼吸暫停,自主呼吸恢復,監測血氣分析正常,符合撤機相關參數標準后撤機。
1.3ROP篩查方法:根據衛生部2004年《早產兒治療用氧和視網膜病變防治指南》由高年資眼科醫師采用間接眼底鏡和廣域數字化照相儀對ROP高危患兒進行篩查,并根據ROP國際分類標準分期,分界線為1期,嵴形隆起為2期,嵴形隆起伴纖維增殖為3期,部分視網膜脫離為4期,全部視網膜脫離為5期。
1.4觀察指標:比較各組患兒篩查ROP發生率及分期構成比例;各組患兒呼吸支持開始時、撤機前均取外周靜脈血1 ml,離心分離血清,采用雙抗體夾心ABC法、ELISA法檢測 IGF-1與VEGF含量。

2 結果
2.1ROP發生及嚴重程度:NCPAP組、HHHFNC組、CMV組ROP發生率分別為26.76%、27.45%、30.12%,且各組ROP1期、2期、3期構成比例差異無統計學意義(P>0.05)。見表2。
表2 早產兒不同呼吸支持模式ROP發生及嚴重程度比較[例(%)]

組別例數1期2期3期ROP總發生NCPAP組14221(14.79)14(9.86)3(2.11)38(26.76)HHHFNC組10217(16.67)10(9.80)1(0.98)28(27.45)CMV組8315(18.07)8(9.64)2(2.41)25(30.12)
注:三組間ROP發生率比較,P>0.05
2.2呼吸支持前、后血清 IGF-1與VEGF 水平變化:組內比較,各組患兒撤機前血清VEGF水平均較呼吸支持開始時明顯降低,差異有統計學意義(P<0.05)。呼吸支持開始時、撤機前IGF-1水平差異無統計學意義(P>0.05)。組間比較,各組呼吸支持開始時、撤機前血清 IGF-1與VEGF 水平差異均無統計學意義(P>0.05)。詳見表3。
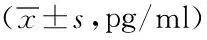

組別例數血清IGF-1呼吸支持開始時撤機前血清VEGF呼吸支持開始時撤機前NCPAP組14235.69±4.8135.94±4.26①②383.27±31.59276.08±22.04①HHHFNC組10235.37±5.1935.52±4.97①②385.63±28.47273.81±21.83①CMV組8336.02±5.0235.68±4.88①②377.91±28.09261.52±23.57①
注:與呼吸支持開始時比較,①P<0.05,②P>0.05;三組間各時間點比較,P>0.05
3 討論
受環境、社會、生物因素的影響,早產兒的出生率在我國有增加趨勢。對于極低出生體重兒、超低出生體重兒的早產兒來講,由于中樞神經系統、呼吸系統發育尚未成熟,易發生呼吸困難[9],因此出生后往往需要根據情況采取適宜的呼吸支持,能糾正高碳酸血癥,并迅速改善患兒缺氧狀態[10-11],這一舉措雖然大大提高了極低出生體重兒、超低出生體重兒的存活率,但長時間過高濃度吸氧會對萌發的視網膜血管造成直接損害,但具體機制尚不明確,可能與吸入高濃度氧時間長,且氧濃度波動大等有關,因此ROP等并發癥的防治成為新生兒醫學研究的重點。本研究結果顯示,NCPAP組、HHHFNC組、CMV組ROP發生率分別為26.76%、27.45%、30.12%,且各組ROP1期、2期、3期構成比例差異無統計學意義。說明不同呼吸支持模式對ROP的發生及嚴重程度無明顯影響。
視網膜不僅包含血管組織,還包含神經元的神經組織、神經膠質及小膠質等[12],其血管生成與血管增生是全身生長因子與局部內皮細胞增生、有絲分裂、遷移和成熟復雜相互作用的結果[13]。ROP的發生要經過2個階段,第一階段表現為血管受損,第二階段為血管增生。其中VEGF在眼神經血管發育中起著重要作用,而IGF-1作為非氧調節因子對于胎兒的體質量增長和生長發育均有重要作用,是ROP發生的關鍵因素[14]。動物實驗研究顯示,ROP的發生與早產兒產后數周內低IGF-1水平相關[15]。在視網膜新生血管形成中,IGF-1是VEGF 的正向調節因子,當IGF-1在一定濃度時,VEGF才能在視網膜新生血管的生長中發揮最大的誘導作用,當IGF-1水平處于低水平時,即使血清VEGF水平較高,對視網膜血管生長的促進作用也發揮有限,但目前尚無IGF-1的最佳臨界值。本研究結果顯示,患兒撤機前血清VEGF水平均較呼吸支持開始時明顯降低,差異有統計學意義(P<0.05)。各組呼吸支持開始時、撤機前血清 IGF-1與VEGF 水平差異均無統計學意義(P>0.05)。可能是早產兒血清IGF-1水平本就偏低,加之呼吸支持后VEGF水平降低,易誘發ROP。

