高血壓合并心功能不全對患者CyP、GDF-15、IL-18水平影響研究
劉曉雨 賈國偉 孫榮國 趙明 張巍
高血壓是臨床上十分常見的心血管系統疾病,該病呈慢性進展,隨著疾病加重可導致心臟功能和結構的改變,導致左心室肥厚、動脈粥樣硬化及心力衰竭等。研究表明[1],隨著高血壓患者年齡增加、血壓升高及病情進展,導致心力衰竭的風險明顯上升,嚴重危害了患者的生存質量。高血壓導致心功能不全的機制復雜,與細胞因子活化、神經內分泌激活及氧化應激反應等多種因素有關。環孢素A 結合蛋白(又稱親環素,cylophilin,CyP)在介導細胞免疫抑制、調節蛋白質運輸、誘導炎性細胞聚集等方面具有重要作用[2]。CyP 參與了血管損傷等生理病理過程,促進了動脈粥樣硬化的發生[3]。生長分化因子-15(Growth differentiation factor 15,GDF-15)屬于應激反應蛋白,在心臟壓負荷過重、缺血再灌注損傷等病理狀態下在心肌細胞中表現為高表達[4]。白細胞介素-18(interleukin-18,IL-18)是重要的促炎性因子,其與心血管疾病的發生發展密切相關。因此,本研究就高血壓合并心功能不全對患者CyP、GDF-15、IL-18水平的影響進行了研究,具體如下。
1 資料與方法
1.1 一般資料
選取本院2016年12月至2019年12月收治的原發性高血壓患者90例。依照患者伴心功能不全程度分為高血壓無心功能不全組(A組,n=36)、高血壓伴輕度心功能不全組(B組,心功能Ⅰ、Ⅱ級,n=32),高血壓伴中重度心功能不全組(C組,心功能為Ⅲ、Ⅳ級,n=22),其中A組男21例,女15例,年齡39~77歲,平均(62.3±3.7)歲;B組男18例,女14例,年齡42~79歲,平均(61.3±3.5)歲;C組男13例,女9例,年齡44~76歲,平均(62.4±3.3)歲。另選擇同期于我院進行體檢的健康志愿者30例作為對照組,男16例,女14例,年齡36~79歲,平均(60.5±3.8)歲。
納入標準:①均符合原發性高血壓(2~3級)的診斷標準[5],靜息狀態下不同日測量3次舒張壓≥90 mmHg 或收縮壓≥140 mmHg;②所有患者均對本研究內容知情同意并簽署知情同意書;③均臨床資料完整,能夠配合完成此研究。排除標準:①繼發性高血壓患者;②合并缺血性心臟病、心包積液、心肌梗死等心臟病患者;③合并嚴重肝腎功能不全、惡性腫瘤、急慢性感染及血液系統疾病患者。高血壓性心功能不全符合《內科學》的相關診斷標準[6],并依據NYHA分級標準評估心功能分級[7]。4組研究對象在性別、年齡上比較,差異無統計學意義(P>0.05),具有可比性。本研究經醫院倫理委員會批準。
1.2 方法
1.2.1 心臟超聲檢測心功能
所有患者采用ViViD3型彩色多普勒超聲(美國GE公司)測定左室舒張末期內徑(Left ventricular end diastolic diameter,LVEDD)、左室收縮末期內徑(Left ventricular end systolic diameter,LVESD)、左房內徑(Left atrial inner diameter,LAD)、室間隔厚度(Interventricular septal thickness,IVS)及左室射血分數(Left ventricular ejection fraction,LVEF)。均采用美國超聲心動圖學會推薦測定方法,探頭頻率1.5~2.5 MHz,所有患者測定均由同一專業醫師操作完成。
1.2.2 血清因子測定
所有研究對象均于清晨空腹抽取5 mL 靜脈血,3 000 r/min 離心10 min 分離血清,-20℃保存待測。采用酶聯免疫吸附法(Enzyme-linked immunosorbent assay,ELISA)檢測各組血清腫瘤壞死因子-α(Tumor necrosis factor-α,TNF-α)、IL-1β、總抗氧化能力(Total antioxidant capacity,T-AOC)、B型腦鈉肽(B-type natriuretic peptide,BNP)、IL-6、CyP-A、CyP-B、GDF-15、IL-18水平,采用CB-372型全自動酶標儀(TRACE公司)測定,室溫490 nm 處讀取OD值,通過標準曲線計算各血清細胞因子濃度,試劑盒購自上海生工生物公司。嚴格依照試劑盒及儀器說明書執行各項操作。
1.3 統計學分析
采用SPSS 20.0軟件進行數據分析,計量資料以()表示,兩組間比較采用t檢驗,多組間比較采用單因素方差分析;Spearman 檢驗分析CyP、GDF-15、IL-18 與高血壓合并心功能不全患者LVEF 的相關性。P<0.05 為差異具有統計學意義。
2 結果
2.1 4組心功能檢測結果比較
4組間LVEDD、LVESD、LAD、IVS 水平比較:對照組<A組<B組<C組,差異有統計學意義(P<0.05);LVEF(%)水平比較:C組<B組<A組<對照組,差異有統計學意義(P<0.05)。見表1。
表1 4組心功能檢測結果比較(±ss)Table1 Comparison of cardiac function test results in the 4 groups(±ss)

表1 4組心功能檢測結果比較(±ss)Table1 Comparison of cardiac function test results in the 4 groups(±ss)
注:與對照組比較,aP<0.05;與A組比較,bP<0.05;與B組比較,cP<0.05。
組別對照組A組B組C組F值P值n 30 36 32 22 LVEDD(mm)45.2±4.9 45.8±5.6 51.3±6.9ab 55.8±6.4abc 6.769 0.000 LVESD(mm)22.2±2.9 23.0±2.4 29.3±3.4ab 38.3±4.3abc。15.208 0.000 LAD(mm)27.7±3.5 27.1±3.3 32.5±5.0ab 36.8±4.6abc 8.107 0.000 IVS(mm)8.8±1.9 9.1±1.6 10.2±1.4ab 11.4±1.6abc 56.036 0.000 LVEF(%)55.8±5.1 54.3±5.7 48.6±4.4ab 38.2±5.2abc 12.194 0.000
2.2 4組炎癥及氧化應激因子水平比較
4組間TNF-α、、IL-6、IL-1β、BNP 水平比較:對照組<A組<B組<C組,差異有統計學意義(P<0.05);T-AOC 水平比較:C組<B組<A組<對照組,差異有統計學意義(P<0.05)。見表2。
表2 4組炎癥及氧化應激因子水平比較(±s)Table2 Comparison of inflammation and oxidative stress factor levels in the 4 groups(±s)

表2 4組炎癥及氧化應激因子水平比較(±s)Table2 Comparison of inflammation and oxidative stress factor levels in the 4 groups(±s)
注:與對照組比較,aP<0.05;與A組比較,bP<0.05;與B組比較,cP<0.05。
組別對照組A組B組C組F值P值n 30 36 32 22 TNF-α(ng/L)2.2±0.6 4.6±1.2a 5.8±2.8ab 11.7±4.4abc 10.059 0.000 IL-6(pg/mL)61.9±14.4 80.8±25.9a 94.7±26.3ab 109.6±28.0abc 7.313 0.000 IL-1β(ng/L)497.6±87.2 602.4±91.1a 790.3±89.6ab 829.7±93.2abc 13.180 0.000 BNP(pg/mL)53.6±6.1 92.4±8.3a 136.4±10.2ab 310.8±16.6abc 39.322 0.000 T-AOC(IU/L)21.9±5.6 17.0±4.8a 11.5±4.5ab 7.4±1.3abc 13.688 0.000
2.3 4組CyP、GDF-15、IL-18水平比較
4組間CyP-A、CyP-B、GDF-15 水平比較:對照組<A組<B組<C組,差異有統計學意義(P<0.05);IL-18水平比較:C組<B組<A組<對照組,差異有統計學意義(P<0.05)。見表3。
表3 4組CyP、GDF-15、IL-18水平比較(±ss)Table3 Comparison of CyP,GDF-15,and IL-18 levels in the 4 groups(±ss)
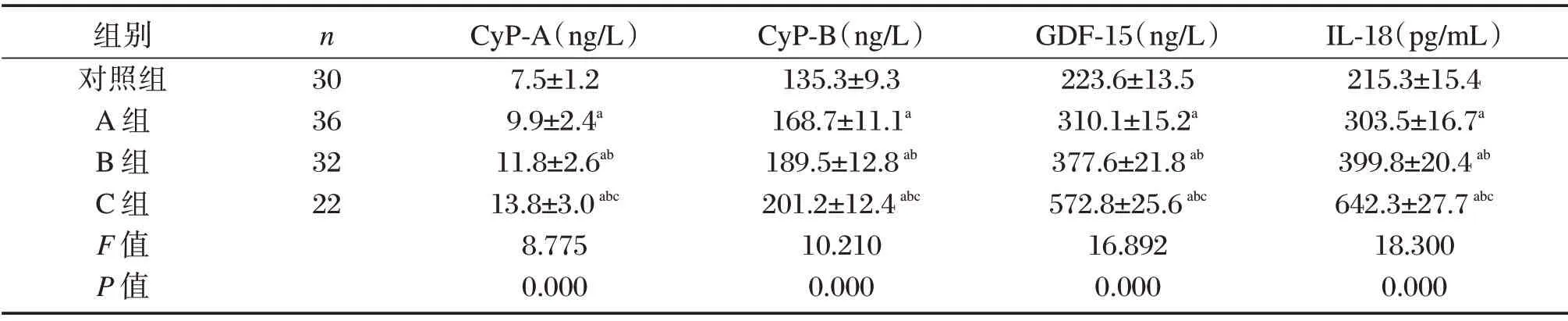
表3 4組CyP、GDF-15、IL-18水平比較(±ss)Table3 Comparison of CyP,GDF-15,and IL-18 levels in the 4 groups(±ss)
注:與對照組比較,aP<0.05;與A組比較,bP<0.05;與B組比較,cP<0.05。
組別對照組A組B組C組F值P值n 30 36 32 22 CyP-A(ng/L)7.5±1.2 9.9±2.4a 11.8±2.6ab 13.8±3.0abc 8.775 0.000 CyP-B(ng/L)135.3±9.3 168.7±11.1a 189.5±12.8ab 201.2±12.4abc 10.210 0.000 GDF-15(ng/L)223.6±13.5 310.1±15.2a 377.6±21.8ab 572.8±25.6abc 16.892 0.000 IL-18(pg/mL)215.3±15.4 303.5±16.7a 399.8±20.4ab 642.3±27.7abc 18.300 0.000
3 討論
高血壓可導致患者左心室負荷過大,心肌細胞受到腎素-血管緊張素-醛固酮系統(Renin-angiotensin-aldosterone system,RAAS)過度激活的影響,導致相關蛋白合成明顯增加,引發間質膠原增加及心肌細胞肥大,從而導致心臟收縮期和舒張末壓張力上升,心排血量降低,左心室功能受損[8]。在高血壓疾病進展中,炎性反應發揮重要作用[10]。TNF-α、IL-6、IL-1β 等均可由單核巨噬細胞產生,這些細胞因子異常激增可導致機體一系列的炎性反應及病理改變。研究表明[9],炎性因子可導致心肌細胞,血管平滑肌細胞及血管內皮細胞一氧化氮合酶(endothelial nitric oxide synthase,eNOS)活性及表達增加,局部NO 增多,NO 介導并降低兒茶酚胺的正性肌力作用,從而導致心肌細胞凋亡,促進心室重構。BNP 為心源性神經激素,其血清水平高低與心室壁張力、心室負荷存在密切關系,BNP是判斷左心室收縮功能不全的敏感指標。T-AOC反應了機體總抗氧化能力,其反映了局部炎癥因子水平及氧化應激水平。本研究中結果證實,炎癥細胞因子過度激活促進了高血壓患者心功能障礙的發生發展。
CyP-A、CyP-B 為CyP家族中較為重要的兩種,研究表明CyP-A、CyP-B 與機體細胞炎性因子及血管細胞因子存在密切關聯[10]。機體存在血管受損及氧化應激狀態時,可導致CyP-A、CyP-B 水平升高。CyP-A、CyP-B 升高進一步促進炎性因子聚集于病發部位,引發機體抗氧化能力降低,促進內皮細胞增殖并導致TNF-α、IL-6、IL-1β 等指標異常[11]。研究顯示[12],在心肌缺血、心肌壓力負荷過大及炎癥反應等情況下,心臟及血清中GDF-15 濃度迅速升高。GDF-15 可抑制細胞凋亡和心肌重塑,是心血管重要的保護因子。但研究還發現[13],GDF-15 在抗心肌細胞肥大的同時,也可促進心肌成纖維細胞增殖及膠原沉積。IL-18 可與其受體結合在機體免疫調節、抗感染、抗腫瘤等過程中發揮重要作用。研究指出[14],IL-18 可促進血管平滑肌細胞增殖、遷徙,引發血管重塑,促進高血壓及其并發癥的進展。近年來研究表明[15],IL-18 與心血管疾病發生發展相關。
本研究中結果提示CyP-A、CyP-B、GDF-15、IL-18 對于反應高血壓合并心功能不全患者疾病程度具有明顯價值。高血壓合并心功能不全患者心血管不良事件的發生風險明顯增大,患者發生心力衰竭導致的猝死率是正常人群的5倍[16]。通過相關指標檢測可提供高血壓患者心功能狀態診斷的準確性和全面性,為患者的預防、危險分層和預后評估提供重要依據。
綜上所述,高血壓合并心功能不全患者機體炎癥因子、CyP、GDF-15、IL-18水平明顯升高,并與心功能障礙程度存在明顯關系,臨床上應注意觀測CyP、GDF-15、IL-18水平變化,以預防和降低高血壓患者心功能損傷的發生。

