橄欖鹽胚表層析出物形成影響因素的研究
丘金輝 , 邱建清 , 周美齡 , 劉清培 , 曾紹校 *, 林少玲
(1.福建農林大學 食品科學學院,福建 福州 350000;2.福建省特種淀粉品質科學與加工技術重點實驗室,福建福州 350000;3.福州大世界橄欖有限公司,福建 福州350002)
橄欖[Canarium album(Lour.)Raeusch],也稱作青果或白欖,是著名的熱帶、亞熱帶特產果品之一[1],迄今已有兩千多年歷史。分布在中國的橄欖屬植物主要有7種,其中成熟果實為黃綠色的普通橄欖(福建)和果實成熟顯紫黑色的烏欖(廣東)[2-3]是人工種植最多的橄欖屬植物。福建省和廣東省是中國橄欖的主要產區[4],其中福建閩侯素有“中國橄欖之鄉”的美譽[5]。橄欖蜜餞是橄欖加工的主要產品,傳統的橄欖蜜餞加工都有鹽漬工序,但自2008年國標規定禁止橄欖蜜餞生產中使用明礬后,橄欖在鹽漬過程中表層極易析出一層灰白色物質,并會帶入橄欖蜜餞終產品中,嚴重影響產品的外觀品質和消費者的購買欲望。
果蔬在加工或貯藏過程中極易產生內源性析出物,表現形式主要為液體的沉淀析出物和固體表面附著物兩種。果蔬的內源性析出物的產生,不僅降低了產品的感官品質及商業價值,還會影響人們對營養物質的吸收。食品中內源性析出物一直是國內外研究的重點與難點,對食品內源性析出物的形成機理的分析研究是探索其控制技術的必不可少的環節之一。目前,國內外關于食品中內源性析出物的相關研究主要集中在蘋果、橙子、胡蘿卜等常見果蔬產品析出物、茶飲料和酒類沉淀析出物等方面[6]。有研究表明果蔬表層析出物主要是由于多酚及蛋白質等大分子相互作用引起,而影響多酚、蛋白質相互作用的因素主要包括多酚、蛋白質濃度及種類、pH、溫度、化學試劑(鹽、乙醇等)、氧氣等[7-8]。
作者比較“饒平”、“惠圓”、“長營”3 種橄欖的基本化學成分、礦質元素、多酚及可溶性蛋白質含量,分析析出物的前體物質;進一步分析橄欖多酚及可溶性蛋白與析出物的相關性和橄欖蜜餞鹽漬過程中pH、鹽(氯化鈉、氯化鈣及焦亞硫酸鈉)等外部環境因素對析出物形成的影響,探究析出物(濁度)與鹽漬液中多酚、可溶性蛋白的變化規律,為控制析出物提供科學的理論依據。
1 材料與方法
1.1 材料與試劑
新鮮橄欖:福建省福州大世界橄欖有限公司提供;牛血清白蛋白:購自Solarbio公司;考馬斯亮藍G-250:購自Beyotime公司;硫酸、焦亞硫酸鈉等常規試劑均為分析純級(AR)。
1.2 主要儀器
SX2-12-12型馬弗爐:上海雷韻實驗儀器制造有限公司產品;HR2104型多功能攪拌機:荷蘭皇家飛利浦電子公司產品;SKD-2000型自動凱式定氮儀:上海沛歐分析儀器有限公司產品;DK-S24型電熱恒溫水浴鍋:上海精宏實驗設備有限公司產品;WGZ-100型散射式光電濁度儀:上海精密儀器廠產品;PHS-3C型精密pH計:上海雷磁儀器廠產品。
1.3 試驗方法
1.3.1 橄欖樣品的前處理 挑選新鮮程度和個頭一致、中后期的“饒平”、“長營”、“惠圓”橄欖,清洗,每個品種的橄欖各自均分為兩部分,一部分去核,只留果肉和果皮;另一部分分離果皮與果肉后去核,得到無皮果肉和果皮。最后分別用果蔬攪拌機破碎并做好標記置于-20℃冰箱中冷凍保存。
1.3.2 橄欖基本化學成分的測定 橄欖水分的測定:參照GB5009.3-2010;橄欖灰分的測定:參照GB5009.4-2010;橄欖蛋白質的測定:參照
GB5009.5-2010;橄欖脂肪的測定:參照GB/T 5009.6-2003;橄欖淀粉的測定:參照GB/T 5009.9-2008;橄欖總酸的測定:參照GB/T 12456-2008;橄欖總糖的測定 采用蒽酮比色法[1]。
1.3.3 橄欖礦質元素的測定 用質量分數1%的硝酸溶液將 K、Ca、Na、Mg、Zn、Fe、Cu、Al和 Mn 標準儲備液(1 mg/mL)配置成 1 μg/mL 的 K、Ca、Na、Mg、Fe及 0.1 μg/mL 的 Cu,Zn、Al、Ba 的混合標準液。 稱取0.100 0 g樣品于消解罐,加濃HNO3冷消解48 h,再微波消解完全,用電爐蒸發至近干,得到的消化產物用質量分數2%的硝酸溶解并定容于50 mL的聚四氟乙烯材質的容量瓶。再按上述流程做空白對照。按表1的ICP-MS的工作條件參數測定預處理的樣品。
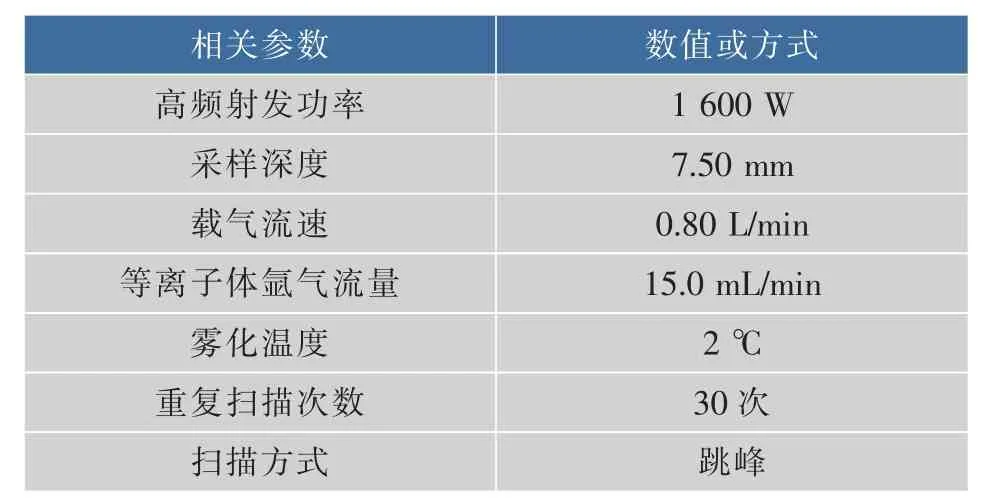
表1 ICP-MS工作條件參數Table 1 Operating condition of the ICP-MS
1.3.4 多酚的測定 參照王振宇等[9]的方法,稱1~2g的樣品于100 mL三角瓶,加入10倍體積的石油醚(30~60℃)去色素脫脂,再加體積分數40%丙酮達到1 g∶40 mL料液質量體積比,封口,搖1 min后在超聲清洗器(100 W,40℃)中處理60 min,取出倒出上清液并加入與第一次等體積的40%丙酮,再次提取,將兩次的提取液以及未溶解的物質合并到離心管中,常溫下4 200 r/min離心20 min,將上清液稀釋50倍,測765 nm處的吸光度。根據謝倩等[10-12]的多酚測定方法繪制沒食子酸標準曲線得到樣品多酚含量。
1.3.5 可溶性蛋白質的測定 稱樣3~4 g,加25 mL去離子水并于超聲波清洗機中處理60 min,設置參數為100 W,40℃,倒出上清液,再加入等量的去離子水再次提取,將2次提取液和未溶解的物質一起倒入離心管,4 200 r/min離心20 min,取上清液。再吸取 0.0、0.4、0.8、1.2、1.6、2.0 mL 的 1 mg/mL 牛血清白蛋白標準溶液于試管,分別加去離子水至2.0 mL。在另7支試管中各加0.1 mL以上溶液與5.0 mL考馬斯亮藍G-250,充分振蕩后靜置10 min,以第1管為對照,測595 nm處吸光值,繪制標準曲線。然后取樣液0.1 mL于試管中,重復以上操作。
1.3.6 橄欖鹽胚濁度測定 從鹽漬容器的上中下各取2顆橄欖,用去離子水輕輕沖洗掉表面食鹽,然后用200 mL離子水搓洗6顆橄欖表面,直至將肉眼可見的表面白色斑點,然后將溶液稀釋合適倍數,最后測定濁度。濁度越大表示析出物越多,橄欖鹽胚的穩定性越差;反之,則穩定性越好。濁度按以下公式計算:
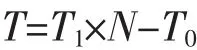
式中:T為最終濁度 (NTU);T1為溶液的測定濁度(NTU);N為溶液稀釋倍數;T0為純溶劑的初始濁度(NTU)。
1.3.7 橄欖多酚與可溶性蛋白質對析出物形成的影響 配置含177.8 g/L氯化鈉、2.5 g/L氯化鈣及12.5 g/L焦亞硫酸鈉的共混鹽漬液。將橄欖與鹽漬液1∶1倒入帶蓋PC桶,置于室溫,第2~3天調節鹽度至240.8 g/L,每2周測定橄欖鹽胚及鹽漬液的濁度、多酚及可溶性蛋白質含量。鹽漬液濁度測定參照1.3.6的方法。
1.3.8 不同鹽漬環境因素對析出物形成的影響
1)鹽漬pH對析出物形成的影響 配置1.3.7中的共混鹽漬液,用0.l mol/L的HCl和0.l mol/L NaOH溶液調節鹽漬液pH值。將橄欖與鹽漬液按質量體積比1 g∶1 mL倒入帶蓋PC桶,置于室溫,第2~3天調節鹽質量濃度至240.8 g/L,每2周測定橄欖鹽胚的濁度。
2)氯化鈉質量濃度對析出物形成的影響 配置含2.5 g/L氯化鈣及12.5 g/L焦亞硫酸鈉的共混鹽漬液,加氯化鈉,使氯化鈉在共混溶液中的初始質量濃度分別為 133.6、155.9、177.8、209.7 g/L。將橄欖與鹽漬液按1 g∶1 mL倒入帶蓋PC桶,置于室溫,第 2~3天調節鹽質量濃度分別至 217.5、229.1、240.8、252.7 g/L,每2周測定橄欖鹽胚的濁度。
3)焦亞硫酸鈉質量濃度對析出物形成的影響配置質量濃度177.8 g/L氯化鈉及2.5 g/L氯化鈣的共混鹽漬液,加入焦亞硫酸鈉,使焦亞硫酸鈉在共混溶液中的質量濃度分別為 10.0、12.5、15.0、17.5、20.0 g/L。將橄欖與鹽漬液按1 g∶1 mL倒入帶蓋PC桶,置于室溫,第2~3天調節鹽質量濃度至240.8 g/L,每2周測定橄欖鹽胚的濁度。
4)氯化鈣質量濃度對析出物形成的影響 配置質量濃度177.8 g/L氯化鈉及12.5 g/L焦亞硫酸鈉的共混鹽漬液,加入氯化鈣,使氯化鈣在共混溶液中的質量濃度分別為 0.00、1.5、2.5、3.5、4.5 g/L。將橄欖與鹽漬液以1 g∶1 mL倒入帶蓋PC桶,置于室溫,第2~3天調節鹽質量濃度至240.8 g/L,每2周測定橄欖鹽胚的濁度。
1.3.9 統計分析 所測結果均重復測定3次,取均值,試驗數據用SPSS 13.0統計分析軟件進行處理分析。
2 結果與分析
2.1 橄欖鹽胚表層析出物的前體物質分析
2.1.1 橄欖的基本化學成分分析 在鹽漬過程中,“饒平”欖比“惠圓”和“長營”欖更易產生析出物。蛋白質是析出物的主要成分之一,但從表2中可以看出100 g“饒平”欖可食部分(未去皮的果肉)的蛋白質質量為(1.05±0.08) g,與“長營”蛋白質含量差異不顯著,但顯著低于“惠圓”,說明“饒平”欖并不是因其蛋白質質量分數較高而產生析出物。根據許多研究表明,參與內源性析出物形成的蛋白質主要為可溶性蛋白質[14],推測析出物形成與蛋白質質量分數和種類有關。
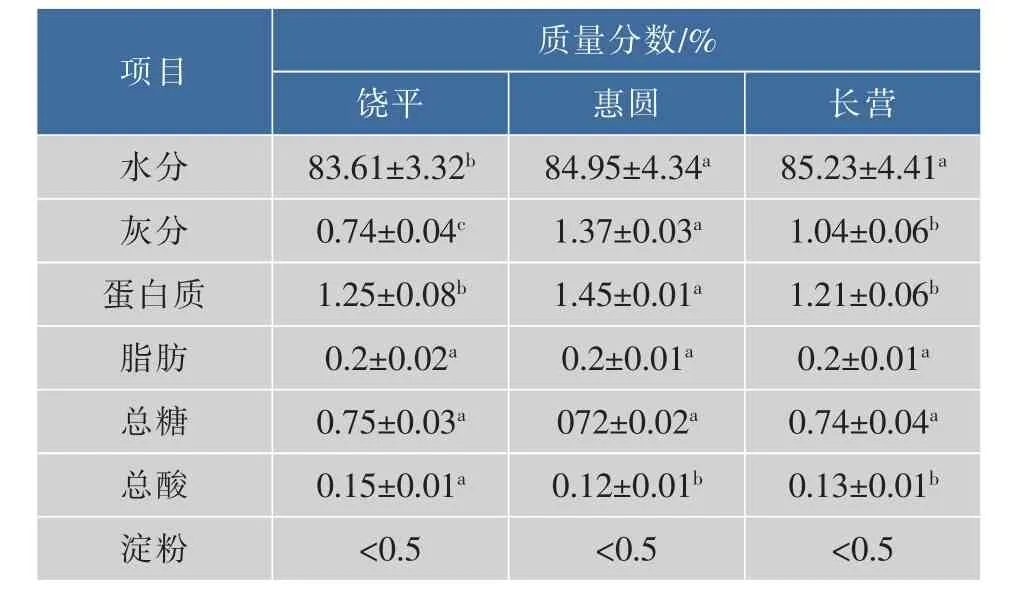
表2 不同品種橄欖基本化學組成Table 2 Main nutrient compositions of different varieties of Canarmm album L
2.1.2 橄欖礦物質元素 雖有研究表明析出物的主要成分不是難溶性鹽,但高價陽離子易與有機大分子絡合形成更大的復合物,此外尤其多酚具有多個酚羥基,可以作為多基配合體絡合金屬離子,且不同金屬離子與多酚的絡合強度不等,絡合強度為:Al3+>Zn2+>Fe3+>Mg2+>Ca2+[15],因此,作者測定了 3種橄欖可食部分的礦質元素。從表3中可以看出新鮮橄欖K元素質量分數高,但未見報道稱其能形成難溶絡合物。同時,測定的可能與大分子絡合形成復合物的金屬元素中,Ca質量分數最高,其中 “饒平”欖Ca含量與“惠圓”水平相當,顯著低于“長營”,表明橄欖本身礦質元素對析出物形成幾乎沒有影響或影響很小。

表3 不同品種橄欖礦質元素分析Table 3 Mineral compositions of different varieties of Canarmm album L
2.1.3 橄欖多酚與可溶性蛋白質質量分數
1)橄欖多酚質量分數 橄欖多酚是影響析出物生成的關鍵成分,從圖1中可以看出,“饒平”欖果皮的多酚質量分數達(26.75±0.35)mg/g、可食部分(未去皮的果肉)及純果肉的多酚質量分數也相對較高, 分別為 (18.02±0.54) mg/g、(12.61±0.41)mg/g,不論哪個部位的多酚質量分數都顯著高于“惠圓”與“長營”;同時,任意品種橄欖,其果皮部位的多酚質量分數都顯著高于可食部分及果肉。此外,“惠圓”的多酚質量分數整體稍高于“長營”,但“長營”果皮多酚質量分數反而比“惠圓”高。由此可見,橄欖多酚質量分數不僅與品種密切相關,也與其所在部位有關,可以通過去除橄欖果皮來控制析出物的形成。
2)橄欖可溶性蛋白質質量分數 目前,國內外關于食品中內源性析出物的相關研究主要集中在蘋果、橙子、胡蘿卜等常見果蔬產品析出物、茶飲料和酒類沉淀析出物等方面[6]。結果表明,許多果蔬沉淀析出物的形成都與其本身的可溶性蛋白質質量分數密切相關,表2顯示“饒平”欖總蛋白質質量分數同“長營”相當,且顯著低于“惠圓”,但從圖2可以看出“饒平”欖可食部分及果肉的可溶性蛋白質質量分數顯著高于“惠圓”與“長營”同部位可溶性蛋白質質量分數。
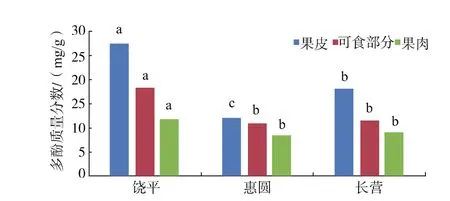
圖1 不同品種橄欖的多酚質量分數Fig.1 Polyphenolcontentsofdifferentvarietiesof Canarmm album L
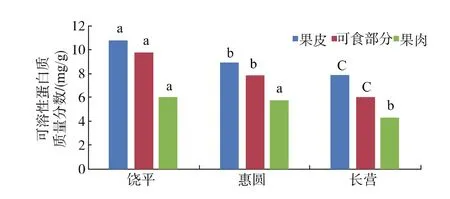
圖2 不同品種橄欖可溶性蛋白質質量分數Fig.2 Soluble protein contents of different varieties of Canarmm album L
2.2 橄欖多酚及可溶性蛋白質與橄欖鹽胚表層析出物的相關性分析
從表4可知,在橄欖鹽胚貯藏期間,橄欖鹽胚的多酚質量分數及可溶性蛋白質質量分數與鹽胚濁度和鹽漬液濁度呈極顯著負相關;從表中還可看出,鹽漬液中的多酚和可溶性蛋白質質量分數與橄欖鹽胚濁度分別呈極顯著正相關和顯著正相關,鹽漬液多酚與鹽漬液濁度為顯著正相關。因為在無氧條件下,多酚易通過氫鍵或疏水作用與可溶性蛋白形成可溶多酚-蛋白質復合物,并聚集可溶復合物形成不溶性化合物[16-17],若存在氧氣,則多酚會在多酚氧化酶作用下發生氧化反應,形成褐色聚合物[18]。
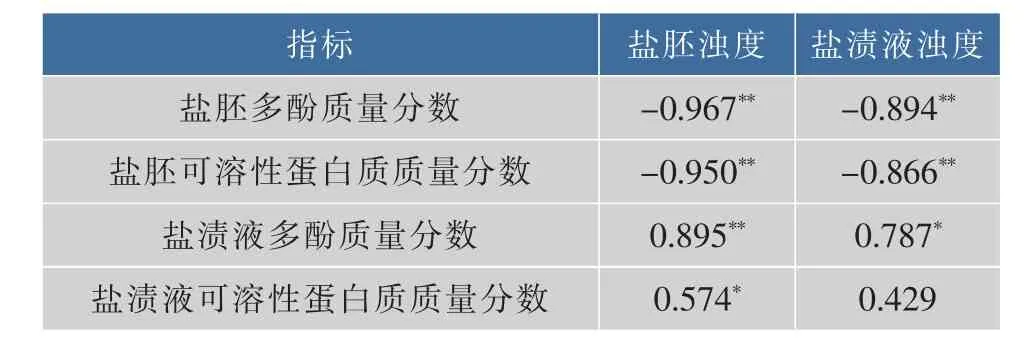
表4 橄欖鹽胚各項指標間的相關分析Table 4 Correlation analysis between the indexes of salted Chinese olive and salted solution
2.3 鹽漬環境因素對橄欖鹽胚表層析出物的影響
2.3.1 pH對橄欖鹽胚表層析出物的影響 圖3為橄欖鹽胚貯藏在不同pH值鹽漬液中濁度的變化情況。由圖可知,當鹽漬液初始pH值為2.25、2.35及2.50時,其貯藏期間濁度變化很小,未出現表層析出物;鹽漬液初始pH值為2.00及4.50時,出現了表層析出物;而鹽漬液初始pH值為3.50時,橄欖鹽胚在第4~6周時濁度增加最快,出現了表層析出物且程度最嚴重,其次是pH值為3.00時。pH影響WSSCO形成的機理是H+可以改變可溶性蛋白質的帶電狀態或所帶靜電荷數,從而影響蛋白質的疏水性,進而影響其與多酚的結合。以上結果說明pH值為3.00~3.50時多酚與蛋白質更容易相互作用形成沉淀析出物,這與綦菁華等多酚-蛋白相互作用影響因素的研究結果一致[7]。
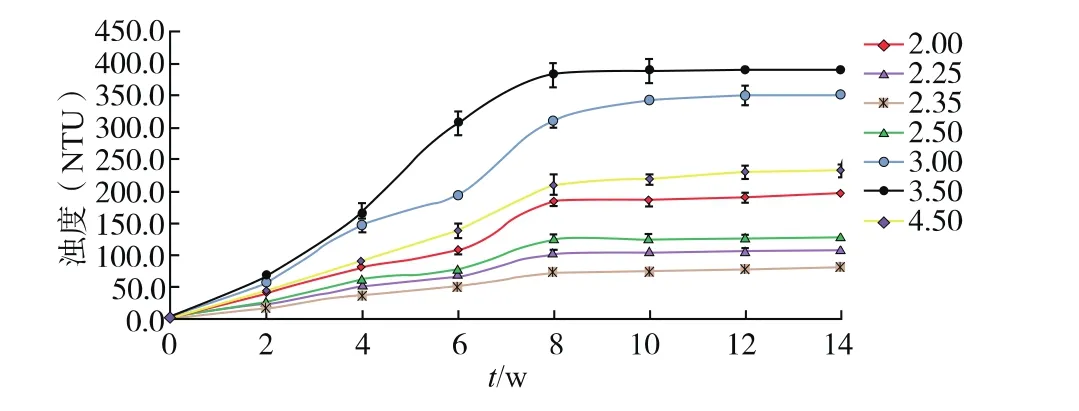
圖3 pH對橄欖鹽胚濁度的影響Fig.3 Effect of pH on turbidity of WSSCO
2.3.2 氯化鈉質量分數對析出物的影響 圖4為攪打橄欖浸泡在初始鹽度不同鹽漬液中濁度的變化情況。由圖可知,初始鹽度不同鹽漬液中橄欖鹽胚濁度的變化趨勢一致,即先逐漸上升,至第8周左右時趨于穩定。結果顯示,橄欖鹽胚濁度(即析出物)隨著初始氯化鈉質量分數的升高而降低。隨著氯化鈉質量分數升高,氯化鈉滲入量及橄欖多酚及可溶性蛋白滲出量增加,而高質量分數氯化鈉使得鹽漬液中蛋白質發生鹽析,從而降低了鹽漬液中易與多酚結合的可溶性蛋白質含量。但初始鹽質量分數過高易導致橄欖鹽胚干癟,因此,初始鹽漬液達到質量分數19%時,橄欖鹽胚開始出現皺縮。
2.3.3 焦亞硫酸鈉質量分數對析出物的影響 隨著焦亞硫酸鈉質量分數的提高,橄欖鹽胚濁度逐漸降低,當焦亞硫酸鈉質量分數達到1.75%時,貯藏期間橄欖鹽胚都未出現表層析出物(圖5)。原因可能是:一方面,作為良好的抗氧化劑和多酚氧化酶抑制劑,焦亞硫酸鈉可以有效防止鹽漬液及橄欖鹽胚中的多酚被氧化為鄰苯醌,形成褐色聚合物;另一方面,由于焦亞硫酸鈉可打斷蛋白質分子中二硫鍵,降低了蛋白質間的交聯度,改變了鹽漬液中蛋白質結構,從而可能導致可溶性蛋白質含量降低[19]。
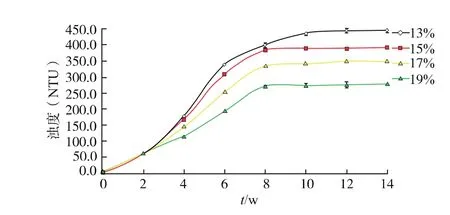
圖4 氯化鈉質量分數對橄欖鹽胚濁度的影響Fig.4 Effect of sodium chloride concentration on turbidity of WSSCO
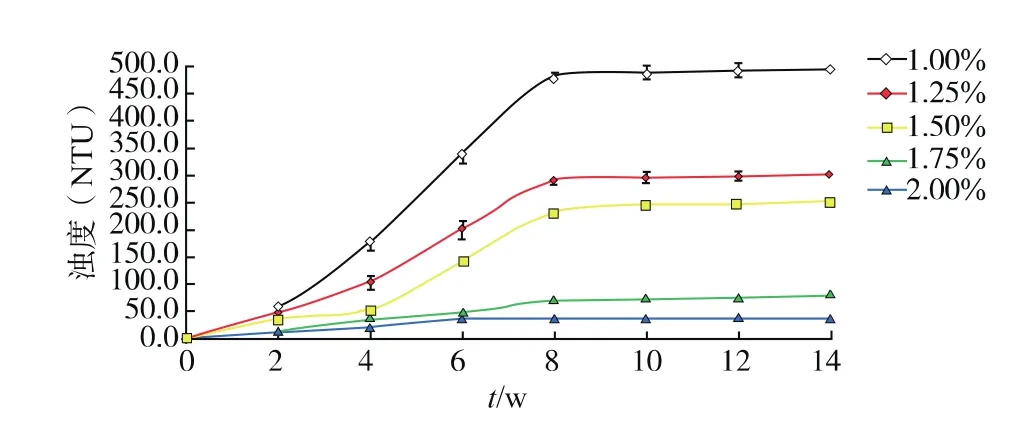
圖5 焦亞硫酸鈉質量分數對橄欖鹽胚濁度的影響Fig.5 Effect of sodium sulfite concentration on turbidity of WSSCO
2.3.4 氯化鈣質量分數對析出物的影響 圖6結果顯示,隨著氯化鈣質量分數的升高,橄欖鹽胚濁度出現小幅度上升,說明鹽漬液中氯化鈣質量分數低于0.25%時對析出物影響很小,高濃度的Ca2+則會促進析出物的形成,這可能是由于Ca2+與多酚的酚羥基絡合,形成低溶解度絡合物有關[20]。
3 結語
橄欖成分分析表明,“饒平”欖可食部分中主要成分和礦質元素的含量與穩定性較強的 “惠圓”與“長營”相比差異很小;但“饒平”欖多酚與可溶性蛋白含量顯著高于“惠圓”與“長營”,且同一品種橄欖不同部位的多酚與可溶性蛋白質含量差異顯著。表明橄欖本身的礦質元素對析出物形成影響很小,析出物的前體物質主要是多酚與可溶性蛋白質。
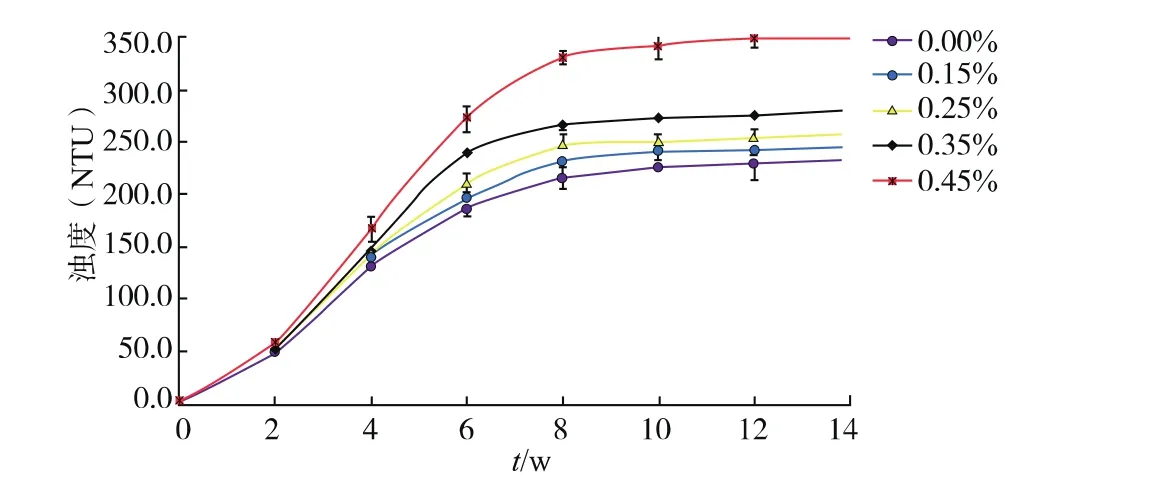
圖6 氯化鈣質量分數對橄欖鹽胚濁度的影響Fig.6 Effect of calcium chloride concentration on turbidity of WSSCO
橄欖鹽胚貯藏過程中多酚及可溶性蛋白質含量與其濁度相關性表明,橄欖鹽胚多酚及可溶性蛋白含量與橄欖鹽胚濁度(表層析出物)及鹽漬液濁度呈極顯著負相關,鹽漬液中多酚含量與橄欖鹽胚濁度(表層析出物)及鹽漬液濁度呈顯著正相關;橄欖鹽胚貯藏過程中多酚、可溶性蛋白質含量及濁度值的變化研究結果表明,析出物的形成主要是由于多酚與可溶性蛋白質相互作用所導致。
鹽漬環境不同因素對析出物形成影響的研究表明鹽漬液初始pH為2.25~2.50時,析出物最少;在初始pH為3.00~3.50的鹽漬液中最容易形成表層析出物;隨著氯化鈉質量分數的增大,橄欖鹽胚濁度呈降低趨勢,但實際生產氯化鈉初始質量分數一般超過19%;此外,結果顯示Ca2+不是引起析出物的主要因素,適量的氯化鈣可以提高橄欖鹽胚的硬度,但過量的氯化鈣對橄欖鹽胚析出物的形成有一定的促進作用;當鹽漬混合液中焦亞硫酸鈉質量分數高于1.75%,橄欖鹽胚未出現表層析出物。

