多排螺旋CT灌注成像聯合圖像三維重建技術定性診斷孤立性肺結節的價值▲
梁海勝 紀 律
(上海交通大學醫學院附屬第九人民醫院放射科,上海市 201999,電子郵箱:lycghxb@163.com)
孤立性肺結節是早期轉移瘤或周圍型肺癌的表現形式,指在肺部單發、球形、邊界清楚、直徑≤3 cm,周圍完全由充氣的肺組織包繞,不伴肺不張、肺門淋巴結腫大和胸腔積液的病變[1]。早期診斷孤立性肺結節并判斷其良惡性,對后續臨床治療方案的選擇以及改善患者的預后具有重要意義,但其良惡性的鑒別一直是困擾臨床醫生的難題,目前國內尚無統一的鑒別標準[2-3]。多排螺旋CT參數如增強峰值、血容量和表面通透性均能反映惡性組織的病變情況,但單靠一種征象難以判斷結節的良惡性[4]。隨著計算機技術的發展,計算機輔助診斷技術尤其是圖像三維重建技術的開發和應用,提高了孤立性肺結節的診斷準確性,但仍存在一定局限性[5]。本研究比較多排螺旋CT灌注成像、圖像三維重建技術以兩者聯合定性診斷孤立性肺結節的效能,旨在為提高孤立性肺結節的診斷準確性提供參考。
1 資料與方法
1.1 臨床資料 選擇2015年1月至2017年1月我院收治的100例孤立性肺結節患者作為研究對象,其中男性68例,女性32例,年齡56~73(62.65±7.28)歲。納入標準:(1)均經胸部X線片或CT證實存在孤立性肺結節,并經病理檢查確診;(2)患者的臨床病歷資料完整;(3)患者未經放化療治療;(4)患者了解本研究流程。排除標準:(1)嚴重心腦肝腎等器質性病變者;(2)無法進行影像學檢查者;(3)對本研究相關藥物過敏者;(4)依從性差,無法完成隨訪者。本研究經醫院倫理委員會審查通過,所有患者均對本研究知情同意,自愿參加。
1.2 方法
1.2.1 多排螺旋CT灌注成像:(1)掃描方法。掃描儀器為飛利浦 Brilliance 128排256層iCT,管電壓和電流分別設置為120 kV和150 mA。首先對胸部進行平掃,待明確結節的具體位置后,選擇灌注范圍為5 mm×8層,灌注范圍應覆蓋整個結節。采用非離子造影劑碘海醇作為對比劑(濃度為320 mg/mL),并用高壓注射器經右前臂靜脈埋置的套管針注入對比劑(速度為3.0 mL/s)。5 s后,在患者屏氣最大時進行掃描,前期掃描維持30 s,暫停5 s,后期掃描20 s。(2)圖像處理。采用飛利浦工作站對圖像進行后處理,首先設定空氣及骨的CT值范圍,輸入動脈選擇與結節同一層面的大血管,在孤立性肺結節最大橫截面處選擇感興趣區,同時避開灶內鈣化、空洞,以及灶周圍的臨近血管,最后計算病變部位的增強峰值、血容量、表面通透性和灌注峰值時間。
1.2.2 圖像三維重建:(1)掃描方法同多排螺旋CT灌注成像。(2)三維重建技術及圖像處理。在飛利浦工作站內進行容積再現、多平面重建、最大密度投影、最小密度投影和表面遮蓋顯示。通過調整以上參數和位置,多角度反復觀察孤立性肺結節的形態、邊界特點及其與血管、胸膜的關系。調整對比度和亮度,獲得圖像的最佳觀察視角。將所得圖像傳輸至影像歸檔和通信系統,由兩名經驗豐富的放射科副主任醫師按照雙盲的原則進行閱片,判斷并記錄有無分葉征和血管集束征。
1.2.3 診斷標準:將隨訪結果和病理檢查結果作為孤立性肺結節的臨床診斷標準(金標準),其中良性結節25例,惡性結節75例。多排螺旋CT灌注成像中,如每分鐘血容量≥5 mL/100 g或每分鐘表面通透性≥20 mL/100 g或增強峰值>20 HU,則診斷為孤立性肺結節;三維重建圖像以存在分葉征和血管集束征為診斷征象,具備其中1項,則診斷為孤立性肺結節。由兩名具有多年閱片經驗的副主任醫師做出診斷(Kappa檢驗值大于0.85),如出現意見不一致時共同討論得出結果。
1.3 統計學分析 采用SPSS 19.0軟件進行統計分析。計數資料以例數和率表示,比較采用χ2檢驗;計量資料以(x±s)表示,比較采用t檢驗或t′檢驗。采用非條件多因素Logistic回歸模型分析孤立性肺結節與CT參數之間的相關性。采用受試者工作特征(receiver operating characteristic,ROC)曲線分析增強峰值、血容量、表面通透性、分葉征、血管集束征以及所有指標聯合診斷孤立性肺結節良惡性的價值,采用z檢驗比較ROC曲線下面積。以P<0.05為差異有統計學意義。
2 結 果
2.1 良惡性孤立性肺結節的螺旋CT參數比較 良性孤立性肺結節的增強峰值、血容量、表面通透性均低于惡性孤立性肺結節,灌注峰值時間長于惡性孤立性肺結節患者(均P<0.05),見表1。
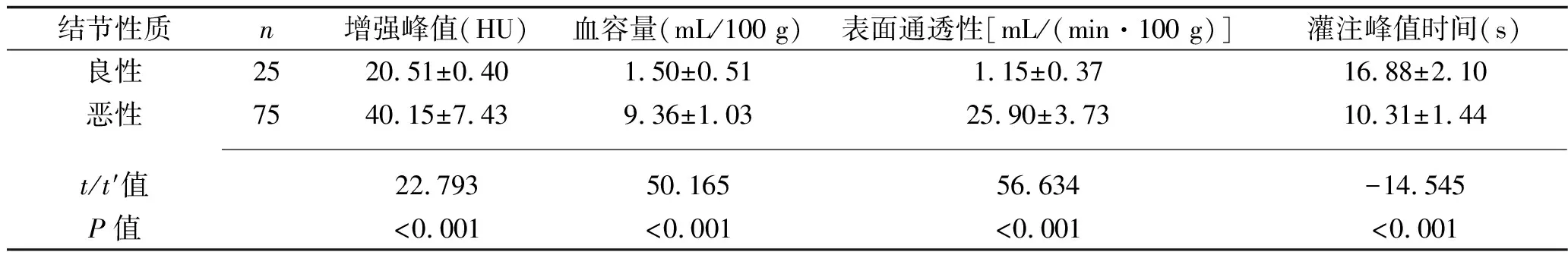
表1 良惡性孤立性肺結節的螺旋CT參數比較(x±s)
2.2 螺旋CT參數和三維重建圖像特征與良惡性孤立性肺結節的相關性 以孤立性肺結節的良惡性情況作為因變量,以螺旋CT參數增強峰值、血容量、表面通透性、灌注峰值時間,以及三維重建圖像特征分葉征和血管集束征作為自變量,納入非條件多因素Logistic回歸模型中進行分析,變量賦值情況見表2。結果顯示,增強峰值、血容量、表面通透性、分葉征、血管集束征均與惡性孤立性肺結節相關(均P<0.05),見表3。

表2 變量賦值情況

表3 良惡性孤立性肺結節與螺旋CT參數的相關性
2.3 多排螺旋CT灌注成像各參數、三維重建技術各參數及其聯合診斷惡性孤立性肺結節的效能 增強峰值、血容量、表面通透性、分葉征、血管集束征五者聯合診斷惡性孤立性肺結節的敏感性、特異性和準確率分別為97.4%、91.3%、96.0%,均高于單一指標。ROC分析結果顯示,各指標聯合診斷惡性孤立性肺結節的曲線下面積最大。見表4~5及圖1。

表4 各個指標診斷良惡性孤立性肺結節結果(n)

表5 各指標診斷惡性孤立性肺結節的診斷效能

圖1 各指標單獨或聯合診斷惡性孤立性肺結節的ROC曲線
3 討 論
孤立性肺結節是圓形或近似圓形的病灶,由于其體積較小,且影像特征缺乏特異性,導致難以定性診斷,容易延誤治療,嚴重影響患者的預后,因而早期診斷至關重要[6]。CT灌注成像的原理是通過靜脈注射造影劑來實現CT增強,隨后進行連續動態掃描以觀察微血管的分布和血流灌注,從而對組織狀況進行判斷[7]。CT檢查可通過橫斷面成像顯示患者大氣道結構,多層螺旋CT灌注成像具有圖像質量穩定、清晰度高、分辨率高、信噪比低等特點,能夠彌補常規CT無法應用于層厚大、掃描速度提升難的弊端。但是CT軸位掃描只能通過計算層厚和層數得出孤立性肺結節的高度,無法顯示周圍血管,因而無法對孤立性肺結節的形態及其與周圍血管的關系進行判斷[8]。圖像三維重建技術可將傳統的二維圖像轉化為三維立體形態學,能夠更清晰地顯示肺結節的形態,為臨床診斷提供更多依據,但該方法常需結合其他方法使用,以顯示病變結構的細微變化,具有一定的局限性。
血容量是指某一區域各血管中血液體積的總和,用于反映血液灌注流量,受血管直徑和毛細血管數量影響較大[9]。增強峰值為選擇區域在灌注時間內所計算出的面積,反映的是掃描時間內感興趣區CT值變化范圍的面積,與局部病變惡化程度和微血管的數量相關[10]。表面通透性可以用來反映局部微血管內皮細胞的完整性和細胞壁的通透性。灌注峰值時間可反映造影劑在局部的擴散速度,與靶組織的血管結構相關[11]。本研究結果顯示,良性孤立性肺結節的增強峰值、血容量、表面通透性均低于惡性結節,灌注峰值時間大于惡性結節(均P<0.05)。分析其原因可能為:肺組織惡性病變部位能夠引起支氣管動脈彎曲、支氣管和微血管數量增加,因此通透性增加,故惡性組織增強峰值、血容量、表面通透性較高。理論上,良惡性組織的灌注峰值時間應該有差異,但本研究多因素分析結果顯示,灌注峰值時間與孤立性肺結節的良惡性無相關性,可能是因為灌注峰值時間也與心排血量和循環相關,而本研究未考慮不同患者之間心排血量和循環功能的差異,因此該結論仍需進一步研究探討。此外ROC曲線分析顯示,多排螺旋CT參數增強峰值、血管容量、表面通透性在良惡性孤立性肺結節的鑒別診斷中均有一定的價值。
分葉征指因惡性病變組織向外周的增生速度不一而導致的多個弧形拱起。血管集束征是一支或多支到達腫塊內部或腫塊邊緣的血管,在三維圖上顯示為多支血管集中于惡性病變組織[12]。本研究ROC曲線分析結果顯示,分葉征和血管集束征對惡性孤立性肺結節均有一定的診斷價值。而相比于單個檢測方法,多排螺旋CT灌注成像參數聯合圖像三維重建參數診斷惡性孤立性肺結節的曲線下面積、靈敏度、特異性和準確性均最大。一方面,多排螺旋CT通過擴大實際掃描范圍能夠有效地減輕容積效應,減少層漏的發生,通過掃描可提高縱軸分辨率,清晰地分辨結節病灶與肺部支氣管[13]。另一方面,三維重建技術可以進行多角度、多層面的立體觀察,其中容積再現可實現三維空間關系,進而充分地顯示孤立性肺結節的形態學特征;多平面重建可通過任意角度全面反映孤立性肺結節的征象及其與周圍組織的相關性;最大密度投影可以完整地展示局部惡變組織供血血管走向;最小密度投影則能更好地顯示支氣管形態及氣道內情況[14-16]。因此,多排螺旋CT灌注成像聯合圖像三維重建技術能夠更靈敏、特異、準確地分辨良惡性孤立性肺結節。
綜上所述,多排螺旋CT灌注成像參數以及三維重建圖像征象在孤立性肺結節的定性診斷中均有一定的應用價值,但兩種技術聯合時,定性診斷的敏感度、特異度和準確性更高。

