一測多評法同時測定芒果止咳片中6種藥效成分的含量
梁梓敏 覃潔萍 郭海姣 羅宇東 胡華

摘 要 目的:建立同時測定芒果止咳片中沒食子酸、原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷含量的方法。方法:采用高效液相色譜法。色譜柱為Phenomenex Gemini C18,流動相為0.1%磷酸水溶液-乙腈(梯度洗脫),流速為1.0 mL/min,檢測波長為258 nm,柱溫為30 ℃,進(jìn)樣量為5 μL。以沒食子酸為內(nèi)參物,計(jì)算原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷的相對校正因子,并將一測多評法與外標(biāo)法測定結(jié)果進(jìn)行比較。結(jié)果:沒食子酸、原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷檢測質(zhì)量濃度的線性范圍分別為45.75~1 830 μg/mL(r=0.999 9)、2.525~101.0 μg/mL(r=0.999 9)、65.33~2 613 μg/mL(r=0.999 6)、9.058~362.3 μg/mL(r=0.999 9)、3.885~155.4 μg/mL(r=0.999 9)、1.870~74.8 μg/mL(r=0.999 9);定量限分別為0.571、0.643、1.053、0.854、0.830、1.500 μg/mL,檢測限分別為0.171、0.193、0.316、0.256、0.249、0.450 μg/mL;精密度、穩(wěn)定性、重復(fù)性試驗(yàn)RSD均小于3%;加樣回收率分別為 98.8%~101.9%(RSD=1.3%,n=6)、94.3%~101.5%(RSD=3.3%,n=6)、97.9%~100.5%(RSD=0.9%,n=6)、98.2%~101.6%(RSD=1.2%,n=6)、102.3%~106.1%%(RSD=1.3%,n=6)、 96.6%~99.3%(RSD=1.0%,n=6)。以沒食子酸為內(nèi)參物,原兒茶酸、芒果苷、高芒果苷、金絲桃苷、異槲皮苷的相對校正因子分別為0.568 3、0.500 3、0.687 6、0.939 1、0.826 3;一測多評法測得原兒茶酸等5種成分的含量范圍分別為0.197~0.440、3.263~11.250、0.201~1.196、0.168~0.381、0.115~0.293 mg/片,外標(biāo)法測得的含量范圍分別為0.198~0.441、3.329~11.570、0.206~1.194、0.171~0.380、0.119~0.298 mg/片,兩種方法測量結(jié)果的相對誤差為-3.80%~0.74%,且差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。結(jié)論:所建一測多評含量測定方法準(zhǔn)確、可靠、重復(fù)性好,可用于同時測定芒果止咳片中6種藥效成分的含量。
關(guān)鍵詞 芒果止咳片;高效液相色譜法;一測多評法;沒食子酸;原兒茶酸;芒果苷;高芒果苷;金絲桃苷;異槲皮苷;含量測定
ABSTRACT? ?OBJECTIVE: To establish a method for simultaneous determination of gallic acid, protocatechuic acid, mangiferin, homomangiferin, hyperoside and isoquercetin in Mangguo zhike tablets. METHODS: HPLC was adopted. The determination was performed on Phenomenex Gemini C18 column with mobile phase consisted of 0.1% phosphoric acid water solution-acetonitrile (gradient elution) at the flow rate of 1.0 mL/min. The detection wavelength was set at 258 nm. The column temperature was set at 30 ℃, and sample size was 5 μL. Gallic acid was used as the internal substance, and the correction factors of gallic acid, protocatechuic acid, mangiferin, homomangiferin, hyperoside and isoquercetin were calculated; the results of quantitative analysis of multi-components by single marker method (QAMS) were compared with those of external standard method (ESM). RESULTS: The linear range of gallic acid, protocatechuic acid, mangiferin, homomangiferin, hyperoside and isoquercetin were 45.75-183 0 μg/mL(r=0.999 9), 2.525-101.0 μg/mL(r=0.999 9), 65.33-261 3 μg/mL(r=0.999 6), 9.058-362.3 μg/mL(r=0.999 9), 3.885-155.4 μg/mL(r=0.999 9), 1.870-74.8 μg/mL(r=0.999 9), respectively. The limits of quantification were 0.571, 0.643, 1.053, 0.854, 0.830, 1.500 μg/mL, respectively. The limits of detection were 0.171, 0.193, 0.316, 0.256, 0.249, 0.450 μg/mL, respectively. RSDs of precision, stability and reproducibility tests were all lower than 3%. The average recoveries were 98.8%-101.9%(RSD=1.3% ,n=6), 94.3%-101.5%(RSD=3.3%,n=6), 97.9%-100.5%(RSD=0.9%,n=6), 98.2%- 101.6%(RSD=1.2%,n=6), 102.3%-106.1% (RSD=1.3%,n=6), 96.6%-99.3% (RSD=1.0%,n=6), respectively. RCFs of protocate-chuic acid, mangiferin, homomangiferin, hyperoside and isoquercetin were 0.568 3, 0.500 3, 0.687 6, 0.939 1 and 0.826 3, using gallic acid as internal substance. The content ranges of protocatechuic acid and other 4 com- ponents measured by QAMS were 0.197-0.440, 3.262-11.250, 0.201-1.196, 0.168-0.381, 0.115-0.293 mg/tablet, respectively. The content ranges measured by ESM were 0.198-0.441, 3.239-11.570, 0.206-1.194, 0.171-0.380, 0.119-0.298 mg/tablet, respectively. By comparing the content determination results by QAMS and ESM, the relative errors were -3.80%-0.74%, and there was no statistical significance (P>0.05).? CONCLUSIONS: The established QAMS method is accurate, reliable and repeatable, and can be used for content determination of 6 medicinal components in Mangguo zhike tablets.
KEYWORDS? ?Mangguo zhike tablets; HPLC; Quantitative analysis of multi-components by single marker method; Gallic acid; Protocatechuic acid; Mangiferin; Homomangiferin; Hyperoside; Isoquercetin; Content determination
芒果止咳片是由芒果葉干浸膏、魚腥草素鈉、馬來酸氯苯那敏制成的中西藥復(fù)方制劑,具有宣肺化痰、止咳平喘的功效,臨床上用于治療咳嗽、氣喘、多痰等癥[1]。現(xiàn)代研究表明,芒果止咳片中的主要原料藥芒果葉具有平喘、止咳、祛痰[2]、抗腫瘤[3]、護(hù)肝[4]等藥理活性。目前,芒果止咳片的質(zhì)量標(biāo)準(zhǔn)參照《國家藥品標(biāo)準(zhǔn)》[5],但該標(biāo)準(zhǔn)僅有理化鑒別方法,未對其相關(guān)成分含量進(jìn)行質(zhì)量控制。近年來,雖然有研究對芒果止咳片中芒果苷、魚腥草素鈉、馬來酸氯苯那敏的含量進(jìn)行了報(bào)道[6-8],但由于芒果葉浸膏成分復(fù)雜,其主要化學(xué)成分除芒果苷外,還有高芒果苷、金絲桃苷、異槲皮苷等黃酮類成分,沒食子酸、原兒茶酸等酚酸類成分及揮發(fā)油[9-10]。有研究發(fā)現(xiàn),沒食子酸、原兒茶酸具有抗炎[11]、抑菌[12]等作用;芒果苷、高芒果苷具有祛痰、止咳[13]、抑制哮喘[14]、抗炎[15]、抑菌[16]等作用;金絲桃苷具有抗炎、鎮(zhèn)痛、止咳[17]、抗氧化[18]等作用,異槲皮苷具抗炎、抑菌、抗病毒等作用[19];以上6種成分均為芒果止咳片的主要藥效成分,因此單一成分的定量檢測無法全面評價(jià)其質(zhì)量。
中藥制劑發(fā)揮療效是多成分、多靶點(diǎn)共同作用的結(jié)果,近年來多指標(biāo)成分的測定已成為中藥質(zhì)量評價(jià)的發(fā)展趨勢之一[20],但多種成分含量測定會增加對照品的消耗量,加之部分對照品存在價(jià)格昂貴、制備困難、不穩(wěn)定或難以獲得的問題,從而導(dǎo)致檢測成本增加。一測多評法(QAMS)是針對上述問題而開發(fā)的一種測量方法[21],該方法只需要1~2個對照品就能實(shí)現(xiàn)對多個成分的同時檢測,近年來已廣泛應(yīng)用于中藥及其制劑的質(zhì)量控制[22-23]。基于此,本研究采用QAMS法同時測定芒果止咳片中沒食子酸、原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷等6種成分的含量;以沒食子酸為內(nèi)標(biāo),計(jì)算其他5種成分的相對校正因子(f),并將QAMS法測定結(jié)果與外標(biāo)法(ESM)測定結(jié)果進(jìn)行比較,旨在為完善其質(zhì)量標(biāo)準(zhǔn)提供參考。
1 材料
1.1 儀器
1260 型高效液相色譜(HPLC)儀,包括紫外檢測器、C0107色譜工作站(美國Agilent公司);e2695型HPLC儀,包括二極管陣列檢測器、Empower 3色譜工作站(美國Waters公司);KQ5200B型超聲波清洗器(昆山市超聲儀器有限公司);CPA225D型十萬分之一電子分析天平[賽多利斯科學(xué)儀器(北京)有限公司];TGL-16G型離心機(jī)(上海安亭科學(xué)儀器廠);HWS-26型電熱恒溫水浴鍋(上海一恒科學(xué)儀器有限公司)。
1.2 藥品與試劑
11批芒果止咳片(廣西中醫(yī)藥大學(xué)制藥廠,批號:20161201、20161202、20170304、20170401、20170501、20170901、20180601、20180602、 20180701、20180702、20181001,規(guī)格:每片相當(dāng)于原藥材2.5 g);芒果葉對照藥材(批號:121507-200501)、沒食子酸對照品(批號:110831-201605,供含量測定用)、原兒茶酸對照品(批號:110809-201205,純度:≥99.9%)均購自中國食品藥品檢定研究院;高芒果苷對照品(批號:ST216701,純度:≥98%)、金絲桃苷對照品(批號:ST008801,純度:≥98%)、異槲皮苷對照品(批號:ST114401,純度:≥98%)均購自上海詩丹德標(biāo)準(zhǔn)技術(shù)服務(wù)有限公司;芒果苷對照品(批號:wkq18050201,純度:≥98%)購自四川維克奇生物科技有限公司;乙腈為色譜純,甲醇為分析純,水為超純水。
2 方法與結(jié)果
2.1 色譜條件
色譜柱:Phenomenex Gemini C18(250 mm ×4.6 mm,5 μm);流動相:0.1%磷酸水溶液(A)-乙腈(B),梯度洗脫(0~10 min,5%B→7%B;10~20 min,7%B→11%B;20~25 min,11%B→13%B;25~40 min,13%B→16%B;40~50 min,16%B→20%B;50~60 min,20%B→25%B;60~70 min,25%B→35%B;70~75 min,35%B);流速:1.0 mL/min;檢測波長:258 nm;柱溫:30 ℃;進(jìn)樣量:5 μL。
2.2 溶液的制備
2.2.1 混合對照品溶液的制備 分別取沒食子酸、原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷對照品適量,精密稱定,加70%甲醇溶解,制成上述6種成分質(zhì)量濃度分別為1.830 0、0.101 0、2.613 0、0.362 3、0.155 4、0.074 8 mg/mL的混合對照品溶液。
2.2.2 供試品溶液的制備 取芒果止咳片20片,去糖衣,研細(xì),取粉末0.3 g,精密稱定,加70%甲醇25 mL,超聲(功率:200 W,頻率:40 kHz,下同)處理40 min,濾過,殘?jiān)?0%甲醇25 mL,超聲處理40 min,濾過,合并濾液,水浴揮干,殘?jiān)?0%甲醇復(fù)溶并定容至10 mL量瓶中,搖勻,以13 000 r/min離心10 min,取上清液,即得供試品溶液。
2.2.3 陰性溶液的制備 按處方工藝制備缺芒果葉的陰性樣品,按“2.2.2”項(xiàng)下方法制備陰性溶液。
2.3 系統(tǒng)適用性試驗(yàn)
分別取“2.2”項(xiàng)下混合對照品溶液、供試品溶液(批號:20180601)和陰性溶液適量,按“2.1”項(xiàng)下色譜條件進(jìn)樣測定,記錄色譜圖。結(jié)果,混合對照品溶液與供試品溶液在相同保留時間處均有相應(yīng)的色譜峰出現(xiàn),各色譜峰分離較好;陰性溶液在相應(yīng)保留時間處沒有色譜峰出現(xiàn),且對測定無干擾;理論板數(shù)以金絲桃苷峰計(jì)不低于120 000,詳見圖1。
2.4 線性關(guān)系考察
取“2.2.1”項(xiàng)下混合對照品溶液0.125、0.5、1.0、2.0、4.0 mL,分別置于5 mL量瓶中,加70%甲醇稀釋至刻度,得到5個不同質(zhì)量濃度的混合對照品溶液,另取 “2.2.1”項(xiàng)下混合對照品溶液(共6種不同質(zhì)量濃度的溶液),按“2.1”項(xiàng)下色譜條件進(jìn)樣測定,記錄峰面積。以各待測成分質(zhì)量濃度(x,μg/mL)為橫坐標(biāo)、峰面積(y)為縱坐標(biāo)進(jìn)行線性回歸,結(jié)果見表1。
2.5 定量限與檢測限考察
取“2.2.1”項(xiàng)下混合對照品溶液適量,加70%甲醇逐級稀釋,按“2.1”項(xiàng)下色譜條件進(jìn)樣測定,記錄峰面積,分別以信噪比10 ∶ 1、3 ∶ 1計(jì)算定量限、檢測限。結(jié)果,沒食子酸、原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷的定量限分別為0.571、0.643、1.053、0.854、0.830、1.500 μg/mL,檢測限分別為0.171、0.193、0.316、0.256、0.249、0.450 μg/mL。
2.6 精密度試驗(yàn)
取“2.2.1”項(xiàng)下混合對照品溶液1.25 mL,置于5 mL量瓶中,加70%甲醇稀釋并定容,按“2.1”項(xiàng)下色譜條件連續(xù)進(jìn)樣測定6次,記錄峰面積。結(jié)果,沒食子酸、原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷峰面積的RSD分別為0.17%、0.18%、0.19%、0.22%、0.17%、0.27%(n=6),表明儀器精密度良好。
2.7 穩(wěn)定性試驗(yàn)
取“2.2.2”項(xiàng)下供試品溶液(批號:20180601)適量,分別于室溫下放置0、2、4、8、12、24 h時,按“2.1”項(xiàng)下色譜條件進(jìn)樣測定,記錄峰面積。結(jié)果,沒食子酸、原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷峰面積的RSD分別為0.29%、0.76%、0.32%、0.48%、0.70%、2.00%(n=6),表明供試品溶液于室溫下放置24 h內(nèi)穩(wěn)定性良好。
2.8 重復(fù)性試驗(yàn)
精密稱取芒果止咳片(批號:20180601)粉末,共6份,每份0.3 g,按“2.2.2”項(xiàng)下方法制備供試品溶液,再按“2.1”項(xiàng)下色譜條件進(jìn)樣測定,記錄峰面積并按標(biāo)ESM法計(jì)算樣品含量。結(jié)果,沒食子酸、原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷的平均含量分別為4.823、0.226 9、10.89、1.198、0.381 3、0.183 6 mg/片,RSD分別為0.39%、0.33%、0.59%、0.50%、1.70%、2.30%(n=6),表明本方法重復(fù)性良好。
2.9 加樣回收率試驗(yàn)
取已知含量的芒果止咳片粉末(批號:20180601)0.15 g,共6 份,分別精密加入含沒食子酸 0.953 6 mg/mL、原兒茶酸0.049 0 mg/mL、芒果苷2.187 mg/mL、高芒果苷0.130 0 mg/mL、金絲桃苷 0.070 0 mg/mL、異槲皮苷0.050 0 mg/mL的混合對照品溶液3 mL,按“2.2.2”項(xiàng)下方法制備供試品溶液,再按“2.1”項(xiàng)下色譜條件進(jìn)樣測定,記錄峰面積并計(jì)算加樣回收率,結(jié)果見表2。
2.10 相對校正因子的測定
2.10.1 不同質(zhì)量濃度混合對照品溶液的相對校正因子 取“2.2.1”項(xiàng)下混合對照品溶液0.5、1.0、2.0、3.0、4.0 mL,分別置于5 mL量瓶中,加70%甲醇稀釋至刻度,得5個不同質(zhì)量濃度的混合對照品溶液,另取 “2.2.1”項(xiàng)下混合對照品溶液(共6種不同質(zhì)量濃度的溶液),按“2.1”項(xiàng)下色譜條件進(jìn)樣測定,記錄峰面積。重復(fù)測定3次。以沒食子酸峰為內(nèi)參峰(S),分別計(jì)算原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷相對于沒食子酸的相對校正因子(fk/s),fk/s=(As×Ci)/(Cs×Ai),式中As為內(nèi)參物對照品峰面積,Cs為內(nèi)參物對照品質(zhì)量濃度,Ai為待測成分峰面積,Ci為待測成分質(zhì)量濃度。計(jì)算結(jié)果見表3。結(jié)果,不同質(zhì)量濃度混合對照品溶液中各成分相對校正因子的RSD均小于2.5%,提示在不同質(zhì)量濃度范圍內(nèi)各成分質(zhì)量濃度變化對其相對校正因子基本無影響。
2.10.2 不同色譜柱的相對校正因子 分別考察不同色譜柱[Phenomenex Gemini C18(250 mm×4.6 mm,5 μm)、Waters SunFireR C18(250 mm×4.6 mm,5 μm)、Shimadzu Shim-pack CLC-ODS C18(6.0 mm×15 cm,5 μm),下同]對各成分相對校正因子的影響。重復(fù)測定3次。以沒食子酸峰為內(nèi)參峰(S),分別計(jì)算原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷相對于沒食子酸的相對校正因子(fk/s),結(jié)果見表4。結(jié)果表明,不同色譜柱下各成分相對校正因子的RSD均小于1.5%,符合QAMS法的相關(guān)規(guī)定[21]。
2.10.3 不同儀器的相對校正因子 分別考察不同色譜柱在不同儀器(Agilent 1260型和Waters e2695型HPLC儀)上對各成分相對校正因子的影響。重復(fù)測定3次。以沒食子酸峰為內(nèi)參峰(S),分別計(jì)算原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷相對于沒食子酸的相對校正因子(fk/s),結(jié)果見表5。結(jié)果提示,不同儀器下各成分相對校正因子的RSD均小于3.0%,符合QAMS法的相關(guān)規(guī)定[21]。
2.10.4 不同柱溫和不同流速的相對校正因子 分別考察不同柱溫(25、30、35 ℃)及不同流速(0.8、1.0、1.2 mL/min)對各成分相對校正因子的影響,以沒食子酸峰為內(nèi)參峰(S),分別計(jì)算原兒茶酸、芒果苷、高芒果苷、金絲桃苷和異槲皮苷相對于沒食子酸的相對校對因子(fk/s),結(jié)果見表6。結(jié)果,不同柱溫和不同流速下各成分相對校正因子的RSD均小于1.5%,符合QAMS法的相關(guān)規(guī)定[21]。
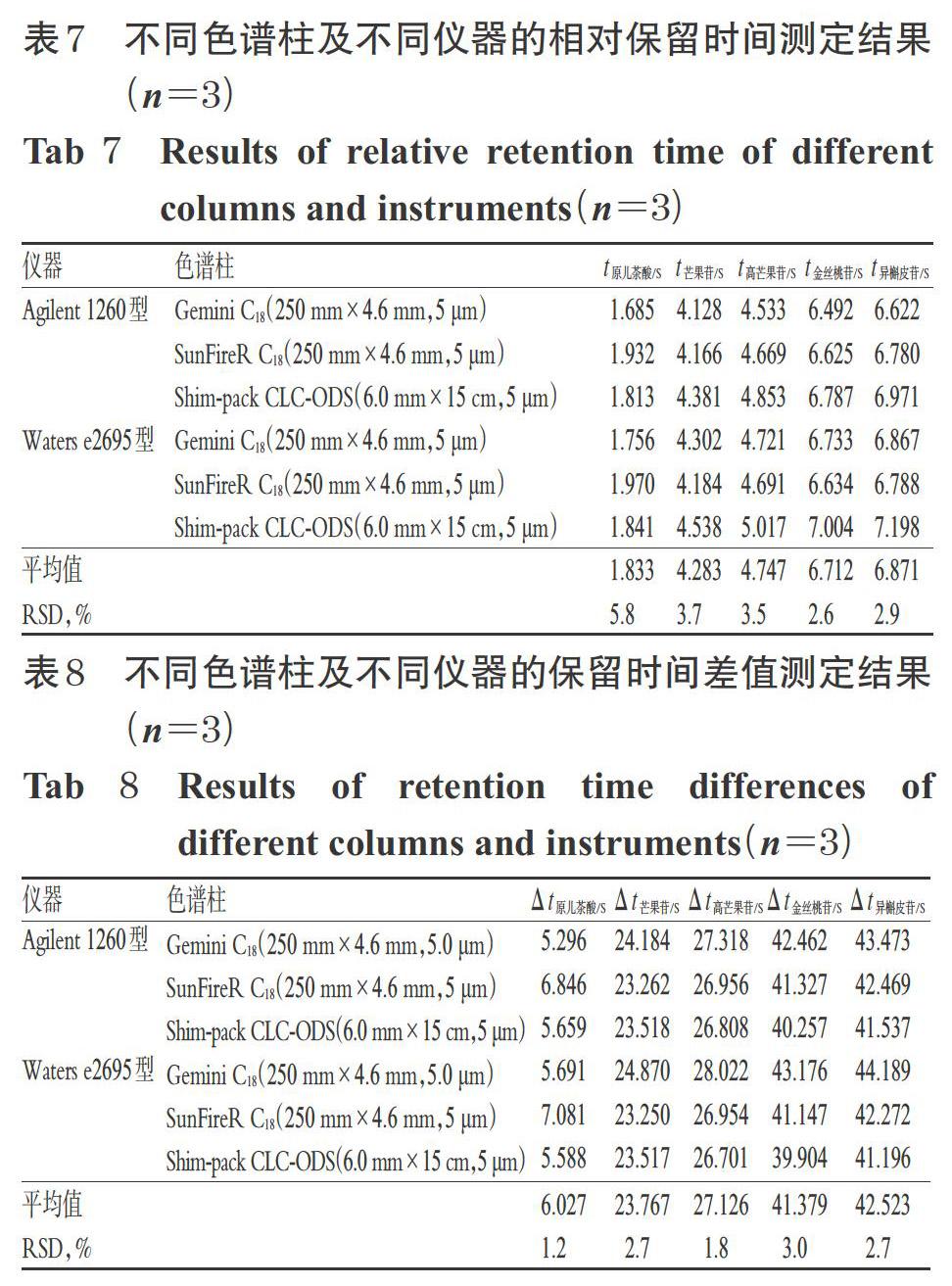
2.10.5 色譜峰的定位 QAMS法用于同時定量多指標(biāo)成分時需要對各待測成分色譜峰進(jìn)行定位[21]。目前,QAMS法用于色譜峰定位的方法主要有相對保留時間定位法和保留時間差值定位法[23]。本研究在Agilent 1260型和Waters e2695型HPLC儀上分別采用3 種不同色譜柱考察了各待測成分色譜峰的相對保留時間(t)和保留時間差值(Δt)的重現(xiàn)性。結(jié)果顯示,在相同色譜條件下,除原兒茶酸的RSD大于5%外,芒果苷、高芒果苷、金絲桃苷和異槲皮苷相對保留時間的RSD≤3.7%;而保留時間差值的RSD≤3.0%。因此,采用QAMS法進(jìn)行含量測定時,除原兒茶酸需用定性對照品進(jìn)行色譜峰定位外,其余成分可采用保留時間差值法定位,結(jié)果見表7、表8。
2.11 QAMS法與ESM法含量測定結(jié)果比較
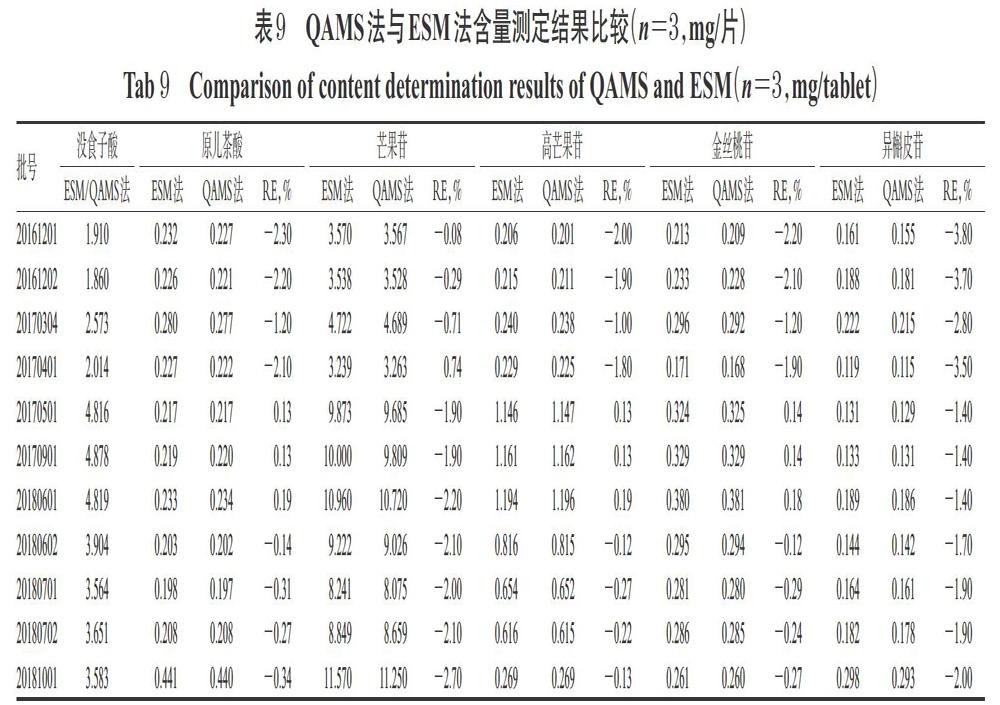
取11批芒果止咳片樣品,按“2.2.2”項(xiàng)下方法制備供試品溶液,按“2.1”項(xiàng)下色譜條件進(jìn)樣,采用QAMS法(按“2.10.5”項(xiàng)下方法對各目標(biāo)成分進(jìn)行色譜峰定位,記錄峰面積,再按“2.10.1”項(xiàng)下建立的校正因子計(jì)算各成分的含量)測定樣品中各成分的含量,并將測定結(jié)果與ESM法進(jìn)行比較,平行測定3 次。兩種方法含量測定結(jié)果的差異采用相對誤差(RE)進(jìn)行評價(jià),結(jié)果見表9。結(jié)果,兩種方法原兒茶酸、芒果苷、高芒果苷、金補(bǔ)桃苷、異桷檞皮苷含量測定結(jié)果的RE為-3.80%~0.74%。經(jīng)SPSS 22.0軟件進(jìn)行t檢驗(yàn),結(jié)果顯示兩種方法上述成分的測定結(jié)果比較差異均無統(tǒng)計(jì)學(xué)意義(P>0.05),提示QAMS法以沒食子酸為內(nèi)參物同時測定芒果止咳片中其余5種成分的準(zhǔn)確性良好。
3 討論
本研究通過對水、甲醇、乙醇、40%甲醇、70%甲醇、40%乙醇、70%乙醇為提取溶劑進(jìn)行考察。結(jié)果顯示,以70%甲醇為提取溶劑時各待測成分提取效率最好,故選擇70%甲醇為提取溶劑。此外,筆者還考察了冷浸、超聲、回流3種提取方式的提取效果。結(jié)果發(fā)現(xiàn),超聲和回流提取的提取率均較高,且差異不大,考慮到操作簡便性,故選擇超聲提取。同時,本研究對不同提取時間(20、30、40、50、60 min)的提取效果進(jìn)行考察。結(jié)果發(fā)現(xiàn),提取40 min時,各待測成分提取率不再增加,故選擇提取時間為40 min;對不同提取溶劑體積(25、50、75 mL)和提取次數(shù)(1、2、3次)進(jìn)行考察。結(jié)果發(fā)現(xiàn),25 mL提取2次和25 mL提取3 次時含量較高,且差異不大,提示以70%甲醇25 mL提取2 次可基本提取完全。與此同時,本研究通過二極管陣列檢測器對各待測成分在190~400 nm全波長范圍內(nèi)進(jìn)行掃描。結(jié)果顯示,在258 nm波長處各待測成分均有較好吸收,且芒果苷、高芒果苷、金絲桃苷和異槲皮苷在258 nm波長處有最大吸收,故選擇258 nm為檢測波長。
沒食子酸為芒果葉中含量較高的酚酸類成分[24],其在芒果止咳片中含量較高,且穩(wěn)定性好,同時沒食子酸對照品價(jià)格便宜、易得,因此本研究以沒食子酸為內(nèi)參物,測定了其他5種成分的相對校正因子,同時考察了不同對照品質(zhì)量濃度、流速、柱溫、儀器、色譜柱對相對校正因子的影響。結(jié)果顯示,相對校正因子的RSD 均小于3%,提示所建QAMS法的相對校正因子耐用性良好,符合相關(guān)規(guī)定(RSD<5%)[21]。
本研究結(jié)果顯示,以沒食子酸峰為內(nèi)參峰進(jìn)行各待測成分色譜峰定位時,除原兒茶酸相對保留時間的RSD大于5%外,其他4種成分無論采用相對保留時間法還是保留時間差值法進(jìn)行定位的RSD均小于4%,但采用保留時間差定位的RSD值相對較小,故除原兒茶酸外的其余成分本研究采用保留時間差法定位。原兒茶酸雖無法采用相對保留時間法定位,但其對照品便宜、易得,故采用QAMS法進(jìn)行含量測定時,原兒茶酸色譜峰可用定性對照品進(jìn)行定位[21,24]。
含量測定結(jié)果顯示,QAMS法與ESM法原兒茶酸、芒果苷、高芒果苷、金絲桃苷、異檞皮苷含量的測定結(jié)果無顯著性差異,表明本方法準(zhǔn)確、可行,結(jié)果可靠,這為芒果止咳片的質(zhì)量控制提供了新的思路;但不同批次芒果止咳片中各成分含量存在差異,其中以芒果苷和高芒果苷的含量差異尤為明顯,其中4批(20161201、20161202、20170304、20170401)的芒果苷和高芒果苷含量較低,其原因可能為存放時間較久造成含量下降,或與芒果葉藥材來源于不同產(chǎn)地或采收季節(jié)不同有關(guān)[26]。
綜上所述,所建QAMS含量測定方法準(zhǔn)確、可靠,重復(fù)性好,可用于同時測定芒果止咳片中6種成分的含量。
參考文獻(xiàn)
[ 1 ] 鄭作文,鄧家剛,林啟云.芒果止咳片的藥效學(xué)研究[J].中醫(yī)藥學(xué)刊,2002,20(3):358-359.
[ 2 ] 鄧家剛,鄭作文,曾春暉.芒果苷的藥效學(xué)實(shí)驗(yàn)研究[J].中醫(yī)藥學(xué)刊,2002,20(6):802-803.
[ 3 ] GARRIDO G,DELGADO R,LEMUS Y,et al. Protection against septic shock and suppression of tumor necrosis factor alpha and nitric oxide production on macrophages and microglia by a standard aqueous extract of Mangifera indica L.(VIMANG):role of mangiferin isolated from the extract[J]. Pharmacol Res,2004,50(2):165-172.
[ 4 ] 楚策.芒果苷抗酒精性肝損傷作用機(jī)制的實(shí)驗(yàn)研究[D]. 保定:河北大學(xué),2018.
[ 5 ] 國家食品藥品監(jiān)督管理總局.國家藥品標(biāo)準(zhǔn)WS3:B- 0920-91-1[S].2014-12-09.
[ 6 ] 劉華鋼,黃海濱,陳燕軍. HPLC法測定芒果止咳片中芒果苷的含量[J].中成藥,1997,19(10):14-15.
[ 7 ] 田輝,陳衛(wèi)衛(wèi),蔡毅.高效液相色譜法測定芒果止咳片中魚腥草素鈉[J].中草藥,2006,37(8):1179-1180.
[ 8 ] 莫慧貞,許則省.對芒果止咳片中馬來酸氯苯那敏的含量測定[J].今日藥學(xué),2009,19(4):40-42.
[ 9 ] 潘晶.芒果葉活性成分研究[D].廣州:廣東藥科大學(xué),2017.
[10] 馮旭,鄧家剛,覃潔萍,等.芒果葉揮發(fā)油化學(xué)成分研究[J].時珍國醫(yī)國藥,2011,22(1):83-84.
[11] PAL C,BINDU S,DEY S,et al. Gallic acid prevents nonsteroidal anti-inflammatory drug-induced gastropathy in rat by blocking oxidative stress and apoptosis[J]. Free Radic Biol Med,2010,49(2):258-267.
[12] 柴貝貝,姜維佳,王莉貞,等.原兒茶酸或綠原酸與抗菌藥聯(lián)用對魚源鏈球菌的抑菌效果[J].南方農(nóng)業(yè)學(xué)報(bào),2018,49(3):580-585.
[13] 周智.芒果苷藥理實(shí)驗(yàn)研究新進(jìn)展[J].內(nèi)科,2011,6(5):462-464.
[14] 郭宏偉,鄧家剛,運(yùn)晨霞,等.芒果苷抑制哮喘小鼠氣道炎癥的機(jī)制[J].中國實(shí)驗(yàn)方劑學(xué)雜志,2012,18(9):187-190.
[15] 衛(wèi)智權(quán),閆莉,鄧家剛,等.芒果苷對脂多糖誘導(dǎo)的慢性炎癥大鼠MAPK通路及血清細(xì)胞因子的影響[J].中草藥,2013,44(1):52-58.
[16] 王志萍,鄧家剛,譚珍媛.芒果苷片體外抑菌殺蟲作用的實(shí)驗(yàn)研究[J].時珍國醫(yī)國藥,2009,20(9):2167-2168.
[17] 舒慶,鄭其萍.金絲桃苷抗心/腦缺血損傷作用的藥理學(xué)研究進(jìn)展[J].中國藥房,2016,27(10):1415-1417.
[18] PIAO MJ,KANG KA,ZHANG R,et al. Hyperoside prevents oxidative damage induced by hydrogen peroxide in lung fibroblast cells via an antioxidant effect[J]. Biochim Biophys Acta,2008,1780(12):1448-1457.
[19] 陳燕,詹羽姣,李晨陽,等.異槲皮苷的生物活性研究進(jìn)展[J].中國現(xiàn)代中藥,2018,20(12):1579-1582、1592.
[20] 譚紅聲,覃潔萍,朱智德,等.十味鵝黃顆粒HPLC指紋圖譜及8種主要成分含量測定[J].中國醫(yī)院藥學(xué)雜志,2019,39(8):826-832.
[21] 王智民,錢忠直,張啟偉,等.一測多評法建立的技術(shù)指南[J].中國中藥雜志,2011,36(6):657-658.
[22] 馬昌豪,李懷偉,仝桂平,等.一測多評法同時測定咽炎片中5種指標(biāo)性成分的含量[J].中國藥房,2019,30(16):2232-2236.
[23] 沈潔,王琴,熊維建,等. HPLC-一測多評法測定參芪延腎顆粒中淫羊藿藥材中的6個黃酮類成分的含量[J].中國藥房,2019,30(17):2327-2331.
[24] 馮旭,王勝波,鄧家剛,等. HPLC法測定芒果葉中沒食子酸的含量[J].山西中醫(yī)學(xué)院學(xué)報(bào),2008,9(1):45-46.
[25] 李金花,馮有龍,張?jiān)倨剑?一測多評法測定西洋參類保健食品中9個皂苷類成分的含量[J].藥物分析雜志,2018,38(12):2160-2166.
[26] 鄧家剛,馮旭,王勤,等.不同產(chǎn)地及不同品種芒果葉中芒果苷的含量對比研究[J].中成藥,2006,28(12):1755-1756.
(收稿日期:2019-09-22 修回日期:2020-02-13)
(編輯:陳 宏)

