大鼠中心靜脈導管相關性血栓模型的建立方法▲
甘 曉 應燕萍 韋 艷 趙慧函 蔣慶娟 文 萃
(廣西醫科大學第一附屬醫院護理部,南寧市 530021,電子郵箱:ganxiao0722@126.com)
中心靜脈血管通路裝置(central venous access device,CVAD)也稱中心靜脈導管,是一種經皮置入體內且末端位于上腔或下腔靜脈的裝置,主要用于化療、輸入血液制品、胃腸外營養及其他療法,或者血流動力學監測[1-2]。CVAD的優越性使得其在臨床上得到廣泛應用,在美國,每年有超過500萬個CVAD被用于臨床[3]。但CVAD可引起許多導管相關并發癥,其中導管相關性血栓(catheter-related thrombosis,CRT)是最常見且最嚴重的并發癥之一。有研究顯示CRT發生率為13.8%,其中近90%的CRT為無癥狀血栓[4]。目前有關CRT的臨床研究很多,但相關的基礎研究較少,CRT的發生機制尚不明確。本研究通過經頸外靜脈留置CVAD的方法建立大鼠CRT模型,為CRT的基礎研究提供模型參考,現報告如下。
1 材料和方法
1.1 材料
1.1.1 實驗動物:無特定病原體級SD大鼠58只,雄性,體重170~220 g,購自廣西醫科大學實驗動物中心,實驗動物生產許可證號:SCXK桂2014-0002。大鼠飼養于室溫為(24±2) ℃,相對濕度為40%~60%的無特定病原體級實驗室中,自由飲水、攝食。
1.1.2 主要試劑與儀器:水合氯醛(天津市大茂化學試劑廠,批號:20180514),10%中性福爾馬林固定液(廣州維格斯生物科技有限公司,生產批號:18101201),頸靜脈導管及接頭(思科諾生物科技北京有限公司,1#),切片機(德國Leica公司,型號:RM2245),正置熒光顯微鏡(日本Olympus公司,型號BX53 )
1.2 方法
1.2.1 動物分組:將58只雄性SD大鼠隨機(計算機法)分為對照組(n=3)、假手術組(n=15)和模型組(n=40)。將假手術組和模型組再隨機(計算機法)平均分為建模后1、4、7、10、14 d組。
1.2.2 CRT模型的建立:參考Terry等[5]提出的手術方法進行置管。模型組采用10%水合氯醛經腹腔注射進行麻醉,右側頸部備皮,常規消毒、鋪巾,沿氣管右側0.5 cm縱切頸部1.5 cm,鈍性游離右頸外靜脈長約1 cm。用3-0絲線結扎游離靜脈的遠心端,于結扎點下將靜脈剪一切口,從靜脈切口將導管往上腔靜脈方向插入2.5 cm,回抽見回血后經導管輸入1 mL生理鹽水封管,3-0絲線分別固定導管突起部上、下端,防止導管脫出或深入血管,見圖1。將導管頭端埋于頸部皮下組織,縫合皮膚,結束手術。假手術組按模型組麻醉大鼠后切開頸部,鈍性分離暴露右頸外靜脈后立即縫合頸部皮膚。對照組不做任何處理,正常飼養。
1.2.3 CRT的評估:假手術組及模型組在建模后相應時間點進行解剖取材,對照組在同期飼養的最后一天解剖取材,各組均取同側靜脈組織。大鼠腹腔注射10%水合氯醛進行麻醉,解剖頸部取右頸外靜脈至上腔靜脈的組織(模型組需拔出靜脈導管后取材),置于10%中性福爾馬林中固定48 h,脫水經石蠟包埋、切片,行蘇木精-伊紅染色法染色,在顯微鏡下觀察置管靜脈的形態學變化。
1.3 統計學分析 采用SPSS 17.0軟件進行統計學分析,計數資料以例數(百分比)表示。
2 結 果
2.1 一般情況 58只SD大鼠中,模型組有1只大鼠因建模時麻醉過量死亡(建模7 d組),其余57只大鼠均存活。大鼠置管成功率100.0%(39/39),導管留置期間無導管脫出。
2.2 CRT形成情況 對照組和假手術組在實驗期間均未見血栓形成;模型組32只大鼠發生CRT,CRT發生率為82.1%(32/39),其中建模后1 d組、建模后4 d組和建模后7 d組分別有6只、5只、5只大鼠發生血栓,血栓發生率為75.0%(6/8)、62.5%(5/8)和71.4%(5/7),建模后10 d和14 d組大鼠均發生血栓,血栓發生率為100.0%(8/8)。
2.3 各組大鼠右頸外靜脈組織病理學結果 顯微鏡下可見對照組和假手術組右頸外靜脈內皮結構光滑、完整,管腔無血栓形成(圖 2A、圖 2B)。顯微鏡下可見模型組右頸外靜脈有CRT形成(圖2C);建模后1 d、4 d和7 d時主要為混合血栓,血管腔有淡粉色無結構血小板小梁,小梁間充滿紅細胞、白細胞;建模后10 d和14 d時主要為血栓機化血管內皮細胞和成纖維細胞及炎癥細胞形成肉芽組織并開始長入血栓內。

圖1 右頸外靜脈置入導管過程
注:A為頸部消毒鋪巾;B為暴露右頸外靜脈;C為右頸外靜脈下方穿過兩條3-0絲線;D為導管插入右頸外靜脈;E為導管固定結束。
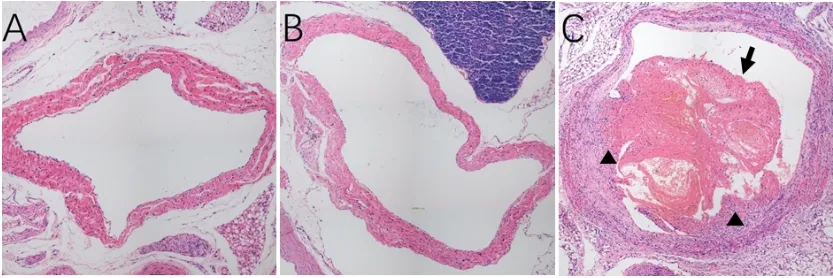
圖2 各組大鼠頸外靜脈組織病理學變化(蘇木精-伊紅染色,20)
注:A為對照組;B為假手術組;C模型組(為血栓;▲為肉芽)。
3 討 論
CRT是指由于穿刺或導管直接損傷血管內膜,以及患者自身狀態等多因素作用,使導管所在的血管內壁及導管附壁形成血凝塊,導致導管部分或完全堵塞,伴或不伴臨床癥狀[6-7]。臨床上CRT患者大多數無癥狀,在因置管發生血栓的患者中,超過90%的患者通過超聲檢查才發現有血栓形成[8]。CRT的主要癥狀有手臂發紅、腫脹或疼痛,頸、臂、胸可見靜脈擴張等[9]。CRT可引起肺栓塞、再發性深靜脈血栓、血栓后綜合征等并發癥,其中肺栓塞和深靜脈血栓統稱為靜脈血栓栓塞,靜脈血栓栓塞的高發生率和病死率使其成為全球疾病的主要負擔[10]。CRT不僅會導致患者治療的中斷,增加患者住院時間和醫療費用,還會影響患者預后,增加病死率,加重社會醫療負擔[11]。早期診斷及有效預防CRT對改善患者的療效及預后有積極的意義。
CRT的發生涉及多因素和多系統,傳統觀點認為,血管內皮損傷、血流速度減慢、血液高凝狀態的共同作用促使血栓的形成。本研究通過手術暴露大鼠右側頸外靜脈,從靜脈置入導管并留置于血管內制作CRT大鼠模型。導管置入后內皮細胞受損,內皮下膠原暴露引起血小板黏附聚集,激活凝血因子Ⅻ,損傷的內皮釋放組織因子,激活凝血因子Ⅶ,啟動了內、外源性凝血過程[12]。靜脈管腔內導管的置入使血液流通空間變窄,血流速度減慢,當血流緩慢或有旋渦時血小板進入邊流,極大增加了與內膜接觸的機會以及黏附內膜的可能性,有利于血栓的形成。本研究結果顯示,建模后7 d時血栓發生率為71.4%,建模后10 d、14 d血栓發生率均為100%,提示該建模方法CRT成功率高,且導管留置10 d以后CRT的發生率最高,筆者認為血栓的形成可能與導管留置的時間有關。本研究中,大鼠置管1 d即可發現有血栓形成,置管1周內,置管的靜脈腔內形成許多血小板梁,其間纖維蛋白網羅大量紅細胞及部分白細胞,從而形成血小板梁與紅細胞交替的混合血栓;建模后10 d和14 d時,肉芽組織開始深入血栓組織,逐漸代替血栓,血栓開始機化。血栓形成后會發生機化、鈣化等現象,但本研究未在顯微鏡下觀察到血栓鈣化,可能與導管留置時間較短有關。
有關CRT動物模型建立的研究報告多以兔子為實驗動物,如鄧婷[13]通過兔頸外靜脈留置靜脈留置針的方法構建CRT模型,觀察不同留置時間CRT的發生情況及置管周圍組織的病理變化,在顯微鏡下觀察到靜脈腔內有不同程度的血栓。艾熙等[14]于家兔右頸外靜脈插入CVAD建立CRT模型,在置管第7天15只家兔全部發生CRT。但兔子體積較大,需單籠飼養,經濟消耗大。本研究采用大鼠作為模型具有動物體積小、可操作性高、可重復性強,價格低廉、適合開展大樣本量研究的優點。大鼠的頸外靜脈較家兔細,靜脈被刺激后會收縮甚至痙攣,導致頸外靜脈置入CVAD難度較大。但本研究中大鼠CVAD的置管成功率為100%(39/39),提示用大鼠建立CRT模型可行性高。然而本研究尚未通過導管對大鼠進行輸液治療,未能說明藥物對CRT的形成是否有促進作用,今后將深入研究。
綜上所述,經右頸外靜脈留置CVAD可以成功建立大鼠CRT模型,且該模型形成的血栓穩定,血栓病理符合人體血栓的結構特點,可為今后深入研究CRT及導管相關疾病提供模型參考。

