例析高考化學實驗中的溫度控制
2020-03-17 02:37:52李大艷
數理化解題研究
2020年1期
關鍵詞:實驗
李大艷
(浙江省紹興市魯迅中學 312050)
化學是一門以實驗為基礎的學科,化學實驗題也成為高考必考題型,實驗過程中的條件的控制,對實驗成敗、產品的產量、質量、安全生產及節約能源等方面有著重要的意義,也備受命卷教師青睞,但卻讓很多學生頭疼,得分率始終居低難高,本文以條件控制的重要一環——溫度的控制為主體,結合歷年高考真題,總結歸納了三大角度來分析實驗中的溫度控制,以期考生能舉一反三,提高答題能力.
一、控制溫度以減少副反應的發生
1.控制溫度防止原料或產品受熱分解
例1(2019年江蘇)實驗室以工業廢渣(主要含CaSO4·2H2O,還含少量SiO2、Al2O3、Fe2O3)為原料制取輕質CaCO3和(NH4)2SO4晶體,其實驗流程如下:

廢渣浸取在如圖所示的裝置中進行.控制反應溫度在60~70 ℃,攪拌,反應3h.溫度過高將會導致CaSO4的轉化率下降,其原因是____.
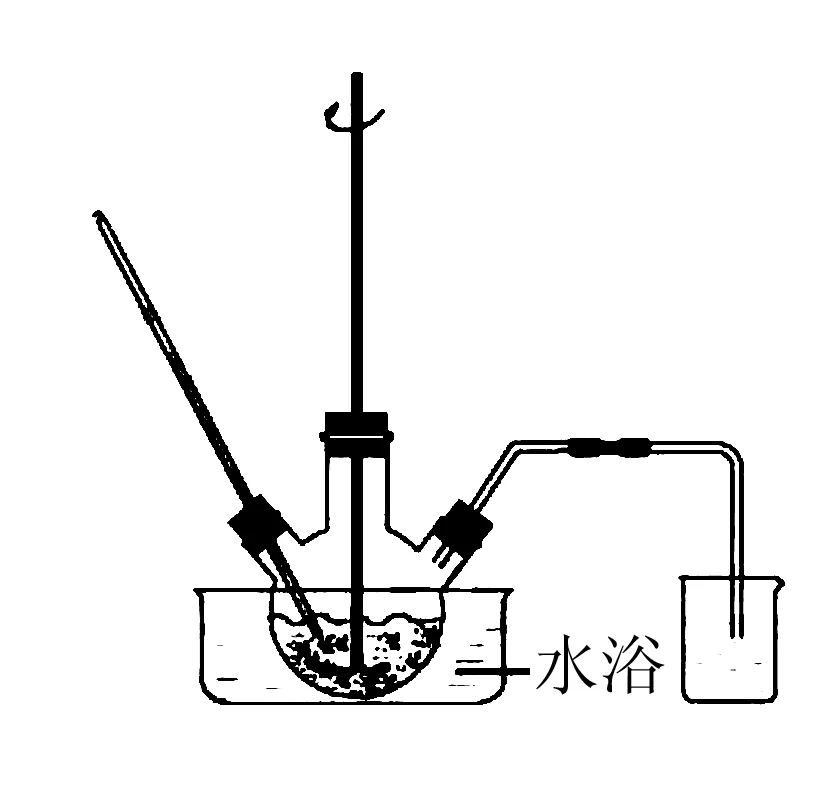

答案溫度過高,(NH4)2CO3分解
特別提醒當原料或產品中存在受熱易分解的物質時,溫控時溫度往往不易過高.常見的受熱易分解的物質有雙氧水(在30℃以下時比較穩定,60℃時,分解率已達50%左右)、草酸、次氯酸、硝酸、氨水、銨鹽、硝酸鹽等等,同時警惕題干中出現的受熱易分解的陌生物質.
2.控制溫度防止原料或產品的水解反應
例2(2009年江蘇)以氯化鉀和鈦白廠的副產品硫酸亞鐵為原料生產硫酸鉀、過二硫酸銨和氧化鐵紅顏料,原料的綜合利用率較高.其主要流程如下:
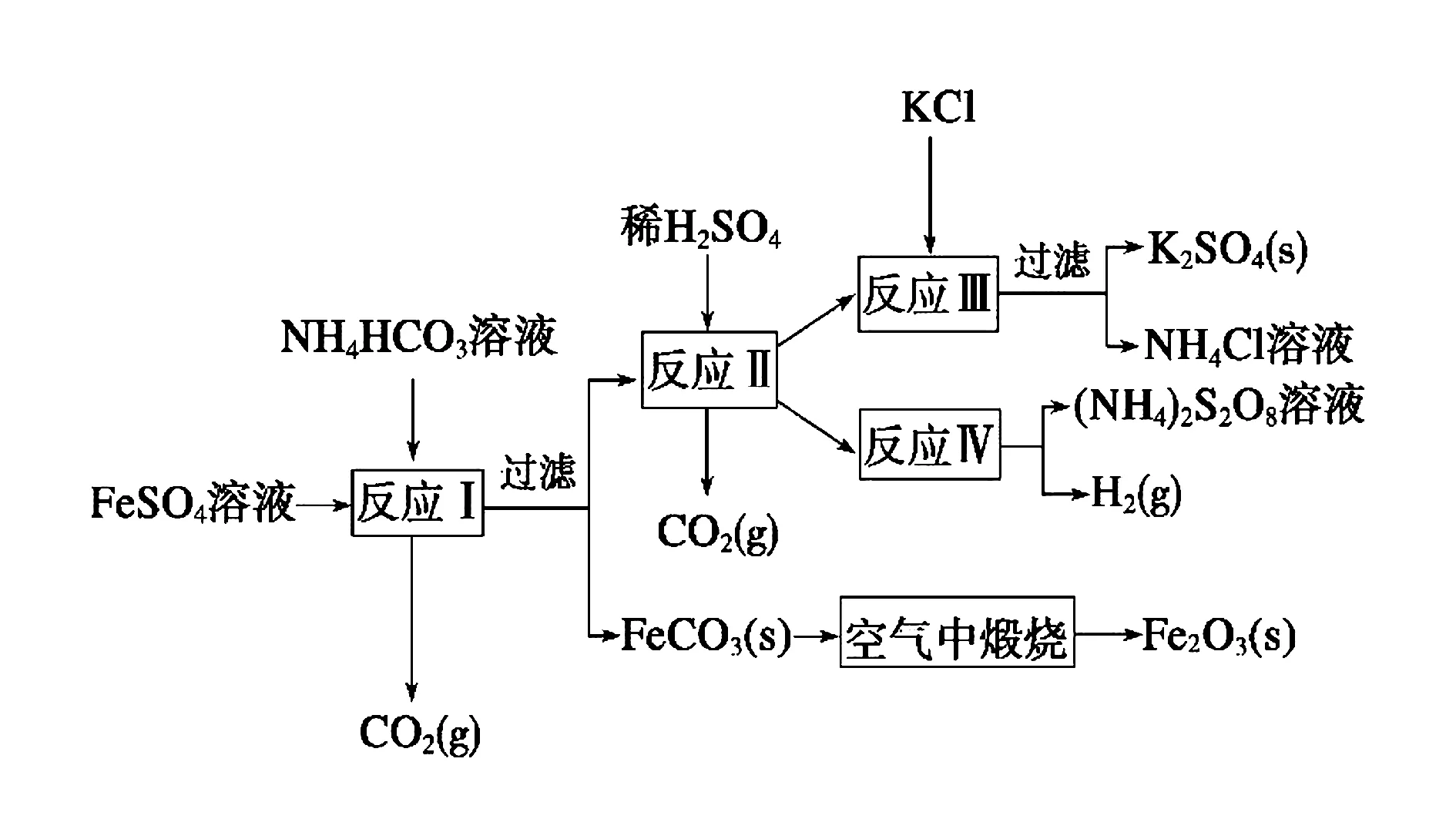
反應Ⅰ需控制反應溫度低35℃,其目的是____ .
解析反應Ⅰ原料有NH4HCO3、FeSO4,溫度若過高,Fe2+水解程度會加大,NH4HCO3會分解,這……
登錄APP查看全文
猜你喜歡
作文·小學低年級(2025年2期)2025-02-13 00:00:00
小雪花·小學生快樂作文(2024年11期)2024-12-31 00:00:00
作文·小學低年級(2024年2期)2024-04-29 00:00:00
作文·小學低年級(2023年3期)2023-04-29 00:00:00
小獼猴智力畫刊(2022年9期)2022-11-04 02:31:42
小主人報(2022年4期)2022-08-09 08:52:06
小哥白尼(趣味科學)(2019年6期)2019-10-10 01:01:50
發明與創新(2016年38期)2016-08-22 03:02:52
太空探索(2016年5期)2016-07-12 15:17:55
實驗流體力學(2011年5期)2011-01-14 01:25:28

