一種蒽醌類熒光探針的合成及對氟離子的檢測性能
王金金, 王芳菲, 徐恩杰, 楊清彪, 宋 巖
(1. 吉林化工學院 材料科學與工程學院,吉林 吉林 132022; 2. 吉林大學 化學學院,吉林 長春 130061)
陰離子的識別傳感技術一直受到廣泛關注[1]。氟是人體健康不可或缺的微量元素,攝入低劑量的氟化物有助于預防骨質疏松癥和齲齒,但攝入過量會導致腎臟中毒和尿石癥等疾病[2-4]。氟離子在自然界中普遍存在,部分地區的含量超標,地方性氟中毒時有發生,而且作為原子半徑最小、電負性最大的陰離子[5],其在化學制藥、化肥和農藥、金屬冶煉、電子、電鍍等行業起著不可或缺的作用,生產過程中的排放不可避免,一旦污染江河水體,經直接飲用或食物鏈富集后,進入人體將引發許多疾病[6-8]。開發性能優異、操作簡單的氟離子檢測技術有重要意義。
在氟離子檢測技術中,傳統的離子色譜、核磁共振和離子選擇電極等方法[9-11]存在儀器昂貴,操作復雜,時間較長,難以現場檢測等問題[12]。熒光檢測法具有操作簡單、成本低廉和靈敏度高等優點,引起了研究者的廣泛關注[13]。以往,人們以半花菁衍生物[14]、奈酰亞胺類衍生物[15]、羅丹明類衍生物[16]和熒光素類衍生物[17]等為熒光團,合成了多種性能較好的氟離子熒光探針。
蒽醌衍生物主要包括1,4-二氨基-9,10-蒽醌、1-氨基-4-羥基-9,10-蒽醌和1,4-二羥基-9,10-蒽醌(1,4-DHAQ),其中1,4-DHAQ含有兩個羥基,能夠形成較強的分子內氫鍵,使得分子的整體結構剛性更強,發光性能較好[18],是構建熒光探針的理想發色團。2005年,Kim等以1,4-DHAQ為熒光團,合成了可檢測堿性磷酸酶的醌茜酯二磷酸[19];隨后Qian等制備了1,4-DHAQ摻雜的纖維素納米纖維,利用1,4-DHAQ與金屬離子形成配合物后發生顯著熒光信號變化的性質,獲得了可檢測Cu2+和Cr3+的傳感材料[20];Wang等利用1,4-DHAQ與Cu2+形成配合物后,還可與S2-作用脫除Cu2+的性質,獲得了可交替檢測Cu2+和S2-的熒光探針[21],Sinha等利用類似性質,獲得了可同時檢測Zn2+和PO43-的熒光探針[22]。目前為止,雖然1,4-DHAQ類熒光探針的研究取得了一些進展,但僅限于少數幾個金屬離子及陰離子,還未發現以其為熒光團的氟離子探針報道。
本文以1,4-二羥基蒽醌為熒光團,叔丁基二甲基氯硅烷為識別基團,設計合成了一種新型氟離子熒光探針AQTB1(Scheme 1),在MeOH/PBS=19/1(V/V)的緩沖體系中實現了氟離子的高效檢測。
1 實驗部分
1.1 儀器與試劑
X-5型顯微熔點測定儀;HitachiF-4500型熒光光譜儀;Hitachi U-3010型紫外-可見吸收光譜儀;Bruker AV 400型核磁共振儀(DMS(ESI)O-d6為溶劑,TMS(ESI)為內標);Bruker Vector-22型傅里葉變換紅外光譜儀(KBr壓片);Bruker Agilent 1290-micro TOF QⅡ型質譜儀;PHS-3C型數顯酸度計。
1,4-二羥基蒽醌(99%,上海睿騰化工有限公司),柱層析提純后使用;四丁基氟化銨(98%,阿拉丁試劑有限公司);叔丁基-二甲基氯硅烷(98%,上海泰坦科技有限公司);叔丁基二苯基氯硅烷(98%,上海泰坦科技有限公司);三-異丙基氯硅烷(98%,上海泰坦科技有限公司);其余所用試劑均為分析純。實驗用水為去離子水。
1.2 探針AQTB(AQTB1~3)的合成通法
在100 mL圓底燒瓶中加入1,4-二羥基蒽醌0.5 g(2.081 mmol)和DMF 50 mL,攪拌使其溶解,加入咪唑0.85 g(12.489 mmol),滴加叔丁基-二甲基氯硅烷1.255 g(8.326 mmol)的DMF(20 mL)溶液,滴畢,攪拌下反應12 h(TLC檢測)。加入大量水除去未反應的咪唑,用乙酸乙酯萃取3次,合并萃有機相,依次用飽和氯化鈉溶液洗滌,無水硫酸鈉干燥,過濾,濾液減壓蒸除溶劑,殘余物經硅膠柱層析(展開劑:PE/EA=20/1,V/V)純化得產物AQTB1~3。
1,4-二-(叔丁基-二甲基-硅氧基)-蒽醌(AQTB1): 橙黃色固體0.561 g,產率57.5%, m.p.77~79 ℃;1H NMR(DMS(ESI)O-d6, 400 MHz)δ: 8.04(dd,J=5.8 Hz, 3.3 Hz, 2H), 7.82(dd,J=5.8, 3.3 Hz, 2H), 7.26(s, 2H), 1.02(s, 18H), 0.22(s, 12H);13C NMR(DMS(ESI)O-d6, 101 MHz)δ: 183.09, 150.76, 134.72, 134.55, 130.51, 126.77, 124.59, 26.63, 19.12, -3.46; MS(ESI)m/z: Calcd for C26H36O4Si2Na{[M+Na]+}491.2044, found 491.2047。
1,4-二-(叔丁基-二苯基-硅氧基)-蒽醌(AQTB2): 橙黃色固體0.254 g,產率17.0%, m.p.198~200 ℃;1H NMR(CDCl3, 400 MHz)
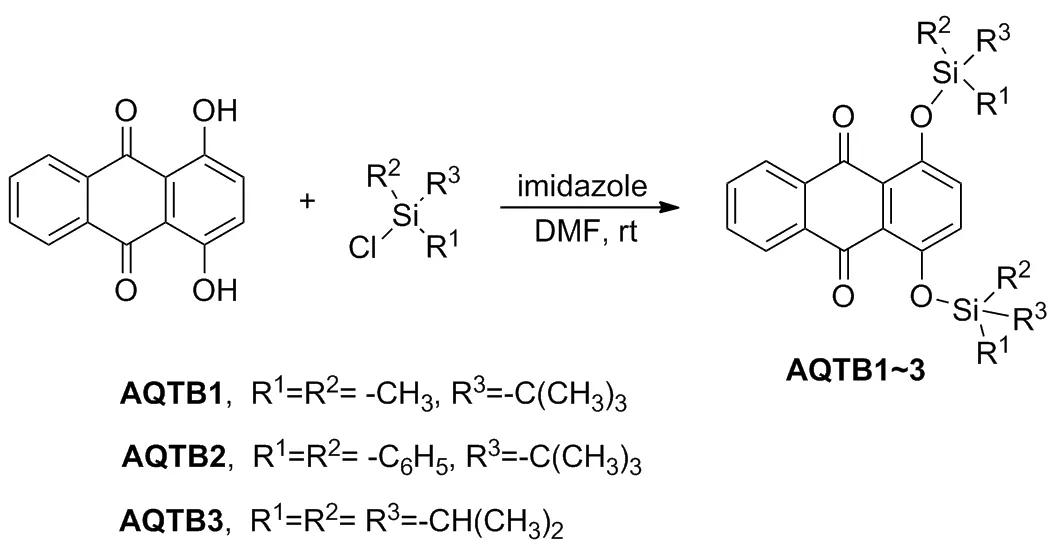
Scheme 1
δ: 8.37~8.33(m, 2H), 8.28(dd,J=7.6 Hz, 1.2 Hz, 2H), 7.86~7.74(m, 9H), 7.67(d,J=1.1 Hz, 1H), 7.41(dt,J=14.1 Hz, 6.9 Hz, 10H), 6.85(d,J=1.2 Hz, 2H), 1.24(d,J=16.5 Hz, 14H), 1.07~1.0(m, 2H), 0.89~0.84(m, 2H);13C NMR(CDCl3, 101 MHz)δ: 188.82, 186.94, 157.88, 150.02, 135.51, 134.49, 133.09, 132.46, 131.85, 130.13, 129.38, 127.96, 127.39, 127.06, 126.29, 125.37, 26.38, 19.67; MS(ESI)m/z: Calcd for C38H33O4Si23-{[M-H]4-}608.1900, found 607.5610; MS(ESI)m/z: Calcd for C28H18O4Si26-{[M+H]5-}475.0800, found 475.4124; MS(ESI)m/z: Calcd for C17H13O4Si25-{[M+H]4-}338.0400, found 338.3405。
1,4-二-(三-(異丙基)-硅氧基)-蒽醌(AQTB3): 橙黃色黏稠液體0.109 g,產率9.4%;1H NMR(CDCl3, 400 MHz)δ: 8.30~8.26(m, 2H), 7.80~7.71(m, 2H), 7.21(d,J=1.0 Hz, 2H), 1.41(dt,J=14.9 Hz, 7.5 Hz, 3H), 1.16(d,J=7.5 Hz, 18H), 1.06(t,J=5.9 Hz, 3H);13C NMR(CDCl3, 101 MHz)δ: 188.79, 181.10, 157.95, 150.80, 135.19, 134.48, 133.04, 132.46, 132.28, 127.26, 126.29, 125.83, 120.57, 115.62, 18.02, 13.44; MS(ESI)m/z: Calcd for C32H48O4Si2{[M-K-H]2-}512.2500, found 512.5015。
1.3 光譜測試
四丁基氟化銨用PBS緩沖溶液溶解,配制氟離子濃度為1×10-3M的溶液。同時配制濃度為1×10-4M的AQTB1甲醇溶液,然后再用MeOH/PBS溶液(MeOH/PBS =19/1,V/V, pH=7.4)將AQTB1溶液濃度稀釋至20 mM,最終光譜測試時,探針AQTB1濃度為10 μM,其他干擾離子濃度為5 mM。
2 結果與討論
2.1 溶液pH值對探針AQTB1檢測性能的影響
加入氟離子前后,改變探針AQTB1溶液的酸堿度,考察AQTB1熒光強度隨溶液pH值的變化情況,結果表明(圖1):未加入氟離子時,當溶液pH值在2~12變化時,AQTB1溶液的熒光強度很小,且基本保持不變;加入氟離子后(50.0 eq.),熒光強度明顯增加,且當pH在3~12變化時基本保持穩定,說明該探針具有良好的酸堿穩定性,能在廣泛pH范圍內實現對氟離子的響應,為研究方便,選擇pH為7.4的溶液進行測試。

pH
2.2 探針AQTB1對氟離子的紫外和熒光響應
在AQTB1緩沖溶液中,加入不同濃度的氟離子(0~100.0 eq.),通過滴定實驗考察溶液光譜的變化情況。紫外滴定實驗結果表明(圖2A),隨氟離子濃度的增加,探針AQTB1在465~510 nm范圍內的紫外吸收逐漸增強,當氟離子加入量為55.0 eq.時達到飽和。以氟離子濃度(0~55.0 eq.)為橫坐標,476 nm處的對應紫外吸收峰強度為縱坐標作圖并進行線性擬合(圖2B),發現氟離子濃度在0~0.55 mM,紫外吸收峰強度與氟離子濃度呈現良好的線性關系(R2=0.9608)。
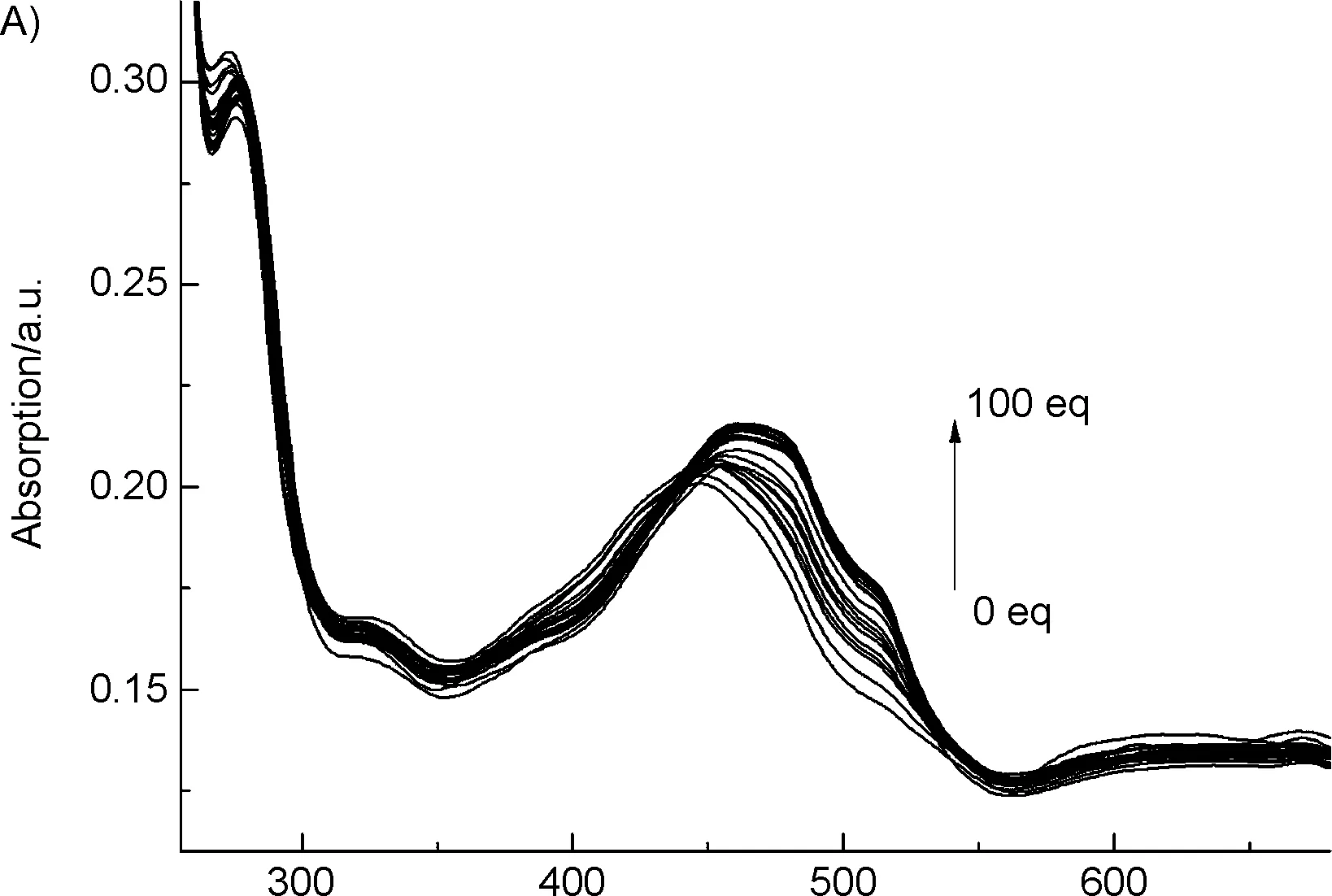
λ/nm
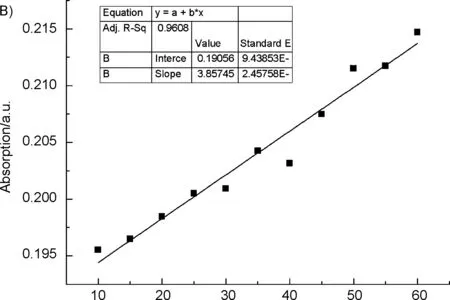
CF-1/10 μΜ
熒光滴定實驗表明(圖3A),AQTB1熒光發射強度隨氟離子濃度的增加而逐漸增強,當氟離子加入量為55.0 eq.時,熒光強度增強了5倍,再加入氟離子則變化不大。以氟離子濃度為橫坐標,476 nm處的熒光強度為縱坐標作圖并進行線性擬合,結果表明(圖3B),當氟離子濃度在0~5.5×10-4M范圍變化時,二者呈現良好的線性關系(R2=0.99128),線性方程為y=3.7442x+58.124,計算得到探針AQTB1對氟離子的檢測限為0.32 μM。

λ/nm
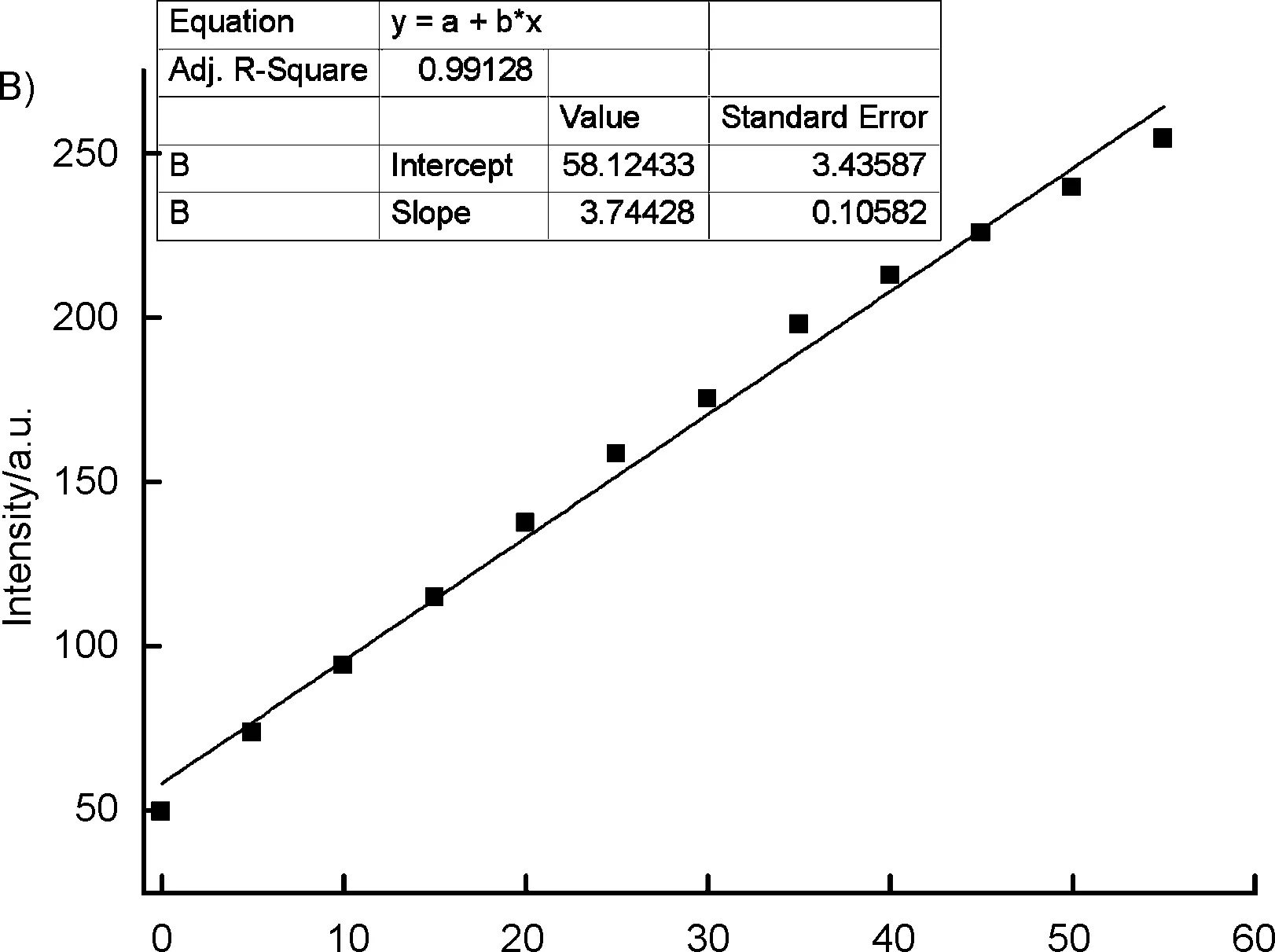
λ/nm
2.3 探針AQTB1對氟離子的選擇性與競爭性實驗
為考察探針AQTB1對F-的檢測靈敏性,分別進行了選擇性和競爭性實驗。其中,在選擇性實驗中,首先選取12種常見陰離子(包括Br-, Cl-, I-, NO3-, N3-, SCN-, H2PO4-, HPO42-, HCO3-, CH3COO-, C2O42-和SO42-)作為干擾物(500 eq.)和F-(50 eq.),分別加到含有AQTB1的緩沖溶液中,放置100 min后測試,結果表明(圖4A),加入F-后,探針AQTB1在562 nm處的熒光發射峰明顯增強,添加其它12種干擾離子時,熒光發射光譜變化不大。
競爭性實驗中,在AQTB1的緩沖溶液中分別上述12種干擾離子(500 eq.),隨后再加入F-(50 eq.),放置100 min后測試。結果表明(圖4B),與未加入F-前比較,探針AQTB1在562 nm處的熒光發射峰明顯增強,說明干擾離子的存在不影響探針AQTB1對F-的檢測。將上述結果進行處理,得到柱狀圖如圖4C所示,探針AQTB1在F-檢測中呈現良好的選擇性和抗干擾能力。
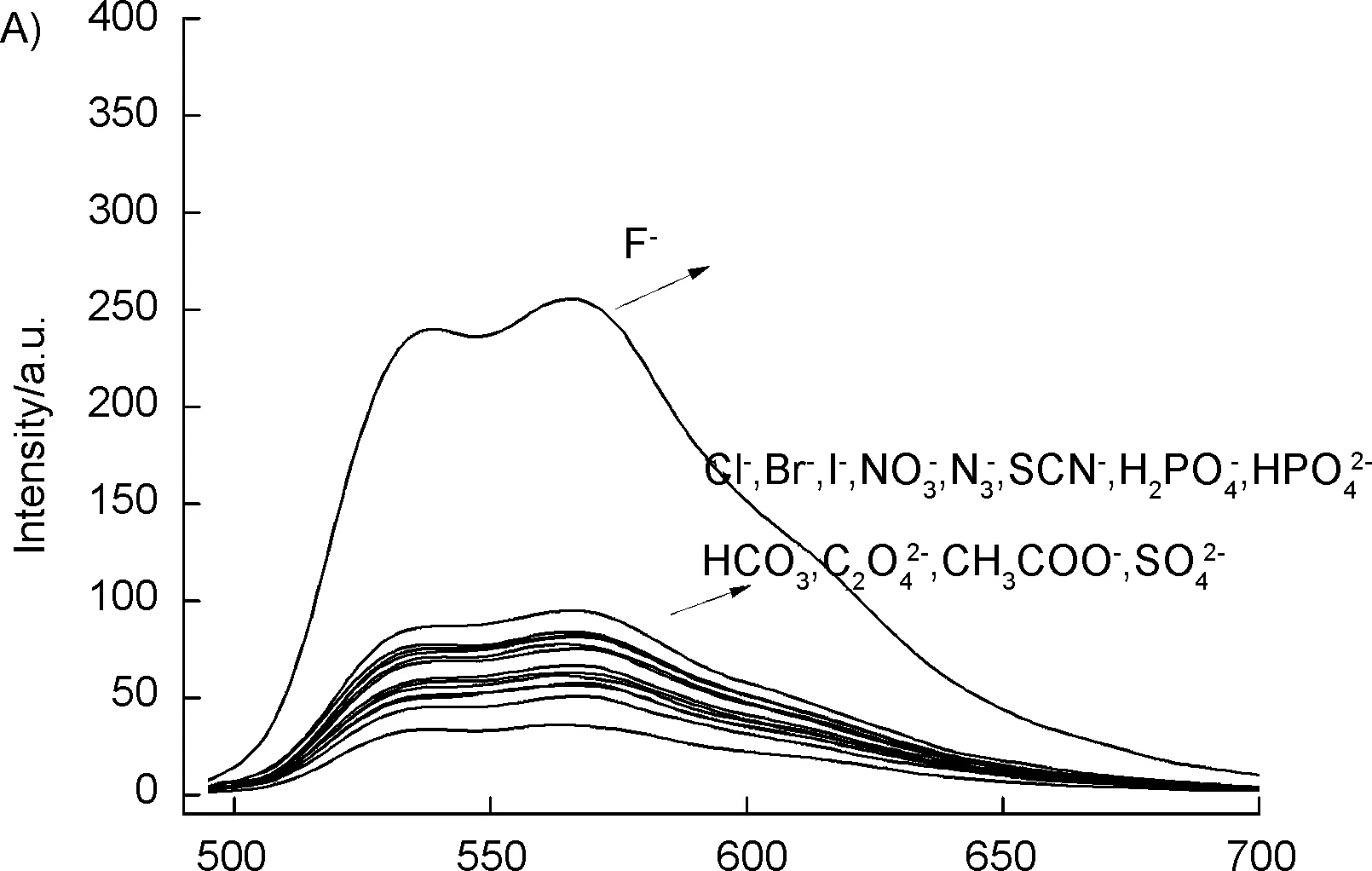
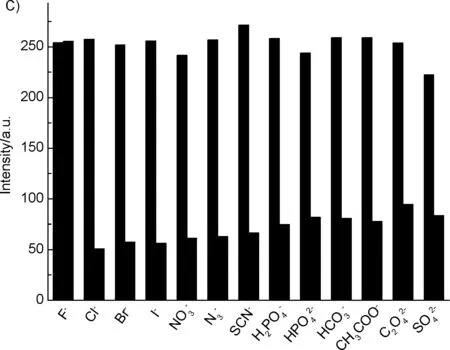
圖 4(A) AQTB1對F-的選擇性實驗 (B) AQTB1對F-的競爭性實驗 (C) AQTB1對F-的選擇性實驗和競爭性實驗的柱狀圖
2.4 識別機理
氟離子具有較強的親硅性,能形成穩定的Si—F鍵,使得許多含硅化合物在氟離子作用下發生脫硅化反應,生成新的化合物。2003年,Kim等首次報導了基于氟離子誘導硅氧鍵斷裂反應的熒光探針,在四氫呋喃溶液中實現了氟離子的定量檢測[23]。隨后研究人員將硅氧烷與不同種類的有機熒光染料相連,設計并合成了多種氟離子探針。
在此基礎上,為了確定探針AQTB1對氟離子的檢測機理,對加入氟離子前后的探針進行了質譜比較。我們認為探針AQTB1在氟離子誘導下后,會發生Si—O鍵的斷裂,使得原來熒光較弱的AQTB1轉化為熒光較強的1,4-二羥基蒽醌,完成對氟離子的定量檢測(圖5)。
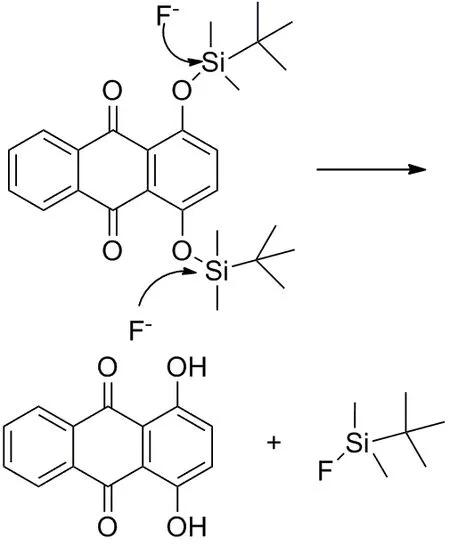
圖 5AQTB1對F-的傳感機理圖

λ/nm
為驗證上述機理,將完成氟離子檢測的AQTB1熒光光譜與1,4-DHAQ的熒光光譜進行了比較,發現二者的熒光發射峰位置基本相同(圖6)。隨后將檢測氟離子前后探針AQTB1的IR譜圖(圖略)進行了對比,發現未加探針氟離子前,AQTB1在981 cm-1和830 cm-1處存在Si—O鍵的伸縮振動峰[24],加入氟離子后,981 cm-1和830 cm-1處的紅外吸收峰消失,結合熒光和質譜數據,說明探針與氟離子反應后,AQTB1中的Si—O鍵斷裂,生成了1,4-DHAQ。
2.5 實際樣品分析
為了進一步探究探針AQTB1在實際水樣中檢測氟離子的可行性,選取了3個不同地方的水樣,加入一定量的氟離子并通過探針AQTB1來進行檢測。其中,南湖水在長春市南湖公園隨機采樣,牡丹水在長春市朝陽區牡丹園隨機采樣,自來水取自本實驗室。
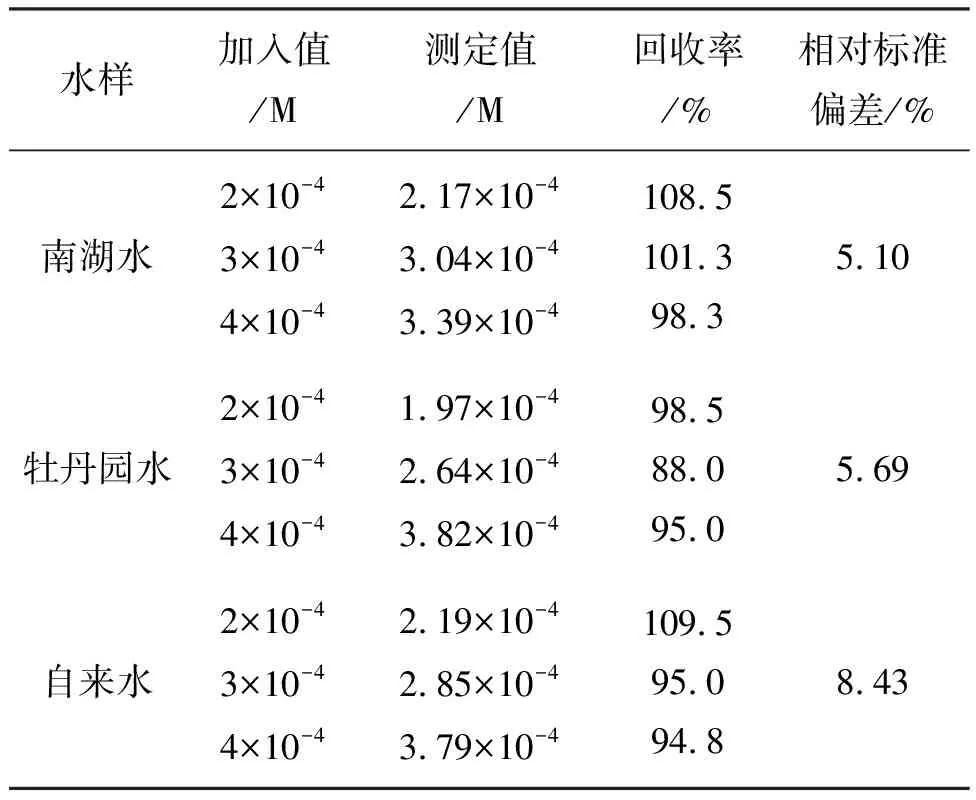
表1 實際水樣中氟離子含量的測定
稱取24.14 mg的四丁基氟化銨(3份)至10 mL的容量瓶中,分別加入3種不同的水樣定容,即可配制成1×10-2M的氟離子溶液。測試時,分別移取80 μL, 120 μL, 160 μL(1×10-2M)的上述配制的氟離子溶液,稀釋至2×10-4M, 3×10-4M, 4×10-4M的濃度測試。測試結果如表1所示,3個水平的氟離子的加標回收率為88.0%~109.5%,相對標準偏差(RSD)低于8.5%,表明探針AQTB1在檢測水體中的氟離子有一定的實用性。
2.6 探針AQTB1~3對氟離子的檢測性能
為了研究其他常見的硅氧烷是否也對氟離子有同樣的響應效果,選取了叔丁基二苯基氯硅烷和三-異丙基氯硅烷這兩個化合物作為探針的識別基團,通過上述的合成通法,得到了熒光探針分子AAQTB2和AQTB3。經過分析后發現(圖7),遇到氟離子后,它們的熒光強度均有所增加,表明該類探針能夠實現對氟離子的定量檢測。

λ/nm
以叔丁基-二甲基硅氧烷為識別基團,設計并合成了一種新型蒽醌類熒光增強型探針AQTB1、AQTB2和AQTB3,能在廣泛pH值(3~12)內實現對氟離子的快速檢測,有望應用于環境污染物的快速檢測。

