探討超聲斑點追蹤技術預測急性心肌梗死患者左心室重塑的臨床價值
石燦燦 鞏 雷 張 慧 刁 軍 武維恒
(1、沛縣嘉華醫院,江蘇徐州 221600;2、徐州醫科大學第二附屬醫院,江蘇徐州 221000)
左心室重塑(Left Ventricular Remodeling,LVR)多發生在缺血性心臟病患者中[1],在急性心肌梗死患者中,LVR 的發生率在30%-35%之間[2],血運重建技術特別是急診經皮冠脈介入治療(percutaneous coronary intervention,PCI)技術的進步,盡早恢復急性ST 段抬高型心肌梗死(ST segment elevation myocardial infarction,STEMI)患者心肌血流灌注,明顯降低心血管事件發生風險和LVR 的發生。LVR可導致左室收縮功能下降,增加心血管事件發生的風險和死亡率[3]。傳統的超聲心動圖技術臨床應用廣泛,超聲心動圖測定左心室收縮末期容積(left ventricular end systolic volumes,LVESV)、左心室舒張末期容積 (left ventricular end diastolic volumes,LVEDV) 以及射血分數 (left ventricularejection fraction,LVEF)等均可判定LVR 的發生[4]。超聲斑點追蹤技術(Speckle Tracking Echocardiography,STE)是一種較新的超聲技術,通過測定心肌應變或應變率來評價心室功能的變化。國外研究顯示STE 的左室整體縱向應變(Global Longitudinal Strain,GLS)可較好地預測急性心肌梗死患者心血管不良事件的發生[5]。
本研究目的是評價GLS 預測急性STEMI 患者在急診PCI 術開通梗死相關血管后3 月LVR 發生的臨床價值,現報道如下。
1 資料和方法
1.1 一般資料
選取2019 年1 月至2020 年2 月入院我院急診科患者85 例,其中男50 例,女35 例。所有參與試驗的患者都簽署入組的知情同意書,本試驗經醫院倫理委員會批準。入選標準:(1)首次發生急性STEMI患者;(2)缺血性胸痛癥狀持續30min 以上;(3)心電圖表現為至少相鄰兩個導聯ST 段明顯抬高;(4)符合2019 年中華醫學會心血管病分會制定《急性ST段抬高型心肌梗死診斷和治療指南》的標準[6];(5)年齡18-75 歲之間;(6)發病時間不超過12h;(7)入院具備行急診血運重建指征;(9)進行急診經皮冠脈介入治療(percutaneous coronary intervention,PCI),成功開通梗死相關血管,恢復心肌血流灌注[6]。
排除標準:(1)既往曾發生心肌梗死;(2)冠狀動脈病變無法進行血運重建;(3)嚴重心律失常;(4)慢性阻塞性肺病;(5)胸部聲窗差無法進行有效的超聲心動圖檢查。
1.2 超聲心動圖
入選患者在首次醫療接觸后,急診采集血液進行超敏C-反應蛋白(high-sensitivity C-reactive protein,hs-CRP)檢測,并遵循指南給予藥物治療和急診PCI 術開通梗死相關血管[6]。PCI 術后24h 內進行超聲心動圖檢查。超聲心動圖檢查由2 名有經驗的超聲心動圖醫生在不知患者其他臨床資料的情況下進行。
多普勒超聲診斷儀(Phillips IE33,美國)S5-1探頭,頻率1-3MHz,頻幀50-70 幀/s,采集3 個心動周期心尖四腔、二腔及左室長軸的二維灰階圖像。采用左心室(Left Ventricular,LV)17 節段分法[8],獲得LV 室壁運動積分、LV 整體縱向應變(Global Longitudinal Strain,GLS)。根據LV 在收縮期室壁厚度的變化,獲得LV 各節段室壁運動積分(運動正常,記為1 分;運動減弱,記為2 分;無運動,記為3分;反常運動;記為4 分)[8]。室壁運動記分指數(Wall motion score index,WMSI)=∑檢查節段記分/檢查節段數。雙平面Simpson 法測定LVESV、LVEDV 和LVEF。
圖像分析,啟用Phillips 軟件進行定量分析,手動描記左室心內膜,手工調節心內膜邊界,獲得包含一定心肌厚度的感興趣區,計算機逐幀追蹤感興趣區內斑點組織的運動,獲得3 個心動周期LV 的GLS 曲線,取其平均值。
1.3 觀察指標
所有患者PCI 術后3 個月進行超聲心動圖復查,測定LVESV、LVEDV、LVEF。LVEDV 較前增長20%以上判定為LVR[10]。
1.4 統計學處理
2 結果
2.1 入選患者基本資料
入院患者均順利完成PCI,在術后3 個月完成隨訪,共85 例患者完成隨訪,平均年齡(60.6±11.3)歲,其中男50 例,占58.8%,女35 例,占41.2%;糖尿病患者44 例,占51.8%;高血壓患者47 例,占55.3%;吸煙患者56 例,占65.9%。胸痛癥狀發生至首次醫療接觸(first meical contact,FMC)平均(154.5±56.6)min,FMC 至開通梗死相關血管平均(83.9±23.7)min。冠狀動脈前降支閉塞患者總計59例,占69.4%,見表1。
根據PCI 術后的3 個月時復查超聲心動圖結果,分為LVR 組和非LVR(non-LVR)組,發生LVR者28 例,57 例患者未發生LVR 現象。兩組患者的年齡構成,男性患者所占比例,高血壓、糖尿病、吸煙等患者構成比未見明顯統計學差異(P 均>0.05)。在胸痛癥狀發生至FMC 時間上,LVR 明顯長于non-LVR 組(185.3±62.7 vs 139.4±46.9min),且差異有統計學意義(P<0.001)。患者FMC 至開通梗死相關血管所用時間上,兩組之間差異無明顯統計學意義(86.4±25.3 vs 82.7±23.0min,P=0.501)。患者進行急診血運重建后,兩組患者在藥物治療上差異無明顯統計學意義(P>0.05),見表1。
2.2 患者血液指標hs-CRP 和超聲心動圖檢查參數
患者血清中hs-CRP 檢測結果,LVR 組明顯高于non-LVR 組(6.06±0.77 vs 5.31±0.87mg/L),差異有統計學意義(P<0.001),提示hs-CRP 水平高容易發生心室重塑。
超聲心動圖檢查結果顯示,基線時,LVR 組的GLS 明顯大于non-LVR 組(-11.95±0.46 vs -12.72±0.68),差異有統計學意義(P<0.001)。在基線和三個月隨訪時,兩組WMSI、LVESV 均未見統計學差異(P>0.05)。在基線時,兩組間LVEDV 和LVEF 未見統計學差異(P>0.05);在三個月隨訪時,LVR 組的LVEDV 明顯大于non-LVR 組,而LVR 組LVEF 明顯小于non-LVR 組,差異有統計學意義(P<0.001),見表2。
表2 左心室重塑組和未重塑組的檢測參數比較(±s)
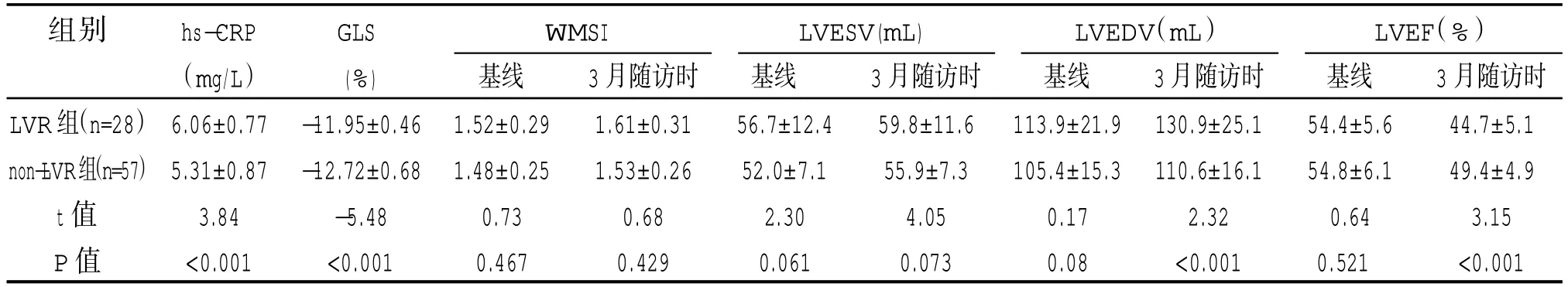
表2 左心室重塑組和未重塑組的檢測參數比較(±s)
hs-CRP 預測急性STEMI 患者在急診PCI 術后3 月LVR 的ROC 曲線下面積為0.752(P<0.001),最佳截斷點為5.57mg/L,敏感度為72.7%,特異度為68.8%(圖1A)。
GLS 預測急性STEMI 患者在急診PCI 術后3月LVR 的ROC 曲線下面積為0.839(P<0.001),最佳截斷點為-12.34%,敏感度為73.7%,特異度為85.7%(圖1B)。
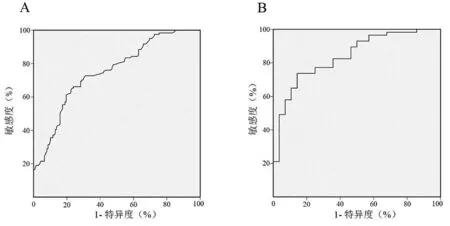
圖1 hs-CRP 和GLS 預測急性STEMI 患者在急診PCI 術后3 月LVR 的ROC 曲線,
3 討論
急性STEMI 發生后導致心肌細胞病理學改變而導致LV 的形態和幾何形狀發生改變,在LVR 中扮演重要的角色,LVR 的發生是病理生理過程的結果,LVR 的發生與心力衰竭的進展速度及長期預后有著密切聯系[11]。超聲心動圖檢查心功能已在臨床中廣泛使用,測定LVEF、LVESV 和LVESD 等參數來檢測LV 是否發生重塑現象[12]。目前國內采用STE檢測急性STEMI 急診PCI 術后LVR 鮮有研究。
急性STEMI 發生,首選急診血運重建開通梗死相關血管恢復心肌血流灌注,減少LVR 發生,從而減少心力衰竭乃至惡性室性心律失常的發生,但仍有30%左右患者出現LVR[13]。本研究入選急性STEMI 患者,進行急診PCI 術,順利開通梗死相關血管,恢復心肌血流灌注最大限度挽救瀕死心肌。本研究中采用hs-CRP 和STE 的檢測指標GLS 預測LVR 的發生,探討hs-CRP 和GLS 預測LVR 的可行性和準確性。隨訪發現本研究中發生LVR 現象的占32.9%,與國外研究基本相似[10]。hs-CRP 在機體免疫中起著舉足輕重的作用,不僅代表炎癥反應,也代表粥樣斑塊的易損性,同時也是STEMI 患者短期死亡率的預測指標[14]。本研究結果顯示hs-CRP 水平的升高提示急性STEMI 患者易發生心室重塑,從而出現左室收縮功能下降,影響患者預后。hs-CRP 水平預測急性STEMI 患者在急診PCI 術后3 月LVR 發生的敏感度、特異度分別為72.7%、68.8%,最佳截斷點為5.57mg/L。hs-CRP 水平越高,提示急性STEMI患者發生心室重塑可能性越大。
Meta 分析顯示,STE 檢測的參數中GLS、環向應變、徑向應變、旋轉以及扭轉均可預測LVR,通過Logistic 回歸顯示GLS 預測LVR 優于其他各項參數[15]。本研究選取的研究人群為急性STEMI 患者,全部進行急診PCI 術,入選不局限于前壁心肌梗死患者,研究左心室17 個節段的整體應變,而Park 等研究入選全部為急性前壁心肌梗死患者,研究僅為左心室前壁7 個節段[16]。本研究選取STE 參數GLS 預測急性STEMI 患者在急診PCI 術后3 月LVR 發生的敏感度、特異度分別為73.7%、85.7%,最佳截斷點為-12.34%,結果與既往文獻研究[16,17]相似。GLS 預測LVR 有良好的敏感度和特異度主要與心肌纖維走向有關,考慮可能與心內膜下的心肌縱向纖維對心肌灌注減少導致心肌受損更為敏感[18]。LVR 的發生與患者胸痛癥狀發生至FMC 時間長短有關,LVR組胸痛癥狀發生至FMC 時間較non-LVR 組明顯延長,且差異有統計學意義,FMC 至開通梗死相關血管時間兩組無統計差異。考慮可能與患者對胸痛癥狀認識不足,就診時間延遲,心肌梗死范圍逐漸擴大有關[19],導致LVR 發生幾率增加,而對胸痛重視和縮短FMC 至開通梗死相關血管時間,盡早恢復心肌血流灌注可有效減少LVR 發生[20]。
本研究顯示GLS 可較準確地預測急性STEMI患者進行急診PCI 術后3 月LVR 發生,GLS 指標通過超聲心動圖即可獲取,且無放射性污染,GLS 可作為獨立的檢測指標適宜在臨床推廣使用。
局限性:GLS 數據獲取受到超聲心動圖圖像的限制,要求圖像清晰,主要是患者心律和心率影響較大,不能進行實時分析。研究樣本量較小,今后應在臨床研究中擴大樣本量進行研究。

