烏頭湯和改良烏頭湯藥代動力學-藥效學動物實驗比較
孫 瑜,田樹成
(遼寧中醫藥大學附屬第三醫院,遼寧 沈陽 110003)
烏頭湯出自《金匱要略》,由制川烏、麻黃、炙甘草、白芍、黃芪等中藥組方,具有溫經散寒、祛濕鎮痛的功效,主要用于治療風濕性關節炎、類風濕關節炎及強直性脊柱炎等[1-2]。名老中醫李可在此基礎上配伍黑豆、防風,以減少烏頭毒性[3-4]。制川烏為烏頭湯及改良烏頭湯的君藥,味辛、苦,性熱,有大毒,具有抗炎、鎮痛、免疫調節作用,臨床常用于治療風濕類疾病。制川烏含有的單酯型生物堿既是活性成分,又是毒性成分,主要表現為對神經、心臟的毒性[5-8]。本研究中采用超高效液相色譜-串聯四級桿質譜(UPLC-MS/MS)技術分析烏頭湯及改良烏頭湯中單酯型生物堿化學成分在體內的變化規律及差異,探討烏頭湯中制川烏不同配伍時單酯型烏頭生物堿含量的變化,并結合現代藥效學對配伍增效減毒的作用進行闡述,為烏頭湯的配伍研究提供參考。
1 材料與方法
1.1 儀器、試藥與動物
儀器:UPLC-MS/MS 分析系統(包括Agilent 1290型高效液相色譜儀和Agilent 6460 型質譜檢測器);LG16-B 型高速離心機(北京雷勃爾離心機有限公司);Vortex-Genie2 型渦旋振蕩器(美國Scientific Industries公司);1208BH 型超聲波清洗器(德國Bandelin Sonorex RK 公司);HWS 24 型電熱恒溫水浴鍋(上海一恒科學儀器有限公司);Miui-Q 型超純水機(美國Mililpore 公司);AB265-S 型電子天平(瑞士Mettler Toledo);PV-200 型足趾腫脹測定儀(成都泰盟軟件有限公司)。
試藥:甲醇、乙腈(美國ACS 恩科化學);乙酸、乙酸銨(美國Sigma 公司),均為色譜純;水為超純水,其余試劑均為分析純;完全弗氏佐劑(CFA)、角叉菜膠(批號為021M0036V)均購自美國Sigma 公司,臨用時配成1%濃度的溶液。制川烏、麻黃、炙甘草、白芍、黃芪、黑豆、防風購于沈陽遼河藥房,均經遼寧中醫藥大學附屬第三醫院田樹成主任中藥師鑒定為正品。苯甲酰烏頭原堿對照品(批號為111794-201303),苯甲酰新烏頭原堿對照品(批號為111795-201303),苯甲酰次烏頭原堿對照品(批號為111796-201303),己酮可可堿對照品(批號為110736-201337),均購自中國食品藥品檢定研究院。
動物:清潔級雄性SD 大鼠96 只,體質量(270±30)g,許可證號為SCXK(黑)2013-001;昆明種小鼠48 只,普 通 級,體 質 量(20±2) g,許 可 證 號 為SCXK( 黑)2015-010,均購自哈爾濱醫科大學實驗動物中心。
1.2 方法
1.2.1 血液濃度檢測方法
1)溶液制備
對照品溶液:取各對照品適量,精密稱定,分別置容量瓶中,以甲醇溶解并定容,搖勻,得對照品溶液;精密吸取各對照品溶液置同一容量瓶中,甲醇定容至刻度,即得混合對照品溶液(苯甲酰新烏頭原堿、苯甲酰次烏頭原堿、苯甲酰烏頭原堿含量分別為5 ~5 000 ng/mL,2.5 ~2 500 ng/mL,2.5 ~2 500 ng/mL)。
供試品溶液:稱取過60 目篩的制川烏、炙甘草、麻黃、黃芪、白芍各3.0 g,精密稱定,置圓底燒瓶中,混合均勻,加10 倍量水浸泡30 min,水浴加熱1 h(微沸),靜置10 min,8 層紗布濾過,合并濾液;殘渣加入8 倍量水,水浴加熱1 h,靜置10 min,8 層紗布濾過,合并濾液;旋蒸濃縮至半流動狀態,得提取浸膏,為烏頭湯浸膏(處方e)。改良烏頭湯處方,根據老中醫李可提出的在原烏頭湯處方基礎上配伍黑豆、防風,稱取過60 目篩的制川烏、炙甘草、麻黃、黃芪、白芍、黑豆、防風各3.0 g,精密稱定,制備方法同上,為改良烏頭湯浸膏(處方b)。
標準曲線血漿樣品及質控樣品:精密吸取上述混合對照品溶液5 μL,加入空白血漿45 μL,渦旋30 s,配制成標準曲線血漿樣品,苯甲酰新烏頭原堿、苯甲酰次烏頭原堿、苯甲酰烏頭原堿含量分別為0.5 ~500 ng/mL,0.25 ~250 ng/mL,0.25 ~250 ng/mL。
2)色譜條件
色譜柱:Waters ACQULTY UPLC C18柱(100 mm×2.1 mm,1.7 μm);流動相:0.1%甲酸水溶液(流動相A)-乙腈(流動相B),梯度洗脫(0 ~2 min 時流動相A為95%→80%,2 ~3 min 時流動相A 為80%→70%,3 ~4 min 時流動相A 為70%→50%,4 ~5 min 時流動相A 為50;流速:0.35 mL/min;進樣量:1 μL;柱溫:30 ℃。
3)質譜條件
電噴霧離子源(ESI 源),正離子檢測。掃描方式:多反應離子監測(MRM);檢測離子質荷比:苯甲酰新烏頭原堿590.3→105.1,苯甲酰烏頭原堿604.1→105.1,苯甲酰次烏頭原堿574.3→105.1,己酮可可堿278.3→180.1;干燥氣(N2)流速:11.0 L/min;Nebulizer:0.103 35 Mpa;干燥氣溫度:300 ℃;檢測器電壓:4 000 V。
4)血漿樣品處理方法
取大鼠血漿50 μL,加入200 μL 己酮可可堿溶液(20.0 ng / mL)渦旋1 min,于4 ℃、15 000 r / min 離心10 min,取上清液置離心管中,氮吹儀下氮氣吹干,殘留物用50 μL 甲醇-水(50 ∶50,V / V)溶解,于4 ℃、15 000 r / min 離心10 min,取上清液置進樣瓶中,取1 μL 進樣。
1.2.2 藥代動力學試驗
烏頭湯組和改良烏頭湯組SD 大鼠(各6 只)自由飲水,給藥前禁食12 h,灌胃給予提取液(給藥體積為20 mL/kg)。分別于給藥后0.083,0.25,0.5,1,1.5,2,4,6,8,12,24 h 時眼底靜脈叢毛細管取血約每只0.1 mL,肝素鈉抗凝,4 500 r/min 離心10 min,分離上層血漿,-40 ℃保存,備用。
1.2.3 大鼠足腫脹藥效學試驗
藥物配制:依據給藥體積為20 mL/kg,處方b、處方e 臨用前以0.3% CMC -Na 配制成不同質量濃度的混懸液,吲哚美辛以0.3% CMC - Na 配制成0.625 mg/mL 的混懸液,攪拌,超聲振蕩,混勻,給藥過程中不斷混勻。
大鼠足腫脹模型建立:取清潔級雄性SD 大鼠,試驗前于試驗環境適應性喂養7 d 后單次口服給藥,3 h 后足跖內注射1%λ-角叉菜膠溶液。分別在致炎前(0 h)及致炎后1,2,3,4 h 時采用足趾測量儀測致炎足容積,計算足腫脹百分率。
腫脹度=致炎后足容積-致炎前足容積
腫脹率(%)= [(致炎后足容積-致炎前足容積)/致炎前足容積] ×100%
1.2.4 小鼠醋酸扭體鎮痛藥效學試驗
藥物配制:依據給藥體積為20 mL/kg,處方b 臨用前以0.3% CMC-Na 配制成1.60,0.80,0.40 g/mL 的混懸液,處方e 臨用前以0.3% CMC-Na 配制成1.28,0.64,0.32 g/mL 的混懸液,羅通定片(山西三裕制藥有限公司,國藥準字H14022278,規格為每片30 mg)研碎后以0.3% CMC-Na 配制成4.5 g/L 的混懸液,攪拌,超聲振蕩,混勻,給藥過程中不斷混勻。
小鼠醋酸扭體模型建立:處方b、處方e 單次灌胃給藥后3 h,羅通定混懸液單次灌胃給藥后0.5 h,空白對照組給予等體積0.3% CMC-Na,每只小鼠腹腔注射0.8%冰醋酸0.1 mL/10 g。由于刺激腹膜可引起扭體反應,表現為腹部收縮、軀體扭曲、后肢伸展及蠕動等。觀察并記錄注射致痛劑后20 min 內各小鼠的扭體次數。
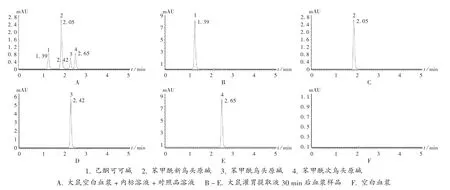
圖1 超高效液相提取色譜圖
2 結果
2.1 方法學考察
專屬性考察:取大鼠空白血漿、空白血漿+內標溶液+對照品、血漿樣品,按1.2.1 項下血漿樣品處理方法處理,依法進樣。結果血漿的內源性物質不干擾各成分和內標的測定,表明液質行為及專屬性良好。色譜圖見圖1。
線性關系考察:取大鼠空白血漿,每份45 μL,加入混合對照品溶液5 μL,渦旋30 s,精密吸取各標準曲線血漿樣品50 μL,依法處理,按擬訂條件進樣測定,記錄色譜圖。采用加權(1/X2)最小二乘法,以待測成分峰面積與內標峰面積的比值(Y)對樣品質量濃度(X)進行曲線擬合回歸,得回歸方程,定量限以信噪比(S/N)≥10計。結果見表1。

表1 線性關系考察結果
準確度和精密度試驗:配制低、中、高3 個質量濃度的對照品血漿樣品,依法處理,每個質量濃度取6 份樣品,1 d 內分別測定6 份樣品,并各取1 份樣品連續測定3 d,計算日內、日間精密度。結果見表2,表明方法準確度好,儀器精密度好。
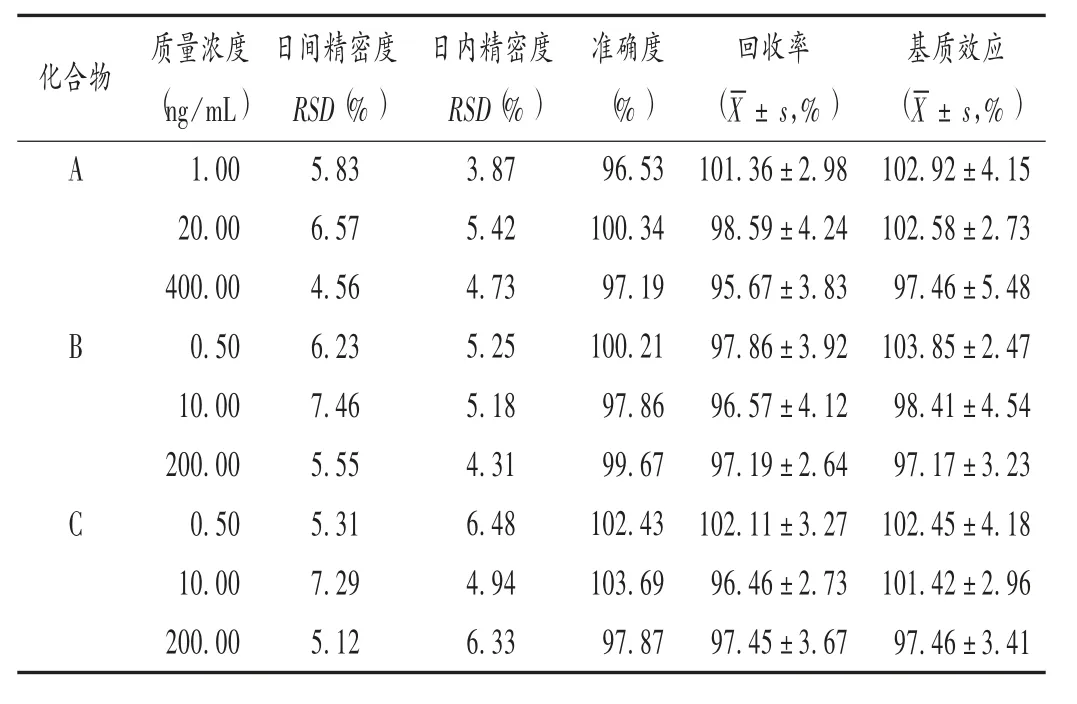
表2 在血漿中化合物回收率、基質效應及日內與日間精密度試驗結果(n=6)
回收率試驗與基質效應測定:分別制備低、中、高質量濃度的含藥質控樣品,依法進樣分析,記錄峰面積,每個質量濃度平行測定6 份,記錄待測物和內標的峰面積比值(A);另取空白血漿,依法加入對應的低、中、高濃度的系列對照品溶液進樣分析,記錄待測物和內標的峰面積比值(B),每個質量濃度平行測定6 份,提取回收率(% ) =A/B×100%。另用流動相將標準系列溶液配制成與上述理論濃度相同的低、中、高質量濃度溶液直接進樣分析,每個質量濃度平行測定6 份,記錄待測物和內標的峰面積比值(C),基質效應(% ) = B/C×100%。低、中、高質量濃度的回收率和基質效應見表2。結果表明,所建方法能滿足生物樣品的測定要求。
穩定性試驗:取各成分低、中、高3 個質量濃度的質控樣品室溫放置、自動進樣器內、-40 ℃長期冷凍、冷凍-解凍3 個循環等不同存儲條件下的穩定性。結果見表3。表明,血漿樣品室溫放置4 h、血漿樣品處理后在自動進樣器內放置24 h、血漿樣品冷凍-解凍循環3 次、血漿樣品長期冷凍于-40 ℃冰箱內30 d,各成分的RSD均小于15%。
2.2 藥代動力學試驗
烏頭堿類化合物在大鼠體內的平均藥-時曲線見圖2。血藥濃度數據采用PKSolver V 2.0 軟件計算,以藥物半衰期(t1/2)、達峰濃度(Cmax)、達峰時間(tmax)和藥-時曲線下面積(AUC)等參數表征該藥物的藥代動力學特征(各時間點血漿中均能檢測到,具有完整的體內過程),運用SPSS 17.0 統計學軟件分析。結果見表4。烏頭湯配伍黑豆、防風后,苯甲酰新烏頭原堿、苯甲酰次烏頭原堿的Cmax,AUC0-t,AUC0-∞均顯著下降。
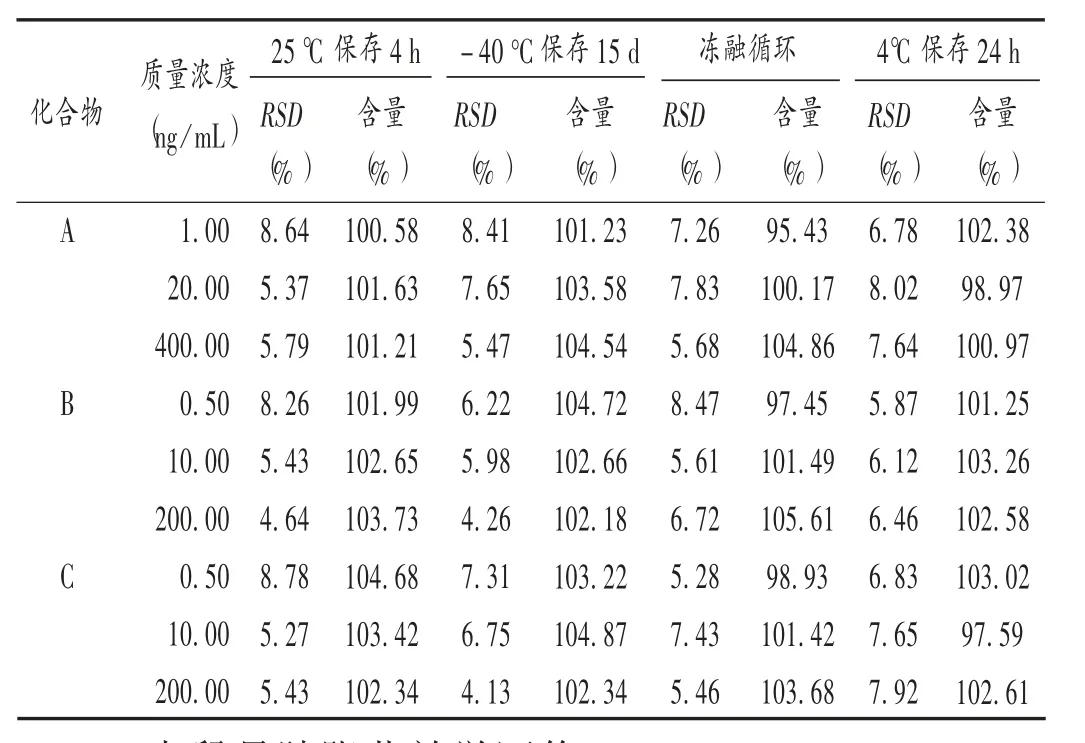
表3 化合物在大鼠血漿的穩定性試驗結果(n=6)
2.3 大鼠足腫脹藥效學評價
處方b 和處方e 不同濃度對角叉菜膠誘導大鼠足腫脹的影響以足腫脹率進行評價。結果見圖3。給藥后,與模型組相比,吲哚美辛具有明顯的抑制足腫脹作用。同時,處方b、處方e 也能劑量依賴性地抑制角叉菜膠誘導大鼠的足腫脹,其中處方b 高、中、低3 個質量濃度水平的效果都優于處方e。
2.4 小鼠醋酸扭體鎮痛效果評價
處方b 和處方e 不同質量濃度對醋酸誘導小鼠腹部疼痛的影響,以一定時間內小鼠扭體次數進行評價。結果見圖4。處方b 和處方e 都對醋酸誘導小鼠的扭體次數有一定的抑制作用,其中處方b 高、中、低3 個質量濃度水平的扭體次數較處方e 的更低,抑制效果明顯,且相對穩定。
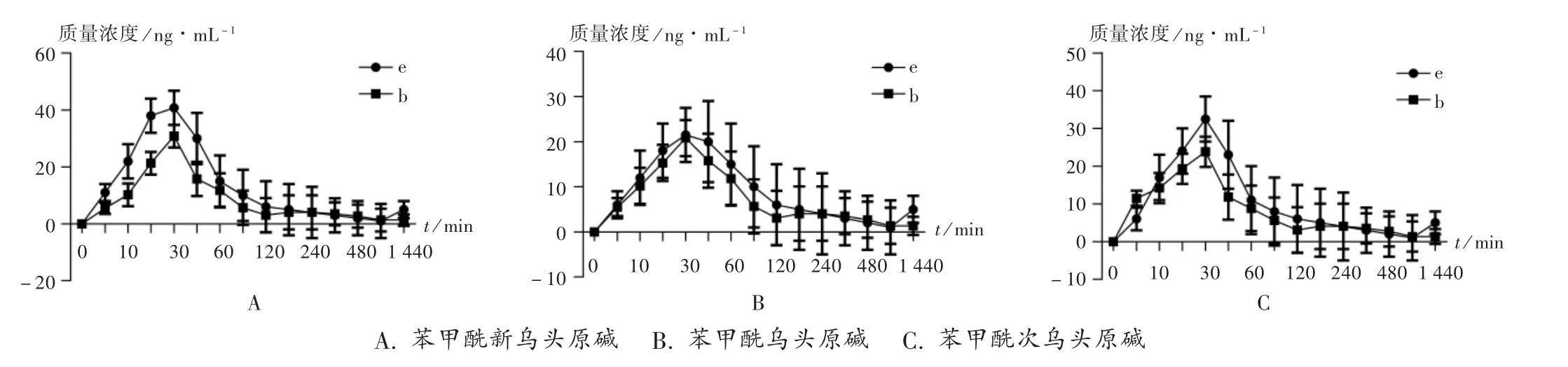
圖2 灌胃處方后3 種單酯型烏頭堿的藥-時曲線圖
表4 大鼠灌胃提取液后烏頭堿類化合物的藥代動力學參數(± s,n=6)
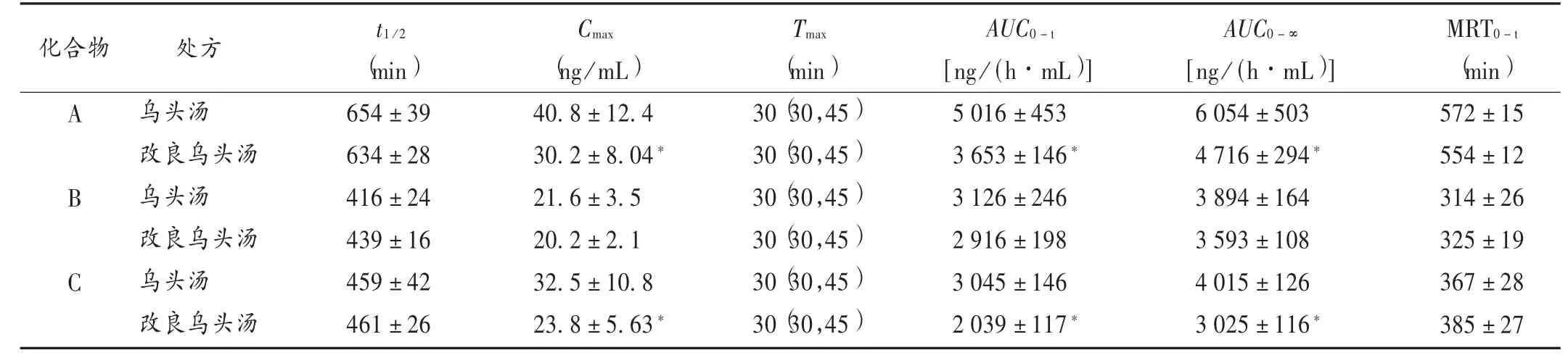
表4 大鼠灌胃提取液后烏頭堿類化合物的藥代動力學參數(± s,n=6)
注:與烏頭湯比較,*P <0.05。MRT 為平均駐留時間。
化合物A B C處方烏頭湯改良烏頭湯烏頭湯改良烏頭湯烏頭湯改良烏頭湯t1 /2(min)654±39 634±28 416±24 439±16 459±42 461±26 Cmax(ng/mL)40.8±12.4 30.2±8.04*21.6±3.5 20.2±2.1 32.5±10.8 23.8±5.63*Tmax(min)30(30,45)30(30,45)30(30,45)30(30,45)30(30,45)30(30,45)AUC0 -t[ng/ (h·mL)]5 016±453 3 653±146*3 126±246 2 916±198 3 045±146 2 039±117*AUC0 -∞[ng/ (h·mL)]6 054±503 4 716±294*3 894±164 3 593±108 4 015±126 3 025±116*MRT0 -t(min)572±15 554±12 314±26 325±19 367±28 385±27
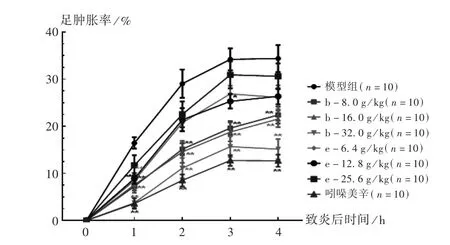
圖3 處方b 和處方e 不同質量濃度對角叉菜膠誘導大鼠足腫脹的影響
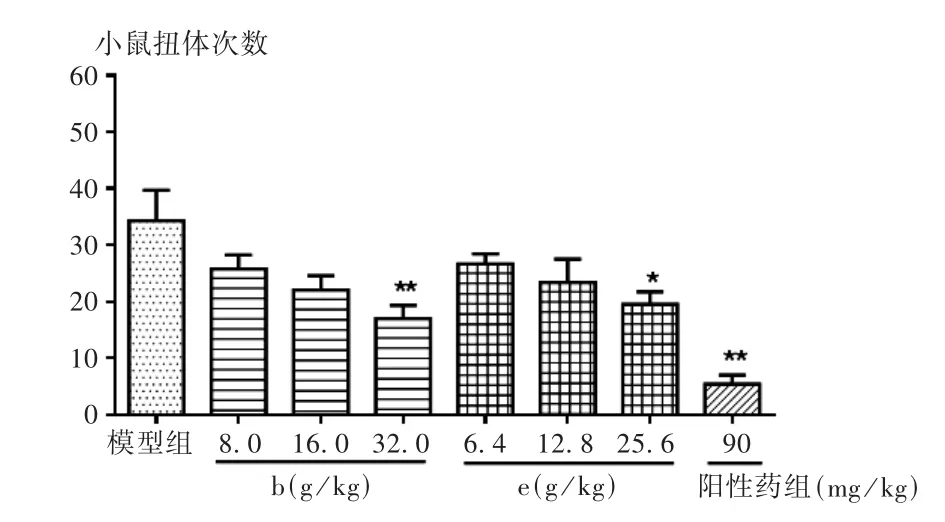
圖4 不同質量濃度處方b 和處方e 對小鼠醋酸扭體鎮痛效果的影響
3 討論
高靈敏度的UPLC-MS/MS 檢測手段逐漸應用到中藥復雜成分的分析及血漿中化學成分的研究[9-11]。本研究結果顯示,本方法準確度、精密度、靈敏度和專屬性較高,符合生物樣品分析方法要求。己酮可可堿性質穩定,易溶于甲醇,在正電離模式下響應良好,不干擾其他內源性成分的測定,可滿足測試需要。
處方b 血漿中發現,黑豆、防風的配伍抑制了苯甲酰新烏頭原堿和苯甲酰次烏頭原堿的吸收,Cmax值和AUC0-t值明顯下降。制川烏配伍防風、黑豆均可明顯降低制川烏中的單酯型烏頭生物堿在體內的含量,說明配伍防風、黑豆可有效地降低烏頭湯的毒性。烏頭堿型二萜生物堿既是川烏的活性成分,也是其毒性成分[12-13],治療量與中毒量非常接近,極易發生中毒事件,配伍防風、黑豆后降低了烏頭堿型二萜生物堿在體內的濃度,達到了減毒的效果。
角叉菜膠致大鼠足腫脹模型常用于評價或篩選藥物抗炎作用的經典急性炎癥模型,在新藥評價中應用非常廣泛。本研究中通過藥物作用于角叉菜膠致大鼠足腫脹模型后,發現處方b、處方e 對角叉菜膠引起的足腫脹均有明顯的抗炎作用[14-15]。小鼠醋酸扭體模型是通過于小鼠的腹膜內腔內注射乙酸誘導急性炎癥疼痛,其特征在于經后肢牽張腹部肌肉系統的收縮波,稱之為扭體反應,扭體發作次數的多少可反映動物對乙酸引起疼痛的反應強弱[16-17]。本研究結果顯示,處方b、處方e 對乙酸刺激小鼠誘導的疼痛反應有明顯的抑制作用,處方b 的鎮痛作用優于處方e。
綜上所述,處方b(即改良烏頭湯)達到了減毒增效的效果,有利于關節炎的治療。該結論可為下一步開展烏頭湯減毒增效配伍的機制研究提供了參考。

